Мелкоочаговая и перивентрикулярная лейкоэнцефалопатия сосудистого генеза что это такое
Лейкоэнцефалопатия сосудистого генеза
Мелкоочаговая лейкоэнцефалопатия сосудистого генеза – диагноз, который чаще ставится пациентам мужского пола, перешагнувших возрастной порог 55 лет, однако не все знают, что это такое.
При лейкоэнцефалопатии головного мозга в его подкорковых структурах разрушается белое вещество.
Этот вид заболевания является одной из разновидностей энцефалопатии, впервые описанной немецким психиатром и невропатологом Отто Бинсвангером в 1894 году, в связи с чем была названа в его честь.
Нечеткое описание заболевания и небольшое количество обследований пациентов с признаками деменции в течение длительного времени не давало возможности признать патологию многими невропатологами и психиатрами.
С появлением компьютерной и магнитно-резонансной томографий были подтверждены изменения в белом веществе головного мозга, связанные с постоянно повышенным артериальным давлением, вызывающие старческое слабоумие.
Лечение заболевания осуществляется невропатологами и психиатрами.
Лейкоэнцефалопатия имеет разновидности, однако практически всегда, речь идет об изменениях в белом веществе головного мозга. Вид заболевания определяет схему лечения.
Лекоэнцефалопатия сосудистого генеза
Лекоэнцефалопатия сосудистого генеза (мелкоочаговая) – цереброваскулярный патологический процесс.
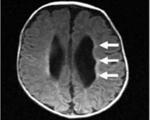
Артериальная гипертензия становится причиной склероза мелких мозговых сосудов – капилляров, их ишемизации, утолщения сосудистых стенок и др. В результате атрофическим изменениям подвергается белое вещество, передающее нервные импульсы. При этом наблюдается:
Желудочки мозга начинают разрушаться.
Обычно, первые признаки мелкоочаговой лейкоэнцефалопатии могут проявиться у пациентов, достигших шестидесятилетнего возраста, а при наследственном факторе и ранее.
Мультифокальная прогрессирующая сосудистая лейкоэнцефалопатия
Мультифокальная прогрессирующая сосудистая лейкоэнцефалопатия проявляется при вирусном поражении центральной нервной системы, способствующем нарушениям функций иммунитета.
Ослабление иммунной защиты ведет к разрушению белого вещества головного мозга.
Патологические изменения провоцирует иммунодефицит: ВИЧ-инфицированные (5%), больные СПИДом (50%).
Также видоизмененные лейкоциты при лейкозе теряют способность бороться с инфекцией, что способствует возникновению иммуннодефицита и, как следствие, к патологическим изменениям в головном мозге.
Воздействие вирусов приводит к очаговому поражению оболочек нервных волокон, увеличению и деформации клеток нервов. Вовлечение в процесс серого вещества не наблюдается. Происходит изменения структуры белого вещества, оно размягчается и приобретает студенистость с появлением на его поверхности множественных небольших впадин.
Проявление когнитивных нарушений может варьироваться от проявления легких нарушений до ярко выраженного слабоумия. К очаговым неврологическим симптомам относятся: нарушение речи и понижение зрения, иногда до полной его потери. Ускоренное прогрессирование двигательных расстройств может спровоцировать тяжелую инвалидность.
Перивентрикулярная (очаговая) лейкоэнцефалопатия
Перивентрикулярная (очаговая) лейкоэнцефалопатия является обширным поражением головного мозга, вызванным недостатком кислорода или хроническим нарушением его кровоснабжения.
Патологии подвергаются области мозжечка, мозгового ствола и подотделы, отвечающие за движения человека. Длительный недостаток кислорода ведет к сухому некрозу (отмиранию) белого вещества. Имеет стремительное развитие и способствует возникновению выраженных нарушений двигательной активности.
Перивентрикулярная лейкоэнцефалопатия может быть спровоцирована гипоксией плода и привести к детскому церебральному параличу (ДЦП).
Исчезновение белого вещества
Этот тип заболевания вызывается мутирующими генами.
Как правило, манифестация патологии обнаруживается у возрастной категории пациентов от 2-х до 6-ти лет, но может проявиться как в младенчестве, так и у взрослых.
При полном исчезновении белого вещества на последней стадии заболевания, стенки желудочков и кора головного мозга сохраняются.
Причины
Прогрессирующая лейкоэнцефалопатия сосудистого происхождения также может развиться вследствие:
Возникновение мелкоочаговой лейкоэнцефалопатии сосудистого генеза вероятно:
Для предупреждения возникновения заболевания, необходимо заблаговременно избавиться от всех факторов риска.
Симптомы
Симптоматика патологических процессов развивается в течение нескольких лет и может проявляться в двух вариантах:
Как правило, ухудшение симптомов наблюдается при повышенном артериальном давлении в течение длительного времени.
На первоначальных стадиях клиническая картина лейкоэнцефалопатии характеризуется:
Далее нарушается сон, увеличивается мышечный тонус, человек становится раздражительным, подверженным депрессивным состояниям, чувству страха, фобиям.
Иногда наблюдаются понижение зрения, головные боли, усиливающиеся во время чихания или кашля.
В итоге пациент становится полностью беспомощным, подверженным эпиприступам, неспособным себя обслуживать, контролировать опорожнение кишечника и мочевого пузыря.
Чаще всего симптомы проявляют себя как:
Психические нарушения
При сосудистой лейкоэнцефалопатии у заболевших наблюдаются психические расстройства, выражающиеся:
Нарушенная память и внимание приводят к полнейшей потере ориентации человека во времени и пространстве.
Проявление личностных изменений напрямую зависит от выраженности слабоумия и имеет большое разнообразие.
Развитие факультативных признаков наблюдается в 70–80% случае. Они характеризуются спутанностью сознания, бредовыми расстройствами, депрессией, тревожными расстройствами, психопатоподобным поведением.
Симптоматика слабоумия зависит от его вида:
Клинические проявления деменции варьируются в широких пределах.
Диагностика
Комплексная диагностика патологических изменений в белом веществе головного мозга включает в себя:
Дальше следует назначение дифференциальной диагностики с болезнями Паркинсона, Альцгеймера, рассеянным склерозом, лучевой энцефалопатией, психическими расстройствами, нормотензивной гидроцефалией.
При возникновении деменции вследствие сосудистой лейкоэнцефалопатии, требуется выявить связь между патологическими изменениями в белом веществе головного мозга и приобретенным слабоумием.
Лечение
Современная медицина не располагает методами, способными полностью избавить человека от сосудистой лейкоэнцефалопатии.
Целью лечения составляет:
Направления лечения включают в себя:
Специалисты прибегают к помощи следующих лекарственных средств:
Не исключена рефлекто– физиотерапия: дыхательная гимнастика, массаж, иглоукалывание, сеансы мануальной терапии.
Профилактические меры и прогноз
Как правило, пациенты с сосудистой лейкоэнцефалопатией живут не более двух лет.
Также, четко выработанных правил для предотвращения патологии не существует. Однако, минимизировать риск возникновения патологических изменений в белом веществе возможно:
Своевременные диагностика и лечение сосудистой лейкоэнцефалопатии помогут продлить жизнь пациенту.
Прогрессирующая сосудистая лейкоэнцефалопатия (I67.3)
Версия: Справочник заболеваний MedElement
Общая информация
Краткое описание
Примечание. Из данной подрубрики исключена «Субкортикальная сосудистая деменция (F01.2).
Этиология и патогенез
Описаны семейные случаи заболевания с началом до 40 лет, без артериальной гипертензии. Более чем в 80% случаев болезнь дебютирует в возрастном промежутке от 50 до 70 лет.
Страдают также и более крупные артерии диаметром до 500 мкм, и все микроциркуляторное русло.
Эпидемиология
Болезнь (энцефалопатия) Бинсвангера встречается довольно часто. По данным клинико-компьютерно-томографического исследования, она составляет около 1/3 всех случаев сосудистой деменции.
Возраст. Более чем в 80% случаев болезнь дебютирует в возрастном промежутке от 50 до 70 лет.
Факторы и группы риска
Клиническая картина
Cимптомы, течение
Клиническая картина болезни Бинсвангера характеризуется прогрессирующими когнитивными нарушениями, нарушениями функции ходьбы и тазовыми расстройствами. На последнем этапе заболевания клиническая картина представлена слабоумием, полной беспомощностью больных (не ходят, не обслуживают себя, не контролируют функцию тазовых органов).
Картина слабоумия может значительно варьироваться по степени тяжести и особенностям симптоматики.
В целом для болезни Бинсвангера характерно неуклонно-прогредиентное течение, но возможны и периоды длительной стабилизации. Причинами слабоумия в этих случаях считаются разобщение корково-подкорковых связей, наступающее в результате поражения подкоркового белого вещества, а также дисфункция базальных ганглиев и таламуса.
Изменение походки на начальных стадиях болезни Бинсвангера заключаются в следующем: походка шаркающая или семенящая, мелкими шажками, «магнитная» (ноги как бы прилипают к полу). На следующей стадии она становится «осторожной», увеличивается опорная площадь стояния, распадается автоматизм ходьбы (диспраксия или апраксия ходьбы) и все более включается произвольный контроль за ходьбой – походка такого больного напоминает походку здорового человека, оказавшегося на ледяном поле.
Основные характеристики лобной диспраксии ходьбы, связанной с дезавтоматизацией ходьбы, следующие:
• замедление ходьбы;
• укорочение шага;
• затруднение в начале ходьбы (инициация ходьбы);
• неустойчивость при поворотах (постуральная дисфункция);
• расширение базы опоры;
• снижение длины шагов.
Для нарушения тазовых функций при болезни Бинсвангера характерно развитие «гиперактивности» («гиперрефлекторности») мочевого пузыря, что проявляется повышенной сократительной активностью детрузора. Гиперактивность мочевого пузыря характеризуется: учащенным мочеиспусканием; императивными позывами на мочеиспускание, которые по мере прогрессирования заболевания переходят в случаи императивного недержания мочи.
Двигательные нарушения могут также характеризоваться (помимо нарушения ходьбы): другой экстрапирамидной патологией в виде паркинсоноподобной симптоматики, а также легкими или умеренными центральными моно- или гемипарезами, часто быстро регрессирующими (регресс очаговой двигательной симптоматики становится неполным по мере прогрессирования заболевания). Характерен псевдобульбарный синдром.
Эмоционально-волевые нарушения представлены астеническим, неврозоподобным или астено-депрессивным синдром. По мере прогрессирования заболевания на первый план выходят не астения и депрессия, а нарастание эмоционального оскудения, сужение круга интересов и спонтанности.
В критериях подчеркивается, что у пациента должны отсутствовать множественные или двухсторонние корковые очаги по данным КТ и МРТ, и тяжелая деменция.
Диагностика
Осложнения
Транзиторные ишемические атаки (ТИА, преходящие нарушения мозгового кровообращения) характеризуются кратковременными симптомами локальной ишемии мозга.
ТИА обычно связаны с гемодинамической недостаточностью, возникающей при выраженном атеросклеротическом стенозе сонных или позвоночных артерий в их дистальных ветвях или артериальной эмболией.
В большинстве случаев транзиторные ишемические атаки разрешаются в течение 5-20 минут.
Клиническое значение ТИА состоит в том, что они служат предвестниками не только инсульта, но и инфаркта миокарда и представляют собой сигналы опасности, требующие от врача быстрых действий. Больных с ТИА необходимо госпитализировать в инсультное отделение для наблюдения, всестороннего обследования и проведения профилактики ишемического инсульта.
ТИА часто проявляются при снижении АД, физической нагрузке, натуживании, приеме пищи; при этом очаговые неврологические симптомы нередко проявляются на фоне предобморочного состояния, иногда по нескольку раз в день. Больные часто жалуются на предобморочное состояние, головокружение, нарушения зрения, слабость в конечностях, тошноту и рвоту, нарушения памяти, шум в ушах, нарушения чувствительности, неожиданную утрату равновесия.
Ишемический инсульт возникает в результате критического снижения или прекращения кровоснабжения участка мозга с последующим развитием очага некроза мозговой ткани.
Внутримозговое кровоизлияние возникает в результате разрыва патологически измененных сосудов мозга, приводящего к кровоизлияниям.
Перивентрикулярная лейкомаляция
Перивентрикулярная лейкомаляция — это гипоксически-ишемическая энцефалопатия, характеризующаяся поражением белого вещества головного мозга новорожденных. Состояние чаще возникает у недоношенных, провоцируется патологиями течения беременности и родов, неадекватной респираторной поддержкой в постнатальном периоде. Заболевание проявляется мышечной дистонией, судорожным синдромом, задержкой психомоторного развития. Для диагностики болезни назначается КТ или МРТ мозга, ЭЭГ, допплерография церебральных сосудов. Лечение лейкомаляции включает медикаменты (нейропротекторы, инфузионные растворы, антиконвульсанты), индивидуальный комплекс физиотерапии, массажа, ЛФК.
МКБ-10
Общие сведения
По разным данным, перивентрикулярная лейкомаляция (ПВЛ) встречается у 4,8-9% младенцев, причем среди больных преобладают недоношенные новорожденные (78%). Наибольшая вероятность появления болезни у детей, родившихся на сроке 27-32 недели. По данным аутопсии умерших младенцев, признаки ПВЛ регистрируются чаще — у 50-75%. Заболевание имеет большую значимость в детской неврологии, поскольку может вызывать тяжелые отдаленные последствия, считается ведущей причиной ДЦП.
Причины
Основной этиологический фактор перивентрикулярной лейкомаляции — внутриутробная гипоксия, которая выступает следствием осложнений протекания беременности, материнских факторов риска либо негативного экзогенного воздействия. Также состояние может возникать при перинатальной гипоксии, которая развивается во время родов, в первые дни жизни младенца (при синдроме дыхательных расстройств, врожденных аномалиях сердца и легких, неонатальном сепсисе).
В группе риска наибольшую по численности категорию составляют недоношенные младенцы. Зачастую лейкомаляция выявляется у детей, которое были рождены от матерей с сахарным диабетом, хронической анемией, гипертиреозом либо страдавших от преэклампсии и эклампсии. Состояние возникает при выполнении экстренного кесарева сечения, неадекватном родовспоможении (травмирующие акушерские пособия). Высокая частота лейкомаляции (до 22%) отмечается при сочетании длительного безводного периода с хориоамнионитом у матери.
Патогенез
Поражение головного мозга связано со снижением кровотока в церебральных сосудах, недостаточным поступлением кислорода и питательных ингредиентов. Перивентрикулярная область наиболее чувствительна к этим изменениям, что обусловлено особенностями кровоснабжения, несовершенством процессов ауторегуляции, нейроонтогенетическими особенностями головного мозга у младенцев.
Недоношенные намного чаще страдают лейкомаляцией, поскольку у них на фоне гипоксии не увеличивается церебральный кровоток, как это бывает у рожденных в срок младенцев. В результате этого резко уменьшается кровоток в зоне между вентрикулофугальными и вентрикулопетальными артериями, быстро формируется гиперкапния и ацидоз. Расстройства микроциркуляции проявляются стазом, тромбозом, вне- и внутриклеточным отеком белого вещества.
При перивентрикулярной лейкомаляции в конечном итоге происходит некроз отельных участков мозгового вещества, образование кист, избыточное накопление медиаторов воспаления. Поскольку на 28-32 неделях в норме происходит активная миелинизация белого вещества, а в условиях гипоксии этот процесс не может происходить, недоношенные новорожденные впоследствии имеют серьезные органические поражения ЦНС.
Формирование ПВЛ возможно не только при недостатке кислорода, но и при гипероксии — при проведении ИВЛ, оказании других видов респираторной поддержки. При избыточном поступлении кислорода повышается рН крови в мозговой ткани, что вызывает рефлекторный спазм сосудов, затруднение венозного оттока. Также кислород активизирует процессы свободнорадикального церебрального повреждения.
Симптомы
Как правило, перивентрикулярная лейкомаляция формируется антенатально или на протяжении первых часов после рождения ребенка, поэтому начальные признаки заметны уже в родильном доме, особенно если младенец рожден недоношенным. При обширном повреждении белого вещества происходят нарушения сознания по типу летаргии или комы, однако возможна обратная симптоматика — повышенная возбудимость, оживление безусловных рефлексов, судорожный синдром.
Типичным проявлением патологии являются изменения тонуса мышц. На первом месяце жизни преобладает слабость мускулатуры ног в сочетании с нормальным формированием мышц верхних конечностей. У недоношенных новорожденных часто отмечается тотальная мышечная гипотония. Такие нарушения сохраняются в среднем до 6 месяцев, после чего они сменяются спастическими явлениями — повышением тонуса мускулатуры нижних конечностей, оживлением коленных рефлексов.
Течение перивентрикулярной лейкомаляции имеет неравномерный характер: периоды обострения симптоматики сменяются «мнимым благополучием», когда ребенок развивается относительно нормально. Затем происходит задержка формирования моторных навыков, развиваются различные сенсорные нарушения, дизартрия. 66% детей, особенно недоношенные, страдают от снижения остроты зрения вплоть до полной слепоты вследствие атрофии зрительных нервов.
Осложнения
Перивентрикулярные поражения белого вещества — крайне тяжелое состояние. Недоношенные дети с ПВЛ умирают в 50% случаев еще в период новорожденности, у выживших обычно наступает инвалидность с полной дезадаптацией. Пациенты с длительно сохраняющимся судорожными приступами в 85% случаев имеют грубую задержку психомоторного развития. У перенесших ПВЛ в будущем в 1,5 раза чаще встречаются фебрильные судороги, в 27 раз чаще формируется эпилепсия.
При множественных кистах в перивентрикулярной зоне у 80-97% больных (чаще — недоношенных) возникает детский церебральный паралич (ДЦП), который сопровождается глубоким психоречевым отставанием. Развитие заболевания связано с повреждением центральной части внутренней капсулы, средне- и заднелобных сегментов белого вещества полушарий. Также лейкомаляция вызывает микроцефалию (у 42% пациентов), нейросенсорную тугоухость (у 28% больных).
Диагностика
Постановка правильного диагноза в неонатальном периоде затруднена, что объясняется полиморфностью клинической картины, отсутствием патогномоничных симптомов. При физикальном осмотре выявляется асимметрия мышечного тонуса, патологическое усиление рефлексов, на более поздних этапах — спастическая диплегия. Особую настороженность следует проявлять в отношении детей, родившихся недоношенными. В план обследования новорожденных с подозрением на ПВЛ включаются:
Лечение перивентрикулярной лейкомаляции
Терапия перивентрикулярной лейкомаляции представляет собой сложную задачу, учитывая необратимый характер повреждений белого вещества, частое сочетание гипоксически-ишемической энцефалопатии с поражениями других систем организма у недоношенных. Медикаментозное лечение подбирается на основе ведущих синдромов болезни и включает следующие группы препаратов:
Учитывая высокую частоту резидуальных неврологических явлений, рекомендовано восстановительное лечение. Чтобы улучшить двигательные способности, назначаются курсы массажа, физиотерапии, лечебной физкультуры. Для развития речевых навыков требуются коррекционные занятия у логопеда, дефектолога. Детям с поражением органов чувств нужна помощь тифлопедагога, сурдопедагога. Пациентам с ДЦП необходимы специальные ходунки, костыли, инвалидные коляски.
Прогноз и профилактика
В большинстве случаев лейкомаляция отличается неблагоприятным течением, отличается высоким уровнем смертности во время младенчества. Для выживших детей прогноз напрямую зависит от тяжести органического дефекта перивентрикулярной зоны, своевременности и полноты проведенного лечения. Профилактика ПВЛ включает рациональное ведение беременности, предупреждение родового травматизма, соблюдение протоколов при респираторной поддержке в роддоме, усиленный контроль за развитием недоношенных.
Что такое энцефалопатия и чем она опасна?
Что такое энцефалопатия?

Энцефалопатия бывает врожденной и приобретенной. В каждом случае причинами заболевания становятся разные факторы, но их объединяет устойчивое нарушение мозгового кровообращения.
В случае с новорожденными детьми наличие заболевания не всегда становится очевидным. Как правило, диагноз ставят ближе к году при наличии специфической симптоматики. У взрослых людей широко распространены патологии, вызванные сосудистыми нарушениями. К примеру, при атеросклерозе уменьшается просвет сосудов в результате отложения на их стенках липидов. Приток крови к мозгу снижается, развивается ишемия. В сложных случаях просвет сосуда перекрывается кровяным сгустком или холестериновой бляшкой, появляется инсульт, в результате которого отмирают клетки головного мозга.
У каждой разновидности заболевания свои специфические признаки и методы терапии. По этой причине важно вовремя обратиться к врачу, чтобы пройти диагностику и лечение. Проявления нарушений зависят от того, какая область головного мозга поражена.
Сосудистая энцефалопатия. Возникает в результате нарушений кровоснабжения головного мозга и кислородного голодания клеток. Патология может иметь атеросклеротический или гипертонический характер. В первом случае в кровеносных сосудах присутствуют атеросклеротические бляшки, а во втором отмечается повышенное артериальное давление с осложнением в виде отека головного мозга.
Травматическая. В этом случае энцефалопатия развивается как результат перенесенной черепно-мозговой травмы. При заболевании могут отмечаться дегенеративные, дистрофические, рубцовые изменения тканей головного мозга. Чаще всего патология наблюдается у спортсменов, водителей и пассажиров транспортных средств, а также новорожденных детей.
Лучевая. Заболевание может стать следствием воздействия на головной мозг ионизирующего излучения. Такая разновидность энцефалопатии может наблюдаться у специалистов, участвующих в устранении последствий радиационных аварий, а также у тех, кто работает с соответствующим оборудованием.
Метаболическая (токсическая). Поражение головного мозга может быть вызвано интоксикацией организма на фоне печеночной недостаточности, сахарного диабета, отравления угарным газом, солями тяжелых металлов и пр. Токсическое отравление также приводит к тяжелым неврологическим нарушениям.
Воспалительная. Чаще всего речь идет о воспалительных процессах в стенках кровеносных сосудов. Выраженность и специфика проявлений зависят от пораженной области.
Вакцинная. Это редкая разновидность неврологического расстройства, которое появляется в ответ на введение вакцины. Чаще всего реакция наблюдается на препараты от коклюша.
Дисциркуляторная. Нарушение работы головного мозга возникает из-за постепенно усиливающейся недостаточности кровоснабжения. Дисциркуляторная энцефалопатия напрямую влияет на когнитивные способности и неврологические расстройства.
Резидуальная энцефалопатия (остаточная). В головном мозге происходит структурное изменение тканей вследствие перенесенных ранее травм, ишемической болезни, инфекций.
Губчатая. Эта разновидность энцефалопатии объединяет тяжелые заболевания, при которых мозг превращается в губчатое тело. Среди них можно выделить синдром Гетсмана-Штрауслера-Шейнкера, болезнь Крейтцфельда-Якоба и др.
Для заболевания характерно разнообразие клинических проявлений, которые зависят от причин, вызвавших нарушения работы головного мозга. Энцефалопатия может иметь острое и хроническое течение.
Во втором случае признаки нарушения работы головного мозга проявляются постепенно в виде головных болей, забывчивости, эмоциональной нестабильности.
Болезнь в своем развитии проходит несколько стадий, для которых характерны следующие проявления:
Современные методы обследования позволяют установить локализацию, характер патологии, механизм ее появления. Диагностика может включать:
Анализы крови для определения уровня гормонов, липидов, холестерина, сахара и других элементов, которые могут указывать на развитие дисциркуляторной энцефалопатии.
Реоэнцефалографию (РЭГ) для измерения кровотока в головном мозге, определения эластичности и напряжения стенок сосудов.
Магнитно-резонансную томографию для анализа морфологических изменений тканей головного мозга. МРТ позволяет дифференцировать энцефалографию от других заболеваний нервной системы: болезни Альцгеймера, инсульта, опухолей и др.
Ультразвуковую допплерографию для определения скорости кровотока в отдельном кровеносном сосуде и уточнения местоположения атеросклеротической бляшки. Дает информацию о состоянии церебрального кровообращения.
Можно ли вылечить энцефалопатию?
Заболевание требует длительной курсовой терапии и наблюдения у врача-невролога. Для успешного лечения и устранения симптомов болезни первостепенное значение имеет диагностика причин ее появления.
Острая энцефалопатия является показанием к срочной госпитализации и проведению дезинтоксикационной терапии в условиях стационара. Хроническая форма патологии требует соблюдения определенной диеты и приема лекарств по назначению врача 2?3 раза в год.

Лекарства от гипертонии требуют строгого соблюдения графика приема, как правило, 2?3 раза в сутки. Многим пациентам требуется пожизненное употребление препаратов для нормализации артериального давления. Дозировку и разновидность лекарства должен назначать лечащий врач, поскольку каждое из них действует с различной интенсивностью и по-разному выводится из организма.
Современные гипотензивные лекарства делятся на следующие группы:
ингибиторы АПФ (ангиотензинпревращающего фермента);
прямые ингибиторы ренина;
комбинированные и другие препараты.
Для улучшения обмена веществ головного мозга назначаются «Кавинтон», «Вазобрал», «Коринфар», «Целипрол», «Никошпан», «Пикамилон» и другие препараты различных групп.
Лекарства помогают восстановить мозговое кровообращение и благодаря этому устранить такие симптомы, как:
головная боль и головокружения;
нарушение координации движений;
проблемы с памятью;
перепады настроения и пр.
Основные группы препаратов для улучшения мозгового кровообращения:
корректоры микроциркуляции крови и др.
При энцефалопатии схема лечения разрабатывается индивидуально для каждого пациента с учетом данных лабораторных и инструментальных исследований. Практически все препараты для лечения хронической формы заболевания отпускаются в аптеках по рецепту врача. Помимо перечисленных групп лекарств, пациенту могут быть назначены противосудорожные, антидепрессантные, антиагреганты и другие средства.
Последствия и осложнения энцефалопатии
Длительное откладывание лечения приводит к обширному повреждению головного мозга. По мере усугубления заболевания у пациента могут отмечаться:
постоянные головные боли;
ухудшение зрения и слуха;
расстройства координации движений;
тремор конечностей, тик, судороги;
расстройство половой функции;
вегетососудистая дистония и многое другое в зависимости от области поражения мозга.
Для успешного лечения, устранения симптоматики болезни и предотвращения дегенеративных процессов в головном мозге пациенту рекомендуется:
регулярно заниматься спортом для поддержания организма в тонусе.
При своевременном обращении к врачу и обнаружении энцефалопатии на ранних стадиях прогноз положительный. Эффективность лечения во многом будет зависеть от причин патологии. Тяжелые сердечно-сосудистые (ишемия, инсульт, инфаркт) и неврологические (остеохондроз, черепно-мозговые травмы) заболевания могут потребовать пожизненной курсовой терапии. В каждом случае программу лечения и профилактики должен составлять лечащий врач.