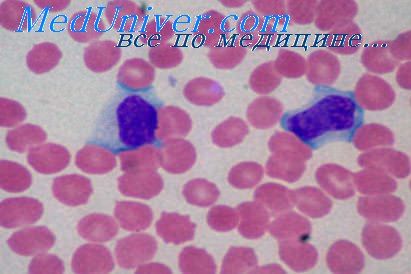
Мононуклеарная инфильтрация что это
Мононуклеарная инфильтрация что это
В селезенке и миндалинах обнаруживаются изменения, аналогичные происходящим в лимфатических узлах. Отек и инфильтрация мононуклеарами капсулы селезенки приводят иногда, особенно при давлении на нее извне, к разрыву.
В измененных миндалинах часто при присоединении вторичной инфекции развиваются некрозы эпителия с изъязвлениями и лейкоцитарными инфильтратами. Пролиферация моионуклеарных клеток обнаруживается также в перитонзиллярной ткани, в интерстиции, окружающем слюнные железы, в глоточном кольце, в стенке глотки.
Характерным морфологическим признаком изменений печени при инфекционном мононуклеозе является наличие значительных инфильтратов, состоящих из лимфоидных, плазматических и крупных мононуклеарных клеток, располагающихся перипортально и внутри долек при сохранности архитектоники печени. Клеточные инфильтраты, распространяясь в соседние печеночные дольки, нарушают непрерывность пограничной пластинки. Наблюдается пролиферация-звездчатых эндотелиоцитов.
Дистрофические изменения гепатоцитов выражены умеренно: мутное набухание, ацидофильная дистрофия, отложение желчного пигмента в цитоплазме гепатоцитов, расположенных вокруг центральной вены, изредка тромбы в желчных капиллярах. Исследования, проводившиеся в период реконвалесценции, показали полное морфологическое восстановление печени, но оно наступает нескольку позже, чем клиническое выздоровление. Описаны единичные наблюдения исхода в цирроз при инфекционном моноиуклеозе.
L. Pelletier и соавт. (1976) описали очень редкое осложнение при инфекционном мононуклеозе — распространенную внутрисосудистую коагуляцию крови и перипортальный некроз печени, явившиеся причиной смерти. Мононуклеарная инфильтрация наблюдается и в других внутренних органах.
Так, в легких диффузные моионуклеарные инфильтраты обнаруживаются в межальвеолярных перегородках, вокруг сосудов в перибронхиальной соединительной ткани, где отмечается гиперплазия лимфоидной ткани с образованием лимфом. В сердце — немногочисленные периваскулярные или субэндокардиальные скопления мононуклеарных клеток.
Описано несколько случаев миокардита и перикардита с инфильтрацией мононуклеарными клетками. Аналогичная инфильтрация обнаруживается в интерстиции почек, поджелудочной железы, в слизистой и подслизистой оболочках желудочно-кишечного тракта, в поперечнополосатой мускулатуре, коже, эндокринных железах. J. Fennel и G. Tomkin (1978) впервые описали наблюдение инфекционного мононуклеоза с гистологически подтвержденным подострым тиреоидитом (биопсия щитовидной железы).
Неврологические осложнения при инфекционном моноиуклеозе проявляются в виде менингоэнцефалита и полирадикулоневрита. При мснингоэнцефалите обнаруживаются стек, полнокровие, пролиферация лимфоидных клеток, гистиоцитов и мононуклеаров в мягких мозговых оболочках и периваскулярные инфильтраты из этих же клеток в ткани мозга, периваскулярные кровоизлияния и дистрофия ганглиозных клеток.
F. Hochberg и соавт. (1976) описали наблюдение подострого склерозирующего панэнцефалита у больной 13 лет, страдающей инфекционным мононуклеозом. Методом непрямой иммунофлюоресценции в коре мозга были выявлены антиген вируса кори и вируса Эпштейна — Барра. Последний впервые обнаружен в ткани мозга. При полирадикулоневрите морфологические изменения локализуются в спинальных нервных корешках и спинномозговых ганглиях, выражаются полнокровием и отеком мозговых оболочек, отеком и набуханием нервных корешков, распространенной мононуклеарной инфильтрацией, набуханием и разрывом миелиновых оболочек. В спинномозговых ганглиях отмечаются также вакуолизация и хроматолиз ганглиозных клеток, пролиферация сателлитов вокруг них, периваскулярные кровоизлияния.
Причинами смерти при инфекционном мононуклеозе бывают чаще всего разрывы селезенки и периферический паралич дыхания в результате полирадикулоневрита, протекающего с картиной прогрессирующих параличей.
Хронический эндометрит
Хронический эндометрит (ХЭ) – воспалительное заболевание слизистой оболочки матки (эндометрия).
Заболевание встречается преимущественно у женщин репродуктивного возраста (26-35 лет), ведет к нарушению менструальной и генеративной функции, служит причиной бесплодия, невынашивания беременности. У женщин с бесплодием частота встречаемости ХЭ составляет от 12 до 68%, а у пациенток с привычным невынашиванием беременности – более 70%. У больных с неудачной попыткой ЭКО и ПЭ хронический эндометрит встречается в 60% случаях.
ХЭ чаще всего развивается после аборта или родов, в результате осложнений внутриматочных манипуляций, таких как выскабливание полости матки, биопсия эндометрия, гистероскопия, гистеросальпингография, использование ВМС. Развитию ХЭ также предшествуют воспалительные заболевания органов малого таза, инфекции влагалища и шейки матки, деформация полости матки с нарушением отторжения эндометрия во время менструации, перенесенные ИППП (инфекции, передающиеся половым путем).
Чаще всего возбудителями ХЭ в современных условиях являются микст – инфекции (сочетание вирусно-бактериальной и условно-патогенной флоры). Особое место занимает герпетическое поражение эндометрия, которое чаще всего бывает у женщин, страдающих различным формами генитального герпеса.
Длительное присутствие инфекционных агентов в эндометрии приводит к выраженным изменениям его структуры и свойств, что вызывает нарушение нормальной имплантации эмбриона и формирования плаценты. Морфологические изменения структуры эндометрия сопровождаются выраженной воспалительной реакцией, в результате которой нарушается местная микроциркуляция.
Клинически ХЭ проявляется циклическими маточными кровотечениями, перименструальными кровянистыми выделениями, болевым синдромом, выделениями из половых путей (гноевидные и серозные бели), бесплодием и невынашиванием беременности. У 9-38% пациенток с ХЭ могут отсутствовать какие-либо симптомы, и заболевание протекает субклинически и бессимптомно.
Диагностика ХЭ
Обязательным этапом диагностики данного заболевания является морфологическое исследование материала, которое проводят в среднюю и позднюю фазу пролиферации эндометрия – на 7-10 день менструального цикла.
Морфологические критерии диагностики ХЭ:
Важным методом диагностики ХЭ является ультразвуковое исследование органов малого таза, которое должно предшествовать морфологическому методу.
Исследование проводят дважды: в первые 1-3 дня после менструации и за 2-3 дня до начала месячных.
Наиболее частые эхографические признаки хронического эндометрита это:
Гистероскопия является инвазивным и окончательным методом при установлении диагноза и состоит из визуализации полости матки и биопсии эндометрия с последующим микробиологическим и морфологическим исследованием ткани.
Наиболее характерные гистероскопические признаки ХЭ:
Лечение ХЭ
На первом этапе необходимо удалить повреждающий агент. С этой целью используют антимикробные и противовирусные лекарственные препараты, обеспечивающие элиминацию широкого спектра возможных патогенных микроорганизмов, включая хламидии, гонококки, трихомонады, грамотрицательные факультативные бактерии, анаэробы и стрептококк. Оправдано назначение нескольких курсов этиотропного лечения со сменой групп препаратов.
Одновременно проводится коррекция иммунных нарушений.
Второй этап лечения направлен на коррекцию метаболических нарушений и последствий ишемии, восстановление гемодинамики и активности рецепторного аппарата эндометрия. С этой целью применяются физические факторы (электроимпульсная терапия, переменное магнитное поле низкой частоты и т.д.). Физиотерапию проводят с 5-7-го дня менструального цикла ежедневно. С целью метаболической терапии используются метаболические препараты не менее 3-4 недель.
Контроль эффективности терапевтических мероприятий проводится через 2 месяца после окончания лечения путем применения аспирационной биопсии эндометрия.
Необходимо помнить, что хороший эндометрий – одно из главных условий успешного прикрепления плодного яйца.
Источники: «Бесплодный брак» под редакцией, В.И.Кулакова, «Хронический эндометрит», Г.Т.Сухих, А.В.Шуршалина, «Женское бесплодие», В.А.Кулавский, «Патология полости матки», В.Н.Демидов, А.И.Гус.
Что такое мононуклеоз инфекционный? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 13 лет.
Определение болезни. Причины заболевания
Инфекционный мононуклеоз (болезнь Филатова, железистая лихорадка, «поцелуйная болезнь», болезнь Пфейфера) — острое инфекционное заболевание, которое вызывается вирусом Эпштейна — Барр (ВЭБ).
Какой урон вирус наносит организму
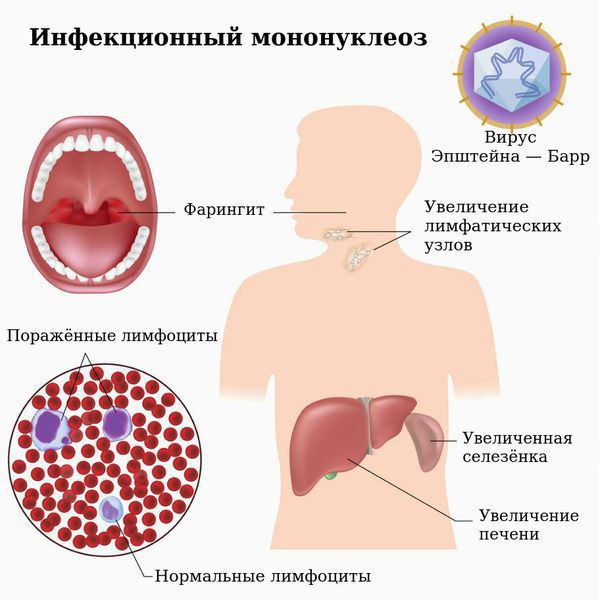
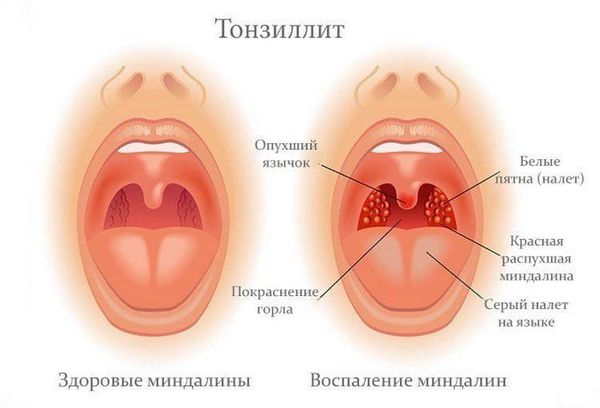
Заболевание характеризуется лихорадкой, поражением лимфатических узлов, тонзиллитом, увеличением печени и селезёнки и выраженным изменением состава крови. Вирус поражает циркулирующие в крови В-лимфоциты и тем самым нарушает клеточный и гуморальный иммунитет.
Этиология
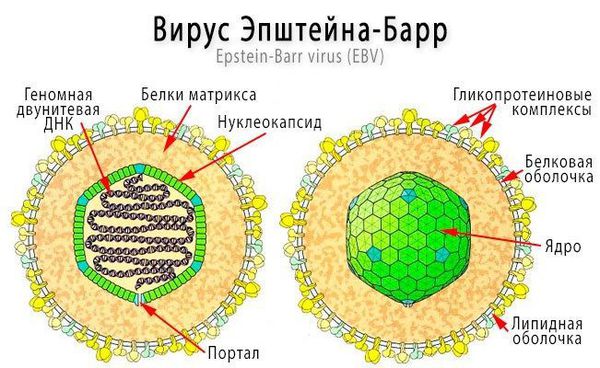
Заболевание впервые описано в 1884 году отечественным педиатром Н. Ф. Филатовым и в 1889 году Р. Ф. Пфейфером. В 1964 году Майкл Энтони Эпштейн и Ивонна Барр выделили возбудителя болезни, который был назван в их честь.
Эпидемиология
Источник инфекции — больной человек с манифестными и стёртыми формами заболевания, но преимущественно — вирусоносители, не имеющие никаких явных признаков заболевания (как клинически, так и лабораторно).
После первичного инфицирования вирус может выделяться в течение 18 месяцев, преимущественно со слюной. Далее возможность выделения значительно снижается и зависит от конкретных условий, в которых происходит жизнедеятельность больного (заболевания, травмы, приём препаратов, снижающих иммунитет).
Максимальная частота инфицирования приходится на возраст 10-18 лет. Чем раньше происходит заражение (за исключением раннего детского возраста), тем менее выраженными будут клинические проявления заболевания. Повышение заболеваемости происходит в зимне-весенний период. Это связано как со снижением общей резистентности организма и сплоченностью коллективов, так и в значительной степени с изменением гормонального фона и повышением романтического влечения молодых людей.
Симптомы инфекционного мононуклеоза
Инкубационный период от 4 до 15 дней, по некоторым данным — до 1 месяца.
При инфицировании в раннем детском возрасте течение заболевания обычно асимптомное или малосимптомное и чаще проходит под маской лёгкого ОРЗ.
Симптомы инфекционного мононуклеоза у взрослых
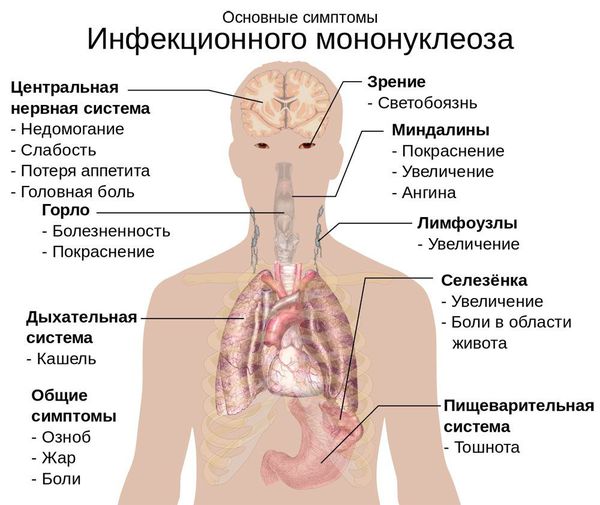
Начало заболевания постепенное, основной синдром появляется позже трёх суток от начала клинических проявлений. Постепенно появляется и нарастает лихорадка с повышением температуры тела до 38-39 ℃. Лихорадка продолжается до трёх недель и более, при этом больной испытывает слабость, отсутствие аппетита. Миалгии (мышечные боли) не характерны.
Симметрично увеличиваются лимфоузлы разных групп, преимущественно заднешейные, переднешейные, затылочные, у некоторых больных также вовлекаются подмышечные, локтевые, паховые, внутрибрюшные группы (мезаденит). Характерной особенностью является их малоболезненность, мягкоэластичность, отсутствие изменений покровной ткани. Увеличение размеров сохраняется до 1 месяца и более и зачастую приводит к значительным дифференциально-диагностическим трудностям. После определённого начального периода в типичных случаях развивается острый тонзиллит (лакунарный, язвенно-некротический) с обильным белым или грязно-серым творожистым налётом, который легко крошится, снимается шпателем и растирается на стекле. К симптомам инфекционного мононуклеоза относятся б оли в горле, которые носят умеренный характер.
В некоторых случаях развивается периорбитальный отёк, проявляющийся двусторонним преходящим отёком век. Практически всегда происходит увеличение селезёнки, которая характеризуется гладкостью, эластичностью, и чувствительностью при пальпации. Достигая иногда больших размеров, селезёнка может разорваться. Нормализация её величины происходит не ранее четырёх недель от начала болезни, может затягиваться на несколько месяцев.
При неверном истолковании симптоматики и применении антибиотиков аминопенициллинового ряда в 70-80 % случаев появляется сыпь (может быть пятнистая, пятнисто-папулёзная, ярко-красная, с тенденцией к слиянию, различной локализации, без явной этапности появления).
При адекватном иммунном ответе течение заболевания обычно доброкачественное и заканчивается формированием вирусоносительства при полном отсутствии симптоматики и лабораторных изменений.
Какие «неправильные» варианты течения болезни возможны у взрослых
В редких случаях болезнь может развиваться по типу «хронического мононуклеоза» (с периодами обострений и ремиссий). Это возможно при врождённых или приобретённых нарушениях в иммунной системе, иммунодепрессивных заболеваниях или приёме цитостатических ( противоопухолевых) препаратов.
Чем опасна хроническая форма инфекционного мононуклеоза
В клинической картине хронического мононуклеоза фигурируют практически все синдромы острого процесса, но они проявляются не так выраженно: тонзиллит, как правило, отсутствует, и на первый план выходит абстинентный синдром. Данное состояние не является самостоятельным заболеванием, это следствие имеющегося основного иммунопатологического процесса, поэтому его следует рассматривать не как мононуклеоз, а как хроническую активную Эпштейна — Барр вирусную инфекцию. Следовательно, к обследованию и лечению необходимо подходить с учётом этой позиции.
Патогенез инфекционного мононуклеоза
Входные ворота инфекции — слизистая оболочка ротоглотки и верхних дыхательных путей.
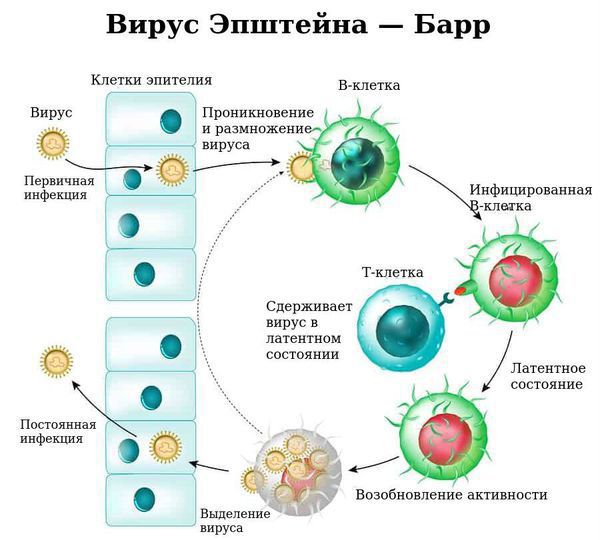
Размножаясь в клетках эпителия, вирус вызывает их разрушение, далее происходит выброс в кровь новых вирионов (вирусных частиц) ВЭБ и медиаторов воспаления, что обуславливает вирусемию (попадание вируса в кровоток) и генерализацию инфекции. В том числе происходит накопление вируса в лимфоидной ткани ротоглотки и слюнных железах, а также развитие интоксикационного синдрома.
Патофизиология: как реагирует иммунитет на инфекционный мононуклеоз
Ввиду тропности ВЭБ к рецепторам B-лимфоцитов (СД-21), вирус внедряется в них и начинает размножаться, стимулируя пролиферацию (разрастание) B-лимфоцитов. В результате развиваются нарушения клеточного и гуморального иммунитета, что ведёт к выраженному иммунодефициту. Следствием этого может стать наслоение бактериальной флоры (гнойный тонзиллит).
С течением времени активируются Т-лимфоциты (СД-8), обладающие супрессорной и цитотоксической активностью, появляются атипичные мононуклеары, что приводит к угнетению вируса и переходу заболевания в фазу неактивного носительства. ВЭБ обладает рядом свойств, позволяющих ему в определённой мере ускользать от иммунного ответа, что особенно ярко проявляется при хронической активной инфекции.
Как вирус, вызывающий инфекционный мононуклеоз, проникает в клетки:
Классификация и стадии развития инфекционного мононуклеоза
По клинической форме:
По течению:
По степени тяжести:
Осложнения инфекционного мононуклеоза
Специфические:
Неспецифические:
Диагностика инфекционного мононуклеоза
Лабораторные методы
Общеклинический анализ мочи. Изменения малоинформативны, указывают на степень интоксикации.
Серологические реакции. Наибольшее значение в современной практике имеют методы выявления антител различных классов к антигенам ВЭБ методом ИФА ( иммуноферментного анализа) и нуклеиновых кислот самого возбудителя в полимеразной цепной реакции (ПЦР). Особо стоит отметить, что обнаружение антител класса G к ядерным, капсидным и ранним протеинам вируса при отсутствии антител класса М (и тем более характерных клинических и общелабораторных признаков ВЭБ-инфекции) не является причиной для постановки диагноза активной (персистирующей) ВЭБ-инфекции и назначения дорогостоящего лечения.
Инструментальные методы
Дифференциальная диагностика
Лечение инфекционного мононуклеоза
Место лечения и лечебно-охранительный режим зависят от степени тяжести процесса и наличия или отсутствия осложнений. Больные с лёгкими формами заболевания вполне могут проходить лечение дома, средней тяжести и более тяжёлые — в инфекционном стационаре, по крайней мере, до нормализации процесса и появления тенденций к выздоровлению.
Показано обильное питьё до 3 л/сут. (тёплая кипячёная вода, чай), назначение стола № 15 (общий стол) при лёгких формах, в некоторых случаях — стол № 2 по Певзнеру (жидкая и полужидкая молочно-растительная пища, не содержащая экстрактивных веществ, богатая витаминами, мясные нежирные бульоны и т. п.). Рекомендовано ограничение физической активности (при тяжёлых формах — строгий постельный режим).
Лечение инфекционного мононуклеоза у взрослых
Достаточно дискутабельным является вопрос о специфическом воздействии на ВЭБ при остром заболевании. Этиотропная терапия показана лишь больным средней степени тяжести (с тенденцией к затяжному течению и осложнениям) и выраженной формой заболевания. Возможности такой терапии достаточно ограничены: отсутствует высокоэффективное средство прямого противовирусного действия (применяются препараты на основе ацикловира и производных, оказывающих лишь частичное влияние на ВЭБ), нередко развивается герпесвирусный гепатит. Поэтому их назначение должно быть взвешено и обосновано в каждом конкретном случае.
Применение иммуномодуляторов в разгар заболевания следует считать нецелесообразным, т. к. их действие является неспецифичным, малопрогнозируемым и при развитии иммунопатологического гиперпролиферативного процесса при ВЭБ-инфекции может привести к непредсказуемым последствиям. В фазе выздоровления их приём, напротив, может ускорить процесс возвращения иммунного гомеостаза в нормальное русло.
При развитии бактериальных осложнений (тонзиллит) показан приём антибиотиков (исключая аминопенициллиновый ряд, сульфаниламиды и левомицетин, т. к. они угнетают кроветворение и могут вызвать развитие высыпаний). В некоторых случаях их назначение может быть оправдано при выявлении резчайшего иммунодефицита (абсолютная нейтропения) даже при отсутствии явного гнойного процесса.
Патогенетическая терапия включает все основные звенья общего патопроцесса: снижение повышенной температуры тела, поливитамины, гепатопротекторы по показаниям, дезинтоксикация и т. п.
Лечение инфекционного мононуклеоза у детей
Дети переносят заболевание легче взрослых, поэтому им, как правило, показано лишь симптоматическое лечение.
Прогноз. Профилактика
За переболевшими инфекционным мононуклеозом устанавливается медицинское наблюдение сроком 6 месяцев (в случаях тяжёлого течения — до 1 года). В первый месяц каждые 10 дней показан осмотр инфекциониста, сдача клинического анализа крови с лейкоцитарной формулой, АЛТ. Далее при нормализации показателей рекомендован осмотр раз в 3 месяца до окончания срока наблюдения, включая анализы крови, двукратное тестирование на ВИЧ и УЗИ органов брюшной полости в конце периода наблюдения.
Специфической профилактики не существует, ведутся эксперименты с вакциной.
Почему развиваются рецидивы инфекционного мононуклеоза
Инфекционный мононуклеоз редко развивается повторно, это может происходить при активации спящей инфекции. В таких случаях, как правило, симптомы болезни отсутствуют и заболевание выявляется только при лабораторном исследовании. Однако у людей со СПИДом или другими иммунодефицитными состояниями отмечаются характерные симптомы: слабость, боли в горле и увеличение лимфатических узлов. Течение болезни в таком случае более длительное, чем при первичной инфекции.
Мононуклеарная инфильтрация что это
Опухолевые клетки отличаются от нормальных нарушениями прочной сопряженности между процессами роста и дифференцировки [9]. Увеличение темпа воспроизводства озлокачествленных клеток обеспечивается не столько через укорочение митотического цикла, сколько за счет возрастания количества тех элементов, которые вместо достижения терминальной степени дифференцировки остаются во фракции роста [6, 11, 13]. В качестве еще одного механизма немалую роль играет «карикатурная» сигнальная связь, то есть нарушенная интеграция между малигнизированными клетками, проходящими через этапы дифференцировки, и микроокружением [2, 4]. Достигнут значительный прогресс в области изучения морфофункциональных особенностей слизистой оболочки желудка при предраке и раке, отчасти связанный с развитием высокочувствительных способов выявления в гистологических срезах отдельных тканевых и клеточных компонентов [1, 3]. Однако многие аспекты структурно-метаболической перестройки слизистой оболочки желудка при ее малигнизации остаются предметом дискуссий, и поиск изменений, предшествующих возникновению опухоли, по-прежнему актуален [5, 10].
Материал и методы исследования
Срезы окрашивали гематоксилином и эозином в комбинации с реакцией Перлса, по ван Гизону с окраской эластических волокон резорцин-фуксином Вейгерта, ставили ШИК-реакцию. Полутонкие срезы окрашивали реактивом Шиффа и азуром II. Исследования проводили в универсальном микроскопе Leica DM 4000B (Германия). Ультратонкие срезы, контрастированные уранилацетатом и цитратом свинца, исследовали в электронном микроскопе JEM 1010 при ускоряющем напряжении 80 кВт.
Результаты исследования и их обсуждение
Светооптическое исследование первичных опухолей пациентов 1-й группы выявило превалирование зрелых форм аденокарцином, характеризующихся формированием папиллярных и тубулярных железистых структур, умеренно выраженной тканевой и клеточной атипией, появлением патологических митозов, в разной степени выраженными фиброзными изменениями стромы. В низкодифференцированной аденокарциноме среди обширных скоплений опухолевых клеток или фиброзных полей с трудом обнаруживались мелкие железы, степень анаплазии опухолевых клеток возрастала. Перстневидно-клеточный рак отличался диффузным распределением клеток типичной перстневидной формы и, как правило, отсутствием десмопластической реакции стромы.
Особый интерес представляло изучение состояния слизистой оболочки желудка в отдаленных от опухоли участках. При кишечном типе рака светооптическое исследование фрагментов пилорического отдела желудка во всех наблюдениях выявило наличие распространенной неполной кишечной метаплазии. Обращала на себя внимание атрофия слизистой оболочки, иногда выраженная, с заметным истончением собственной пластинки, дистрофическими изменениями покровно-ямочного эпителия и уменьшением количества желез [7]. Диспластические изменения эпителия от слабой до тяжелой степени (увеличение ядерно-цитоплазматического соотношения, снижение секреции мукоида, псевдомногорядность, повышение митотической активности) обнаружены в большинстве исследованных фрагментов. Характерна многофокусность диспластических изменений, нарастающих по направлению к опухолевому очагу.
В фундальном отделе желудка очаговая кишечная метаплазия эпителиоцитов отмечена у 25% пациентов. Диспластические изменения энтеролизованного и интактного эпителия выявлены в половине наблюдений. Мононуклеарная инфильтрация отличалась слабой интенсивностью и поверхностной локализацией. В целом, патологические изменения в фундальном отделе желудка носили менее выраженный характер по сравнению с пилорическим отделом.
При изучении регионарных лимфатических узлов обращали внимание на наличие, размер и множественность метастазов. У пациентов с аденокарциномами метастазы в лимфатических узлах обнаружили у 37% больных.
Таким образом, светооптическое исследование первичных опухолей желудка пациентов 1-й группы выявило преобладание зрелых форм аденокарцином, характеризующихся формированием капиллярных и тубулярных железистых структур, умеренно выраженной тканевой и клеточной атипией. В большинстве случаев зрелых аденокарцином опухолевый очаг хорошо отграничен от окружающих тканей стенки желудка. Перстневидно-клеточный рак отличался диффузным распределением изолированных округлой формы клеток, содержащих в цитоплазме большое количество слизи. Опухоль характеризовалась инфильтративным ростом и была плохо отграничена от окружающих тканей [8, 12].
Новообразования у пациентов 2-й группы состояли из полиморфных либо мономорфных по составу анапластических клеток, располагающихся в виде тяжей, комплексов, или изолированно друг от друга. Клеточные ядра различались по основным светооптическим характеристикам: форме, размерам, окраске. Наиболее часто в клетках недифференцированного рака желудка встречались крупные гиперхромные угловатой формы ядра, а также небольшие светлые пузырьковые ядра. Цитоплазма была, как правило, скудная и плохо различима. Анализ частоты и выраженности патологических изменений нетрансформированной слизистой оболочки обнаружил их сходство с перифокальными процессами при диффузном типе карцином в первой группе наблюдений, что свидетельствует об определенном гистогенетическом единстве этих вариантов рака желудка. Ведущим патологическим изменением являлась дисплазия генеративных зон желудочного эпителия на фоне атрофически-склеротических процессов. Метастазы в регионарных лимфатических узлах обнаружены у 38% пациентов, что соответствует аналогичному показателю в первой группе.
Таким образом, светооптическое исследование опухолей желудка пациентов 2-й группы выявило наличие недифференцированного рака с солидным или скиррозным характером роста. Опухолевый очаг был плохо отграничен от окружающих тканей стенки желудка, отличался инфильтративным ростом и латеральным распространением опухоли по подслизистому слою.
Смешанные формы (3-я группа) сочетали в одном опухолевом очаге участки аденокарцином с различной степенью дифференцировки (часто с перстневидными клетками) либо разные патогистологические варианты рака желудка. Морфологическая картина отражала направление «дедифференцировки» клеточных популяций от центра к периферии опухоли. Практически во всех исследованных случаях карцинома распространялась в глубь желудочной стенки, инвазируя подслизистый, мышечный, иногда серозный слои, в ряде наблюдений комплексы раковых клеток выявлялись в большом сальнике или брыжейке поперечной ободочной кишки.
В слизистой оболочке вне опухолевого очага у 60% пациентов имелась кишечная метаплазия, ограниченная пилорическим отделом желудка; с такой же частотой встречались атрофия, склероз и густая полиморфно-клеточная инфильтрация. Наличие метастазов в регионарных лимфатических узлах выявлено у 60% оперированных больных этой группы, что значительно превышало данные первых двух анализируемых групп.
Таким образом, светооптический анализ перифокальных процессов в слизистой оболочке при различных патогистологических формах рака желудка показал, что при высоко- и умереннодифференцированных аденокарциномах наиболее типичными изменениями являются распространенная неполная кишечная метаплазия и ассоциированная с этими участками дисплазия на фоне диффузной атрофии эпителия. При низкодифференцированной и перстневидно-клеточной аденокарциномах, а также при недифференцированном раке желудка на первый план выходят атрофические изменения слизистой оболочки и дисплазия генеративных зон эпителия [14].
Электронно-микроскопический анализ аденокарциномы желудка выявил множественные патологические изменения ультраструктуры малигнизированных клеток: большие, неправильной формы ядра с изрезанными контурами и неравномерным распределением крупноглыбчатого гетерохроматина в кариоплазме, увеличенным количеством ядрышек, иногда атипичными митозами.
При перстневидно-клеточном раке желудка преобладали опухолевые клетки с переполненной секреторными гранулами цитоплазмой и эксцентрически расположенным ядром аномальной формы. Слизистая оболочка желудка вне опухолевого очага отличалась мозаичностью ультраструктурной картины. В очагах кишечной метаплазии, кроме типичных покровно-ямочных эпителиоцитов, обнаружены также каемчатые и бокаловидные клетки, цитоплазма которых была переполнена крупными электронно-прозрачными глобулами слизи, а уплощенные ядра оттеснены к базальному полюсу клеток. На апикальной поверхности каемчатых эпителиоцитов выявлялись высокие, нерегулярно расположенные микроворсинки. В цитоплазматическом матриксе большое число митохондрий и развитая гранулярная цитоплазматическая сеть. Отражением атрофических процессов в слизистой оболочке желудка было наличие большого числа эпителиоцитов, почти лишенных микроворсинок, имеющих электронно-плотную цитоплазму с едва различимыми органеллами. В дистрофически измененных клетках покровно-ямочного эпителия наблюдалось уменьшение количества секреторных мукоидных гранул, среди которых преобладали незрелые, с плотным содержимым и неровными контурами. Диспластические изменения эпителиоцитов выражались в увеличении размеров ядер, появлении крупных ядрышек, значительном снижении содержания внутриклеточного муцина.
При недифференцированном раке желудка преобладали атипичные клетки с гладкими, лишенными микроворсинок контурами. Клеточные ядра отличались большими размерами, с глубокими инвагинациями в нуклеолемме, придающими ядру причудливую двухлопастную или трехлопастную форму. Изучение желудка при недифференцированном раке на отдалении от первичной опухоли показало высокую степень развития атрофически-склеротических процессов слизистой оболочки и наличие диспластических изменений эпителия, ассоциированных с генеративными зонами (желудочные ямки, верхние отделы шеек желез). Неполная кишечная метаплазия носила очаговый характер и была ограничена, как правило, пилорическим отделом желудка. Анализ частоты и выраженности патологических изменений нетрансформированной слизистой оболочки при недифференцированном раке выявил их сходство с перифокальными процессами при диффузном типе карцином в первой группе наблюдений, что свидетельствует об определенном гистогенетическом единстве этих вариантов рака желудка.
Ультраструктурный анализ карцином желудка со смешанным типом строения подтвердил полиморфизм тканей и клеточную атипию, обнаруженные при светооптическом исследовании. В участках опухоли обнаружили злокачественные клетки с признаками секреции слизи в виде различных по размеру гранул, содержащих муцин. При снижении уровня дифференцировки по направлению к периферии опухоли наблюдалось прогрессирующее изменение ядерно-цитоплазматического соотношения в сторону увеличения размеров ядер. В слизистой оболочке желудка на отдалении от опухолевого очага в ряде случаев отсутствовали патологические изменения покровно-ямочного эпителия. По мере приближения к опухолевому очагу нарастала выраженность и гетерогенность изменений эпителиальных структур слизистой оболочки желудка. Анализ перифокальных процессов в окружающей слизистой оболочке желудка выявил меньшую распространенность и частоту предраковых изменений (дисплазии, неполные кишечные метаплазии и атрофии эпителия), чем в других исследованных группах пациентов. В целом, это свидетельствует о более высоких темпах опухолевой прогрессии смешанных форм карцином желудка.
Проведен комплексный морфологический анализ, включающий световую и электронную микроскопию опухолевых очагов, нетрансформированной слизистой оболочки, и регионарных лимфатических узлов при раке желудка. По результатам микроскопического исследования слизистой оболочки желудка на отдалении от опухолевого очага у пациентов с высоко- и умереннодифференцированными карциномами желудка установлено, что наиболее типичными изменениями являются распространенная неполная кишечная метаплазия и ассоциированная с этими участками дисплазия. В прилежащих к опухоли участках слизистой оболочки нередко обнаруживалась неравномерная гиперплазия эпителия. При низкодифференцированной и перстневидно-клеточной карциномах, а также при недифференцированном раке желудка на первый план выходит дисплазия генеративных зон эпителия; неполная кишечная метаплазия носит очаговый характер.