На рентгене легких усилен легочный рисунок что это значит
На рентгене легких усилен легочный рисунок что это значит
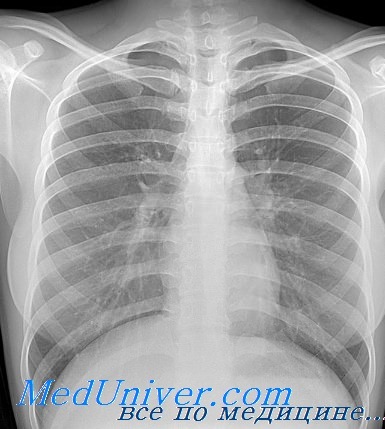
При исследовании в прямой передней проекции выявляются два светлых легочных поля (легкие), между которыми располагается интенсивная срединная тень, образованная суммарными тенями сердца, крупных сосудов, позвоночника и грудины.
Внизу легочные поля ограничены куполами диафрагмы. Правый купол диафрагмы находится несколько выше левого. С грудной стенкой диафрагма образует реберно-диафрагмальные, а с тенью сердца— сердечно-диафрагмальные синусы.
На фоне светлых легочных полей отчетливо выделяются тени ребер. Как передние, так и задние отделы ребер располагаются параллельно. Передние отделы ребер имеют направление сверху вниз и к грудине, а задние отделы ребер идут от позвоночника книзу и кнаружи. Задние отделы ребер идут от позвоночника книзу и кнаружи. Задние отделы более рельефно, чем передние, выступают на фоне воздушных легких ввиду большей плотности костной ткани в этих частях ребер.
При определении границ тенеобразования в области грудной клетки принято вести счет по передним отделам ребер.
Верхнюю часть легочных полей пересекают интенсивные тени ключиц. Ниже в латеральных отделах легочных полей проецируются тени лопаток.
Легочный рисунок. В средней части легочных полей по обеим сторонам срединной тени видны довольно интенсивные затенения в виде запятых или бабочки. Это тени корня легкого (тени хилюсов). От корней легких во все стороны — вверх, вниз и кнаружи отходят однородные древовидно ветвящиеся теневые полоски, постепенно суживающиеся к периферии и оканчивающиеся У-образной формы разветвлениями. Вся совокупность указанных теневых изображений называется легочным рисунком. Особой интенсивности и густоты легочный рисунок достигает в области корней в виде массивных, веерообразно расходящихся тенеобразований. Местами элементы легочного рисунка выявляются в виде множественной переплетающейся сетчатой структуры, которая более рельефно выявляется на технически хорошо сделанных рентгенограммах. Рентгенологическими элементами легочного рисунка являются тенеобразования в виде полосок, кружков, овалов и иногда в виде мелких просветлений с кольцевидным ободком.
Анатомической основой легочного рисунка являются разветвления легочной артерии, в меньшей степени легочных вен, а в патологических условиях также разветвления бронхов и окружающих их перибронхиальных лимфатических сосудов и изменения межуточной ткани различного происхождения.
На рентгенограммах без патологии разветвления сосудов легочного рисунка не доходят до наружных краев легочных полей 1—2 см.
Полосковидные линейные тени легочного рисунка являются отображением сосудов, расположенных длинником перпендикулярно к ходу рентгеновых лучей, круглые тени — сосуды, попавшие ортоградно, а овальные — это тени от сосудов, расположенных косо к ходу рентгеновых лучей.
Мелкие одиночные просветления с кольцевидным ободком как элемент легочного рисунка есть тень от бронха в ортоградной проекции.
Топографоанатомическая схема взаимоотношений бронхов, артерий и вен представляется в следующей последовательности: расположение артерии, бронха, вены — слева — по ходу часовой стрелки, справа — против хода.
При анализе легочного рисунка необходимо дифференцировать артериальные сосуды от венозных. Бронхиальное дерево, как компонент легочного рисунка, в обычных условиях выявляется редко, за исключением изображений поперечных, реже продольных сечений долевых и сегментарных бронхов, которые располагаются рядом с изображением крупных сосудистых стволов и выглядят как ровные четкие кольцевидные тени.
Лимфатические сосуды располагаются вокруг артерий, бронхов, междолевых и межацинозных перегородок.
Медицинские интернет-конференции
Языки
Первичная легочная гипертензия (клинический случай)
Таинкин А.А., Ирлык К. И., Круглова М. П., Бецуков И. О., Лобачёва Д. Н., Мартынова И. Р., Капьёва А. А.
Резюме
В статье представлен клинический случай первичной легочной гипертензии у молодого мужчины.
Ключевые слова
Статья
Проблема легочной гипертензии в настоящее время стала очень популярной. Если гипертоническая болезнь сейчас относительно хорошо контролируется, в ведении больных с легочной гипертензией существуют проблемы. Среди пациентов с данным заболеванием есть когорта больных с первичной легочной гипертензией. Этиология ее не известна. Актуальность проблемы высока в связи с малой продолжительностью жизни пациентов при отсутствии своевременно назначенной специфической терапии. Цель нашей работы – на примере клинического случая рассказать о принципах и сложностях ведения больных с первичной легочной гипертензией.
Клинический случай
Больной А., 39 лет поступил в кардиологическое отделение 25.02.2019 с жалобами: на одышку с затрудненным вдохом, головокружение, слабость при подъеме на один лестничный пролет, головные боли при повышении артериального давления, периодически перебои в работе сердца, учащенное сердцебиение.
С 2012 г. повышается артериальное давление максимально до 160 и 90 мм рт ст. Обращался в поликлинику по месту жительства, принимал антигипертензивные препараты. С 2014 г. беспокоит одышка при привычных физических нагрузках, проходил обследование в кардиологическом отделении и был направлен в кардиохирургический стационар с подозрением на врожденный порок сердца, куда обратился в 2017 г. в связи с усилением ордышки. Выполнено зондирование полостей сердца (25.09.2017): давление в легочной артерии 81 и 50 мм рт ст (среднее 61 мм рт ст), в правом желудочке 76 и 24 мм рт ст (44 мм рт ст), в правом предсердии 21 и 15 мм рт ст (среднее 18 мм рт ст). При мультиспиральной компьютерной томографии сердца 22.09.2017 (рис. 1) КТ-признаки изолированной артериальной легочной гипертензии. Расширение правых отделов сердца, гипертрофия миокарда правого предсердия и правого желудочка, расширение ствола и крупных ветвей легочной артерии. Данных за врожденный порок сердца не получено. Выписан с диагнозом «первичная легочная гипертензия. Рекомендовано наблюдение кардиолога по месту жительства, прием лекарственных препаратов: тромбо Асс 100 мг в сутки, периндоприл 2,5 мг 1 раз в сутки, беталок зок 50 мг 1 раз в сутки, амлодипин 5 мг 1 раз в сутки, торасемид 10 мг 1 раз в сутки. Был запланирован контроль допплерэхокардиографии через 3 месяца с последующей консультацией главного внештатного кардиолога. На фоне приема данных препаратов отмечал улучшение самочувствия, наблюдался в поликлинике по месту жительства. С ноября 2018 г. признан инвалидом 2 группы. Ухудшение состояния около двух месяцев, когда снизилась толерантность к физической нагрузке, появилась одышка при подъеме на один лестничный пролет, головокружение, слабость при выполнении физических нагрузок на работе. Госпитализирован для обследования, подбора специфической терапии легочной артериальной гипертензии.
Из анамнеза жизни известно, что пациент в течение 6 лет служил в армии: обслуживал самолеты. Работал на заводе по производству стеклопластика. В настоящее время работает слесарем: ремонтирует автомобили. Курит.
При осмотре отеков не было. При пальпации определялся сердечный толчок, эпигастральная пульсация, усиливающаяся на вдохе. При перкуссии левая граница относительной сердечной тупости располагалась по левой среднеключичной линии. При аускультации тоны сердца были ритмичными, частота сердечных сокращений составляла 60 в минуту, на верхушке сердца первый тон был ослаблен. Над легочной артерией определялся акцент второго тона. При аускультации легких выслушивалось везикулярное дыхание. Частота дыхательных движений составляла 20 в минуту. Живот при пальпации был мягким, безболезненным. Печень имела нормальные размеры.
В общем анализе крови обращал на себя внимание эритроцитоз 6,19 млн в 1 мкл, повышение уровня гемоглобина до 187 г/л.
При электрокардиографии 25.02.2019 (рис. 2) регистрировалось отклонение электрической оси сердца вправо, неполная блокада правой ножки пучка Гиса, признаки гипертрофии правого предсердия и правого желудочка.
При холтеровском мониторировании ЭКГ 27.02.2019 в течение всего периода мониторинга ритм синусовый, средняя частота сердечных сокращений составила 80 в минуту. За сутки было зарегистрировано 35 одиночных желудочковых экстрасистол и 3 одиночных наджелудочковых экстрасистолы. Сердечный ритм пациента включал 11 минут 45 секунд синусовой тахикардии с максимальной частотой сердечных сокращений 120 в минуту.
При рентгенографии органов грудной клетки 26.02.2019 (рис. 3) выявлялись признаки артериальной легочной гипертензии, признаки увеличения правых камер сердца, расширения легочной артерии.
Легочные поля были прозрачными. Отмечалось усиление легочного рисунка за счет сосудистого компонента в прикорневых отделах. Корни легких были структурны, расширены: нисходящая ветвь правой легочной артерии 28 мм (норма менее 16 мм), левая легочная артерия 34 мм (норма менее 24 мм). На тени сердца в прямой проекции выявлялось увеличение второй и четвертой дуги по левому контуру. Аорта была уплотнена. В первой (правой косой) проекции по переднему контуру выявлялось увеличение пульмонального конуса и дуги левого желудочка. Во второй (левой косой) проекции отмечалось незначительное увеличение дуг правого предсердия и дуги правого желудочка.
Пациенту был выставлен диагноз:
Первичная легочная гипертензия. Артериальная гипертензия 3 стадии риск 4.
Осложнение: Хроническая сердечная недостаточность 2 А стадии, функциональный класс 3.
Помимо аспирина (ацекардол 100 мг в 20:00), ингибиторов АПФ (престариум 2,5 мг в 8:00), бета-блокаторов (бисопролол 5 мг в 8:00), антагонистов кальция (лотонел 10 мг в 8:00), антагонистов минералокортикоидных рецепторов (верошпирон 100 мг в 14:00) к лечению были добавлены препараты для специфической терапии легочной артериальной гипертензии: силденафил кардио по 20 мг 2 раза в день и бозенекс 125 мг по ½ таблетки 2 раза в день с последующим увеличением дозировки до 125 мг 2 раза в сутки.
25% спорадических случаев первичной лёгочной гипертензии ассоциируется с мутацией гена BMPR2, обусловливающей нарушениеангиогенеза, сосудистой дифференциации, органогенеза легких и почек [1].
В патогенезе заболевания важное значение имеет эндотелиальная дисфункция. Она проявляется снижением образования оксида азота и простациклина – веществ, обладающих антипролиферативным и вазодилатирующим действием, и увеличением продукции тромбоксана А2 и эндотелина 1, обладающих вазоконстрикторным и пролиферативным действием [3]. Значительную роль играет редукция легочного сосудистого русла, снижение эластичности, облитерация легочных сосудов вследствие пролиферации гладкомышечных клеток, тромбоза in situ [1]: генетические изменения обусловливают усиление тенденции к тромбообразованию [2]. Все это приводит к повышению легочного сосудистого сопротивления, и, следовательно, увеличению нагрузки на правый желудочек [1], его гипертрофии, дилатации, развитию правожелудочковой сердечной недостаточности.
Симптомы первичной легочной гипертензии неспецифичны [2, 4]. Нашего пациента больше всего беспокоила инспираторная одышка при физической нагрузке. По данным литературы в начале заболевания эта жалоба является наиболее частой [1, 4]. Реже встречаются обмороки; давящие, ноющие, колющие боли в грудной клетке, длящиеся от нескольких минут до суток, усиливающиеся при физической нагрузке, не купирующиеся приемом нитратов [4]; перебои в работе сердца; кашель; кровохарканье [1].
При объективном исследовании больных обычно выявляют сердечный толчок, эпигастральную пульсацию, обусловленные гипертрофией или дилатацией правого желудочка, акцент второго тона над легочной артерией. Может выслушиваться систолический шум у основания мечевидного отростка грудины, обусловленный недостаточностью трехстворчатого клапана, диастолический шум над легочной артерией, связанный с регургитацией через клапан легочной артерии [1, 2]. При развитии правожелудочковой сердечной недостаточности появляются отеки, акроцианоз, набухание яремных вен, асцит [1, 2]. У больного А признаков правожелудочковой недостаточности не было, что свидетельствует о недавнем начале заболевания и своевременном назначении лечения.
Эритроцитоз и увеличение уровня гемоглобина, имевшие место у нашего пациента, объясняются компенсаторной реакцией на гипоксемию [1].
Для исключения других форм легочной гипертензии в план обследования помимо общего, биохимического анализов крови включают определение уровня гормонов щитовидной железы, серологические исследования для исключения системных заболеваний соедтинительной ткани, ВИЧ-инфекции, гепатита [5].
Перечень необходимых инструментальных методов исследования включает в себя ЭКГ, рентгенографию органов грудной клетки, эхокардиографию, катетеризацию правых камер сердца, которая выполняется для подтверждения диагноза, оценки тяжести гемодинамических изменений и проведения теста на вазореактивность сосудов легких [5].
При установлении диагноза первичной легочной гипертензии необходимо немедленное назначение специфической медикаментозной терапии. Для лечения легочной гипертензии применяются: антагонисты рецепторов эндотелина (амбризентан, бозентан); аналоги простациклина (илопрост, эпопростенол), агонисты его рецепторов (селексипаг); оксид азота, ингибиторы фосфодиэстеразы 5-го типа (силденафил), стимуляторы гуанилатциклазы (риоцигуат). Антагонисты кальция эффективны при положительном остром тесте на вазореактивность [5].
При тяжелой легочной гипертензии, неэффективности медикаментозной терапии выполняется балонная предсердная септостомия, билатеральная трансплантация легких или трансплантация комплекса сердце-легкие.
Прогноз у больных с первичной легочной гипертензией неблагоприятный. Выживаемость без специфической медикаментозной терапии в течение 1 года составляет 68%, 3 лет – 48%, 5 лет – 34% [4], а на фоне лечения выживаемость существенно выше: 90%, 75% и 65% соответственно [3].
Заключение
Первичная легочная гипертензия – редкое тяжелое заболевание с неблагоприятным прогнозом. Симптомы его неспецифичны, поэтому диагноз часто ставится не сразу. Своевременная диагностика и назначение специфической медикаментозной терапии позволяют значительно улучшить выживаемость больных.
Литература
1. Анализ случаев идиопатической лёгочной гипертензии по данным амурской областной клинической больницы / О. Н. Сивякова, В. В. Войцеховский, Е. С. Скрипкина [и др.] / Бюллетень физиологии и патологии дыхания. 2017. Вып. 64. С. 88 – 93
3. Клинический случай 10-летнего успешного применения амбризентана у пациентки с идиопатической легочной гипертензией / Т. В. Мартынюк [и др.] // Евразийский кардиологический журнал. 2015. № 4. С. 48 – 55
4. Стентирование межпредсердной перегородки при идиопатической лёгочной гипертензии / Б. Г. Алекян, С. В. Горбачевский, М. Г. Пурсанов [и др.]// Грудная и сердечно-сосудистая хирургия. 2015. № 5. С. 26 – 33
5. 2015 ESC/ERS Guidelines for the diagnosis and treatment of pulmonary hypertension / Nazzareno Galiè [et al.] // European Heart Journal. 2016. Vol. 37, № 1. P. 67 – 119
Рентгенодиагностика диффузных интерстициальных и диссеминированных процессов легких
| Диффузные интерстициальные и диссеминированные процессы легких представляют одну из сложнейших проблем клинической медицины. По данным консультативных центров, этот вид патологии составляет около 5% всех поражений легких. По мнению М.Ильковича и Л.Новиковой (1998), на интерстициальные пневмопатии приходится 20% всех болезней легких. Причем, как отмечают авторы, в каждом втором подобном случае природа легочной патологии остается неясной. |
Интерстициальные болезни легких представляют собой гетерогенную группу, объединяемую общими клиническими проявлениями, изменениями физиологии дыхания и определенным патоморфологическим сходством (А.Чучалин, 2000; J.Fulmer, 1982). Многие авторы сходятся на том, что большинство интерстициальных болезней имеет разную этиологию, но общий патогенез. В некоторых случаях пусковым механизмом являются экзогенные токсические факторы, непосредственно поражающие альвеолярные клетки или клетки эндотелия капилляров. Органические виды пыли и некоторые лекарства действуют на легкие через иммунные механизмы.
Широкое применение антибиотиков и других лекарственных средств, различного рода химических препаратов в промышленном производстве и повседневной жизни, биостимуляторов, дефолиантов, гербицидов и пестицидов существенно повлияло на иммунологический статус населения. Все это изменило структуру патологии, с которой приходится сталкиваться врачу в повседневной клинической практике. Подсчитано, что число нозологических форм, сопровождающихся диффузными интерстициальными и узелковыми процессами в легких, превышает 150 наименований (С.Рейнберг, 1962; C.Carrington и E.Gaesner, 1978; T.McLoud et al., 1983), однако в клинической практике 90% подобных состояний приходится на 8-10 наиболее распространенных заболеваний. Все они могут быть условно разделены на две группы. В первую входят болезни, преобладающим морфологическим признаком которых является наличие гранулем, определяющих клинико-морфологическую сущность каждой гранулематозной патологии. Вторую группу интерстициальных заболеваний составляют поражения легких, характеризующиеся диффузными, преимущественно интерстициальными, поражениями легочной ткани без формирования гранулем.
Недостаточное знакомство врачей общей практики с клинико-рентгенологическими проявления заболеваний, сопровождающимися диффузным фиброзом и узелковой диссеминацией, является причиной частых диагностических ошибок. По крайней мере 50-70% больным с диффузными и диссеминированными поражениями легких первоначально ставится ошибочный диагноз «туберкулез легких», следствием чего является необоснованная противотуберкулезная химиотерапия (С.Борисов, 1987; М.Илькович и Л.Новикова, 1998; А.Хоменко с соавт., 1991; Е.Шмелев, 2001).
Эти разнообразные по патогенезу процессы сопровождаются сходными клиническими и рентгенологическими проявлениями, в связи с чем объединяются общим методологическим подходом к диагностике.
В диагностике диффузных и диссеминированных процессов ведущая роль принадлежит рентгенологическому исследованию органов грудной клетки, которое начинается с обзорной рентгенографии. К сожалению, на обзорных рентгенограммах грудной клетки мы получаем скиалогическую картину, являющуюся результатом суммации тенеобразований различной величины и формы. Вследствие эффекта суперпозиции и субтракции в проекции на плоскости получается картина, мало похожая на изображение каждого патологического образования в отдельности. Многие очаги сливаются и уходят в фон, вместе с тем появляются новые тенеобразования, для которых нет конкретного морфологического субстрата. При диффузных интерстициальных процессах и очаговой диссеминации неоднородная рассеивающая среда нивелирует нормальные элементы легочного рисунка, а именно сосуды среднего и малого калибра.
Линейная томография при диффузном пневмосклерозе и мелкой диссеминации малоэффективна: мелкие очажки и линейные анатомические структуры вследствие меньшей разрешающей способности при традиционной томографии не выявляются.
Проблему проекционного и суммационного искажения с успехом решает рентгенокомпьютерная томография (РКТ), которая благодаря высокой чувствительности детекторной системы и, соответственно, способности охвата широкого спектра слабых плотностей, а также в силу исключения эффекта проекционной суммации обладает способностью выявлять детали, недоступные традиционному рентгенологическому исследованию.
На КТ чаще и более отчетливо выявляются такие тонкие структурные изменения, как сотовое легкое, лучше выявляются участки буллезной эмфиземы. Компьютерная томография позволяет оценивать состояние легочной ткани, перекрываемой массивными инфильтратами, выраженным фиброзом легочной ткани, значительным плевральным выпотом и массивными плевральными наслоениями.
Причем чем выше разрешающая способность РКТ, тем точнее и реальнее отображаются узелковые и тяжистые структуры. Cовременная компьютерная томография с программой высокого разрешения (ВРКТ) обладает заметными преимуществами перед обычной рентгенографией, линейной томографией и даже компьютерной томографией толстыми срезами в выявлении мелких узелковых образований в интерстиции и паренхиме легкого, линейных и сетчатых структур. ВРКТ выявляет мелкие узелковые образования диаметром около 2 мм, тонкие изменения интерстициального легочного рисунка, нормальные и патологически измененные сосуды и бронхи. Хорошо выявляется тонкая сетка изменений междольковых и внутридольковых перегородок.
С помощью ВРКТ открыт ряд новых рентгенологических симптомов, таких, как симптом матового стекла, симптом неравномерной булыжной мостовой, намного чаще стало выявляться сотовое легкое.
Несмотря на определенное сходство рентгенологической картины широкого круга болезней, сопровождающихся узелковой диссеминацией и диффузным усилением интерстициального легочного рисунка, многие заболевания этой группы имеют определенную специфику, присущую каждой из них и позволяющую приблизиться к правильному диагнозу.
Хроническая форма саркоидоза на ранних стадиях болезни обычно протекает без каких-либо клинических проявлений. Общее самочувствие больного обычно нормальное. Иногда пациенты предъявляют жалобы на сухой кашель со скудным выделением мокроты. Лабораторные исследования также не дают надежных критериев для диагностики.
На ранних стадиях развития саркоидоза на рентгенограммах выявляется увеличение различных групп лимфатических узлов. Наиболее характерным является симметричное билатеральное увеличение бронхопульмональных и медиастинальных лимфатических узлов.
Диагностические трудности возникают главным образом во II стадии заболевания, когда происходит генерализация процесса с распространенным поражением легких интерстициального и узелкового характера. Диффузные формы саркоидоза, по данным З.Костиной (1989), составляют 6% среди всех пациентов с саркоидозом органов дыхания. На этой стадии заболевание чаще всего принимают за гематогенно-диссеминированный туберкулез. Согласно данным А.Рабухина с соавт. (1975), примерно у 20% больных на этой стадии происходит редукция увеличенных бронхопульмональных и медиастинальных лимфатических узлов. Поражение легких, по-видимому, носит лимфогематогенный характер.
Для саркоидоза II-III стадии типичным является несоответствие между степенью выраженности рентгенологических изменений легких и довольно скромной клинической симптоматикой. Тем не менее с прогрессированием заболевания при нарастании фиброзных изменений в легких развиваются респираторная недостаточность, причиной которой является нарушение растяжимости легкого, и нарушение диффузии кислорода. Вследствие межальвеолярного фиброза нарушается газообмен между альвеолой и капиллярами, возникает альвеоло-капиллярный блок. Обширный фиброз легочной ткани с вторичной периацинарной эмфиземой может привести к развитию легочного сердца. По причине легочно-сердечной недостаточности у многих больных с далеко зашедшей стадией саркоидоза выражены цианоз и одышка.
Идиопатический фиброзирующий альвеолит
Идиопатический легочный фиброз относится к группе прогрессирующих интерстициальных заболеваний легких невыясненной природы. В их основе лежат воспалительные изменения стенки альвеол, которые при прогрессировании болезни заканчиваются интерстициальным фиброзом. При морфологическом исследовании легкие характеризуются чередованием более старых бесклеточных коллагеновых очажков и участков с активной пролиферативной функцией фибробластов и миофибробластов. Пролиферирующие островки состоят из веретенообразных остроконечных клеток, расположенных вдоль альвеолярных перегородок. В альвеолярных пространствах обнаруживаются скопления макрофагов, большинство из которых является мононуклеарами.
Описано несколько вариантов фиброзирующего альвеолита, различающихся главным образом активностью воспалительного процесса и темпами развития дыхательной недостаточности. Обе формы ведут к прогрессирующему развитию соединительной ткани в строме легкого. При большом морфологическом многообразии воспалительного процесса при ИФА отсутствуют патогномоничные признаки, позволяющие отличить его от других форм легочного фиброза (А.Чучалин, 2000).
Основными патоморфологическими субстратами, определяющими клиническую картину легочной недостаточности, являются утолщение интерстициальной стромы легких, фиброз, гиалинизация межальвеолярных перегородок и альвеоло-капиллярных мембран, а также облитерация альвеол и капилляров. Изменения, как правило, более выражены в периферических (субплевральных) отделах легких.
Легкие, как никакой иной орган, богаты эластической тканью, и при пневмосклерозе происходит уменьшение эластического резерва легочной ткани. Увеличение эластического сопротивления легочной ткани, ее ригидность ведут к ограничению растяжимости легкого и, соответственно, уменьшению альвеолярной вентиляции. Повреждение альвеоло-капиллярных мембран затрудняет перфузию кислорода и диффузию углекислоты. В результате развивается респираторная и легочно-сердечная недостаточность, которая в конечном счете ведет к летальному исходу (М.Илькович, 1984, 1998; Н.Путов с соавт., 1986).
Фиброзирующим альвеолитом чаще страдают женщины среднего возраста. Обычно болезнь развивается подостро, но примерно у трети больных начало заболевания острое. При этом повышается температура тела до 38-40 С, появляются одышка, слабость, сухой кашель. Иногда в мокроте обнаруживаются прожилки крови, в редких случаях развивается кровохарканье.
При хроническом фиброзирующем альвеолите на рентгенограммах обычно выявляется двустороннее симметричное усиление легочного рисунка. В противоположность саркоидозу, для которого характерно преобладание изменений в прикорневых отделах легких, при фиброзирующем альвеолите легочная ткань поражается более равномерно. Отмечено некоторое преобладание изменений в базальных и периферических субплевральных отделах. Диффузная пролиферация фиброзной ткани ведет к деформации и перестройке архитектоники легочного рисунка по сетчатому типу. Легочный рисунок приобретает вид пчелиных сот, формируется картина сотового легкого: утолщенные межальвеолярные, периацинарные и междольковые перегородки охватывают эмфизематозно вздутые дольки и ацинусы. Для фиброзирующего альвеолита типичным является развитие буллезной эмфиземы, которая развивается раньше других изменений легочного рисунка. Эмфизематозные буллы лопаются, вследствие чего иногда возникает спонтанный пневмоторакс, который может повторяться несколько раз.
В отличие от саркоидоза при ИФА не наблюдается увеличение бронхопульмональных и медиастинальных лимфатических узлов. Расширение корней легких при фиброзирующем альвеолите объясняется увеличением калибра магистральных сосудов, как следствие гипертензии малого круга кровообращения. Описанные признаки легочной гипертензии в далеко зашедшей стадии заболевания сочетаются с картиной так называемого легочного сердца.
При фиброзирующем альвеолите вследствие уменьшения объема легких диафрагма обычно занимает высокое положение. И.Васильчук (1985) отметила уменьшение объема легких и высокое положение диафрагмы с ограничением ее подвижности более чем у половины пациентов с идиопатическим фиброзирующим альвеолитом. Признаки легочной гипертензии отмечены у 30% больных. Нередко появляются дисковидные ателектазы.
Функциональные исследования подтверждают наличие высокой степени респираторной недостаточности. Реография позволяет выявить признаки гипертензии малого круга кровообращения и дать ей количественную оценку. Сцинтиграфия может показать значительное понижение капиллярного кровотока в местах наиболее выраженных изменений рентгенологической картины.
Системная красная волчанка
Системную красную волчанку большинство авторов относят к коллагенозам. Б.Визнер (1984) описывает поражение легких при системной красной волчанке как воспалительное заболевание соединительной ткани. Болезнь характеризуется множественным поражением органов (кожа, слизистые оболочки, суставы, плевра, сердце, почки, лимфатические узлы, селезенка, печень, кроветворная система, легкие).
Системной красной волчанкой страдают преимущественно молодые женщины, они составляют 80-90% всех заболевших. Наиболее частыми жалобами являются боли в грудной клетке, одышка, кашель, реже кровохарканье.
Для системной красной волчанки характерна стойкая лихорадка, резистентная к противоинфекционной терапии. Как правило, неосложненная лихорадка протекает с лейкопенией. Характерны значительное увеличение СОЭ, анемия и умеренная тромбоцитопения.
На рентгенограммах органов грудной клетки определяются уменьшение объема легких и ограничение эластичности легочной ткани, диффузное усиление и деформация легочного рисунка, участки очагового или сегментарного понижения пневматизации, дисковидные ателектазы, высокое стояние диафрагмы и ограничение ее подвижности, наличие жидкости в плевральной полости.
Морфологические изменения легких создают предпосылки к нарушению диффузии кислорода из-за развития альвеоло-капиллярного блока и снижению парциального давления кислорода, что является причиной часто наблюдаемого при волчаночном поражении легких нарушения дыхательной функции легкого. По этой же причине развивается гипертония малого круга кровообращения с перегрузкой правого сердца.
У 30-50% больных системной красной волчанкой имеет место выпот в плевральной полости (E.Dubois, 1966). Примерно в 4% случаев плеврит является первичным проявлением заболевания.
Поражение легких при этих двух формах гистиоцитоза встречается в 20-50% случаев. Оно характеризуется диффузной двусторонней интерстициальной инфильтрацией, на фоне которой рассеяны множественные мелкие узелки размерами 2-3 мм. Примерно у 20% больных обнаруживаются полостные образования. В периферических отделах легких обычно развивается буллезная эмфизема, которая нередко ведет к спонтанному пневмотораксу.
На рентгенологическом изображении изменения легких при гистиоцитозе Х характеризуются двусторонним симметричным усилением легочного рисунка, вызванным диффузной гистиоцитарной пролиферацией в интерстициальной ткани и межальвеолярных перегородках, распространяющейся на альвеолы. Ведущим компонентом рентгенологической картины является склеротический процесс. Л.Дмитриева и В.Ерохин (1989) выделяют три типа изменений легких при гистиоцитозе Х: интерстициальный, интерстициально-гранулематозный и фокусный. При интерстициальном варианте в фазе инфильтрации изменения характеризуются двусторонним диффузным симметричным поражением легочного рисунка за счет инфильтрации на уровне периальвеолярных, периацинарных формирований. При этом можно видеть диффузное понижение пневматизации легочной ткани типа матового стекла. На томограммах выявляется утолщение бронхиальных стенок с формированием перибронхиальных муфт. Инфильтрация и фиброз межальвеолярных перегородок вызывают формирование густой мелкоячеистой сети, на фоне которой видны буллезные вздутия. Все это придает легочному рисунку характер пчелиных сот. Изменения преобладают в верхних и наружных участках легких. На месте пересечения тяжистых структур появляются утолщения, симулирующие мелкие узелки. Альвеолы местами полностью облитерированы, местами буллезно вздуты. На компьютерных томограммах выявляются реальные узелковые образования, обусловленные мелкоузелковым фиброзом.
На конечной стадии гистиоцитоза Х развившийся пневмосклероз практически неотличим от легочного фиброза при других болезнях, в частности саркоидозе, фиброзирующем альвеолите и некоторых формах пневмокониоза.
Патоморфологическое исследование выявляет развитие грануляционных бляшек в мелких дыхательных путях, которые распространяются на альвеолярные ходы и альвеолы.
На рентгенограммах в обоих легких обнаруживаются изменения очагово-инфильтративного характера. На компьютерных томограммах высокой разрешающей способности паренхиматозные изменения выявляются в виде мелкоузелковых образований диаметром менее 5 мм, участков пониженной прозрачности слабой интенсивности в виде матового стекла при сохраненном сосудисто-бронхиальном рисунке или участков более интенсивного понижения пневматизации легочной ткани при исчезновении сосудисто-бронхиального рисунка. Интерстициальные изменения проявляются в виде сетчатости, вызванной утолщением междольковых перегородок и других линейных образований. Часто выявляются буллезное вздутие легочной паренхимы и трансформация легочной ткани по типу сотового легкого.
Экзогенный аллергический альвеолит
Группа экзогенного аллергического альвеолита (ЭАА) включает большое число легочных заболеваний, вызванных гиперергической реакцией организма на вдыхание органической пыли, представляющей собой специфический антиген. Характер антигена разнообразный.
В зависимости от количества и продолжительности вдыхаемого антигена болезнь развивается остро, подостро или приобретает хроническое течение. Основу морфологических изменений составляет картина, характерная для аллергического васкулита, аллергического альвеолита и диффузного фиброза. Происходит диффузная мононуклеарная инфильтрация альвеолярных стенок, терминальных бронхиол и интерстиции. В стенках сосудов развиваются фибриноидное набухание, гиалиноз. Воспаление иногда сопровождается развитием гранулем, которые переходят в фиброз. В отличие от других гранулематозных процессов инфекционной и неинфекционной природы изменения при аллергическом альвеолите ограничиваются легкими. При иммунологическом исследовании обнаруживаются антигенспецифические («иммунные») розеткообразующие клетки.
Острая форма аллергического альвеолита сопровождается лихорадкой, ознобами, миалгиями, кашлем, одышкой, приступами удушья с признаками бронхоспазма. Ведущим симптомом хронической формы экзогенного аллергического альвеолита является прогрессирующая одышка рестриктивного характера, гипоксемия. Нарушение функции внешнего дыхания характеризуется снижением диффузионной способности легких и оксигенации артериальной крови.
Морфологические изменения могут быть настолько слабыми, что при обычном рентгенологическом исследовании на стандартных рентгенограммах выявляются не всегда. Методом выбора является компьютерная томография.
На компьютерных томограммах высокой разрешающей способности паренхиматозные изменения выявляются в виде мелкоузелковых образований диаметром менее 5 мм, участков пониженной прозрачности слабой интенсивности в виде матового стекла при сохраненном сосудисто-бронхиальном рисунке или участков более интенсивного понижения пневматизации легочной ткани. Интерстициальные изменения проявляются в виде сетчатости, вызванной утолщением междольковых перегородок и других линейных образований. Часто выявляются буллезное вздутие легочной паренхимы и трансформация легочной ткани по типу сотового легкого. Иногда наблюдается симптом воздушной ловушки. Изменения имеют много общего с идиопатическим фиброзирующим альвеолитом и облитерирующим бронхиолитом. После прекращения контакта с пылевым аллергическим агентом морфологические и рентгенологические изменения в легких могут заметно уменьшиться или исчезнуть.
Основным методом выявления альвеолярного протеиноза является рентгенологическое исследование, причем наибольшей информативностью обладает компьютерная томография высокой разрешающей способности. Рентгенологическая картина альвеолярного протеиноза варьирует в широких пределах. Характерным является двустороннее слабоинтенсивное однородное затемнение большей или меньшей протяженности в виде матового стекла, по форме напоминающее географическую карту, которое встречается с частотой от 85 до 100%. Вследствие неполного заполнения альвеол жидкостью при протеинозе на фоне слабо интенсивного затемнения определяется сосудистый рисунок. Вторым по частоте признаком является очаговое уплотнение легочной ткани, его частота составляет около 80%. В этих случаях в легочной ткани определяются либо мелкие очаговые, либо более массивные фокусные тенеобразования. В некоторых случаях картина напоминает диссеминацию милиарного типа. Реже (примерно в 7% случаев) встречается выраженный междольковый и внутридольковый фиброз. Характерным для этого заболевания считается симптом «неравномерной булыжной мостовой» (crazy paving).
Диагноз обычно удается верифицировать с помощью биопсийного материала, взятого путем бронхоальвеолярного лаважа, трансторакальной пункции, трансбронхиальной или открытой биопсии.
Итак, несколько заболеваний легких (саркоидоз, идиопатический фиброзирующий альвеолит, облитерирующий бронхиолит, экзогенный аллергический альвеолит, альвеолярный протеиноз, гистиоцитоз Х) объединяются в одну группу в силу определенного сходства рентгено-морфологических изменений, основу которых составляет глубокое и распространенное поражение респираторного аппарата, дыхательных путей и интерстиция легких. Изменения характеризуются воспалением дистальных отделов дыхательных путей, пролиферацией респираторного и покровного эпителия, облитерацией альвеол и бронхиол, развитием гранулем и прогрессирующим диффузным пневмосклерозом. Общность морфологических изменений при разных заболеваниях данной группы, по-видимому, объясняется генетически обусловленным стереотипом тканевой реакции на различные этиологические факторы.
Имеются определенные основания объединять описанные заболевания под рубрикой неспецифических интерстициальных пневмоний, поскольку при гистологическом исследовании постоянно присутствуют элементы воспаления. Вместе с тем при каждом заболевании и в каждом конкретном случае имеется некоторая специфика, определяющая характер клинических проявлений болезни, темпы развития и прогноз.
В рентгенологических проявлениях всех рассмотренных болезней имеется много общего. Наиболее постоянными компонентами рентгенологической картины являются диффузный сетчато-линейный фиброз, развитие буллезной эмфиземы, формирование картины сотового легкого. Несмотря на развитие буллезного вздутия легких при всех рассмотренных заболеваниях происходит уменьшение их объема. Этим они отличаются от первичной идиопатической эмфиземы.
Дифференциальная диагностика описанного круга заболеваний довольно трудна. Тем не менее, несмотря на определенное сходство морфологических изменений и рентгенологической картины поражений легких диффузного интерстициального и диссеминированного характера при различных заболеваниях, точная нозологическая диагностика в большинстве случаев возможна при условии использования комплекса клинических, лабораторных и рентгенологических данных. В сложных случаях методом выбора является бронхоскопия в сочетании с бронхоальвеолярным лаважем, трансбронхиальной легочной биопсией и трансбронхиальной пункцией лимфоузлов.
В данной работе мы не смогли рассмотреть все заболевания, сопровождающиеся диффузным и узелковым пневмосклерозом (пневмокониозы, диссеминированный туберкулез легких), природа которых хорошо известна. Мы ограничились кругом заболеваний неизвестного генеза, представляющих наибольшие трудности при дифференциальной диагностике.