Как определить что клетка старая
Ученые нашли способ обратить процесс старения клеток
Многие люди мечтают, что при их жизни найдут способ остановить старение. Теперь можно перестать мечтать. Реальная жизнь переплюнула научную фантастику. Исследователи смогли не только остановить, но и обратить процесс старения – вернув человеческие клетки обратно к их «молодому» состоянию. Правда, пока что только в лаборатории. Ученые рассчитывают, что скоро их открытие позволит создавать лекарства против естественной дегенерации тканей. И указывают на то, какие продукты нам нужно употреблять, чтобы достичь похожего эффекта в своём организме.
Главный вопрос: почему мы стареем
Старение можно рассматривать как прогрессирующее снижение качества работы человеческого тела. С ним связывают большинство хронических заболеваний, включая рак, диабет и деменцию. Есть масса причин, по которым наши клетки и ткани перестают функционировать. Но в последнее время ученые считают, что главным виновником является накопление так называемых «старых» клеток.
«Старые клетки» – поврежденные клетки, которые не только не работают должным образом (например, перестают делиться), но и нарушают функции клеток вокруг них. Они демонстрируют радикально измененный дегенеративный фенотип в сравнении с их растущими аналогами. Чем меньше внутри вас стареющих клеток или чем быстрее они заменяются новыми – тем вы физически моложе.

Старая клетка
Устранение этих старых, плохо работающих клеток в животных в 2011 году показало замедление прогрессирования болезней, связанных со старением. Например, оно позволило избежать развития катаракты в мышах.
Ученые до сих пор точно не уверены, почему у нас появляется всё больше таких «старых» клеток по мере того, как мы взрослеем. В числе вероятных виновников – случайные повреждения ДНК, воздействия воспалений в тканях и повреждение со временем защитных молекул (теломер) на конце хромосом. До 70-х годов бытовало мнение, что у каждой клетки есть определенное число циклов деления, после которого она останавливается и умирает, но потом доказали, что это не так: клетка может «устареть» в любой момент, с определенным шансом, зависящим от окружающей её среды.
Одна из последних теорий, которая набрала популярность, – причиной старения клеток является потеря их способности включать и выключать гены в нужное время и в нужном месте.
Гены и их сообщения
По мере взросления мы теряем способность контролировать работу своих генов. Каждая клетка в теле содержит всю информацию, необходимую для развития жизни: даже из вашей слюны в теории можно вырастить вашего клона. Но не все гены «включены» в разных тканях и разных ситуациях. Это и позволяет клеткам сердца отличаться от клеток печени или почки, несмотря на то, что все они содержат одни и те же гены.

Слева – нормальная клетка, справа – старая клетка
Когда ген активируется сигналами изнутри или снаружи клетки, он отсылает молекулярное сообщение (РНК). В этом послании хранится вся информация, необходимая для создания того, что будет делать этот ген. С 2008 года мы знаем, что 95% наших генов могут отсылать несколько разных типов сообщений – в зависимости от потребностей клетки. Так клетка «сообщает» своей ткани, в чем она сейчас нуждается для нормального развития. Каждый ген можно считать «рецептом» того, что хочет сделать клетка: если она родилась на кухне, делающей шоколадные пироги, а все полки вокруг забиты только сахаром и ванилью, это её единственный способ попросить организм сходить в магазин за новыми покупками. А если рецепты перестают отправляться, клетка постепенно «худеет» и перестает выполнять свою функцию.
Решение о том, какой тип сообщения выдаст клетка в любой момент времени, производится группой из примерно 300 белков, которые сейчас называют «факторами сращивания» («факторами соединения»). Со временем объем таких факторов, которые производятся организмом, снижается. В результате возникает накопление «старых» клеток, которые не способны включать нужные им гены и реагировать на изменения в окружающей среде.
Последние исследования показали, что уровни этих важных белков-регуляторов снижаются в образцах крови пожилых людей, а также в изолированных человеческих стареющих клетках разных типов тканей.
Как восстановить «старые» клетки
Белки-регуляторы и, соответственно, гены в «старых» клетках можно заставить снова работать. Клетка не умирает, она просто теряет возможность правильно выполнять свою функцию. Значит, надо её «встряхнуть», и дать ей снова вернуться к выполнению своих задач. Недавно способ возвращения наших клеток обратно к своему «молодому» состоянию продемонстрировали Лорна Харрис, Мэтт Вайтмен и их команда из Эксетерского университета (здесь их работу можно почитать бесплатно).

Профессор Лорна Харрис
В своём докладе ученые объясняют, как они пытались найти способы запустить обратно выпуск «факторов сращивания». Оказалось, что если обработать старые клетки химическим веществом, содержащим небольшое количество сероводорода (H2S), число «факторов сращивания» вырастает, гены начинают включаться, и клетка снова возобновляет свою нормальную работу.
Ранее, в апреле этого года, группа из 12 ученых показала, что H2S снижает связанные со старением болезни в животных. Но вещество очень токсично в больших дозах, и исследователи не могли найти способ его безопасной доставки в нужную часть клетки. Были протестированы разные модуляторы – химические соединения, которые могли бы «приплыть» к клетке, произвести с ней химическую реакцию, и отдать ей сероводород.
Из исследования 2013 года было известно, что донор сероводорода GYY4137 может помогать с атеросклерозом, если давать его мышам. Он медленно отдает H2S, мимикрируя стандартную активность здорового организма. С его помощью ученые и смогли доставить молекулу H2S прямо к митохондрии – структуре, отвечающей за производство энергии в клетке.
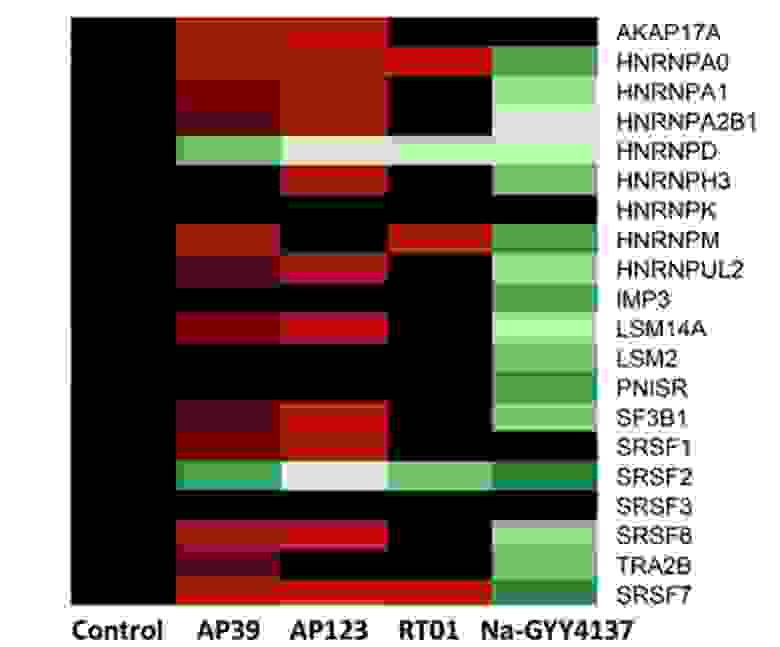
Доставка H2S в человеческую клетку разными методами, результат через 24 часа (чем чернее – тем клетка старее, то есть тем меньше в ней работающих генов-регуляторов)
На протяжении 24 часов клеткам давалось 100 мкг/мл Na-GYY4137 (также тестировалось несколько других вариантов доноров H2S – AP39, AP123 и RT01). Доктор Ева Латорре, помогавшая в исследовании, была поражена масштабом и быстротой изменений в клетках:
Когда я увидела, как много клеток в культуре начали возвращаться к активности, я не могла в это поверить. Старые клетки стали выглядеть, как молодые.
Профессор Харрис рассказывает в докладе:
Наше исследование показывает, что если вы воздействуете на старые клетки молекулами, которые восстанавливают уровни факторов сращивания, эти клетки могут снова начать демонстрировать некоторые особенности молодости. Они снова начинают расти, а их теломеры – окончания хромосом, сокращающиеся с возрастом – становятся длиннее, будто они находятся на молодых клетках. Сейчас требуется больше исследований, чтобы установить истинный потенциал для такого рода подходов к решению дегенеративных последствий старения.
Харрис и Вайтмен рассчитывают, что с помощью таких молекулярных инструментов можно будет устранять «старые» клетки в живых людях и возвращать их к нормальной работе. Они не уверены, что это позволит радикально продлить длительность жизни человека (скажем, до 150 лет), но говорят, что это однозначно повысит качество жизни старых людей, позволив им уменьшить эффекты от хронических болезней, а также снизить шансы инсульта, сердечных заболеваний и рака.
Фонтан молодости
Из прочтения всех этих исследований я для себя вынес одну важную вещь. Оказывается, очень полезно есть чеснок. Он содержит аллицин (который и является причиной характерного резкого запаха). А в результате реакции аллицина с эритроцитами образуется небольшое количество сероводорода. Это помогает снизить напряжение кровеносных сосудов (в исследованиях – до 72%). Сероводород в небольших дозах защищает организм от сердечно-сосудистых заболеваний и показывает противовоспалительные, спазмолитические, вазодилатирующие и цитопротективные свойства. Он также (дамы, закройте глаза) играет роль в расширении сосудов полового члена, необходимом для осуществления эрекции. А теперь еще и подтвердилось, что при благоприятных условиях он может обращать процесс старения клеток, восстанавливая нормальную работу их генов.
Один из руководителей научной группы, исследовавшей этот эффект, доктор Дэвид Краус, говорит, что:
Результаты нашей работы показывают, что крайне полезно включать чеснок в свой рацион. В странах с высоким потреблением чеснока, в Средиземноморье и на Ближнем Востоке, отмечается низкий уровень сердечно-сосудистых заболеваний.
Исследователи также предлагают использовать уровень выделения сероводорода эритроцитами для стандартизации пищевых добавок на основе чеснока.
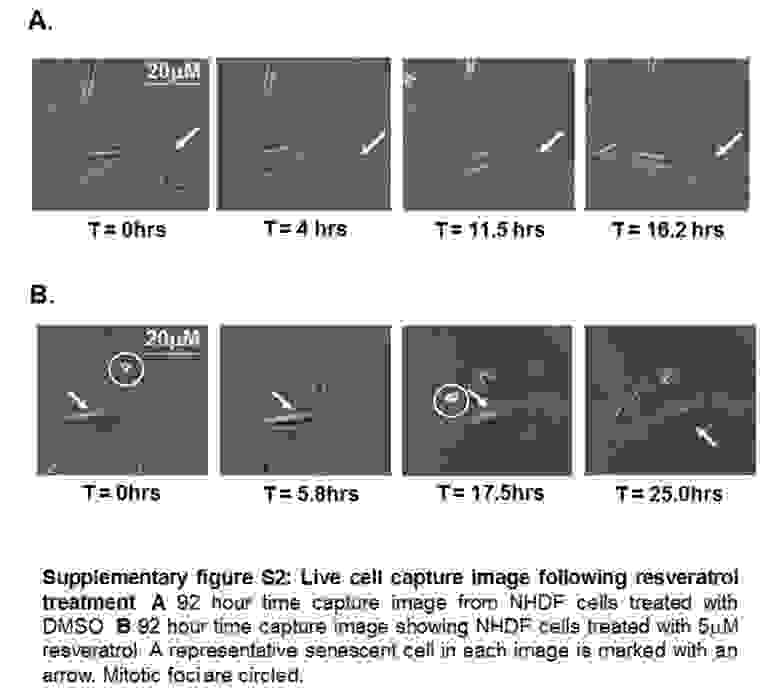
Результаты исследования ресвератола (та же команда работала с ним в 2017 году)
Употребление чеснока не рекомендуется при заболеваниях почек, желчекаменной болезни, язве желудка или кишечника, гепатите и других заболеваниях печени. Альтернатива, которую ранее тоже тестировали Лорна Харрис и Мэтт Вайтмен, пусть и с меньшим эффектом, – аналоги ресвератола. Это вещество можно найти в красном вине, черном шоколаде, кожуре красного винограда и черники, какао и арахисе. Биологические эффекты не настолько сильны, как в аллицине, но ресвератол тоже однозначно омолаживает человеческие клетки – по крайней мере, в пробирке.
О других исследованиях способов борьбы со старением в прошлом году отличный пост написала @mary_arti.
Чем отличается старая клетка от молодой клетки
Важнейшие процессы, происходящие в любом живом организме, являются результатом жизнедеятельности клеток. Обмен веществ, рост, развитие, размножение – последствия упорядоченных химических реакций. Каждая клетка проживает определенный цикл с момента своего появления до полного отмирания. Как же отличить старую клетку от молодой?
Степень активности протекания химических процессов внутри клетки зависит от фазы ее жизненного цикла. Принято выделять интерфазу и деление (фаза М). Интерфаза начинается с образования клетки и заканчивается делением или гибелью. Если клетка начала размножаться, наступила фаза М. Основные обменные процессы активнее всего протекают в интерфазе и замедляются в фазе М вплоть до полной остановки. Некоторые клетки могут переживать фазу покоя, когда не происходит никаких процессов.
Основным процессом жизнедеятельности любой клетки считается обмен веществ. Именно он обуславливает протекание внутриклеточных и межклеточных реакций. Обмен веществ происходит по организованной схеме, отступление от которой недопустимо. К другим процессам жизнедеятельности клетки относятся дыхание, питание, раздражимость и т.д. Сразу после образования они проходят очень интенсивно, но со временем замедляются. В клетке начинаются преобразования, завершающей стадией которых является деление. Дальнейшее существование клетки невозможно. Деление – это формирование новых клеток с увеличенным потенциалом и обменом веществ.
Таким образом, ключевым отличием молодой клетки является высокая скорость протекания обменных процессов. А особенностью старой клетки можно считать способность к делению. В старой клетке хлоропласты быстро двигаются вместе с цитоплазмой.
Ядро молодой клетки располагается точно в центре, и оно крупнее, чем у старой клетки. Цитоплазма с ядром старой клетки располагается в непосредственной близости к оболочке. Обратная ситуация обстоит с вакуолью. В молодой клетке содержится множество мелких вакуолей, которые со временем соединяются в одну большую вакуоль. Следовательно, отличить молодую клетку от старой можно по числу вакуолей.
Рассматривая клетки под микроскопом, можно увидеть капельки жиров. Это также показатель возраста клетки. В молодых клетках жиры отсутствуют или присутствуют в незначительных количествах. Чем больше капель обнаружено, тем старее клетка.
С каждым клеточным циклом линейная молекула ДНК укорачивается. Поэтому старую клетку можно отличить по данному признаку.
Выводы:
Репликативное старение соматических клеток
Репликативное старение соматических клеток
В данном обзоре изложены механизмы репликативного старения соматических клеток млекопитающих, влияние старых клеток на окружающие ткани и организм человека, патологии, связанные с дисфункциями теломер.
Введение.
Термин можно определить как совокупность изменений, которые постепенно и необратимо приводят к гибели организма. Длительность процессов старения в организме делает затруднительным их изучение в системе in vivo, поэтому механизмы старения во многом остаются загадкой. Самым простым способом изучения старения является наблюдение за клеточными культурами. Такой путь изучения старения вполне обоснован, поскольку старение всего организма, прежде всего, связано со старением клеток в нем. Другими словами, изменения, происходящие на клеточном уровне, в полной мере отражаются на состоянии организма в целом.
Репликативное старение. Модель Хайфлика.
Не так давно учеными были обнаружены более специфические биологические маркеры для определения репликативного старения, которые можно разделить на несколько категорий. (1) Компоненты сигнальных путей, которые индуцируют и поддерживают состояние старения (например, индукция ингибиторов циклин-зависимых киназ р16 и р21); (2) маркеры генотоксического стресса (такие как, очаги повреждения ДНК и их колокализация с теломерами); (3) появление характерного типа факультативного гетерохроматина, ассоциированного со старением; (4) секреция определенных воспалительных цитокинов и факторов, модифицирующих ткань.
В классическом варианте термин применяется для описания необратимого ареста клеточного цикла, связанного с дисфункцией теломер, в частности с их укорочением. Однако в последнее время ученые все чаще используют этот термин в более широком смысле. А именно, применяют этот термин для описания стресс-индуцированного старения. Объясняется это тем, что определенные виды стрессов могут индуцировать дисфункциональность теломер, в том числе и их укорочение, что в свою очередь приводит к тем же механизмам, что и при классическом репликативном старении. В данном компасе будут описаны механизмы клеточного старения, связанного с дисфункциональностью теломер, то есть механизмы репликативного старения в классическом его варианте.
Вследствие ряда процессов (например, повреждения ДНК, многократных делений клетки в отсутствии активной теломеразы, изменения белков, ассоциированных с теломерой) теломеры могут утрачиваться или становиться нефункциональными. В ответ на нефункциональные или поврежденные теломеры клетки могут умереть, состариться, что сопровождается арестом клеточного цикла, или приобрести ряд мутаций. Подобные эффекты, безусловно, могут вызвать сильные последствия для всего организма, особенно для сложных организмов, которые содержат как митотические, так и постмитотические клетки. Сейчас доподлинно известно, что нефункциональные теломеры могут способствовать развитию опухоли. Однако при развитии опухоли для того, чтобы выжить раковые клетки должны приобрести механизмы стабилизации и восстановления теломерной функции. С другой стороны, существуют доказательства того, что нефункциональные теломеры могут способствовать старению клеток и индуцировать развитие возрастных патологий, таких как сосудистые заболевания, слабое заживление ран и иммунологическое старение. Более того, в определенных тканях стабилизация теломер может, при некоторых условиях, предотвращать или замедлять развитие ассоциированных со старением процессов.
Состав и структура теломер. Теломерная ДНК.
Длина TTAGGG участков варьирует от вида к виду. Например, человеческие теломеры имеют размер 10-15 kb (килобаз), а лабораторные мыши (Mus musculus) имеют теломеры более длинные (>30kb) и более гетерогенные. С другой стороны, теломеры родственного вида мышей (Mus spretus) немногим короче, чем у людей. Длина теломер также варьирует в разных соматических клетках одного организма.
Важна ли общая длина теломеры для ее функционирования? Сравнение продолжительности жизни разных видов жиовтных показало, что длина теломеры не оказывает большого влияния на старение клеток или организма. Так, Homo sapiens и Mus spretus имеют теломеры практически одинаковой длины, но при этом существенно отличаются по скорости развития опухолей и срокам наступления старения. Наоборот, лабораторные мыши Mus musculus имеют более длинные теломеры, чем их дикие сородичи Mus spretus, тем не менее, все эти виды имеют практически одинаковую продолжительность жизни. Вероятно, что теломерная функция скорее зависит от структуры в целом, чем исключительно от ее длины.
Белки, ассоциированные с теломерой.
Было идентифицировано несколько белков, которые ассоциированы с теломерами млекопитающих. Они регулируют структуру и контролируют длину теломер. Некоторые связаны исключительно с теломерами, тогда как другие локализуются в других ядерных или клеточных компартментах.
У млекопитающих два белка, TRF1 и TRF2, напрямую и специфически связаны с двуцепочечной теломерной ДНК, а третий белок, POT1, специфически связан с одноцепочечным G-хвостом. TRF2 и POT1 особенно важны для стабилизации структуры теломеры и защиты концов хромосом от деградации и слипания. Два дополнительных ассоциированных с теломерой белка у млекопитающих, TIN2 и hRAP1 также специфически локализованы на теломере, но не напрямую, а за счет связывания с TRF1 и TRF2, соответственно. Эти белки вместе с TRF1 контролируют длину теломер. Они не действуют подобно теломеразе, а скорее регулируют теломерную структуру и, поэтому, способны открывать доступ теломеразе к G-хвосту. TRF1, hRAP1 и TIN2 также помогают стабилизировать структуру теломеры.
Две неклассических поли-АДФ рибоз-полимеразы (PARP), TANK1 и TANK2, ферменты, обычно ассоциированные с репарацией ДНК и сохранением стабильности хромосом, также взаимодействуют с TRF1. Их роль в сохранении структуры и функциональности теломер пока не до конца изучена.
Недавно было обнаружено, что несколько известных белков, участвующих в репарации ДНК, также локализуются вблизи теломер. Одним из примеров является Ku, компонент ДНК-зависимой протеин киназы (DNA-PK), связывающий концы ДНК, который важен для репарации двуцепочечных разрывов путем негомологичного соединения концов (NHEJ). Таким образом, DNA-PK, помимо ее роли в репарации ДНК, может играть роль в сохранении теломер. Эта идея подтверждается недавно полученными данными, показывающими, что DNA-PK совместно с TRF2 необходимы для специфичного процессинга теломер после их репликации в S фазе. Более того, комплекс RMN, важный для репарации ДНК, может функционировать вблизи теломеры. У млекопитающих этот комплекс связан с теломерами, по крайней мере, в течение S фазы.
Структура теломеры.
Недавно было показано, что концы теломер представляют собой большую петлю, наподобие лассо, которая называется t петлей. Теломерные t петли были выделены из мышей, людей и простейших, что свидетельствует об их эволюционно консервативной структуре. У мышей и людей размер t петли коррелирует с длиной теломеры, варьируя от 3 kb в нормальных человеческих лимфоцитах до 18 kb в мышиных клетках печени. Простейшие, напротив, имеют t петли меньшего (1 kb) размера, несмотря на длину теломер 10-20 kb.
Формирование теломерных t петель зависит от TRF2. Кроме этого, формирование и/или сохранение теломерных t петель стабилизируется за счет других ассоциированных с теломерой белков, особенно за счет TRF1 и TIN2. Каким же образом t петли защищают теломеры от деградации и склеивания и регулируют длину теломер? Известно, что G-хвост утоплен в теломерную двуцепочечную ДНК в месте соединения t петли и хвоста. Таким образом, t петля может обеспечивать структуру, которая лишена распознаваемых ДНК и поэтому не имеет сходства с двуцепочечными разрывами. Она также может защищать G-хвост от деградации и ограничивать доступ теломеразы к ее субстрату. Разрушение t петли приводит к клеточному ответу, который, по крайней мере, в некоторых случаях имеет сходство с клеточным ответом на двойные разрывы ДНК.
Молекулярные механизмы репликативного старения.
Теломеры укорачиваются с каждым циклом удвоения генома, то есть при каждом клеточном делении. Минимальная скорость укорочения теломер в человеческих клетках составляет 30-50 пар оснований на каждое деление. Прогрессивное укорочение теломер приводит, в конечном счете, к урезанию теломер до критической длины или вызывает изменения в структуре теломер, что приводит к потере теломер-связывающих белков и впоследствии к активации процесса старения. Подтверждением такой гипотезы может служить тот факт, что дополнительная экспрессия каталитической субъединицы теломеразы (TERT) может предотвращать укорочение теломер и отменять арест клеточного роста, опосредованный старением. Напротив, было обнаружено, что ингибирование теломеразы в иммортализованных клетках ограничивает их репликативный срок жизни. Однако большинство клеток не экспрессируют теломеразу и отвечают на дисфункцию теломер необратимым арестом клеточного цикла.
Учеными были предприняты огромные усилия для того, чтобы объяснить молекулярные механизмы старения. Так, были идентифицированы гены, экспрессия которых изменяется при старении клеток. Однако до сих пор, не доказано являются ли эти изменения экспрессии генов причиной или следствием старения. Исследования молекулярных механизмов старения осложняются тем фактом, что старение не является уникальным клеточным процессом. Механизмы старения существенно отличаются у клеток, полученных из различных видов животных. Так, например, в отличие от человеческих фибробластов, мышиные фибробласты экспрессируют теломеразу и имеют очень длинные теломеры, однако после нескольких пассажей в культуре мышиные фибробласты начинают стареть, что не зависит от укорочения теломер и, возможно, опосредуется окислительным стрессом. Даже разные типы клеток, полученные из одного и того же животного, могут существенно различаться по механизмам старения. Человеческие фибробласты начинают стареть после ограниченного числа клеточных делений в культуре, а экспрессия теломеразы отменяет этот процесс. Напротив, человеческие эпителиальные клетки молочной железы быстро переходят в состояние ареста клеточного роста, которое не связано с укорочением теломер, но опосредуется активацией ингибитора циклин-зависимых киназ р16. Субпопуляция клеток с инактивированным р16 выходит из состояния ареста и продолжает делиться до наступления вторичного ареста клеточного роста, который на этот раз уже связан с укорочением теломер. Эти отличия являются отражением различий в экспрессии ряда генов в этих старых клетках, что говорит о том, что существует множество путей старения. Различные пути старения, тем не менее, сходятся на двух белках p53 и pRb.
Пути репликативного старения.
Исследования, в которых с использованием разных подходов подавлялась активность или экспрессия р53, четко установили его специфическую роль в старении. Инактивация р53 способна задерживать, хотя и не отменять, репликативное старение в человеческих клетках. В старых клетках р53 мРНК и уровни белка по большому счету не изменяются, но р53 становится фосфорилированным и его активность, как транскрипционного фактора, повышается в процессе старения. Каким образом р53 активируется за счет укорочения теломер, пока остается неясным. Недавно полученные результаты свидетельствуют о том, что критически короткие теломеры, утратившие свою структуру и связь с регуляторными белками, индуцируют клеточный ответ, такой же, как индуцируется на повреждения ДНК, что приводит к активации ATM/ATR и Chk1/Chk2, которые, в свою очередь, приводят к фосфорилированию и активации р53.
Одной из мишеней р53 является ингибитор циклин-зависимых киназ, р21. Экспрессия р21 повышается в процессе репликативного старения, и его активация зависит от сигналов, инициируемых укорочением теломер, поскольку экспрессия TERT блокирует эту активацию. Было обнаружено, что экспрессия р21 в течение репликативного старения регулируется по двум механизмам, р53-зависимому и р53-независимому. Гиперэкспрессия р21 индуцирует арест клеточного роста в некоторых клетках, тогда как делеция р21 может отсрочивать арест, связанный со старением. Совместно эти исследования говорят о том, что функции р53 в старении заключаются, по крайней мере, частично, в индукции р21.
Ингибирование р53 и pRb дает возможность клеткам достигать более 50 делений. Эти результаты привели к развитию концепции, что два пути ответственны за индукцию старения, и они действуют параллельно друг другу.
Ингибиторы циклин-зависимых киназ (CDKI) ингибируют активность CDK. CDKI р16 нарушает и ингибирует активности CDK4 и CDK6, таким образом, предотвращая прохождение клеточного цикла. Экспрессия р16 увеличивается в некоторых старых человеческих фибробластах, но существуют данные, которые показывают, что индукция р16 не всегда связана с укорочением теломер. Экспрессия р16 повышается после запуска старения в клетках, в отличие от быстрого увеличения экспрессии р21 в клетках только входящих в состояние репликативного старения. Старая популяция человеческих клеток в культуре представляет собой некую мозаику, в которой некоторые клетки экспрессируют р16, тогда как другие экспрессируют р21. При этом индукция р16 не отменяется смещением экспрессии TERT, а функциональная инактивация р16 не предотвращает репликативное старение в человеческих фибробластах, что говорит о том, что р16 не связан с репликативным старением, опосредованным укорочением теломер.
Существует ли связь между укорочением теломер и pRb путем? Предполагается, что точкой пересечения этих двух путей может служить р21. В ответ на укорочение теломер активация р21 может приводить к ингибированию фосфорилирования pRb, что выстраивает р53-р21 и pRb в один общий процесс. Существуют примеры, что инактивация либо р53, либо pRb может существенно задерживать начало старения, подтверждая линейность пути р53-pRb. В других примерах необходимо ингибировать оба и р53 и pRb, чтобы предотвратить начало репликативного старения в человеческих клетках, что говорит о наличии двух параллельных путей. Опять же следует заметить, что р53-р21-pRb путь преимущественно ответственен за старение, индуцированное укорочением теломер, тогда как р16-pRb путь опосредует преждевременное старение, индуцированное стрессом. В зависимости от типа клеток, культуральных условий и стрессирующих воздействий для предотвращения старения необходима инактивация либо р53-р21-pRb, либо р16-pRb путей по отдельности или обоих путей вместе. Таким образом, можно сделать вывод, что р53 и pRb/p16 пути работают совместно для остановки пролиферации клеток. Возможно, что путь р53, вовлекающий р21, активируется заблаговременно, тогда, как р16 превалирует при сильном физиологическом стрессе и сохраняет клетки в состоянии ареста.
Старение клеток как механизм, подавляющий развитие опухоли.
Существует четкая связь между состоянием теломер и подавлением опухоли. Экспрессия теломеразы в нормальных человеческих фибробластах усиливает их неопластическую трансформацию в культуре, и, наоборот, ингибирование теломеразы в опухолевых клетках ограничивает их рост. Генетические исследования мышей, дефицитных по теломеразе, показали, что укорочение теломер участвует в подавлении опухоли. Мыши, дефицитные по РНК, входящей в состав теломеразы, постепенно утрачивали теломеры и становились устойчивыми к неоплазиям. Однако происходит ли репликативное старение в ответ на укорочение теломер in vivo, и является ли последующая индукция старения механизмом, подавляющим формирование опухоли в этих генетически модифицированных мышах, пока остается неизвестным.
Недавно несколькими группами исследователей было продемонстрировано присутствие старых клеток в некоторых предраковых тканях людей и мышей. Эти исследования показывают, что онкоген-индуцированное старение является процессом, который действительно происходит in vivo. Наиболее важно, что эти исследования показывают, что онкоген-индуцированное старение является активным процессом в ответ на онкогенный стимул, и, зачастую, является защитным механизмом, направленным против развития опухоли.
Взаимосвязь между старением клеток и старением организма.
Сейчас ясно, что старение клеток может быть индуцировано различными типами клеточных стрессов, включая теломерную дисфункцию. Более того, старые клетки устойчивы к апоптозу, что говорит о том, что они могут накапливаться в течение всей жизни организма. Реальная скорость накопления старых клеток in vivo не известна. При запуске процесса старения клеток экспрессия их генов претерпевает впечатляющие изменения. В ряде исследований было показано, что старые фибробласты изменяют экспрессию некоторых генов, включая те, которые кодируют протеазы, ингибиторы протеаз, ростовые факторы, хемокины, ангиогенные факторы и белки внеклеточного матрикса. Поскольку каждая клетка в организме находится в окружении других клеток, взаимодействующих друг с другом, то изменения секреторного профиля старых клеток меняют тканевое микроокружение и влияют на функции соседних клеток. Кроме того, что старение клеток понижает способность тканей к самообновлению, этот процесс может также способствовать старению организма путем влияния на соседние клетки через секреторные молекулы и за счет нарушения целостности и гомеостаза тканей.
Обнаружение маркеров, ассоциированных со старением, в местах развития возрастных патологий дает дополнительные основания предполагать о наличии связи между клеточным старением и старением организма. Несколькими группами исследователей были представлены доказательства присутствия старых эндотелиальных клеток в атеросклеротических бляшках. Изменения экспрессии генов в старых клетках являются факторами развития атеросклероза. Также была обнаружена связь между клеточным старением и другим возрастным заболеванием, остеоартрозом. Старые клетки обнаруживались в кластерах хондроцитов вблизи остеоартрического повреждения. В норме уровень обновления хондроцитов в хряще низок, но он увеличивается при развитии заболевания, что в свою очередь способствует изнашиванию теломер. Характерным заболеванием пожилых мужчин является доброкачественная гиперплазия простаты, которая характеризуется ростом зоны перехода простаты вследствие пролиферации эпителиальных и стромальных клеток. Интересно, что эта пролиферация происходит из-за наличия старых эпителиальных клеток, обнаруженных в этой области. Эти клетки секретируют цитокины ИЛ-1 и ИЛ-8, которые стимулируют секрецию стромальных факторов роста, что в свою очередь индуцирует пролиферацию нестарых эпителиальных клеток. Таким образом, присутствие старых клеток может способствовать прогрессированию соседних предраковых клеток и, следовательно, развитию рака в старых тканях.
С другой стороны, как было упомянуто выше, клеточное старение может защитить организм млекопитающих от опухоли. Однако если клеточное старение также способствует старению организма, вероятно, что это является примером эволюционно антагонистической плейотропии. Эта теория предполагает, что некоторые особенности, которые в процессе эволюции развивались, как защитные механизмы многоклеточных организмов, в частности млекопитающих, оптимальны для молодых организмов, но могут иметь вредное влияние на старые организмы. Арест клеточного цикла, связанный с клеточным старением, может быть той самой особенностью, которая подавляет развитие опухоли в молодых индивидуумах. Напротив, измененные функции старых клеток могут оказывать вредные воздействия на пожилые организмы. По-видимому, эти вредные эффекты также присутствуют и в молодых тканях, однако, в связи с тем, что количество старых клеток в организме молодых индивидуумов невелико, их вредные воздействия не являются системными. Когда организм стареет, старые клетки накапливаются. Возможно, что накопление этих клеток с измененными функциями и секреторным профилем, приводит к физиологическим изменениям и к нарушению целостности ткани и организма в целом.
Секреторный профиль старых клеток может нарушать микроокружение ткани, которое важно для подавления роста и пролиферации клеток с онкогенными мутациями. Таким образом, повреждения, теломерная дисфункция или ошибки в митогенной сигнализации могут приводить к накоплению старых клеток, но их влияние может становиться значимым и вредоносным только в более позднем возрасте, когда они накопятся в достаточном количестве. Поскольку с возрастом количество клеток с онкогенными мутациями увеличивается, то вероятность их встречи со старыми клетками повышается у пожилых людей. Если это случается, старые клетки создают микроокружение, которое способствует усиленной пролиферации и злокачественной трансформации мутантных клеток. Таким образом, несмотря на защиту от опухоли в молодых организмах, клеточное старение, индуцированное дисфункцией теломер, может способствовать прогрессированию опухоли у старых организмов.
Репликативное старение как основной механизм развития преждевременного старения организма.
Было показано, что некоторые заболевания человека связаны с неадекватным укорочением теломер. Хотя подобные патологии могут в некоторой степени варьировать в своем проявлении, все они приводят к преждевременному старению и ранней гибели организма. В настоящее время известны три синдрома, причиной которых являются мутации в генах, кодирующих голоферменты теломеразы: врожденный дискератоз, апластическая анемия, и некоторые случаи идиопатического легочного фиброза. Пациенты, страдающие врожденным дискератозом, обладают маленьким ростом, страдают от недоразвития половой системы и бесплодия, имеют дефекты кожи и гемопоэтической системы и обычно умирают от недостатка клеток костного мозга. Многие из этих патологий также развиваются у мышей, нокаутных по теломеразе. Совсем недавно обнаруженный синдром, идиопатический легочный фиброз, является гипертрофическим летальным заболеванием, связанным с прогрессивным образованием рубцов в легких, вследствие чего развивается легочная недостаточность.
Также было показано, что человеческие сегментарные прогероидные синдромы связаны с клеточным старением, а клетки, полученные из таких пациентов, обычно обладают ограниченной жизнеспособностью in vitro. Наиболее изученными являются синдром Вернера, или прогерия взрослых, и синдром Хатчинсона-Гилфорда, или прогерия детей. Синдром Вернера является аутосомальным рецессивным расстройством, причиной которого служат мутации в гене WRN, кодирующем хеликазы семейства RecQ, которые вовлечены в репарацию ДНК и транскрипцию. Пациенты с синдромом Вернера проявляют фенотип старых людей, для которого характерны поседение волос, плешивость, двусторонняя катаракта, диабет 2 типа, недоразвитие половой системы, остеопороз и атеросклероз; продолжительность жизни таких пациентов составляет в среднем не более 47 лет, причиной смерти обычно является развитие рака или заболевание сосудов. Синдром Хатчинсона-Гилфорда является аутосомальным доминантным расстройством, причиной которого служит мутация в гене LMNA, кодирующем ламин А/С, что приводит к экспрессии сплайсингового варианта прогерина. Пациенты, страдающие синдромом Хатчинсона-Гилфорда, также проявляют фенотип старых людей, включая очень маленький рост, характерные особенности старости на лице, утрату волос, липодистрофию, склеродермию, остеолиз и атеросклероз; гибель наступает в среднем в возрасте 12 лет, как результат инфаркта миокарда или инсульта. Хотя генетические дефекты при синдроме Вернера и синдроме Хатчинсона-Гилфорда различны, были представлены доказательства, что в обоих случаях усиленное клеточное старение связано с повышенной скоростью укорочения теломер.
Синдром Вернера
Заключение.
Изучение роли клеточного старения в многообразии возрастных патологий становится все более востребованной темой. Как обсуждалось выше, неоспоримые экспериментальные доказательства сейчас существуют и показывают связь между повышенной скоростью клеточного старения и усиленным старением организма. Степень, с которой клеточное старение способствует природной продолжительности жизни разных видов животных, сейчас остается неустановленной. Вероятно, что клеточное старение является одним из нескольких (или многих?) факторов, которые влияют или способствуют старению организма.
За исключением р53-р21 и р16-pRb путей, немного известно о компонентах генетических путей старения. Было идентифицировано множество генов, экспрессия которых изменяется в старых клетках, но остается неизвестным, являются ли эти изменения в генной экспрессии причиной или следствием процесса старения. Идентификация и характеристика новых генетических компонентов путей старения сможет обеспечить понимание молекулярных механизмов старения, а также предоставить необходимые инструменты для модулирования путей старения in vivo. Имея возможность манипулировать процессами старения in vivo, можно будет предотвращать или хотя бы замедлять развитие патологических состояний, связанных с возрастными изменениями организма.
Литература
2. Pazolli E., Stewart S.A. «Senescence: the good, the bad and the dysfunctional».
3. Itahana K., Campisi J., Dimri G.P. «Mechanisms of cellular senescence in human and mouse cells».
4. Magalhaes J.P., Faragher R.G.A. «Cell divisions and mammalian aging: integrative biology insights from genes that regulate longevity».
5. Martin J.E., Sheaff M.T. «The pathology of ageing: concepts and mechanisms».
6. Shay J.W., Wright W.E. «Hallmarks of telomeres in ageing research».
7. Zhang H. «Molecular signaling and genetic pathways of senescence: Its role in tumorigenesis and aging».
8. Chen J.-H., Hales C.N., Ozanne S.E. «DNA damage, cellular senescence and organismal ageing: causal or correlative?»
9. Campisi J. «Senescent cells, tumor suppression and organismal ageing: good citizens, bad neighbors».
10. Jeyapalan J.C., Sedivy J.M. «Cellular senescence and organismal aging».
11. Shay J.W., Wright W.E. «Senescence and immortalization: role of telomeres and telomerase».














