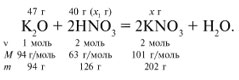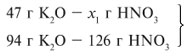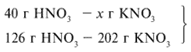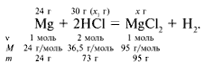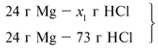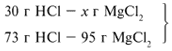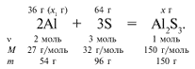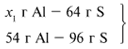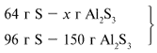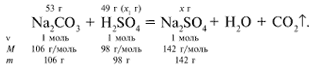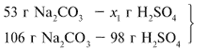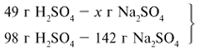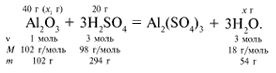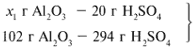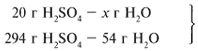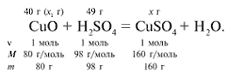Как понять что в избытке что в недостатке
Химия, Биология, подготовка к ГИА и ЕГЭ
Задачи такого типа (точнее, это может быть даже не самой задачей, а частью задачи) есть в части С ГИА, они входят в часть С ЕГЭ, теперь они появились и в части B.
Классический пример задачи на избыток и недостаток.
Этапы решения задачи:
1. Записываем уравнение реакции и уравниваем его:
2. Находим количество моль тех веществ, массы которых нам даны в условии:
n(Cu) = m\Ar =3.2 г \ 63.5 г\моль = 0,05 моль
m(Hg(NO3)2) = m\Mr = 20 \ 324 = 0,06 моль
3. Сравниваем количество моль веществ и определяем недостаток:
по уравнению реакции меди и нитрат ртути реагируют 1:1, значит, их количество моль тоже должно быть одинаковым
0,05 моль ПО НЕДОСТАТКУ
Почему по недостатку? Это аналогично вопросу — «сколько целых яблок можно сложить из 5 половинок? «
4. Вычисляем массу продукта по количеству моль, соответствующему недостатку:
0,05 моль ——> 0,05 моль
m(Hg)= n*Ar = 0,05 моль * 200 г\моль = 10 г
______________________________________________________________________________________
Пример задачи на избыток и недостаток,
где вещества в другом соотношении:
те же самые этапы решения:
1. Записываем уравнение реакции и уравниваем его:
2. Находим количество моль тех веществ, массы которых нам даны в условии:
n(N2 ) = m\Mr = 14\28=0.5 моль
3. Сравниваем количество моль веществ и определяем недостаток:
в этом уравнении все не так очевидно, как в предыдущем, поэтому нужно просто прикинуть:
4. Вычисляем массу продукта по количеству моль, соответствующему недостатку:
m(N2O5) = n*Mr = 2* 0.5\5 моль * 108 г\моль = 21 г
______________________________________________________________________________________
Есть задачи, очень похожие на задачи избыток-недостаток,
1. Записываем уравнение реакции и уравниваем его:
здесь у нас возможно 2 варианта — образование средней и кислой соли:
2. Находим количество моль тех веществ, массы которых нам даны в условии:
n(CO2 ) = V\22.4 л\моль = 24.9 \ 22.4 = 1,11 моль
n(NaOH)= m\Mr = 44.4\40 = 1,11 моль
т.к. количество моль веществ одинаково, то делаем вывод, что реакция протекает по схеме образования кислой соли:
4. Вычисляем массу продукта по количеству моль:
m ( NaHCO3) = n*Mr = 1,11 * 84 = 93,24 г
_____________________________________________________________________________________ _
Задачи на избыток и недостаток не трудные, зачастую они являются частью более сложных задач, поэтому все, что нужно сделать, это натренироваться — порешать как можно больше таких примеров, внимательно уравнивая и работая с коэффициентами.
Как понять что в избытке что в недостатке
В условиях задач такого типа указаны массы или объёмы двух реагирующих веществ, одно из которых дано в избытке, поэтому при решении таких задач нужно определить, какое вещество взято в избытке. Расчёт массы или объёма продукта реакции ведётся по данным вещества взятого в недостатке.
I. Алгоритм решения задачи: «Вычисление массы или количества продукта реакции, если один из реагентов взят в избытке»
Пример 1. Смешали два раствора, содержащих соответственно 33,3г хлорида кальция и 16,4г фосфата натрия. Вычислите массу осадка.
Последовательность выполнения действий
Оформление решения задачи
1. Записываем условие задачи
2. Вычислим молярные массы для формул, записанных вдано
3. Вычислим количества веществ, масса которых дана в условии
4. Запишем УХР. Расставим коэффициенты.
Под формулами напишем стехиометрические соотношения, отображаемые уравнением реакции.
5. Определим, какой из реагентов взят в избытке. Для этого сравним дроби.
CaCl2 – взят в избытке, расчёт ведём по недостатку, т.е. поNa3PO4.
6. Вычислим количество вещества, массу которого нужно найт
7.Вычислим искомую массу
Пример 2. Вычислите объём водорода (н.у.), который образуется при взаимодействии 6,5 г цинка с соляной кислотой массой 7,5 г.
Последовательность выполнения действий
Оформление решения задачи
1. Записываем условие задачи
2. Вычислим молярные массы для веществ с известной массой, записанных в дано
3. Вычислим количества веществ, масса которых дана в условии
ν(Zn) = m/M= 6,5/65г/моль=0,1моль
4. Запишем УХР. Расставим коэффициенты.
Под формулами напишем стехиометрические соотношения, отображаемые уравнением реакции.
5. Определим, какой из реагентов взят в избытке. Для этого сравним дроби.
НCl – взят в избытке, расчёт ведём по недостатку, т.е. по Zn.
6. Вычислим количество вещества, объём которого нужно найти
7.Вычислим искомый объём
Расчёты по уравнению реакции, если один из реагентов взят в избытке
Дано: m (ν, V, W) реагентов
Найти: m (ν, V, W) продукта
1. Составляем уравнение реакции
2. Нахождение количества вещества реагентов ν(А) и ν(В):
3. Сравнение дробей – нахождение недостатка:
Если, ν(А)/a > ν(В)/b, то вещество В в недостатке, расчёт ν(С) ведём по ν(В)
© 2017 Персональный сайт учителя химии Кардаевой Татьяны Александровны. Все права защищены.
Hекоторые файлы и информация, находящиеся на данном сайте, были взяты из методической литературы, найдены в сети Интернет, как свободно распространяемые (авторство данных материалов сохранено). Если Вы являетесь правообладателем той или иной продукции или информации, и условия, на которых она представлена на данном ресурсе, не соответствуют действительности, просьба сообщить об этом с целью устранения правонарушения.
4.3.5. Расчеты массы (объема, количества вещества) продуктов реакции, если одно из веществ дано в избытке (имеет примеси).
Очень часто при проведении реакции между веществами оказывается, что один реагент прореагировал полностью, а другой нет. В таком случае говорят, что вещество, которое полностью израсходовалось, было в недостатке, а то вещество, которое осталось – в избытке. Поскольку избыток реагента не участвует в реакции, количество продукта зависит только от количества вещества, которое было в недостатке.
Предположим, что осуществляется реакция между веществами А и B, которая протекает в соответствии с уравнением:
Для осуществления этой реакции было взято количество вещества A, равное nA, и количество вещества B, равное nB. Определить то, какое вещество в избытке, а какое в недостатке, можно, сравнив выражения:
В зависимости от того, какое выражение окажется меньше, то вещество соответственно и будет в недостатке.
Примечание: распространенной ошибкой является то, что вместо выражений (1) сравнивают просто количества веществ. Так делать категорически не допускается! Если n(A) > n(B), то это еще не значит, что вещество A в избытке!
После того, как будет установлено то, какое вещество было в недостатке, расчеты ведутся по его количеству аналогично рассмотренным в главе 4.3.3.
Пример задачи на избыток и недостаток
Нагрели смесь 54 г алюминия и 80 г серы. Вычислите массу образовавшегося сульфида алюминия.
Решение
Запишем уравнение реакции:
Рассчитаем количества веществ алюминия и серы:
n(Al) = m(Al)/M(Al) = 54/27 = 2 моль;
n(S) = m(S)/M(S) = 80/32 = 2,5 моль
Для того чтобы выяснить, какое из исходных веществ в недостатке, разделим количества молей веществ на коэффициенты перед этими веществами в уравнении и сравним рассчитанные выражения:
Значит сера в недостатке. Расчеты далее ведем по количеству вещества серы.
Исходя из уравнения реакции
следует, что количество прореагировавшей серы и образовавшегося в результате реакции сульфида алюминия связаны выражением:
где 3 и 1 – коэффициенты перед S и Al2S3 соответственно. Отсюда:
Следовательно, масса сульфида алюминия будет равна:
В случае, если вместо массовой доли чистого вещества дается массовая доля примесей, то учитывая, что:
мы можем записать, что:
Пример задачи на расчет количества продукта, зная массу реагента с примесями
Какой объем углекислого газа (н.у.) выделится при действии избытка соляной кислоты на технический карбонат кальция массой 150 г, содержащий 10% некарбонатных примесей.
Решение:
Запишем уравнение взаимодействия карбоната кальция с соляной кислотой:
Массовая доля примесей в техническом карбонате кальция составляет 10%, значит массовая доля чистого карбоната кальция будет составлять:
ω(CaCO3) = 100% — ω(прим.) = 100% — 10% = 90%.
Масса чистого карбоната кальция будет равна:
m(CaCO3) = ω(CaCO3) ∙ m(CaCO3 техн.)/100% = 90% ∙ 150 г/100% = 135 г,
Следовательно, количество вещества карбоната кальция равно:
n(CaCO3) = m(CaCO3)/M(CaCO3) = 135 г / 100 г/моль = 1,35 моль
В соответствии с уравнением реакции:
Количества веществ карбоната кальция и углекислого газа равны (одинаковые коэффициенты в уравнении), следовательно:
Тогда, зная, что один моль любого газа при нормальных условиях занимает объем 22,4 л, мы можем рассчитать объем выделившегося CO2:
V(CO2) = n(CO2) ∙ Vm = 1,35 моль ∙ 22,4 л/моль = 30,24 л
Как распознать симптомы дефицита и избытка жизненно важных витаминов
Главным источником витаминов и микроэлементов должен служить рацион, однако далеко не всегда человеку удается сбалансированно питаться, чтобы насытить организм необходимыми веществами. Дефицит витаминов – авитоминоз – нарушает практически все функции организма, но это редкое заболевание в современном мире. Такой диагноз ставит только врач после обследования. По этой и многим другими причинам нельзя самостоятельно назначать курс витаминов во время мнимого «весеннего авитоминоза».
Чтобы разобраться, в чем проявляется норма и недостаток витаминов в организме и нужно ли принимать синтетические витамины (поливитамины, витамины определенной группы) обычному человеку поговорим с экспертом лаборатории персонифицированной медицины ЛабКвест Ириной Валентиновной Мартиросовой.
Витамин С
Наиболее ярким примером авитоминоза служит диагноз цинга. Эта «болезнь моряков» в прошлом была связана с дефицитом витамина С из-за скудного рациона. Сегодня дойти до такого состояния достаточно сложно, однако обо всем по порядку.
Витамин С отвечает за защитные функции организма. Он усиливает иммунный ответ в ответ на чужеродный патоген в организме, участвует в росте и развитии тканей, способствует заживлению ран.
Наиболее богатыми источниками витамина С считается: зелень, шиповник, зеленые овощи, цитрусовые, томаты, картофель.
Недостаток этого витамина проявляется выпадением волос, сухостью и бледностью кожи, воспалительными процессами в полости рта и кровоточивостью десен, повышенной утомляемостью, хрупкостью костей, усиленной склонностью с вирусам и инфекциям и другими последствиями.
Устоявшийся миф о необходимости принимать аскорбиновую кислоту практически в любых количествах может привести к избытку витамина, который не менее опасен, чем дефицит. Он нередко сопровождается похожими симптомами, вызванными недостатком витамина, к которым также добавляются острые проблемы с желудочно-кишечным трактом и предрасположенность к образованию камней в почках. Однако все эти признаки могут проявиться у человека, который действительно «перебрал» с витамином С из баночки. Вообще, избыток витамина организм старается выводить самостоятельно с калом и мочей.
Витамин D
Витамин D – наиболее «противоречивый», поскольку нередко в исследованиях и метаанализах ученые приводят противоречащие выводы о пользе или даже бесполезности синтетического витамина.
Витамин D – прогормон, который участвует в различных биохимических процессах организма. Он необходим для нормальной функции иммунной системы, профилактики сердечно-сосудистых и аутоиммунных заболеваний, является онкопротектором.
Различают витамин D2 и D3. Первая форма витамина содержится в пище, а вторая образуется в коже из D2 под воздействием солнечного света.
Избыток витамина для жителей России труднодостижим, поэтому врачи часто рекомендуют прием синтетического витамина в течение всего года взрослым и детям. О дозах необходимо проконсультироваться со специалистом.
Витамин В12
Основным источником витамина В12 являются продукты животного происхождения, поэтому люди, которым по тем или иным причинам исключили из рациона мясо, рыбу и молочные продукты, находятся в повышенной группе риска.
Витамин имеет жизненно важное значение для кроветворения и нервной системы, он участвует в синтезе компонентов ДНК.
Недостаток В12 проявляется слабостью, головокружениями и шумом в ушах, повышенной раздражительностью, снижением памяти, признаками депрессии. Избытку сопутствует крапивница, а по некоторым данным и проблемы с кожей, включая прыщи и акне. У людей могут возникать аллергические реакции, наблюдаться повышенная возбудимость. Есть и другие симптомы, однако о них можно узнать из лабораторных исследований.
Витамин В9 или фолиевая кислота
Этот витамин обычно назначается в тандеме с В12 для синергетического эффекта. Фолиевая кислота также необходима для иммунной и кровеносной систем, участвует в образовании новых клеток, нужна для здорового метаболизма.
Недостаток проявляется неврологическими симптомами – тревожностью, агрессией, повышенным чувством страха, а также способствует риску развития панических атак и депрессии. На фоне избытка также сохраняется агрессия и повышенная возбудимость, появляются симптомы нарушения пищеварения.
Беременным женщинам и молодым мамам дополнительный прием В9 необходим в течение длительного времени. Остальным людям, как впрочем и беременным женщинам, показан контроль и рекомендации специалиста.
Витамин А
Провитамин А – мощный антиоксидант, защищает от сердечно-сосудистых заболеваний, является онкопротектором, необходим для иммунной и репродуктивной систем организма.
Недостаток витамина также легко определить по внешним факторам, которые тем не менее перекликаются с симптомами дефицита других витаминов. К недостатку бета-каротина относят: сухость кожи и глаз, выпадение волос, проблемы со зрением (развитие «куриной слепоты»), кожные заболевания, нарушения развития скелетной ткани и другие проблемы.
На избыток витамина А, в первую очередь, следует обратить внимание курильщиков, поскольку он повышает риск развития злокачественных опухолей. Симптомы переизбытка могут быть разными, однако к главным относят: выпадение волос и облысение, нарушение аппетита, кожные воспаления, диарею, повышенную усталость, мышечные боли.
Грамотный подход к приему витаминов
Витамины должен назначать врач – аксиома, которая постоянно требует доказательств среди россиян. Мы привыкли покупать поливитамины весной или какую-то конкретную баночку с синтетическим витамином по чьему-либо совету, однако это в корне неверно.
Человек может нести недостаток одного витамина и переизбыток другого, поэтому поливитамины могут быть для него вредными. Еще, прием одной группы витаминов может нейтрализовать другую, и тогда это потерянное время и деньги.
Врачи подчеркивают, что необязательно сдавать комплексные анализы на статус запаса витаминов в организме. Человеку необходимо проконсультироваться с терапевтом, который выслушает жалобы, осмотрит и уже потом порекомендует конкретные лабораторные исследования. А возможно, просто посоветует разнообразить ежедневный рацион.
Методика решения задач
на «избыток–недостаток»
в курсе основной
общеобразовательной школы
Умение решать химические задачи – важная составляющая знаний по предмету. Согласно государственному стандарту образования по химии учащиеся, оканчивающие школу, должны уметь решать более десятка типов стандартных задач. Среди них и задачи на «избыток–недостаток».
Предлагаю свой вариант подачи материала по решению таких задач в курсе химии 9-го класса.
На изучение этой темы отвожу 2–2,5 урока, в зависимости от уровня способностей учеников класса. Ознакомление с алгоритмом решения задач данного типа происходит в рамках изучения темы «Теория электролитической диссоциации». Однако если класс сильный, то в рамках эксперимента этот тип задач иногда изучаем и в конце 8-го класса в главе «Галогены», а высвободившееся время можно потратить на изучение органической химии в курсе 9-го класса.
На первом уроке разбираю два типа задач на «избыток–недостаток»:


В качестве домашнего задания обязательно предлагаются две-три задачи, подобные изученным на уроке.
На втором уроке закрепляю и углубляю изученный материал, ввожу понятия «процентная концентрация растворов веществ», вступивших в реакцию, «плотность растворов». Кроме того, усложняю задачи, вводя «процентное содержание примесей в исходном веществе» и т. д. Такой прием позволяет повторить элементы уже изученного материала, сэкономить время. В конце второго урока изучения темы или в начале третьего провожу небольшую самостоятельную работу на закрепление изученного материала, включающую одну-две задачи, причем самостоятельная работа предлагается в трех уровнях сложности, в зависимости от способностей ученика.
Урок 1
Решение задач на «избыток–недостаток»
ХОД УРОКА

Решая химические задачи, следует не забывать о правилах их грамотного оформления по схеме: дано, найти, решение, ответ.
ЗАДАЧА 1. На 47 г оксида калия подействовали раствором, содержащим 40 г азотной кислоты. Найдите массу образовавшегося нитрата калия.
Решение
Рассчитаем относительные молекулярные массы интересующих нас веществ:
Для удобства расчета за х1 примем массу НNО3 и найдем, какое из веществ, вступивших в реакцию, дано в избытке, какое – в недостатке.
Следовательно, азотная кислота дана в недостатке, т. к. по условию ее 40 г, а по расчету необходимо 63 г, поэтому расчет ведем по HNO3:
ЗАДАЧА 2. На 24 г металлического магния подействовали 100 г 30%-го раствора соляной кислоты. Найдите массу образовавшегося хлорида магния.
m(Mg) = 24 г,
m(р-р HCl) = 100 г, 
Решение
Рассчитаем относительные молекулярные массы интересующих нас веществ:
Для удобства расчета за х1 примем массу соляной кислоты и найдем, какое из веществ, вступивших в реакцию, дано в избытке, какое – в недостатке.
Из расчета видно, что соляная кислота дана в недостатке, т. к. по условию задачи ее дано 30 г, а для реакции требуется 73 г. Следовательно, расчет ведем по соляной кислоте:

ЗАДАЧА 1. На 36 г алюминия подействовали 64 г серы. Найдите массу образовавшегося сульфида алюминия.
Решение
Примем массу Al за х1 и найдем, какое из веществ, вступивших в реакцию, дано в избытке, какое – в недостатке.
В данном случае вещества, вступившие в реакцию, взяты в стехиометрических количествах, поэтому расчет можно вести по любому из них:
ЗАДАЧА 2. На раствор, содержащий 53 г карбоната натрия, подействовали раствором, содержащим 49 г серной кислоты. Найдите массу образовавшейся соли.
Решение
Рассчитаем относительные молекулярные массы интересующих нас веществ:
Примем за х1 массу cерной кислоты, чтобы узнать, какое вещество дано в избытке, какое – в недостатке.
В данном случае оба вещества взяты в стехиометрических количествах, поэтому расчет можно вести по любому из них:
Однако учитель, подбирая задачи для решения в классе, должен помнить, что в некоторых случаях (например, если кислота или кислотный оксид дан в избытке) решение задачи не ограничивается расчетом двух пропорций, т. к. реакция будет протекать дальше с образованием кислой соли. Это повысит сложность материала. На первых уроках при решении задач данного типа я не включаю в материал задачи на прохождение реакций с образованием кислых или основных солей.
Домашнее задание
ЗАДАЧА 1. На 200 г 10%-го раствора серной кислоты подействовали 40 г оксида алюминия. Найдите массу образовавшейся воды.
M(р-р H2SO4) = 200 г, 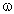
m(Al2O3) = 40 г.
Решение
Рассчитаем относительные молекулярные массы интересующих нас веществ:
Найдем, какое из вступивших в реакцию веществ дано в избытке, а какое – в недостатке.
Из расчета видно, что Al2O3 дан в избытке, следовательно, расчет ведем по кислоте:
ЗАДАЧА 2. На 40 г оксида меди(II) подействовали раствором серной кислоты, содержащим 49 г безводного вещества. Найдите массу образовавшейся соли.
Решение
Найдем, какое из веществ, вступивших в реакцию, дано в избытке, а какое – в недостатке.
Cогласно уравнению данной реакции вещества взяты в стехиометрических количествах, поэтому расчет можно вести по любому из них: