Маб в онкологии что это
Маб в онкологии что это
После многолетних исследований mAb заняли свое место среди противоопухолевых препаратов. Это стало возможным благодаря техническим достижениям, среди которых следующие.
1. Гуманизация мышиных антител, не приводящая к образованию к ним антител у человека.
2. Получение высокоаффинных антител с использованием бактериофагов.
3. Получение антител различного размера и обладающих различным сродством, а также различной способностью проникать в ткани.
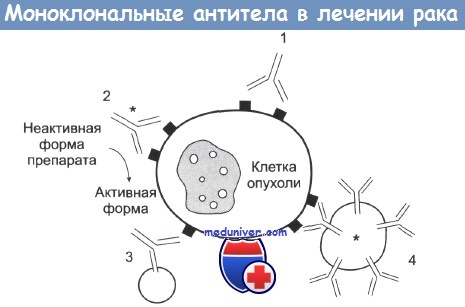
1 — антитело mAb связывается с антигеном опухолевой клетки и вызывает или ее комплемент-зависимую гибель, или гибель в результате антителозависимой атаки макрофагами.
2 — с mAb связан радиоактивный изотоп, токсин или цитокин, вызывающие гибель клетки. Также с антителами может быть связан фермент, участвующий в превращении препарата в активную форму.
3 — биспецифические mAb. Один сайт связывается с опухолевой клеткой, другой — с киллерной эффекторной клеткой.
4 — антитела mAb связаны с липосомами, которые содержат химотерапевтические препараты или токсины.
Существует много способов изменения антител для проявления у них противоопухолевого эффекта. Наиболее часто использующийся прием схематически представлен на рисунке. Подробности приведены в подписи к рисунку. Каждый из способов имеет свои возможности и ограничения.
1. Прямое цитотоксическое действие, вызываемое комплементом или антителами. При этом Fc-часть молекулы антитела должна связаться с Fc-рецептором (I или II) эффекторной клетки, но во избежание проявления ингибирующего эффекта не должна присоединяться к FcRIII. Таким механизмом цито-токсического действия обладает трастузумаб, который связывается с ERB В2 рецепторами опухоли молочной железы, а также ритуксимаб — mAb к CD20, применяющееся для лечении больных с В-клеточной лимфомой.
2. Примером mAb, доставляющих к раковой клетке токсин или радиоактивный изотоп, являются гуманизированные анти-CD33, конъюгированные с калихеамицином (гемтузумаб). Калихеамицин представляет собой агент, связывающийся с ДНК в области малой бороздки. CD33 экспрессируется на поверхности бластных клеток при остром миелоидном лейкозе. При рецидивах, устойчивых к медикаментозным препаратам, гемтузумаб вызывает ремиссию.
Подход с применением токсинов, например рицина, конъюгированных с mAb, не привел к получению клинических препаратов из-за высокой их токсичности для кровеносных сосудов. Присоединение к антителам радиоактивных изотопов (иттрия-90 или йода-131) представляет собой привлекательный путь, поскольку при этом появляется возможность воздействовать на опухолевые клетки, расположенные на некотором расстоянии от клетки-мишени. В настоящее время проходят клинические испытания aнmu-CD20, меченые иттрием-90 и анти-СЕА, меченые иодом-131.
Антитела, содержащие фермент, способный переводить лекарственный препарат в активную форму (ADEPT, antibody-dependent enzyme prodrug therapy), показали обнадеживающие результаты при лечении больных с метастазирующими колоректальными раками. Ферменты, конъюгированные с антителами, проявляют иммуногенные свойства, что ограничивает диапазон назначаемых доз.
3. Подход с использованием биспецифических антител пока еще находится на ранней стадии развития. Присоединение антител к эффекторным Т-клеткам вызывает мощный выброс цитокинов, приводящий к токсическим проявлениям. Это ограничивает применение подобных препаратов.
4. Иммунолипосомальные препараты являются эффективными средствами адресной доставки токсинов или радиоактивных изотопов к клеткам опухоли, однако получение их технически трудно. Эти препараты могут оказаться перспективными в случае, когда необходимо воздействовать на сосудистую систему опухоли.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Гормональное лечение рака предстательной железы
Рецензент материала
Профессор Капранов С.А. — Доктор медицинских наук, дважды Лауреат Государственных Премий Правительства Российской Федерации в области науки и техники, Лауреат Премии Ленинского Комсомола, автор более 350 научных работ по медицине, 7 монографий, и 10 патентов на изобретения по медицине, за 30 лет личного опыта провел более чем 10 000 различных эндоваскулярных операций
Рак простаты – один из самых акутальныхвопросов современной онкомедицины. Ключевая проблема заключается в том, что по уровню летальности злокачественные образования, формирующиеся на предстательной железе, занимают 2-3 место среди прочих видов онкологии. План лечения рака предстательной железы определяет исключительно профильный специалист. Часто обращаются к гормональной разновидности медикаментозной терапии. Подробнее о нюансах и особенностях гормонального лечения рака предстательной железы узнайте из этой статьи.
Причины появления опухолей
Однозначного ответа о том, каковы причины, по которым формируется рак предстательной железы, до сих пор не существует. Можно выделить массу провоцирующих факторов, которые статистически имеют место в жизни мужчин, страдающих от онкологии с такой локализацией. В этот перечень входит:
Внимание! Рекомендуется не только отказаться от животных жиров, но и насытить свой ежедневный рацион соей, фитоэстрогенами, изофлавоноидами, токоферолом, селеном и каротиноидами.
Показания к гормональному лечению
Не всегда гормональная терапия рака простаты является действенным методом. Дать корректное назначение может только лечащий врач, имеющий полное представление о клинической картине ведомого пациента. Востребована гормонотерапия среди мужчин, чей возраст превышает 67-70 лет. Также прибегают к гормональному типу лечения на следующих стадиях развития образования:
Статистически наибольшая эффективность у лечения рака простаты при помощи радикальной простатэктомии с полным иссечением предстательной железы. Однако оперативные процедуры не всегда возможны, как и альтернативная им терапия (химическая, лучевая). Фактически гормонотерапией пользуются как методом, который, если и не помогает излечить рак простаты, то хотя бы продлевает жизнь пациенту.
Разновидности гормонотерапии
Ранее лечение рака простаты посредством гормонального контроля заключалось в проведении двусторонней орхиэктомии (удаление яичек) – это позволяло снизить уровень тестостерона в организме (считается, что именно переизбыток этого гормона в организме является одной из причин рака предстательной железы). Современная онкомедицина исключает необходимость операции, т.к. можно использовать специальные медикаменты, понижающие уровень тестостерона до необходимого в целях лечения.
В здоровом мужском организме содержание тестостерона составляет от 300 до 1000 нг/дл. Медикаментозно этот уровень может быть понижен до 50 нг/дл, но зачастую медики стремятся к минимально возможному уровню гормона – 20-30 нг/дл. Рассмотрим подробнее, какие виды гормональных препаратов используются при лечении поражения простаты.
Агонисты ЛГРГ
Освобождающий лютеинизирующий гормон (ЛГРГ) – это пептидный гормон, направляющий химическую реакцию к мозговым клеткам, вызывая продукцию тестостерона. Агонисты данного гормона отвечают за блокировку его функций, соответственно предотвращая выработку тестостерона половой системой.
Данные медикаментозный вариант лечения является одним из самых распространенных и востребованных при борьбе с раком предстательной железы. Выпускается необходимый препарат не в таблеточном, а в жидком ампульном виде для введения через мышечные или жировые ткани, поскольку пептиды растворяются в ЖКТ, не достигая цели.
Введение препарата осуществляется раз в месяц, либо для его автоматической подачи в организм используется специальный имплантат, вводимый под кожу. В этом случае вещество поступает в организм медленно, а установленный элемент заменяется раз в полгода или год.
Стоит отметить, что в первые 3-4 недели после первичного введения агонистов ЛГРГ уровень тестостерона возрастает, вызывая обострение симптоматики рака предстательной железы. При сильном болевом синдроме или выявлении активного роста опухоли за пределы простаты врач может назначить вспомогательный курс антиандрогенов. Со временем дискомфорт и плохое самочувствие уйдут, а уровень тестостерона начнет снижаться, что и требуется для эффективного лечения.
Побочные эффекты от гормонотерапии с использованием агонистов ЛГРГ:
Крайне популярно при терапии рака с помощью агонистов ЛГРГ использовать схему дискретного дозирования. Суть такого лечения заключается в периодической приостановке введения препаратов и последующем возобновлении. Статистика показывает, что выраженность побочных эффектов при таком подходе уменьшается. Однако преимущества и эффективность такой терапии не изучены до конца.
Антагонисты ЛГРГ
В сравнении с агонистами данный вид препаратов используется крайне редко. На данный момент является изученной и производимой лишь одна форма такого медикамента для гормонотерапии – дегареликс (отечественный вариант – «Фирмагон»). В онкомедицине к нему обращаются преимущественно на 3-4 стадии развития рака предстательной железы с метастазированием в костную ткань. Медикамент позволяет предотвратить компрессию спинного мозга, вызываемую сдавливанием опухолью.
Антагонист ЛГРГ не повышает уровень тестостерона, а симптоматика, которой сопровождается рак простаты, блокируется. Первичная доза составляет 2 шприца по 120 мг, а потом 80 мг через 1 месяц. В дальнейшем процедура повторяется раз в месяц.
Зачастую побочные эффекты такой гормонотерапии:
Случаев передозировки препаратом не выявлено.
Антиандрогены
Это препараты периферического действия, которые блокируют продукцию мужских гормонов надпочечниками. Стоит отметить, что действующие компоненты антиандрогенов вызывают минимум побочных эффектов в сравнении с другими препаратами, используемыми при лечении посредством гормонотерапии. Однако эффективность данных средств снижается, если рак предстательной железы начинает распространяться в ближайшие органы и ткани.
Первичный эффект от использования в сочетании с агонистами ЛГРГ – это сильнейшее увеличение уровня тестостерона в организме, что приводит к росту предстательной железы в размерах и усложнению мочеиспускательного процесса. Если рак простаты метастазировал в костную ткань, то использование антиандрогенов усиливает болевой синдром в костях, повышает риск получения травмы, перелома или ущемления нервных окончаний.
Если же проводить гормонотерапию попеременно, сначала используя антиандрогенные медикаменты, а затем переходя на агонисты ЛГРГ, то количество побочных эффектов уменьшится. Как показывает практика, если от использования антиандрогенов нет эффекта, то временное прекращение лечения способствует улучшению самочувствия пациента. Медицинская терминология определяет для такого состояния название «андрогенное отторжение».
Эстрогены
Синтетически выведенный гормон эстроген (он является сугубо женским) может быть использован в гормонотерапии при лечении у мужчин рака предстательной железы. Снижение уровня тестостерона в этом случае происходит за счет принудительного выделения лютеинизирующего вещества гипоталамусом. Даже при допустимой дозировке в 3-5 мг эстрогеносодержащие препараты провоцируют образование хронических патологий сердечно-сосудистой системы, а также увеличивают риск сердечного приступа.
В качестве защитной меры для организма пациента в процессе лечения медики снижают дозировку до суточного приёма в 1 мг. Но при этом уже через 6-12 месяцев тестостерон вновь начинает накапливаться в организме, что сводит борьбу с раком предстательной железы на нет, если положительный эффект от проводимого лечения не был достигнут ранее.
Орхиэктомия
Если всё же врач прибегает к использованию орхиэктомии, то проводится оперативное вмешательство с иссечением яичек. На их место для сохранения эстетичности в мошонку могут быть помещены искусственные заменители (имплантаты). Подобная операция эффективно уменьшает уровень тестостерона в организме. Вся процедура занимает около 1,5 часа и небольшого реабилитационного периода вплоть до снятия швов со сделанных ранее надрезов. При всей радикальности операции у неё те же побочные эффекты, что и агонистов ЛГРГ.
Однако, как уже было сказано ранее, оперативное вмешательство – это не безальтернативный вариант. Современные медикаментозные подходы к лечению поражения предстательной железы достаточно эффективны. От них отказываются в случае нехватки финансов или продолжительного отсутствия положительных результатов. Также орхиэктомия назначается пожилым пациентам, которые не могут посещать медкабинет с целью проведения гормональной терапии (введения препаратов по графику).
Сочетанная блокировка андрогенов
Гормональная терапия при раке, проводимая по этому принципу, заключается в одновременном приёме медикаментов, воздействующих на мозговую активность и периферически на функционал надпочечников. Тестостерон не только перестаёт вырабатываться, но и прекращает действовать непосредственно в простате. Однако количество побочных эффектов от такого метода лечения превышает его положительные качества. Выраженными проявлениями зачастую являются: отсутствие сексуального желания, импотенция, понос, тошнота, дисфункция печени.
Общие побочные эффекты гормональной терапии
Помимо того, что у конкретных методов имеются собственные недостатки, стоит указать на те проявления, которые могут формироваться при приёме любых медикаментов. К ним относятся:
Однако столь широкий перечень побочных эффектов проявляется в полном объеме крайне редко. Грамотно спланированный процесс лечения, построенный на использовании оптимальных медикаментозных средств, имеет предельно высокую эффективность и даёт положительные результаты в борьбе со злокачественной опухолью. Однако полного выздоровления посредством терапии добиться крайне сложно, если быть точнее, то она должна применяться в комплексе с другими современными методами лечения.
Зачастую гормональную терапию используют для замедления интенсивности развития онкологического образования. Она необходима для контроля над онкологической патологией и сохранения привычного режима жизнедеятельности пациента. С помощью терапии можно повышать эффективность других методов, либо просто продлевать срок жизни для мужчины, чей клинический случай является бесперспективным в ракурсе полного выздоровления.
Прогноз и оценка эффективности метода
Когда онкологическое поражение только диагностируется, прогноз может быть рассчитан исходя из результатов дифференцирования выявленного новообразования (злокачественное или доброкачественное) и определения стадии его развития. Для мужчин с опухолью М1 (1-2 стадия) уровень выживаемости составляет от 28 до 53 месяцев. Для малой доли пациентов (7%), прошедших курс терапии при раке простаты, он составляет более 10 лет.
Важно! «Уровень выживаемости» – это не термин, который становится приговором. Это срок, который прошел с момента прохождения лечебного курса конкретным пациентом. По истечению данного срока он был снят с учета, потому в историю болезни записывается обозримый период жизни.
Прогнозировать перспективы развития опухоли и лечебного воздействия на неё можно, основываясь на следующие показатели:
В случае местно-распространенного развития рака выживаемость составляет более 10 лет.
Именно уровень ПСА является контрольным значением. Нормальным уровнем его понижения спустя 1,5-2 месяца после того, как было начато гормональное лечение рака предстательной железы, является значение в 1/10 нг/мл. Однако и при уровне в 5/10 нг/мл можно рассчитывать на благоприятный прогноз. Помимо контроля за уровнем ПСА многое зависит от агрессивности злокачественного образования и схематики воздействия метастазов на организм пациента.
Профилактические меры
Завершение лечебного курса – это не последняя стадия борьбы с заболеванием. В случае со злокачественными опухолями необходимо предотвращать возможный рецидив, контролируя каждый свой шаг вне стен медицинского учреждения. К набору профилактических мероприятий, которые назначаются мужчинам, прошедшим один из вышеперечисленных лечебных курсов, относятся:
Мужчина также должен быть ограждён от стресса и нервного перенапряжения. Осторожность в целях предотвращения механических повреждений также должна стать ключевым принципом жизнедеятельности.
Обращение в Центр эндоваскулярной хирургии
Медицинский центр профессора Капранова – это профильное учреждение, где помощь может получить любой онкобольной. Обращение к нашим специалистам гарантирует вам качественную диагностику с точным дифференцированием и определением стадии развития опухоли. Врачи центра находят индивидуальный подход к каждому пациенту, формируя оптимальный план лечебных курсов. При этом хирургическое вмешательство не назначается никогда, если существует возможность альтернативного подхода к борьбе с раковым образованием.
Изучите внимательно наш сайт, ознакомившись с ключевыми особенностями работы центра. Прочитайте и другие статьи, чтобы узнать о методах онкомедицины. Имейте представление о наших возможностях. Многое о нас можно узнать из отзывов других пациентов, прошедших лечебные курсы у медиков центра. Можно оставить собственный комментарий, если у вас уже сложилось впечатление о нас.
Ответственность и профессионализм – это лишь малая часть достоинств наших врачей и медперсонала. Всем обратившимся гарантируются выгодные условия и комфорт пребывания в центре. Будьте здоровы, а мы вам в этом поможем, исходя из особенностей и потребностей каждого пациента!
Основные направления деятельности центра эндоваскулярной хирургии а также другие популярные материалы:
Эмболизация маточных артерий в гинекологии
ЭМА в Москве
Эмболизация сосудов аденомы простаты
Материалы конгрессов и конференций
IV РОССИЙСКАЯ ОНКОЛОГИЧЕСКАЯ КОНФЕРЕНЦИЯ
РАЦИОНАЛЬНЫЕ ВАРИАНТЫ ГОРМОНОТЕРАПИИ РАСПРОСТРАНЕННОГО РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ.
Б.П. Матвеев, Б.В. Бухаркин.
ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России, Москва
С тех пор, как Huggins и Hodges показали гормональную зависимость рака предстательной железы, прошло уже более 50 лет, однако гормонотерапия по-прежнему остается ведущим методом лечения распространенных форм этой опухоли. Необходимо, между тем, четко понимать, что речь идет о паллиативном лечении, эффект от которого временный. При наличии отдаленных метастазов прогрессирование заболевания возникает обычно в течение первых двух лет, а продолжительность жизни после появления признаков прогрессии, как правило, исчисляется месяцами.
Стандартные методы гормонотерапии рака предстательной железы хорошо известны клиницистам, многократно обсуждались. Поэтому мы хотим остановиться лишь на некоторых современных концепциях лечения этого заболевания, которые, на наш взгляд, представляются важными. Когда начинать лечение? Что может дать монотерапия антиандрогенами в высоких дозах? Насколько необходима максимальная андрогенная блокада (МАБ)? Каковы возможности интермиттирующей терапии?
Сразу после внедрения в клиническую практику гормонотерапии начались споры об оптимальном времени ее проведения. В настоящее время гормонотерапию при распространенном раке предстательной железы стараются назначать как можно раньше в надежде на более позднее появление болевого синдрома и увеличение продолжительности жизни. Однако правильность такого подхода некоторыми исследователями (Lepor H., et al.,1982) ставится под сомнение.
Некоторые авторы предлагают альтернативную тактику лечения, исходя из того, что проведение гормонотерапии можно отложить до появления признаков прогрессирования заболевания. В этом случае лечение может позволить добиться ремиссии, и продолжительность жизни больного будет не меньше, чем при немедленном начале лечения. На основании данных рандомизированных исследований Объединенной группы исследований в урологии The Veterans Administration Cooperative Urological Research Group (VACURG) Byar D.P. делает вывод о том, что «гормонотерапия при раке предстательной железы может быть отсрочена. «. В этих работах не было выявлено неблагоприятных последствий отсроченного лечения и было отмечено, что многие больные с распространенным раком предстательной железы (по данным VACURG- 41%) умирают от сопутствующих заболеваний. Таким образом, ряд исследователей считает, что отсроченная гормонотерапия при раке предстательной железы имеет преимущества перед начатой сразу после постановки диагноза (Kirk D.,1987).
Более поздние исследования (Рабочая группа по изучению рака предстательной железы Совета по исследованиям в медицине, Англия), предварительные результаты которых были опубликованы в 1997 году, позволили авторам сделать вывод о более высокой эффективности раннего, сразу после постановки диагноза, начала гормонотерапии. Однако данные для подгрупп больных, у которых на момент постановки диагноза отсутствовали отдаленные метастазы, еще не окончательны.
Большинство методов эндокринотерапии рака предстательной железы направлено на снижение уровня тестостерона в крови путем подавления его синтеза в яичках и коре надпочечников. Возможные варианты и методы андрогенной блокады представлены в таблице.
Идеальная терапия рака предстательной железы включает блокаду действия андрогенов на клеточном уровне предстательной железы, что реализуется снижением связывания дигидротестостерона с ядерным рецептором при конкурентном торможении или снижении концентрации цитоплазматического рецептора андрогенов.
Для блокады циркулирующих андрогенов используются как стероидные, так и нестероидные антиандрогены (андрокур, флуцином, анандрон, касодекс). Эти препараты нашли широкое применение в клинической практике, их эффективность хорошо изучена и прекрасно известна клиницистам.
Из современных концепций лечения распространенного рака предстательной железы заслуживает внимание монотерапия антиандрогенами. Результаты всех исследований, в которых оценивали эффективность монотерапии антиандрогенами, предоставили убедительные доказательства активности и в целом хорошей переносимости нестероидных антиандрогенов. Важным остается вопрос, можно ли добиться повышения эффективности лечения при повышении дозы, и какова эффективность монотерапии антиандрогенами в сравнении с таким стандартным методом, как кастрация. Целью ряда международных исследований стало установление эффективности больших доз касодекса (150 мг) в монотерапии. Значительный интерес представляют результаты, приведенные Iversen P. с соавт. (1998), проведших сравнительный анализ монотерапии касодексом и кастрации (хирургической или медикаментозной). В исследование были включены 1453 пациента с распространенным раком предстательной железы Т3-4М0 или доказанным М1. Анализ проводился после 4 лет наблюдения. В результате было показано, что для пациентов без метастазов действие касодекса эквивалентно кастрации и может являться альтернативой как хирургической, так и медикаментозной кастрации. У пациентов с отдаленными метастазами продолжительность жизни была на 42 дня больше в группе кастрации. Однако анализ качества жизни продемонстрировал значительное преимущество касодекса. Так, пациенты, получавшие 150 мг касодекса, сохраняли либидо и половую потенцию, а также физическую работоспособность на достоверно более высоком уровне, чем больные подвергнутые кастрации. Эти преимущества в качестве жизни чрезвычайно важны, учитывая паллиативный характер лечения. Таким образом, некоторое уменьшение времени выживания компенсируется значительным улучшением качества жизни. Аналогичные результаты представлены и в исследованиях Р. Schellhammer (1999), F.H. Schroder (1999), G.J. Kolvenbag, A. Nash (1999) и ряда других авторов. Однако на сегодняшний день еще нет достоверных данных о преимущественной эффективности данного вида лечения по сравнению со стандартными методами.
Использование аналогов ЛГРГ (LHRH) позволило добиться эффекта кастрации медикаментозным путем. Препараты этой группы (золадекс, лейопролид, декапептил, деферелин и др.) достаточно давно и прочно вошли в арсенал гормональных средств, применяемых для лечения распространенных форм рака предстательной железы.
В лечении диссеминированного рака предстательной железы в последние два десятилетия нашло широкое распространение использование комбинации кастрации (хирургической или медикаментозной) и антиандрогенов. Такая комбинация получила название максимальной андрогенной блокады (МАБ).
Итоги многолетнего опыта применения МАБ подведены на двух международных консультациях по раку простаты (Монако,1996 и Париж,1999). Было отмечено, что в большинстве случаев применение МАБ по результатам сравнимо с кастрацией. Небольшое преимущество данный метод лечения имеет у больных с минимальным распространением болезни (единичные костные метастазы или поражение регионарных лимфатических узлов). Использование МАБ оказывает хорошее симптоматическое действие и способствует улучшению качества жизни больных, имеющих метастазы.
Однако, как при любом виде гормональной терапии, через какой-то промежуток времени МАБ теряет эффективность. В случае прогрессирования заболевания на фоне МАБ рекомендуется отменить лечение антиандрогенами, так как известен так называемый «синдром отмены антиандрогенов». После отмены антиандрогенов у 10-15% больных наступает временная стабилизация заболевания. Немаловажным аспектом, особенно для России, является экономическая сторона вопроса. Стоимость проведения МАБ очень высока, так как требует длительного применения дорогостоящих препаратов.
В последнее время появились сообщения о возможности проведения прерывистого лечения, так называемой интермитирующей блокады. Результаты рандомизированных исследований еще не получены. Однако предварительные данные свидетельствуют о том, что прерывистое назначение гормональных препаратов может длительно сохранить чувствительность к антиандрогенам и улучшает качество жизни, что связывается с восстановлением сексуальной функции и уменьшением побочных эффектов от длительного применения препаратов. При данном подходе значительно снижается стоимость лечения. Интермиттирующая блокада становится популярным методом лечения распространенного рака предстательной железы, однако, еще нет убедительных данных, что такой подход имеет преимущество в отношении продолжительности жизни по сравнению со стандартными видами лечения.
На 2-й международной консультации по раку простаты (Париж,1999) обсуждалась новая стратегия «step-up», при которой лечение начинается с монотерапии антиандрогенами, а аналоги LHRH добавляются при прогрессировании процесса (Reijke T.,1999). Все эти новые концепции пока находятся в стадии разработки, однако, они представляются прогрессивными по сравнению с принятыми стандартами.
В настоящее время большинство специалистов, занимающихся лечением больных раком предстательной железы, назначая тот или иной вид терапии, обязательно руководствуются не только стадией заболевания, но и анализом прогностических факторов, таких как уровень ПСА и динамика его изменения в процессе лечения, степень активности пациента, степень злокачественности опухоли и рядом других.
Исходя из анализа современной литературы и собственного опыта, мы рекомендуем обсудить следующую тактику первой линии лечения больных распространенным раком предстательной железы.

