Макрофаги с гемосидерином что это такое
Макрофаги в молочной и щитовидной железе
Осмотр и пальпация (ощупывание) щитовидной железы 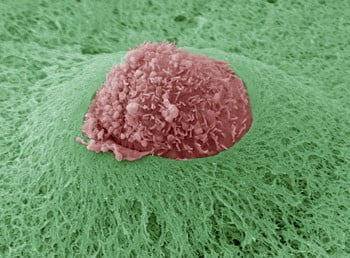
В молочной и щитовидной железе при этом можно определить уплотнения и другие изменения, которые могут быть признаком растущей опухоли. Однако не всегда узел в тканях говорит о раке. Также это может быть киста, доброкачественное новообразование и т.д. Чтобы сделать предположение о диагнозе и запланировать лечение, делают биопсию желез – добывают кусочек ткани и под микроскопом изучают его клеточный состав. Если речь идет о молочной железе, то женщинам также могут провести исследование выделений из соска. В зависимости от результатов микроскопии устанавливают, что у человека за болезнь и как ее лечить. Наличие определенных клеток во взятой пробе указывает на наличие конкретного заболевания.
В этом посте мы не будем детально описывать разные картины биоптата щитовидной и молочных желез, разберем лишь частный вопрос: присутствие в этих органах клеток-макрофагов.
Макрофаги в молочной железе:

Совершенно правильная логическая цепочка. Если в ткани молочной железы и выделениях из соска много фагоцитов, это говорит о патологии. Так, когда в препарате присутствуют нейтрофилы, макрофаги и гистиоциты (это разновидность макрофагов, находящаяся в норме в соединительной ткани), то это прямо указывает на наличие воспалительного процесса.
Перед лаборантом, изучающим добытый от пациента образец, стоит задача не только обнаружить, но и изучить строение найденных макрофагов. В них всегда немало всякого «мусора», который представляет собой остатки и фрагменты перевариваемых или уже переваренных ими агрессоров. Если удается распознать, что именно находится внутри макрофагов, это помогает понять, против чего боролись эти фагоциты, а значит, сделать вывод, что за болезнь у пациента.
Так, иногда встречаются макрофаги в молочной железе с включениями «обломков» эритроцитов и гемосидерина (гемосидерин – один из конечных продуктов разрушения гемоглобина). Если макрофаги с гемосидерином находят в препарате, это говорит о присутствии в железе полости, внутри которой находится кровь. Последнее встречается при посттравматических изменениях, при некоторых формах мастопатии.
Макрофаги в щитовидной железе:
Макрофаги и нейтрофилы в щитовидной железе также в большом количестве обнаруживаются при заболеваниях. Довольно распространена такая патология этого органа как киста. Сделав пункцию (прокол) кисты, специалисты получают жидкость. В ней мало клеток, среди них преобладают макрофаги с гемосидерином – их еще называют сидерофагами.
Также макрофаги в щитовидной железе могут встречаться при других заболеваниях, например, при воспалительном процессе. Однако при аутоиммунном тиреоидите, который является основным воспалительным заболеванием этого органа, таких фагоцитов в биоптате немного – в железе преобладают лимфоциты, а другие иммунные клетки встречаются реже.
Итак, присутствие большого количества макрофагов в описанных 
Кстати, когда речь идет о выздоровлении, важно не только непосредственно воздействовать на причину болезни (онкологический, воспалительный, дисгормональный процесс), но и уделять внимание поддержке иммунной системы, частью которой являются пресловутые макрофаги. Прием препарата Трансфер Фактор позволяет нормализовать деятельность иммунитета и помочь макрофагам в осуществлении их благого дела – борьбы с возбудителями заболеваний и другими вредоносными факторами.
Регулярная терапия этим средством может помочь выздороветь от большинства заболеваний молочной и щитовидной желез, а при профилактическом приеме предупредить их появление. При устойчивой и слаженной работе всех звеньев иммунитета, что достигается благодаря Трансфер Фактору, риск заболеть аутоиммунными, воспалительными и даже онкологическими процессами этих органов многократно уменьшается.
Гемосидероз
БЕСПЛАТНАЯ КОНСУЛЬТАЦИЯ: поможем врачам и владельцам клиник выбрать оборудование для лечения гемосидероза
Оглавление
Гемосидерозы кожи (поттравматические гемосидерозы, пигментные капилляриты, геморрагически-пигментные дерматозы, пигментные пурпурные дерматозы) — это состояние, возникающее после травмы с попаданием крови в мягкие ткани (появлением гематомы), либо в результате заболеваний, общим проявлением которых является отложение гемосидерина в коже.
В нашей компании Вы можете приобрести следующее оборудование для лечения гемосидерозов кожи:
Гемосидерин представляет собой пигмент темно-желтого цвета, состоящий из оксида железа. Он образуется при распаде двух белков — гемоглобина и ферритина, например после попадания крови в ткани организма. Это может происходить после травмы (ушиба, инъекции), когда под кожей формируется гематома. Макрофаги не всегда успевают утилизировать «подкожную» кровь, в результате чего в области повреждения начинает скапливаться гемосидерин. Он формирует довольно стойкие локальные изменения окраски, которые могут вызывать эстетический дискомфорт у пациентов.
Гемосидерозами также являются следующие заболевания:
Ниже будет сделан упор на наиболее часто встречающихся состояниях и патологиях.
Этиология и патогенез
Посттравматический гемосидероз
Его появлению предшествует травма — ушиб, инъекция, надрез кожи и др. В результате кровь попадает в мягкие ткани, где происходит окисление гемоглобина и ферритина с последующим накоплением гемосидерина. Другими причинами и предрасполагающими факторами являются:
Пигментный прогрессирующий дерматоз Шамберга
Впервые описан в 1901 году английским дерматологом Джеем Франком Шамбергом. Основной причиной дерматоза считается повышенная проницаемость мелких сосудов и капилляров, располагающихся у поверхности кожи, через которые могут проходить эритроциты. Попав в ткани, они разрушаются, в результате чего из эритроцитов высвобождается гемоглобин и в дальнейшем — железо. Оно постепенно накапливается в определенной области, формируя специфический оттенок кожи.
Кольцевидная телеангиэктатическая пурпура Майокки
Описана итальянским дерматологом Доминико Майокки в конце XIX века. Этиологию заболевания связывают с несколькими факторами: повышение артериального давления, нарушение кровообращения в ногах, хронический спазм мелких сосудов, диапедез (просачивание) форменных элементов крови в ткани.
Лихеноидный пурпурозный пигментный дерматит Гужеро-Блюма
Описан дерматологами Генри Гужеро и Полом Блюмом в 1925 году. Точная причина заболевания неизвестна, определенную роль играет венозная гипертензия, системные болезни, инфекции, прием разжижающих кровь лекарственных препаратов, повышенная ломкость капилляров и др.
Экзематидоподобная пурпура Дукаса-Капетанакиса
Этиология неизвестна. Возможно участие в патогенезе повышенной проницаемости мелких сосудов с последующим диапедезом форменных элементов крови.
Клинические проявления
Посттравматический гемосидероз
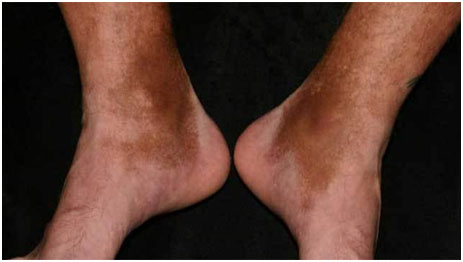
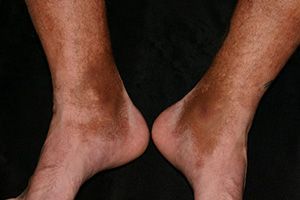
Пятна могут быть любого размера и формы, цвета от желтого до коричневого или черного. Они возникают в любой области тела (даже вокруг глаз), но чаще на нижних конечностях (рис. 1).
Пигментный прогрессирующий дерматоз Шамберга
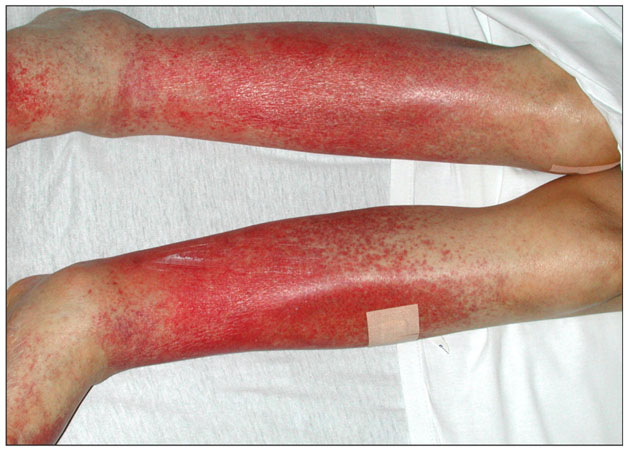
Проявляется в виде точек красно-коричневого или желто-бурого оттенка диаметром в несколько миллиметров, которые сам Шамберг сравнивал с размолотыми зернами кайенского перца. Эти точки чаще всего расположены на ногах, но могут встречаться и на других участках тела (рис. 2). Высыпания несколько возвышаются над поверхностью кожи и со временем могут сливаться в более крупные элементы неправильной формы. Постепенно они бледнеют, а на их месте формируются очаги кожной атрофии. Субъективные ощущения отсутствуют, в редких случаях может присутствовать небольшой зуд в области поражений.
Кольцевидная телеангиэктатическая пурпура Майокки
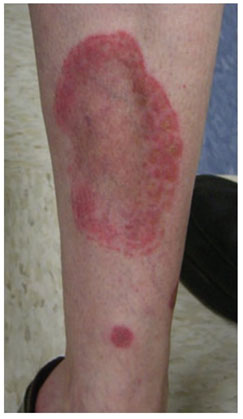
На коже появляются розоватые или красноватые пятна неправильной формы диаметром от одного до нескольких сантиметров. По мере их роста края пятен становятся более темными, а центр, наоборот, светлеет (рис. 3). Постепенно в центральной части развивается атрофия кожи с выпадением мелких волос. Субъективные ощущения отсутствуют.
Лихеноидный пурпурозный пигментный дерматит Гужеро-Блюма
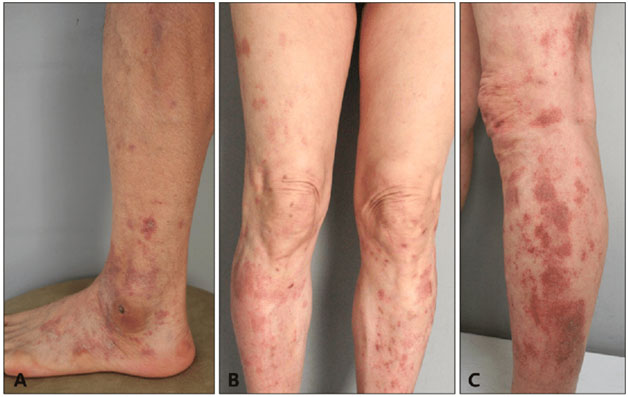
Характеризуется появлением небольших лихеновидных узелков с мелкими высыпаниями среди них. Отмечается точечное расширение мелких подкожных сосудов с локальным потемнением кожи из-за гемосидероза (рис. 4А). Типичная локализация — в нижней части ног, реже на бедрах и туловище.
Экзематидоподобная пурпура Дукаса-Капетанакиса
На коже голеней появляются отдельные петехии со склонностью к объединению в крупные пятна. Сперва они красного цвета, но постепенно становятся желтыми или коричневыми, бледнеют и со временем могут исчезнуть. Иногда поражения переходят на бедра, туловище и руки (рис. 4В,С). Дополнительно отмечаются явления паракератоза, зуд и гиперпигментация.
В табл. 1 представлены наиболее часто встречающиеся гемосидерозы и основные различия между ними.
Табл. 1. Дифференциальный диагноз наиболее часто встречающихся гемосидерозов кожи
Характеристика
Посттравматический гемосидероз
Пурпура Майокки
Дерматоз Шамберга
Дерматит Гужеро-Блюма
Пурпура Дукаса-Капетанакиса
Частота встречаемости
Самый частый тип гемосидерозов
Пик заболеваемости
В любом возрасте, но по мере старения организма вероятность растет
Подростки и молодые люди
Люди среднего возраста
Динамика поражений
Поражения возникают в месте предшествующей травмы. Чаще они бывают на ногах вследствие эндокринных патологий, нарушений работы венозной системы и других факторов
Поражения возникают сперва симметрично на ногах, далее могут распространяться на туловище и руки
Поражения чаще всего образуются симметрично в области голеней, но могут быть и только на одной ноге. Болезнь может затрагивать область бедер, ягодицы, туловище или руки
Чаще в нижней части ног и очень редко — бедрах и на туловище
На ногах, постепенно переходя на бедра, туловище и руки
Клинические проявления
Пятна различного размера и формы, цвета от желтого до коричневого или черного
Различное число кольцевидных эритематозных бляшек и пятен, часто с побледнением и атрофией в центре
Отдельные красно-коричневые пятна, не выступающие над кожей и выглядящие как зерна молотого кайенского перца
Мельчайшие лихеноидные папулы с тенденцией к объединению в крупные бляшки различного оттенка
Поражения, как правило, обширны. Пациенты жалуются на сильный зуд
Гистология
Расширение капилляров в сосочковом слое дермы, диапедез, пролиферация эндотелия капилляров с отложением гемосидерина в виде глыбок в межуточном веществе, гистиоцитах, эндотелиальных клетках. Незначительный неспецифический периваскулярный инфильтрат
Периваскулярная лимфоцитарная инфильтрация, которая распространяется на эпидермис. Вакуолярное изменение базального слоя, спонгиоз. Выявляются нагруженные гемосидерином макрофаги, внутри лихеноидного инфильтрата отмечается экстравазация эритроцитов
Периваскулярная мононуклеарная инфильтрация в верхней дерме, отек сосудистого эндотелия. Наличие экстравазальных эритроцитов и нагруженных гемосидерином макрофагов
Периваскулярная лимфоцитарная инфильтрация. Лихеноидная тканевая реакция. Отек эндотелия и сужение просвета мелких сосудов
Спонгиоз (отек шиповатого слоя эпидермиса) с воспалительными изменениями
Вероятность ремиссии
Течение чаще хроническое, но возможна спонтанная ремиссия
Возможна как спонтанная ремиссия, так и внезапное обострение заболевания
Лечение
Топические кортикостероиды, аппаратные методики
Заболевание является врожденным и проходит самостоятельно. Однако через некоторое время поражения могут появиться снова
Системные кортикостероиды, антигистаминные препараты, витамин С, ПУВА-терапия (см. ниже)
Терапия затруднена. Используются топические и системные кортикостероиды, антигистаминные и противозудные препараты. Рекомендовано ношение компрессионного трикотажа. Возможно применение ПУВА-терапии (см. ниже), гризеофульвина, циклоспорина А, витамина С и биофлавоноидов
Топические кортикостероиды и антигистаминные препараты
Рис. 1. Посттравматический гемосидероз на ногах (www.healthline.com; Photo: MavCure)
Рис. 2. Пигментный прогрессирующий дерматоз Шамберга (Chatterjee S. Schamberg disease: uncommon reaction to a common drug. CMAJ 2009; 181(12): E275)
Рис. 3. Кольцевидная телеангиэктатическая пурпура Майокки — в центре крупного очага заметна область осветления кожи (Hoesly F. J., et al. Purpura annularis telangiectodes of Majocchi: case report and review of the literature. Int J Dermato 2009; 48(10): 1129–1133)
Рис. 4. Дерматит Гужеро-Блюма (А) и пурпура Дукаса-Капетанакиса (В, С) (Kim D.H., et al. Characteristics and clinical manifestations of pigmented purpuric dermatosis. Ann Dermatol 2015; 27: 404–410)
Принципы лечения
На сегодняшний день считается, что ни одно лекарственное средство не имеет 100-процентной доказательной базы по эффективности при гемосидерозах. Таким образом, лечение этих болезней представляет собой проблему и является вызовом для врачей. При этом некоторые гемосидерозы могут проходить самостоятельно, а затем неожиданно рецидивировать.
В снижении воспаления и подавлении зуда при некоторых гемосидерозах эффективны кортикостероидные средства. Антигистаминные препараты угнетают эндогенную выработку гистамина и также снижают ощущение зуда у пациентов.
Определенную пользу несет назначение гризеофульвина, циклоспорина А, витамина С и биофлавоноидов. Есть данные о положительном влиянии ПУВА-терапии (psoralen (P) + ultraviolet A (UVA) = PUVA или ПУВА) — облучении кожи ультрафиолетом спектра А с предварительным приемом фотосенсибилизатора (псоралена) для большей эффективности светового воздействия.
В комплексной терапии гемосидерозов, особенно локальных подкожных отложений гемосидерина, вызванных предшествующей гематомой, могут применяться аппаратные методики, направленные на избирательное разрушение пигмента. Для локальной деструкции гемосидерина в эстетических целях может использоваться IPL-терапия: метод, при котором высокоинтенсивный импульсный свет разрушает пигмент, делая его более доступным для эвакуации в ходе фагоцитоза.
Гемосидероз
Гемосидероз (капиллярит, геморрагический пигментный дерматоз) – болезнь из разряда пигментных дистрофий, связанная с нарушением процессов обмена и избыточным накоплением гемосидерина в тканях и сосудах. Поражаются кожные покровы и внутренние органы. Отложения гемоглобиногенного пигмента могут быть распространенными либо местными. Установление природы заболевания затруднительно. Лечением занимаются дерматологи, пульмонологи, гематологи, иммунологи и другие специалисты.
Генерализованный гемосидероз
Общий или распространенный капиллярит характеризуется накоплением железосодержащего пигмента в структурах костного мозга, в клетках селезенки и печени. Ткани и органы приобретают буро-красный цвет. Пигментные изменения обусловлены системными процессами, следствием которых является эндоваскулярный (внутрисосудистый) гемолиз клеток крови.
Локальный гемосидероз
Местный капиллярит развивается из-за внесосудистого гемолиза эритроцитов. Гемосидерин накапливается в очаге кровоизлияний с образованием гематом в пределах кожи, легкого, печени, почек. Если депонирование железосодержащего пигмента влечет нарушение работы органа, развивается гемохроматоз.
Отдельные формы заболевания:
О причинах развития гемосидероза
Гемосидероз кожи может быть первичным и вторичным, развивающимся из-за повреждений и кожных инфекций.
Причинами первичного капиллярита кожи могут быть следующие факторы:
Вторичный гемосидероз дермы может быть обусловлен:
К факторам риска, способным спровоцировать развитие недуга, относят:
Генерализованный гемосидероз развивается на фоне предшествующих заболеваний. Чаще всего основными причинами являются системные заболевания крови, аутоиммунные болезни, тяжелые интоксикации и воздействие инфекционных агентов. Увеличенное депонирование гемосидерина может быть обусловлено:
Почему железосодержащий пигмент накапливается в легких – не вполне понятно. Часто причины кроются в генетической предрасположенности, во врожденной аномалии легочных капилляров, в имеющихся сердечных заболеваниях.
Характерные симптомы
Клинические проявления зависят от того, где накапливается гемоглобиногенный пигмент.
Гемосидероз легких
Идиопатический (первичный) гемосидероз легких проявляется следующими признаками:
Бурая пурпура легких, как правило, встречается в детском и в молодом возрасте, является серьезным заболеванием. При затяжном течении болезни очень часто развиваются рецидивирующие инфаркт-пневмонии и другие патологии.
Гемосидероз кожи
Характерны следующие симптомы:
Хронический гемосидероз дермы обычно диагностируют у мужчин старше 30 лет. Заболевание протекает без поражения внутренних органов.
Пурпурозно-пигментный дерматоз печени проявляется увеличением органа, его болезненностью, желтушностью покровов, наличием пигментной сыпи на руках, в области подмышек, на лице. При поражении почек появляется отечность в ногах, диспепсия, изменения вкуса, боли в пояснице и пр.
Наши врачи
Диагностика
Врач-дерматолог осматривает пациента, исследует характер высыпаний, наличие характерных признаков. Обязательно проводятся лабораторные исследования – биохимия крови с определением уровня железа, общие анализы мочи, ПЦР-тесты. Анализируется содержание мокроты и мочи с проведением десфералового теста. Для уточнения диагноза пораженные сегменты направляют на биопсию. Гистологические исследования кожных покровов, костного мозга, легких, лимфатических тканей, печени, почек помогают обнаружить отложения пигмента. С целью диагностики может проводиться бронхоскопия с исследованием промывных вод, делается рентген грудной клетки, МРТ, компьютерная томография.
Лечебная тактика гемосидероза
Лечение назначается врачом-дерматологом и зависит от клинических проявлений и тяжести заболевания.
В тяжелых случаях врачи проводят спленэктомию, пациентам удаляют селезенку, чтобы добиться стойкой ремиссии. Прибегают к гемотрансфузии, PUVA-терапии, назначают препараты, способствующие выведению железа из организма.
Осложнения
Если пациент с капилляритом не получает должного лечения, то формируются опасные осложнения, способные привести к инвалидизации и летальному исходу. Особенно трудно поддается лечению запущенные формы гемосидероза легких, когда патологический процесс затрагивает альвеолы.
Гемосидероз кожи отличается благоприятным течением. При запущенных формах заболевания появляются косметические дефекты, которые требуют должной коррекции.
Профилактика
Рекомендации общие, так как механизм развития болезни изучен не до конца и не всегда удается установить причины гемосидероза.
Функции макрофагов в различных условиях микроокружения опухоли
Связанные с опухолью макрофаги, как известно, стимулируют ключевые этапы прогрессирования опухоли. В этом обзоре рассказывается о многочисленных экспериментальных и клинических исследованиях, проведенных с целью изучения функций, регуляции и клинической значимости опухолевых макрофагов. В отношении клинической значимости наиболее интересны три участка инвазии раковых клеток: опухолевые гнезда, пограничная зона между стромой и опухолевыми клетками, а также области, близкие к сосудистой сети опухоли или удаленные от нее. Более полное понимание разнообразия опухолевых макрофагов может привести к разработке избирательных методов лечения, основанных на восстановлении противораковых функций этих клеток.
Вступление
Опухолевые макрофаги (ОМ) изобилуют в большинстве типов злокачественных новообразований, способствуют опухолевому ангиогенезу, выходу раковых клеток из опухоли в кровоток, способствуют их выживанию и постоянному росту в метастатических колониях, подавлению противоопухолевых иммунных механизмов. В то же время ОМ могут подавлять, дополнять или опосредовать противоопухолевые эффекты цитотоксических агентов, лучевой терапии, антиангиогенных препаратов и ингибиторов контрольных точек.
Происхождение этих клеток в настоящее время является предметом обсуждения. Недавние исследования показали, что макрофаги во многих тканях происходят не из циркулирующих моноцитов, как первоначально предполагалось, а из эмбриональных макрофагов (особенно из макрофагов желточного мешка), которые закладываются в тканях во время развития. Эти предшественники остаются в тканях взрослого организма и размножаются, таким образом, сохраняясь независимо от гемопоэтической системы взрослого человека. В некоторых органах, например, в кишечнике, основные популяции макрофагов развиваются путем рекрутирования моноцитов. Выборочное истощение каждого из этих двух подтипов ОМ показало, что только эмбриональные макрофаги поддерживают опухолевый рост.
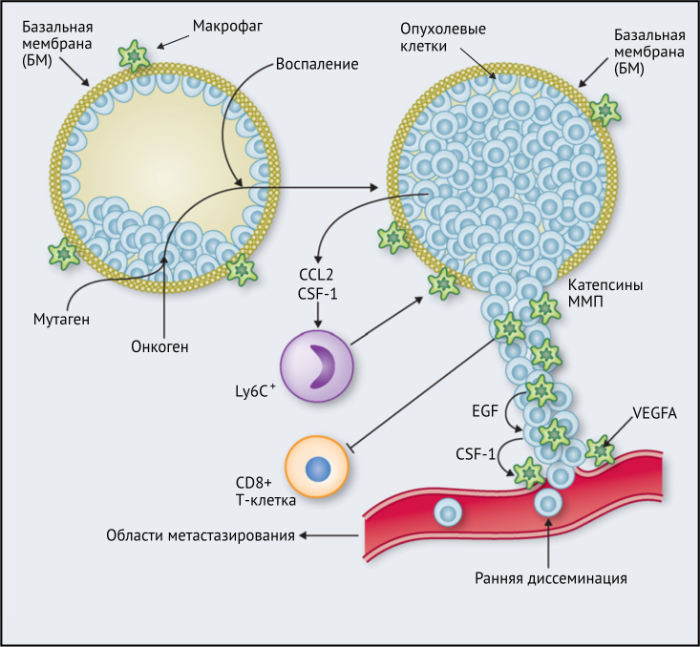
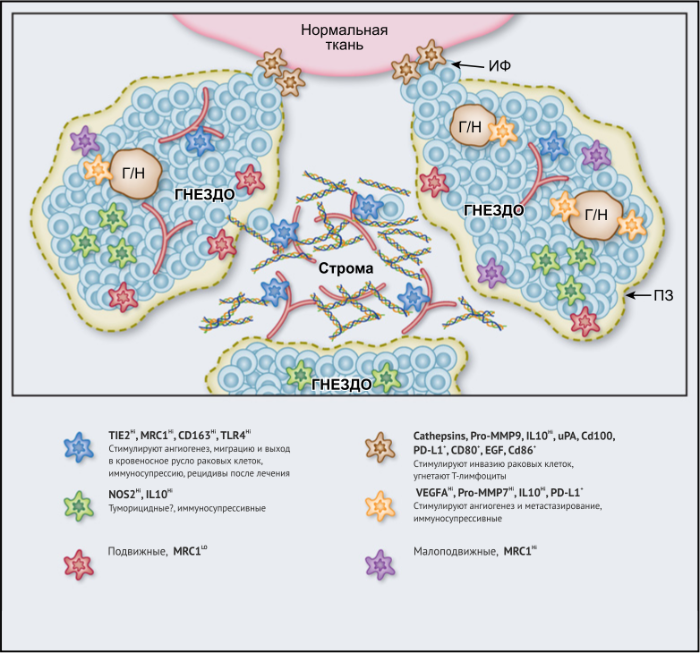
ОМ могут находиться в различных состояниях активации. Обычно они отклоняются от «классически» активированного, агрессивного по отношению к опухоли фенотипа (иногда называемого M1) в сторону «альтернативно» активированного опухолевого промотора (M2). Однако как и макрофаги во многих других тканях, ОM обладают замечательной функциональной пластичностью и часто экспрессируют маркеры, характерные для обоих состояний активации, что делает такой полярный подход к их классификации неточным. Предполагается, что функции ОМ могут, по крайней мере частично, регулироваться их расположением в опухоли; что они проявляют разные функции по меньшей мере в трех областях инвазии раковых клеток: области высокой плотности раковых клеток (так называемом «опухолевом гнезде»); периваскулярной (ПВ) нише; и плохо васкуляризованных гипоксических/некротических областях опухоли (Рис.1 и 2).
Области инвазии
Существует по крайней мере три основных локализации, в которых прогрессия опухоли была ассоциирована с повышенной инвазией клеток.
Результаты исследований, проведенных на мышах, показывают, что макрофаги способствуют развитию злокачественных опухолей различными способами: реконструируют внеклеточный матрикс, опосредуют разрушение базальной мембраны, увеличивают подвижность раковых клеток, и их способность к миграции, способствуют прогрессированию преинвазивных поражений, выделяют фактор роста эндотелия сосудов A (VEGF-A). Макрофаги вокруг преинвазивных поражений молочных желез у мышей высвобождают CXCR2-связывающие хемокины CXCL1 и CXCL5, которые способствуют миграции и инвазии соседних предростопластических (предраковых) эпителиальных клеток. В то же время подавление активности макрофагов вызывало замедление развития инвазии опухолевых клеток и развития опухоли в целом.
Недавнее исследование на модели рака легких Kras G12D показало, что нарушение регуляции онкогенов, таких как Myc, в раковых клетках вызывает трансформацию медленно прогрессирующей аденомы легкого в агрессивную аденокарциному. Это связано с тем, что изменения в Myc стимулировали увеличение экспрессии CCL9 и IL-23 эпителиальными клетками легких. CCL9 затем стимулировал накопление VEGFA + макрофагов и, следовательно, ангиогенез опухоли, а также PD-L1-зависимое вытеснение T- и B-клеток. Кроме того, IL-23 стимулировал гибель Т- и В-клеток и цитотоксических NK-клеток (Рис.1).
Следует отметить, что антитела против CD68 продолжают широко использоваться в качестве иммунных меток ОМ в опухолях (Таблица 1). Однако как и многие другие антитела, маркирующие отдельные типы клеток, человеческие анти-CD68 иногда маркируют клетки, отличные от ОM. Например, методом качественного анализа с помощью иммуноокрашивания удалось установить, что некоторые клетки CD68 + в опухолях молочной железы человека не экспрессируют рецептор к КСФ-1 (КСФ-1Р), CD45 или другие маркеры эпителиальных клеток, эндотелиальных клеток или клеток стенок сосудов (то есть гладкомышечных клеток, перицитов или фибробластов). Остается неизвестной как принадлежность этих клеток, так и то, маркируются ли они антителами к CD68 иного происхождения.
ОМ в ИФ опухоли поджелудочной железы RIP1-Tag2 мыши усиливают инвазивный потенциал раковых клеток посредством экспрессии катепсинов B и S, двух ферментов, регулируемых IL-4, высвобождаемым раковыми клетками и инфильтрирующими опухоль Т-клетками. Кроме того, было показано, что CD4 + Т-клетки в опухолях MMTV-PyMT увеличивают инвазивность раковых клеток благодаря IL-4, что затем стимулирует ОM экспрессировать эпидермальный фактора роста (EGF).
Эти экспериментальные данные хорошо согласуются с данными исследований, согласно которым ОM в ИФ опухолей желудка человека выделяют MMP9 — фермент, разрушающий матрикс, — и рецептор сериновых протеаз, урокиназный активатор плазминогена (УАП, урокиназа). Интересно, что ОМ вдоль ИФ первичной карциномы толстой кишки экспрессируют CD80 и CD86 (костимуляторные сигналы, необходимые для активации Т-клеток), что указывает на то, что они могут иметь потенциал для стимулирования противоопухолевого иммунитета при этом типе рака. Это может объяснить наблюдение, что повышенное количество CD68 + ОM в ИФ колоректальных опухолей человека коррелируют с более высокой выживаемостью без рецидива (RFS) (Таблица 1). Тем не менее, в ИФ опухолей могут присутствовать различные ОM-подмножества, причем некоторые из них являются иммуносупрессивными. Например, ОM в ИФ гепатоцеллюлярных карцином (ГЦК) экспрессируют более высокое количество лиганда иммуносупрессивной контрольной точки PD-L1, чем ОМ в других опухолевых гнездах, и связаны с плохой выживаемостью. Кроме того, было показано, что семафорин 4D (SEMA4D, CD100) — цитокин, экспрессия которого особенно выражена в ИФ опухоли толстой кишки Colon26, стимулирует ОM, которые экспрессируют иммуносупрессивный цитокин IL-10 в ИФ, и таким образом подавляют активированные CD8 + Т-клетки. Блокада антител SEMA4D подавляла ОМ в ИФ и повышала эффективность лечения ингибиторами контрольных анти-PD-1 и анти-CTLA4 (Рис.2).
Опухолевые гнезда
Возможные функции ОМ в непосредственной близости от раковых клеток в опухолевых «гнездах», по-видимому, варьируются в зависимости от типа опухоли. Например, ОM, экспрессирующие NOS2 — фермент, связанный с их цитотоксическим потенциалом, — обнаруживаются в тесном контакте с раковыми клетками в некоторых опухолях предстательной железы, а большое количество ОM в опухолевых гнездах коррелирует с улучшенным прогнозом при раке эндометрия, а также снижением количества рецидивов рака желудка (Таблица 1). Повышенное количество ОM коррелирует с уменьшенной общей выживаемостью и RFS при злокачественных меланомах, а также опухолях молочной железы и пищевода (Таблица 1). ОМ в гнездах ГЦК человека экспрессируют IL-10 и рекрутируют иммуносупрессивные клетки FoxP3 + Treg, хотя нет данных, что эти Treg влияют на исход заболевания (Рис. 2).
Интересно, что ОМ экспрессируют сигнальный регуляторный белок альфа (SIRP-α) на своей поверхности, который связывается с трансмембранным белком CD47 на злокачественных клетках. Когда это происходит, подавляется способность ОM обнаруживать и фагоцитировать опухолевые клетки. Различные исследования показали, что блокирование CD47 прерывает этот сигнал «не ешь меня» и вызывает разрушение опухолей при посредстве ОM у мышей, а высокая экспрессия CD47 обуславливает плохой прогноз рака мочевого пузыря, острого миелоидного лейкоза, неходжкинских лимфом и рака молочной железы. Так опухолевые клетки уклоняются от наблюдения ОМ.
Строма
В области стромы большинства солидных опухолей опухолевых клеток обычно мало либо нет вовсе. Она состоит из сложной сети макромолекул, формирующих внеклеточный матрикс(ВКМ), к которым относятся коллагеновые фибриллы, ламинин, фибронектин, тенасцин C и гиалуроновая кислоту (ГК). В нем часто находятся популяции различных клеток, включая фибробласты, эндотелиальные клетки, перициты, лимфоциты и миелоидные клетки. Ряд исследований показал, что компоненты ВКМ (и/или продукты его протеолиза), такие как фибронектин, ламинин-10, версикан (хондроитинсульфатсодержащий протеогликан) и фрагменты ГК, регулируют фенотип макрофагов. Пинто и его коллеги в исследованиях in vitro показали, что бесклеточный ВКМ, выделенный из колоректальных опухолей, стимулирует макрофаги экспрессировать IL-10, TGF-β и снижает экспрессию рецепторов хемокинов C-C 7 (CCR7), TNF-α и IL-6. Кроме того, повышенная экспрессия стромальными ОМ лигандов хемокинов C-C 18 (CCL18) связана с повышенным метастазированием и снижением выживаемости у пациентов при раке молочной железы. Это согласуется с рядом исследований, свидетельствующих о корреляции между большим количеством стромальных ОМ и низкой общей выживаемостью и RFS при опухолях молочной железы, пищевода, желудка, поджелудочной железы, орофациальных, кожных (Таблица 1). Существует зависимость от типа опухоли, поскольку такой корреляции при раке эндометрия, шейки матки и легких не выявлено, а при раке мочевого пузыря прослеживается уменьшение метастазирования в лимфатических узлах и улучшение выживаемости (Таблица 1).
Помимо описанных выше химических компонентов стромы опухоли, функции ОМ также регулируют ее биофизические свойства. Архитектоника и плотность ВКМ регулирует экспрессию различных провоспалительных генов макрофагами in vitro путем активации сигнальных путей TLR4 в этих клетках. Высокие уровни 22 общих составляющих матрикса («меток матрикса») положительно коррелируют как с плотностью опухоли, так и с инфильтрацией ОМ при метастазах рака яичников, хотя еще предстоит выяснить, есть ли причинно-следственная связь между инфильтрацией и структурой опухоли. Также следует отметить, что разные области стромы при данной опухоли могут различаться по своим химическим и биофизическим свойствам и влиять на ОМ по-разному (Рис. 2).
Периваскулярная ниша
Подмножество ОМ лежит близко или на поверхности кровеносных сосудов в опухолях мышей и человека. Эти клетки часто экспрессируют большое количество маркеров, связанных с M2: TIE2 (основной рецептор ангиопоэтина), MRC1 и CD163, — и играют ключевую роль в стимулировании ангиогенеза опухоли, метастазирования и рецидива после терапии первой линии. Из-за их относительно высокой экспрессии TIE2 эти клетки первоначально назывались «TIE2-экспрессирующие моноциты/макрофаги (TEM)». Частота TEM также положительно коррелирует с плотностью микрососудов (MVD) у некоторых типов опухолей человека (Табл. 1).
Генетическая делеция периваскулярных (ПВ) TIE2 + ОМ или фармакологическая блокада основного лиганда TIE2 — ангиопоэтина 2 (AGPT2), — продемонстрировали важную роль этого подмножества ОM в ангиогенезе опухоли и ее росте у различных мышиных моделей рака. Стимуляция экспрессии генов TEM, выделенных из опухолей мыши, привела к более высокой экспрессии ряда генов, способствующих развитию опухолей, включая Mmp9, Vegfa, Cxcl12, Tlr4 и Nrp1, чем TIE2- ОM из тех же опухолей.
ПВ TIE2 + ОM также участвовали в рецидиве первичных опухолей мыши после различных форм лечения. Они учащают рецидивы глиомы после местного облучения, а также при опухолях легких и молочной железы после химиотерапии. В такие моменты они экспрессируют большое количество CXCR4 и рекрутируются с помощью активированного CXCL12 в ПВ нише. Это подмножество ОМ затем стимулирует реваскуляризацию и рост опухоли посредством высвобождения VEGF-A. Позднее исследование подтвердило, что экспрессия TIE2 в ОМ необходима для стимуляции васкуляризации после химиотерапии у мышей. Кроме того, недавно рекрутированные моноциты также мигрируют вокруг опухолей, не подвергавшихся терапии, зависимым от CXCR4 образом. Меченые моноциты проникали в ПВ зону опухоли PyMT, где они затем подвергались воздействию TGFβ, выделяемого раковыми клетками, что стимулировало эти моноциты повышать свою экспрессию CXCR4 и мигрировать к CXCL12-экспрессирующим фибробластам вокруг опухолевых кровеносных сосудов в богатых коллагеном стромальных областях. Как только они примыкают к сосудам, моноциты дифференцируются в «метастаз-ассистирующие» ПВ ОM, участвующие в TMEM.
Наконец, в метастатических областях, таких, как легкие, подмножество макрофагов CCR2 + Ly6C + способствует выходу раковых клеток в кровеносное русло и образованию из них метастазов. Эти «метастаз-ассоциированные макрофаги» (MAM) были использованы в мышиных моделях опухолей, чтобы напрямую связать молекулу адгезии сосудистых клеток-1 (VCAM-1) с раковыми клетками через их α4-интегрины. Этот процесс впоследствии увеличивает выживаемость раковых клеток в таких метастатических областях. Кроме того, связывание CCL2 с CCR2 на MAM стимулирует высвобождение ими CCL3, который связывается с CCR1 на раковых клетках и облегчает их удержание в легких. Эти MAM также способствуют постоянному росту метастатических повреждений с помощью сигналов VEGFR1 и CSF-1R.
Гипоксические/некротические области
Гипоксия является отличительной чертой солидных опухолей и связана с увеличением инвазии и метастазов, сопротивлением терапии и плохим клиническим исходом. Гипоксические области обычно имеют парциальное давление кислорода (рО2) ниже 10 мм рт. ст. Они расположены более чем в 150 мкм от опухолевых кровеносных сосудов. Они образуются в опухолях, когда потребность клеток в кислороде опережает их снабжение плохо организованными опухолевыми сосудами. Эти области были идентифицированы в опухолевых срезах с использованием маркеров гипоксических клеток, например, пимонидазола, или иммуноблока для индуцируемой гипоксией альфа-субъединицы транскрипционных факторов HIF 1 и 2. Большое количество гипоксических ОМ ассоциируется с повышенным уровнем ангиогенеза опухолей, метастазами, сниженной RFS и/или снижением общей выживаемости при раке молочной железы, эндометрия и шейки матки (Таблица 1).
ОM в таких областях регулируют HIF 1 и 2 и различные гены-мишени HIF, такие как VEGF-A, GLUT1 и MMP7. Хемокины, усиливающие гипоксию, рекрутируют в гипоксические области ОМ, в том числе хемокин C-X-C 12 (CXCL12), полипептид-активирующий эндотелий-клеточный моноцит II (EMAP-II), эндотелин 2, VEGF-A и SEMA3A. Гипоксические ОМ иммобилизируются в этих областях прямым ингибирующим действием гипоксии на их подвижность и снижением экспрессии их рецепторов опухолевых хемокинов CCR2, CCR5 и NRP1.
Гипоксические ОМ способствуют ангиогенезу опухоли, уклонению от иммунитета и метастазированию в различных экспериментальных моделях. Например, они регулируют экспрессию большого количества проангиогенных и иммуносупрессивных цитокинов в гипоксических зонах опухоли, а когда их проникновение в гипоксические области опухолей затруднено сигнальной блокадой SEMA3A/NRP1, опухолевый ангиогенез заметно снижается и противоопухолевый иммунитет восстанавливается. Гипоксические ОМ также способны подавлять активацию Т-клеток различными способами, влияя на IL-10 и на контрольные точки, например, через лиганд PD-L1. Макрофаги, кокультивированные с клетками ГЦК в гипоксических условиях, увеличивают экспрессию индоламин 2,3-диоксигеназы (IDO), которая подавляет пролиферацию местных цитотоксических Т-клеток и увеличивает популяцию клеток Treg.
Хотя воздействие гипоксии само по себе не может изменить фенотип ОМ в отношении стимуляции роста опухоли, некоторые исследования показали, что низкий уровень рН и лактат (которые накапливаются в слабо васкуляризированных, гипоксических областях из-за плохого сосудистого питания) совместно индуцируют проангиогенный фенотип ОМ, который, в свою очередь, восстанавливает перфузию крови. Действительно, молочная кислота может стимулировать экспрессию VEGF-A макрофагами. Как упоминалось ранее, этот цитокин является не только проангиогенным в опухолях, но также способен стимулировать выход в сосуды раковых клеток.
Опухолевая гипоксия также может модулировать функции ОМ опосредованно, стимулируя раковые клетки выделить белок группы 1 с высокой подвижностью (HMGB1), который, в свою очередь, стимулирует продукцию IL-10 ОM. Гипоксия также индуцирует метаболические изменения в ОМ, которые затем непосредственно влияют на функции соседних клеток. Например, гипоксия стимулирует экспрессию REDD1, ингибитора mTOR и ключевого модулятора метаболизма в ответ на доступность питательных веществ и потребность в энергии. Ингибирование mTOR в ОM сильно снижает их поглощение глюкозы и активность гликолиза, оставляя больше глюкозы для соседних эндотелиальных клеток. Это повышает способность раковых клеток проникать в сосудистое русло, соответственно, приводит к формированию отдаленных метастазов.
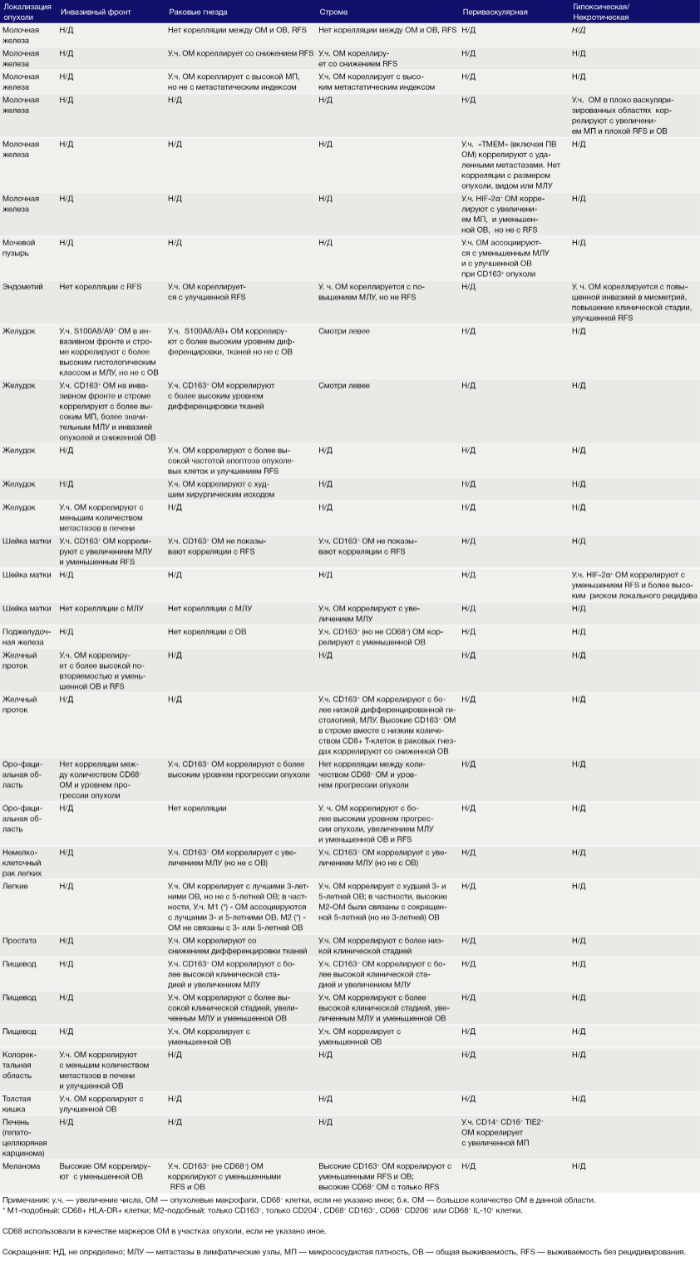
Таблица 1. Опухолевые макрофаги в различных злокачественных новообразованиях человека: корреляция с клинико-патологическими проявлениями
Заключение
Ряд экспериментальных исследований на мышах подтвердил способность различных опухолевых популяций дифференцированно регулировать фенотип ОМ. Важность этого подчеркивается клиническими отчетами, показывающими, что число или фенотип ОМ в определенных областях опухоли коррелируют с RFS и выживаемостью (Таблица 1).
Имеются данные о роли подмножеств ОM в определенных областях опухолей, ограничивающих ответ опухолей на лечение. Например, облучение, сосудистые разрушающие агенты и цитотоксические препараты индуцируют пролиферацию ПВ ОM, что способствует ангиогенезу опухоли и рецидиву после терапии. Гипоксические ОМ также были вовлечены в устойчивость опухолей к противоопухолевой терапии и способствуют рецидиву.
Демонстрация того, что ОМ стимулируют ряд механизмов опухолеобразования на мышиных моделях опухолей, побудила к развитию терапевтических подходов к истощению или перепрограммированию ОМ. На сегодняшний день общие ингибиторы ОМ, включая те, которые нацелены на CSF-1-CSF-1R и CCL-CCR2, в значительной степени не показали эффективности в клинических испытаниях в качестве монотерапии рака, хотя они могут оказаться эффективными в сочетании с другими терапевтическими агентами. Ингибитор CSF-1-R PLX3397 показал значительную эффективность при лечении теносиновиальной гигантоклеточной опухоли, лечение также выявило побочное действие, вызванное долгосрочным истощением всех макрофагов.
Таргетная терапия в отношении определенных ОM-подмножеств в опухолях может стать отличным методом в качестве противоопухолевой терапии посредством истощения или перепрограммирования тех ОМ, которые способствуют с помощью различных механизмов опухолевой прогрессии, при этом она должна оставлять или усиливать те подмножества ОМ, которые способствуют противоопухолевому иммунитету. Прогресс в нашем понимании того, как фенотип подмножеств ОМ в различных областях опухоли зависит от их онтогенеза, статуса активации и сложного комплекса местных взаимодействий поможет разработать такой терапевтический подход. Раскрытие сложного массива влияний на поведение ОM потребует многогранного подхода к исследованиям, однако это может привести к появлению новых возможностей в лечении опухолевых заболеваний, появлению новых таргетных противоопухолевых препаратов.
Источник: Yang M. et al. Diverse Functions of Macrophages in Different Tumor Microenvironments //Cancer research. – 2018. – Т. 78. – №. 19. – С. 5492-5503.