Манифестный сахарный диабет что это
Диабет беременных: влияние на малыша
Поделиться:
Новости о рождении очередного ребенка-богатыря весом 6–7 кг СМИ всегда преподносят нам как повод для радости. Фотографиями нового Ильи Муромца пестрят не только региональные, но и федеральные издания. Читатели радостно желают ребенку вырасти «настоящим мужиком», а «специалисты» связывают рождение детей-гигантов с социальными факторами — стабильностью в обществе, повышением уровня жизни, улучшением питания. Высказывается «экспертное» мнение, что крупновесные дети рождаются благодаря приему витаминно-минеральных комплексов во время беременности. И только гинекологи и эндокринологи не торопятся разделить общенародный восторг…
Признаки гестационной фетопатии
Печальные последствия
Увы, но показатели смертности плода и новорожденного с массой тела 4 кг и более — в 1,5−3 раза выше, чем у детей с нормальными весовыми параметрами. Раньше считалось, что у выживших «богатырей» к 2–3-месячному возрасту признаки диабетической фетопатии полностью регрессируют. Однако исследователи доказали, что избыточный вес детей при рождении приводит в дальнейшем к развитию подросткового ожирения и артериальной гипертензии, а впоследствии и к развитию сахарного диабета (СД) 2-го типа. По данным исследований, у 39,5 % таких детей в дошкольном периоде и у 60 % в начальной школе отмечаются проблемы с речью, у 9,3 % — проблемы с физической активностью
Читайте также:
Диагноз: диабет
Гестационный СД — совсем не редкость. Частота этой патологии в разных странах колеблется от 1 до 14 %. Пропустить развитие гестационного диабета у беременных очень легко — специфических симптомов практически нет, обычное лабораторное обследование может не показывать никаких изменений. По данным Московского областного НИИ акушерства и гинекологии, в 50–60 % случаев диагноз «гестационный диабет» врачи ставят с серьезным опозданием.
Коварство гестационного диабета в том, что даже при относительно «мягком» течении он увеличивает частоту нежелательных исходов беременности и для матери, и для плода, являясь фактором риска развития ожирения, сахарного диабета 2-го типа и сердечно-сосудистых заболеваний у матери и у ребенка в будущем. У 20–50 % женщин, перенесших гестационный диабет, он возникает при последующей беременности, а у 25–75 % через 16–20 лет после родов развивается самый настоящий манифестный сахарный диабет.
Новые рекомендации по диагностике
ВОЗ прогнозирует, что заболеваемость гестационным сахарным диабетом будет неуклонно увеличиваться, потому что в мире растет число больных ожирением. Отложенное «на потом» материнство также повышает риски развития диабета во время беременности. По оценкам ВОЗ, к 2030 году число больных сахарным диабетом удвоится.
В настоящее время скрининг на гестационный сахарный диабет должен проводиться — в соответствии с рекомендациями — на всей территории Российской Федерации, это единственный способ обнаружить проблему вовремя. В частности, с января 2016 года в России строго обязательным стало проведение глюкозотолерантного теста, который позволяет точно диагностировать диабет. Об особенностях проведения этого теста мы расскажем вам в следующей статье.
1. Бурумкулова Ф. Ф. и др. Диабетическая фетопатия и перинатальная патология при беременности, осложненной гестозом // Лечение и профилактика. — 2013 — № 2 (6). — С. 124–131.
2. HAPO Study Cooperative Research Group. The hyperglycemia and adverse pregnancy outcome (HAPO) study // Int J Obstet Gynaecol. — 2002 Jul; 78 (1): 69–77.
3. Дедов И. И., Краснопольский В. И., Сухих Г. Т. и др. Проект Российского консенсуса «Гестационный сахарный диабет: диагностика, лечение, послеродовое наблюдение» / Сахарный диабет. — 2012. — № 4. — С. 4–10.
Сахарный диабет беременных: рекомендации и дневник
Консультации ведут сотрудники кафедры эндокринологии и диабетологии Факультета Дополнительного Профессионального образования Федерального Государственного Автономного Образовательного Учреждения Высшего Образования «Российский Национальный Исследовательский Медицинский Университет имени Н. И. Пирогова» Министерства Здравоохранения Российской Федерации.
Гестационный сахарный диабет — заболевание, характеризующееся гипергликемией (повышением уровня глюкозы крови), которое впервые было выявлено во время беременности. Чаще всего у женщины гликемия нормализуется после родов, но сохраняется высокий риск развития сахарного диабета в последующие беременности и в будущем.
Гестационный сахарный диабет при беременности – достаточно распространенное заболевание в России и мире в целом. Частота встречаемости гипергликемии во время беременности по данным международных исследований составляет до 18%.
Нарушение углеводного обмена может развиваться у любой беременной с учетом тех гормональных и метаболических изменений, которые последовательно происходят на разных этапах беременности. Но наиболее высокий риск развития гестационного сахарного диабета у беременных с:
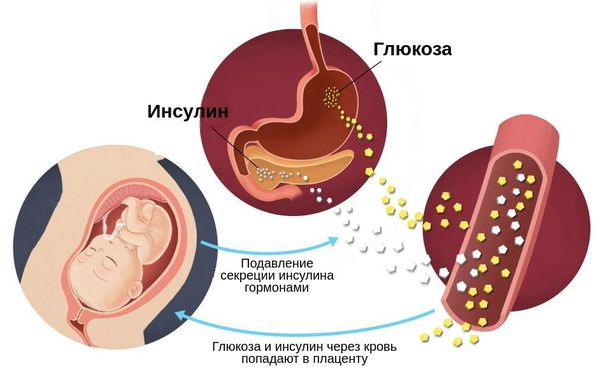
У здоровой беременной для преодоления физиологической инсулинорезистентности и поддержания нормального для беременности уровня глюкозы в крови происходит компенсаторное повышение секреции инсулина поджелудочной железой примерно в три раза (масса бета-клеток при этом увеличивается на 10-15%). Однако, у беременных, особенно при наличии наследственной предрасположенности к сахарному диабету, ожирении (ИМТ более 30 кг/м 2 ) и т. д. существующая секреция инсулина не всегда позволяет преодолеть развивающуюся во второй половине беременности физиологическую инсулинорезистентность. Это и приводит к повышению уровня глюкозы в крови и развитию гестационного сахарного диабета. С током крови глюкоза незамедлительно и беспрепятственно переносится через плаценту к плоду, способствуя у него выработке собственного инсулина. Инсулин плода, обладая «ростоподобным» эффектом, приводит к стимуляции роста его внутренних органов на фоне замедления их функционального развития, а избыток глюкозы, поступающей от матери посредством его инсулина откладывается с 28 недели беременности в подкожное депо в виде жира.
В результате хроническая гипергликемия матери наносит вред развитию плода и приводит к формированию, так называемой, «диабетической фетопатии». Это болезни плода, возникающие с 12-й недели внутриутробной жизни до родов:
При рождении детей с диабетической фетопатией чаще встречаются:
У детей, рожденных от матерей с недиагностированным, некомпенсированным гестационным сахарным диабетом, чаще встречаются:
Со стороны беременной при гестационном сахарном диабете чаще встречаются:
Гестационный сахарный диабет не имеет никаких клинических проявлений, связанных с гипергликемией (сухость во рту, жажда, увеличение объема выделенной за сутки мочи, зуд и т. д.), и поэтому требуется активное выявление этого заболевания у всех беременных.
Анализ и исследования на диабет у беременных
Всем беременным в обязательном порядке необходимо исследовать глюкозу в плазме венозной крови натощак, в условиях лаборатории – на фоне обычной диеты и физической активности – при первом обращении в женскую консультацию или перинатальный центр, не позднее 24 недели беременности.
Если результаты исследования соответствуют нормальным показателям во время беременности, то в обязательном порядке на 24-28 неделях беременности проводится пероральный глюкозотолерантный тест – ПГТТ («нагрузочный тест» с 75 г глюкозы) с целью активного выявления возможных нарушений со стороны углеводного обмена.
ПГТТ с 75 г глюкозы является безопасным и единственным диагностическим тестом для выявления нарушений углеводного обмена во время беременности.
Правила проведения ПГТТ
Этапы выполнения ПГТТ
После забора первой пробы плазмы венозной крови натощак пациентка в течение 5 минут выпивает раствор глюкозы, состоящий из 75 г сухой глюкозы, растворенной в 250-300 мл питьевой негазированной воды, или 82,5 мг глюкозы моногидрата. Начало приема раствора глюкозы считается началом теста.
Следующие пробы крови для определения уровня глюкозы венозной плазмы берутся через 1 и 2 часа после нагрузки глюкозой.
Нормы глюкоза венозной плазмы для беременных:
Правила хранения инсулина и проведения инъекций
Гипогликемия – состояние, характеризующееся низким уровнем сахара в крови. Гипогликемией считается сахар крови ниже 3,9 ммоль/л во время беременности только на фоне инсулинотерапии. Встречается при гестационном сахарном диабете очень редко.
Причины развития гипогликемии при гестационном сахарном диабете:
Признаки гипогликемии:
Что могут отметить окружающие, если у вас возникла гипогликемия:
Алгоритм действия при признаках гипогликемии
Самый надежный метод профилактики гипогликемии – регулярный самоконтроль гликемии.
Гестационный сахарный диабет у беременных
Программа наблюдения беременных с гестационным сахарным диабетом до родов эндокринологом:
Сахарный диабет 1-го типа у детей и подростков: этиопатогенез, клиника, лечение
В обзоре представлены современные взгляды на этиологию, патофизиологию развития сахарного диабета 1-го типа у детей и подростков, критерии диагностики и особенности инсулинотерапии. Освещены основные признаки диабетического кетоацидоза и его лечения.
The review presents modern views on the etiology, pathophysiology of type 1 diabetes in children and adolescents, diagnostic criteria and features of insulin. It highlights the key features of diabetic ketoacidosis and treatment.
Сахарный диабет (СД) — этиологически неоднородная группа метаболических заболеваний, которые характеризуются хронической гипергликемией, обусловленной нарушением секреции или действием инсулина либо сочетанием этих нарушений.
Впервые СД описан в древней Индии более 2 тыс. лет назад. В настоящее время в мире насчитывается более 230 млн больных СД, в России — 2 076 000. В действительности распространенность СД выше, т. к. не учитывают его латентные формы, т. е. наблюдается «неинфекционная пандемия» СД.
Классификация СД
Согласно современной классификации выделяют [1]:
Самые распространенные типы сахарного диабета это СД 1-го и СД 2-го типа. Длительное время считалось, что в детском возрасте свойственен СД 1-го типа. Однако исследования последнего десятилетия поколебали это утверждение. Все чаще стал диагностироваться у детей СД 2-го типа, который преобладает у взрослых людей после 40 лет. В некоторых странах СД 2-го типа у детей встречается чаще, чем СД 1-го типа, что связано с генетическими особенностями популяции и увеличивающейся распространенностью ожирения.
Эпидемиология СД
Созданные национальные и региональные регистры СД 1-го типа у детей и подростков выявили широкую вариабельность заболеваемости и распространенности в зависимости от популяции и географической широты в разных странах мира (от 7 до 40 случаев на 100 тыс. детского населения в год).За последние два десятилетия заболеваемость СД 1-го типа среди детей неуклонно увеличивается. Четверть больных приходится на возраст до четырех лет жизни. На начало 2010 г. в мире зарегистрировано 479,6 тысяч детей с СД 1-го типа. Число впервые выявленных 75 800. Ежегодный прирост 3%.
По данным Государственного регистра на 01.01.2011 г. в РФ зарегистрировано 17 519 детей с СД 1-го типа, из них 2911 новых случаев. Средний показатель заболеваемости детей по РФ 11,2 на 100 тыс. детского населения [1].Заболевание проявляется в любом возрасте (существует врожденный диабет), но наиболее часто дети заболевают в периоды интенсивного роста (4–6 лет, 8–12 лет, пубертатный период). Дети грудного возраста поражаются в 0,5% случаев СД.
В отличие от стран с высоким уровнем заболеваемости, в которых максимальный прирост ее приходится на младший возраст, в московской популяции нарастание заболеваемости наблюдается за счет подростков.
Этиология и патогенез СД 1-го типа
СД 1-го типа — аутоиммунное заболевание у генетически предрасположенных лиц, при котором хронически протекающий лимфоцитарный инсулит приводит к деструкции β-клеток, с последующим развитием абсолютной инсулиновой недостаточности. Для СД 1-го типа характерна склонность к развитию кетоацидоза.
Предрасположенность к аутоиммунному СД 1-го типа определяется взаимодействием множества генов, при этом имеет значение взаимное влияние не только различных генетических систем, но и взаимодействие предрасполагающих и защитных гаплотипов.
Период от начала аутоиммунного процесса до развития СД 1-го типа может занимать от нескольких месяцев до 10 лет.
В запуске процессов разрушения островковых клеток могут принимать участие вирусные инфекции (коксаки В, краснуха и др.), химические вещества (аллоксан, нитраты и др.).
Аутоиммунное разрушение β-клеток сложный, многоэтапный процесс, в ходе которого активируется как клеточное, так и гуморальное звено иммунитета. Главную роль в развитии инсулита играют цитотоксические (СД8+) Т-лимфоциты [2].
По современным представлениям иммунной дисрегуляции принадлежит значительная роль в возникновении заболевания от начала до клинической манифестации диабета.
К маркерам аутоиммунной деструкции β-клеток относят:
1) островково-клеточные цитоплазматические аутоантитела (ICA);
2) антиинсулиновые антитела (IAA);
3) антитела к протеину островковых клеток с молекулярной массой 64 тыс. кД (они состоят из трех молекул):
В позднем доклиническом периоде популяция β-клеток уменьшается на 50–70% по сравнению с нормой, а оставшиеся — еще поддерживают базальный уровень инсулина, но секреторная их активность снижена.
Клинические признаки диабета появляются, когда оставшееся количество β-клеток неспособно компенсировать повышенные потребности в инсулине.
Инсулин — гормон, регулирующий все виды обмена веществ. Он обеспечивает энергетические и пластические процессы в организме. Основные органы-мишени инсулина — печень, мышечная и жировая ткань. В них инсулин оказывает анаболическое и катаболическое действие.
Влияние инсулина на углеводный обмен
Влияние инсулина на жировой обмен
Недостаток инсулина вызывает усиление липолиза (расщепление триглицеридов до свободных жирных кислот (СЖК) в адипоцитах). Повышение количества СЖК является причиной жировой инфильтрации печени и увеличения ее размеров. Усиливается распад СЖК с образованием кетоновых тел.
Влияние инсулина на белковый обмен
Инсулин способствует синтезу белка в мышечной ткани. Недостаточность инсулина вызывает распад (катаболизм) мышечной ткани, накопление азотсодержащих продуктов (аминокислот) и стимулирует в печени глюконеогенез [3].
Дефицит инсулина увеличивает выброс контринсулярных гормонов, активацию гликогенолиза, глюконеогенеза. Все это ведет к гипергликемии, повышению осмолярности крови, обезвоживанию тканей, глюкозурии.
Стадия иммулогической дисрегуляции может длиться месяцы и годы, при этом могут выявляться антитела, являющиеся маркерами аутоиммунности к β-клеткам (ICA, IAA, GAD, IA-L) и генетические маркеры СД 1-го типа (предрасполагающих и протекторных гаплотипов HLA, которые по относительному риску могут отличаться у различных этнических групп).
Латентный сахарный диабет
В этой стадии болезни нет клинических симптомов. Содержание глюкозы в крови натощак периодически может находиться от 5,6 до 6,9 ммоль/л, а в течение суток остается в пределах нормы, в моче глюкозы нет. Тогда ставится диагноз «нарушение глюкозы натощак (НГН)».
У здорового человека глюкоза в моче отсутствует. Глюкозурия возникает при содержании глюкозы выше 8,88 ммоль/л.
Кетоновые тела (ацетоацетат, β-оксибутират и ацетон) образуются в печени из свободных жирных кислот. Увеличение их наблюдается при дефиците инсулина. Существуют тест-полоски для определения ацетоацетата в моче и уровня β-оксибутирата в крови (> 0,5 ммоль/л). В фазе декомпенсации СД 1-го типа без кетоацидоза отсутствуют ацетоновые тела и ацидоз.
Гликилированный гемоглобин. В крови глюкоза необратимо связывается с молекулой гемоглобина с образованием гликированного гемоглобина (общего НВА1 или его фракции «С» НВА1с), т. е. отражает состояние углеводного обмена за 3 месяца. Уровень НВА1 — 5–7,8% в норме, уровень минорной фракции (НВА1с) — 4–6%. При гипергликемии показатели гликированного гемоглобина высокие.
Иммунологические маркеры аутоиммунного инсулита: аутоантитела к антигенам β-клеток (ICA, IAA, GAD, IA-L) могут быть повышены. Содержание С-пептида в сыворотке крови низкое.
Дифференциальная диагностика
До настоящего времени диагностика СД 1-го типа остается актуальной. Более чем у 80% детей сахарный диабет диагностируется в состоянии кетоацидоза. В зависимости от превалирования тех или иных клинических симптомов приходится дифференцировать с:
1) хирургической патологией (острый аппендицит, «острый живот»);
2) инфекционными заболеваниями (грипп, пневмония, менингит);
3) заболеваниями желудочно-кишечного тракта (пищевая токсикоинфекция, гастроэнтерит и др.);
4) заболеваниями почек (пиелонефрит);
5) заболеваниями нервной системы (опухоль головного мозга, вегетососудистая дистония);
6) несахарным диабетом.
При постепенном и медленном развитии заболевания дифференциальный диагноз проводится между СД 1-го типа, СД 2-го типа и диабетом взрослого типа у молодых (MODY).
Лечение сахарного диабета 1-го типа
СД 1-го типа развивается в результате абсолютной инсулиновой недостаточности. Всем больным с манифестной формой СД 1-го типа проводится заместительная инсулинотерапия.
У здорового человека секреция инсулина постоянно происходит независимо от приема пищи (базальная). Но в ответ на прием пищи его секреция усиливается (болюсная) в ответ на посталиментарную гипергликемию. Инсулин секретируется β-клетками в портальную систему. 50% его потребляется в печени для превращения глюкозы в гликоген, оставшиеся 50% разносятся по большому кругу кровообращения к органам.
У больных СД 1-го типа экзогенный инсулин вводится подкожно, и он медленно поступает в общий кровоток (не в печень, как у здоровых), где концентрация его длительное время остается высокой. В результате посталиментарная гликемия у них более высокая, а в поздние часы имеется склонность к гипогликемиям.
С другой стороны, гликоген у больных СД в первую очередь депонируется в мышцах, а запасы в печени его снижаются. Мышечный гликоген не участвует в поддержании нормогликемии.
У детей применяются человеческие инсулины, полученные биосинтетическим (генно-инженерным) методом с помощью рекомбинантной ДНК-технологии.
Доза инсулина зависит от возраста и стажа диабета. В первые 2 года потребность в инсулине составляет 0,5–0,6 ЕД/кг массы тела в сутки. Набольшее распространение в настоящее время получила интенсифицированная (болюсно-базисная) схема введения инсулина [6].
Начинают инсулинотерапию с введения инсулина ультракороткого или короткого действия (табл. 1). Первая доза у детей первых лет жизни 0,5–1 ЕД, у школьников 2–4 ЕД, у подростков 4–6 ЕД. Дальнейшая коррекция дозы инсулина проводится в зависимости от уровня глюкозы в крови. При нормализации метаболических показателей больного переводят на болюсно-базисную схему, комбинируя инсулины короткого и длительного действия.
Инсулины выпускаются во флаконах и картриджах. Наибольшее распространение получили инсулиновые шприц-ручки.
Для подбора оптимальной дозы инсулина широкое применение нашла система продолжительного глюкозного мониторинга (CGMS). Эта мобильная система, носимая на поясе пациента, фиксирует уровень глюкозы в крови каждые 5 минут на протяжении 3 суток. Эти данные подвергаются компьютерной обработке и представлены в виде таблиц и графика, на которых отмечены колебания гликемии.
Инсулиновые помпы. Это мобильное электронное устройство, носимое на поясе. Управляемая компьютером (чипом) инсулиновая помпа содержит инсулин короткого действия и подается в двух режимах, болюсном и базисном [7].
Диета
Важным фактором компенсации СД является диета. Общие принципы питания такие же, как и здорового ребенка. Соотношение белков, жиров, углеводов, калорий должно соответствовать возрасту ребенка.
Некоторые особенности диеты у детей с СД:
Сахароповышающий эффект пищи в основном обусловлен количеством и качеством углеводов.
В соответствии с гликемическим индексом выделяют пищевые продукты, которые очень быстро повышают уровень сахара в крови (сладкие). Они используются для купирования гипогликемии.
Физические нагрузки
Физическая активность — важный фактор, регулирующий углеводный обмен. При физической нагрузке у здоровых людей происходит снижение секреции инсулина с одновременным повышением выработки контринсулярных гормонов. В печени усиливается продукция глюкозы из неуглеводных (глюконеогенез) соединений. Это служит важным источником ее при физической нагрузке и эквивалентно степени утилизации глюкозы мышцами.
Продукция глюкозы повышается по мере увеличения интенсивности физических упражнений. Уровень глюкозы остается стабильным.
При СД 1-го типа действие экзогенного инсулина не зависит от физической активности, а влияние контринсулярных гормонов недостаточно для коррекции уровня глюкозы. В связи с этим во время физической нагрузки или сразу после нее может наблюдаться гипогликемия. Почти все формы физической активности продолжительностью более 30 минут требуют корректировки диеты и/или дозы инсулина.
Самоконтроль
Цель самоконтроля — обучение больного диабетом и членов его семьи самостоятельно оказывать себе помощь. Он включает [8]:
Социальная адаптация
При выявлении сахарного диабета у ребенка родители часто пребывают в растерянности, так как болезнь влияет на образ жизни семьи. Возникают проблемы с постоянным лечением, питанием, гипогликемиями, сопутствующими заболеваниями. По мере роста у ребенка формируется свое отношение к болезни. В пубертатный период многочисленные физиологические и психосоциальные факторы усложняют контроль над уровнем глюкозы. Все это требует всесторонней психосоциальной помощи членов семьи, эндокринолога и психолога.
Целевые уровни показателей углеводного обмена у больных СД 1-го типа (табл. 2)
Натощак (предпрандиальный) сахар крови 5–8 ммоль/л.
Через 2 часа после приема пищи (постпрандиальный) 5–10 ммоль/л.
Гликированный гемоглобин (НВА1c)
ГБОУ ВПО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва
Что такое гестационный сахарный диабет? Причины возникновения, диагностику и методы лечения разберем в статье доктора Кирдянкиной Н.О., эндокринолога со стажем в 11 лет.
Определение болезни. Причины заболевания
Гестационный сахарный диабет (ГСД) — это нарушение углеводного обмена, которое развилось во время беременности. При этом на момент зачатия уровень глюкозы в крови будущей мамы не был высоким. Данный вид сахарного диабета может возникнуть при любой беременности, особенно многоплодной и наступившей в результате ЭКО.
Снизить риск развития ГСД у беременной можно, если вовремя его диагностировать и компенсировать нарушение обмена углеводов.
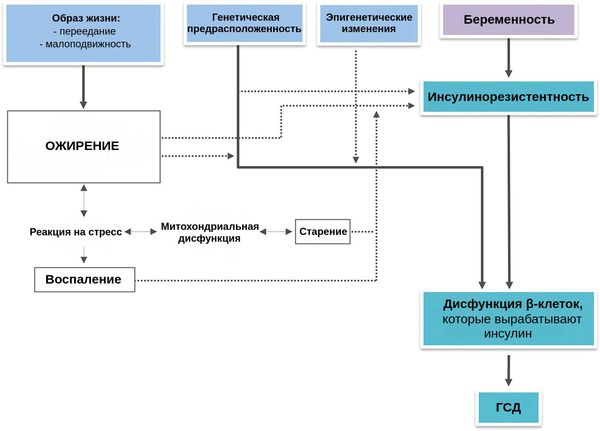
Развитие ГСД связано с генетической предрасположенностью. Она «активируется» под воздействием множества факторов риска [2] [3] [4] :
Симптомы гестационного сахарного диабета
Симптомы гипергликемии — высокого уровня глюкозы в крови — будут наблюдаться уже в первом триместре. Они могут быть схожи с признаками токсикоза беременных, поэтому таким пациенткам рекомендуется определить концентрацию глюкозы в крови натощак.
При обращении к врачу беременные могут жаловаться на сухость во рту, жажду, увеличение количества выпиваемой жидкости (больше 2 л), обильное выделение мочи, повышенный или пониженный аппетит, слабость, похудание, кожный зуд, особенно в области промежности, нарушение сна. Они склонны к гнойничковым заболеваниям кожи и фурункулёзу. Однако все эти признаки более характерны для пациенток с манифестным сахарным диабетом.
Если же углеводный обмен у женщины был нарушен до беременности, то она может жаловаться на ухудшение зрения, снижение чувствительности ног и отёчность.
Патогенез гестационного сахарного диабета
Во время здоровой беременности организм матери изменяется, чтобы обеспечить потребности растущего плода: адаптируется сердечно-сосудистая, почечная, дыхательная, метаболическая и эндокринная системы. Изменяется и чувствительность к инсулину: она увеличивается, способствуя усвоению глюкозы и её отложению в виде жировых запасов. Однако в дальнейшем также увеличивается выработка материнских и плацентарных гормонов, таких как эстроген, прогестерон, лептин, кортизол, плацентарный лактоген и плацентарный гормон роста. Они подавляют действие инсулина и приводят к развитию физиологической инсулинорезистентности — устойчивости к инсулину. В итоге уровень глюкозы в крови слегка повышается. Эта глюкоза легко транспортируется через плаценту к плоду, она необходима для его роста.
В большинстве случаев эти нарушения существуют ещё до беременности и могут прогрессировать. По этой причине повышается риск развития сахарного диабета 2-го типа после беременности, осложнённой ГСД.
ГСД и микробиота кишечника
Появляются доказательства того, что кишечный микробиом — сообщество микробов, обитающих в кишечнике — может воздействовать на метаболические заболевания, в том числе на развитие ГСД.
На состав кишечного микробиома влияют как события в начале жизни (преждевременные роды, кормление грудью), так и события в более позднем возрасте (диетические привычки и пристрастия, применение антибиотиков).
Firmicutes перерабатывают растительные полисахариды, поэтому высокое содержание клетчатки в пище увеличивает концентрацию этих бактерий, а животные белки, наоборот, снижают. По-видимому, это свойства Firmicutes имеют отношение к патогенезу ГСД, хотя механизмы, лежащие в основе этого влияния, неизвестны.
Классификация и стадии развития гестационного сахарного диабета
Собственной классификации у ГСД не существует. Он относится к разновидностям сахарного диабета, который подразделяют на следующие виды:
Сахарный диабет 1-го типа чаще всего встречается в детском и подростковом возрасте. Он связан с наличием аутоантител к инсулину, тирозинфосфатазе и островковым клеткам поджелудочной железы. Аутоантитела приводят к деструкции β-клеток и, как следствие, к абсолютной недостаточности инсулина.
Сахарный диабет 2-го типа чаще диагностируется с возрастом. Его патогенез похож на патогенез ГСД. В основе также лежит инсулинорезистентность — относительная недостаточность инсулина из-за нарушения работы β-клеток, которое приводит к гипергликемии. Так как выработка своего собственного инсулина в организме не нарушена, симптомы гипергликемии носят менее выраженный характер.
Диабет MODY — это диабет зрелого типа, который встречается у молодых людей и обусловлен генетически. Начинается это заболевание у людей до 25 лет. Сопровождается первичным дефектом в работе β-клеток поджелудочной железы.
Манифестный сахарный диабет — это нарушение концентрации глюкозы в крови, которое существовало ещё до беременности, но было диагностировано только во время беременности. Манифестным может быть как сахарный диабет 1-го и 2-го типа, так и другие специфические типы этого заболевания. Точный диагноз устанавливается уже после родов.
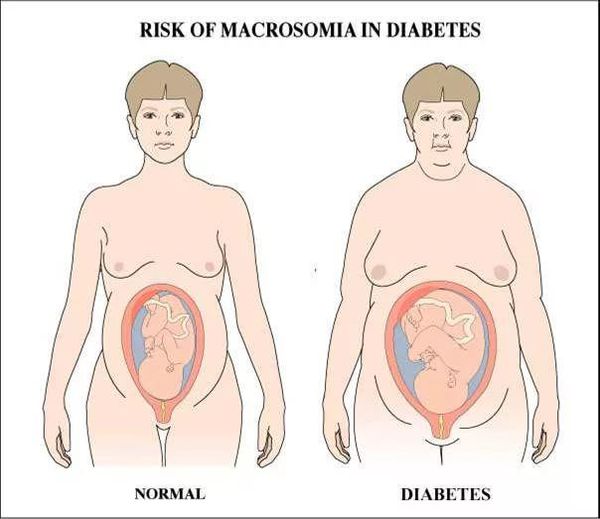
Осложнения гестационного сахарного диабета
ГСД может спровоцировать значительные неблагоприятные последствия у матери и у ребёнка, причём как ближайшие, так и отдалённые.
Осложнения у ребёнка
Макросомия является одной из наиболее важных проблем. Чрезмерное увеличение плода стимулируется влиянием инсулина. Он приводит к отложению большого количества подкожного жира и широким плечам ребёнка, которые не соответствуют тазу матери, из-за чего во время родов возникают травмы.
Младенцы матерей с ГСД, которые родились недоношенными, более склонны к развитию респираторного дистресс-синдрома (воспалительному поражению лёгких) и других проблем, связанных с рождением раньше срока.
При рождении младенцы с гиперинсулинемией склонны к гипогликемии — пониженному уровню глюкозы в крови. Она связана с внезапной изоляцией ребёнка от материнского источника глюкозы на фоне высокой концентрации собственного циркулирующего инсулина. Гипогликемия — экстренное состояние. Оно требует наблюдения, а иногда — интенсивной терапии и введения глюкозы внутривенно.
Помимо гипогликемии у детей часто наблюдается снижение кальция и повышение билирубина в крови, а также полицитемия — увеличение эритроцитов, лейкоцитов и тромбоцитов.
Осложнения у матери
Диагностика гестационного сахарного диабета
Диагностика ГСД сводится к определению уровня глюкозы в крови натощак. Кровь для анализа берётся только из вены. Определять гликемию с помощью анализа крови из пальца по уровню цельной капиллярной крови или глюкометром недопустимо, так как эти исследования не могут обнаружить нарушения углеводного обмена.
Перед измерением уровня глюкозы в венозной крови нельзя есть в течение 8-12 часов.
Полностью исключить ГСД это рутинное исследование не может, так как гликемия натощак у беременных всегда ниже, чем есть на самом деле. Поэтому всем беременным настоятельно рекомендуется проводить нагрузочный тест ПГТТ — пероральный глюкозотолерантный тест. Иначе его называют «тест на толерантность к глюкозе».
ПГТТ является оптимальным способом диагностики ГСД. Его проводят на 24-32 недели беременности только в лаборатории. Использование глюкометров запрещено.
Этапы ПГТТ [24] :
Во время теста пациентка должна сидеть на стуле, дёргаться и ходить запрещено, можно пить воду.
Как подготовиться к ПГТТ [24] :
Противопоказания к ПГТТ [24] :
Для установления диагноза ГСД по результатам ПГТТ достаточно одного из указанных изменений глюкозы [24] :
Пациенткам с ГСД рекомендовано динамическое выполнение УЗИ для поиска признаков диабетической фетопатии у плода. К основным признакам протокола УЗИ, на которые следует обращать пристальное внимание, относятся [3] [25] :
Дифференциальная диагностика
ГСД необходимо отличить от манифестного сахарного диабета. На него будут указывать следующие значения [24] :
Лечение гестационного сахарного диабета
Как только врач-эндокринолог или акушер-гинеколог установили диагноз ГСД, пациентке нужно рассказать о принципах рационального сбалансированного питания, необходимости ведения дневника питания, самоконтроля гликемии и контроля кетонурии — кетоновых тел в моче.
Диетотерапия
Питание беременной женщины должно содержать достаточное количество углеводов, исключая легко-усваиваемые (содержатся в белом хлебе, сладостях, некоторых фруктах и т. п.). Оптимальное количество углеводов в сутки — 175 г. Его нужно распределять на три основных приёма пищи и 2-3 перекуса.
Принципы диетотерапии:
Каждый приём пищи должен содержать медленно-усваиваемые углеводы, белок, моно- и полиненасыщенные жиры, пищевые волокна. Это повышает чувствительность к инсулину, способствует меньшей прибавке в весе, снижает частоту назначаемой инсулинотерапии при ГСД. Беременным с ожирением и патологической прибавкой веса рекомендуется ограничить калорийность питания, но не меньше чем на 1800 ккал/сут во избежание кетоза.
На фоне диетотерапии проводится самоконтроль гликемии: измерение глюкозы в крови натощак, в течение дня и перед основными приёмами пищи, на ночь (до 5,1 ммоль/л), через час после еды (до 7,0 ммоль/л).
Диетические рекомендации при ГСД [2] [3] [25] :
Молочные продукты лучше всего употреблять как перекус между основными приёмами пищи. С кефиром и молоком можно делать ягодные смузи.
Витаминотерапия
Как показывают различные исследования, витамина D влияет на выработку и дисфункцию инсулина, а также повышает чувствительность к этому гормону.
Инсулинотерапия
Схема инсулинотерапии подбирается врачом-эндокринологом индивидуально в зависимости от показателей самоконтроля гликемии:
На фоне инсулинотерапии самоконтроль гликемии проводится не менее семи раз в сутки:
НПХ-инсулин ( суспензия из инсулина и протамина ) обладает средней продолжительностью действия (12-16 часов). Его можно совмещать с инсулинами короткого действия.
Прогноз. Профилактика
Роды при ГСД проводятся на 38-39 недели беременности. Более ранее родоразрешение показано пациенткам с неконтролируемым ГСД. Тактику и показания к родам определяет акушер.
ГСД не является основанием для назначения досрочного родоразрешения и кесарева сечения.
Так как пациентки с ГСД находятся в группе риска развития ГСД в последующие беременности, ожирения и сахарного диабета 2-го типа в будущем, им нужно тщательно контролировать углеводный обмен. На сроке 4-12 недели после родов рекомендуется пройти повторный тест с нагрузкой (ПГТТ) для уточнения нарушений обмена углеводов.
Лечение пациенток с ГСД является идеальной платформой для предотвращения и профилактики диабета 2-го типа. Питание матери во время беременности может инициировать у ребенка каскад метаболических и воспалительных иммунных реакций, которые проявятся на более поздних этапах жизни. Поэтому условия питания в этот период могут обратить вспять растущую тенденцию заболеваний, связанных с западным образом жизни.

 Читайте также:
Читайте также: 

.gif)