Машадо жозефа что за болезнь
Спиноцеребеллярная атаксия
OMIM 164400
Наша команда профессионалов ответит на ваши вопросы
В Центре Молекулярной Генетики проводится прямая молекулярно-генетическая диагностика наиболее частых форм спиноцеребеллярной атаксии: SCA 1, 2, 3, 6, 7, 8, 12 и 17 типов, которая основана на оценке числа CAG-повторов, локализованных в генах ATXN1, ATXN2, ATXN3, CACNA1A, ATXN7, ATXN8, PPP2R2B и TBP .
Спиноцеребеллярная атаксия 1 (SCA 1, OMIM 164400).
Заболевание обычно начинается в возрасте от 30 до 40 лет (возможный разброс – от 4 до 74 лет). Основные клинические симптомы – атаксия, офтальмоплегия, пирамидные и экстрапирамидные расстройства.
Молекулярно-генетической причиной SCA1 является увеличение числа тринуклеотидных САG повторов в гене ATXN1, располагающемся на 6-й хромосоме (сегмент 6р23). Длина гена составляет 450000 нуклеотидов. Ген содержит девять экзонов. Транскрипт состоит из 10660 нуклеотидов. В гене имеется участок тринуклеотидных повторов CAG (в норме их меньше 36; при болезни больше 40). Нормальные аллели гена обычно содержат в составе тринуклеотидного участка вставки от одного до трех CAT-триплетов, отсутствующие в мутантном гене. Их наличие рассматривается как важный фактор стабилизации нормальных аллелей при мейозе.
Спиноцеребеллярная атаксия 2 (SCA 2, OMIM 183090).
Спиноцеребеллярная атаксия 3 (SCA3, болезнь Мачадо-Джозефа, OMIM 109150)
Спиноцеребеллярная атаксия 6 (SCA6, OMIM 183086)
Спиноцеребеллярная атаксия 7 (SCA7, OMIM 164500)
Спиноцеребеллярная атаксия 7 типа (оливопонтоцеребеллярная атрофия 3 типа) – прогрессирующее аутосомно-доминантное нейродегенеративное заболевание, клинически характеризующееся церебеллярной атаксией, ассоциированной с дистрофией желтого пятна. Средний возраст манифестации заболевания – 32 года. Степень тяжести, скорость прогрессии и возраст начала заболевания варьируют как между семьями так и внутри семей. Основные клинические симптомы – офтальмоплегия, пирамидные и экстрапирамидные знаки, дизартрия, дисфагия, хорея, гиперрефлексия, спастика, потеря глубокой чувствительности, пигментная дегенерация сетчатки, прогрессирующая потеря зрения, медленные саккады, атрофия зрительного нерва.
Молекулярно-генетическая причина SCA7 –экспансия тринуклеотидных CAG-повторов гена ATXN7 (3p21.1-p12), находящихся в полиглутаминовом тракте белка ataxin-7.В норме количество повторов варьирует от 4 до 35, при болезни обнаруживается от 36 до 306 повторов.
Спиноцеребеллярная атаксия 8 (SCA8, OMIM 608768)
Спиноцеребеллярная атаксия 8 типа – медленно прогрессирующее аутосомно-доминантное заболевание, возраст начала которого варьирует от 18 до 65 лет. Основные клинические симптомы – прогрессирующая церебеллярная атаксия, нарушение координации походки, движения конечностей, речи, брадикинезия (замедленные движения). У больных часто наблюдается дизартрия, тремор, дисфагия, нистагм, замедление саккадических движений глазных яблок, дизметрические саккады, потеря чувствительности. При МРТ обнаруживается атрофия полушарий и червя мозжечка. Молекулярно-генетической причиной SCA8 является увеличение числа тринуклеотидных СAG повторов в гене ATXN8. В норме количество повторов варьирует от 15 до 50, при болезни обнаруживается от 71 до 1300.
Спиноцеребеллярная атаксия 12 (SCA12, OMIM 604326)
Молекулярно-генетическая причина SCA12 – увеличение числа тринуклеотидных CAG повторов в гене PPP2R2B, распологающемся на 5-ой хромосоме (сегмент q31-q33). В норме количество повторов от 7 до 32, при болезни обнаруживаются от 51 до 78. Клиническое значение экспансии повторов в диапазоне от 33 до 50 до сих пор не установлено. Ген PPP2R2B кодирует регуляторную субъединицу В белка фосфатазы 2 участвующего в таких регуляторных процессах, как рост и деление клеток, сокращение мышц и транскрипция генов.
Спиноцеребеллярная атаксия 17 (SCA 17, OMIM: 607136)
Молекулярно-генетической причиной SCA17 является увеличение числа тринуклеотидных CAG (или CAA) повторов в гене TBP, расположенном на длинном плече 6 хромосомы (сегмент q27). Ген TBP кодирует фактор транскрипции-белок, связывающий последовательность ТАТА-бокса (ТВР). В норме количество повторов варьирует от 25 до 44, при болезни обнаруживается от 47 до 63 повторов. Описана связь 45 и 46 повторов с неполной пенетрантностью заболевания.
Болезнь Мачадо-Джозефа — генетически обусловленная спиноцеребеллярная атаксия, клинически представленная полиморфными сочетаниями мозжечкового синдрома с проявлениями вторичного паркинсонизма, гиперкинезами, пирамидными расстройствами в виде спастических параличей и офтальмоплегии, амиотрофиями. Диагностируется на основании тщательного изучения клинических проявлений у пациента и его родственников, генеалогического анализа, данных МРТ и КТ, выявления при исследовании ДНК превышающего норму количества копий триплета ЦАГ. Лечение симптоматическое. Прогноз неблагоприятный.
МКБ-10
Общие сведения
Болезнь Мачадо-Джозефа описана в средине 70-х годов 20 века. Предположительно, заболевание первоначально возникло у жителей Азорских островов, в связи с чем оно иногда встречается под названием «азорская болезнь». На сегодняшний день болезнь Мачадо-Джозефа распространена по всему миру. Ее случаи диагностированы у жителей США, Бразилии, Японии, Индии, Европы, Китая, Австралии, Канады. Она является наиболее встречаемой формой наследственной мозжечковой атаксии.
В рамках современной международной классификации заболеваний данная патология верифицируется как СЦА З — спиноцеребеллярная атаксия III тип. Характерна большая вариабельность времени дебюта (от 10 до 70 лет) и полиморфность клинических симптомов, обусловленная мультисистемным поражением церебральных и спинальных структур. В зависимости от комбинации основных клинических синдромов различают 3 варианта заболевания. Полиморфизм проявлений влечет за собой определенные затруднения в диагностике заболевания, которая может быть правильно реализована только при тесном сотрудничестве специалистов в области неврологии и генетики.
Причины болезни Мачадо-Джозефа
Ранее этиология была неизвестна. Благодаря развитию ДНК-исследований, выяснилось, что основным субстратом патологии выступает генная мутация, которая передается потомству аутосомно-доминантным путем. Аберрация локализуется в 14-й хромосоме (локус 14q24.3-q32) и заключается в экспансии (увеличении количества повторов) тринуклеотидного сочетания «цитозин-аденин-гуанин». Число повторов триплета ЦАГ существенно варьирует и в среднем составляет 62-84, в то время как в норме не превышает 37. Чем оно больше, тем ранее возникает манифестация болезни.
Морфологически наблюдается апоптоз нейронов зернистого слоя и клеток Пуркинье в коре мозжечка, дегенеративные изменения зубчатого и красного ядер, черной субстанции, моторных ядер черепно-мозговых нервов и передних рогов спинного мозга, спиномозжечковых трактов. В полосатом теле выявляются глиальные разрастания. Отличительной особенностью является интактность олив продолговатого мозга.
Клинические варианты болезни Мачадо-Джозефа
Болезнь Мачадо-Джозефа I тип манифестирует в возрастном периоде 10-30 лет. Характеризуется сочетанием пирамидных и экстрапирамидных симптомов. Пирамидный синдром (поражение кортикоспинальных трактов) обычно дебютирует спастическим парапарезом, затем присоединяется слабость в руках, парез мышц глотки с развитием дисфагии и дизартрии, парез глазодвигательных нервов с офтальмоплегией (симптом «фиксированных глазных яблок»). Наблюдается клонус стоп, патологические рефлексы. Экстрапирамидный синдром проявляется симптомами торсионной дистонии, атетозом, вторичным паркинсонизмом. Формируется скованная медленная походка с широкой расстановкой ног. Отмечается шаткость при ходьбе, обусловленная спастикой мышц, а не атаксией. Типичен экзофтальм, крупные фасцикулярные сокращения языка, не сопровождающиеся его атрофией. Возможны фасцикуляции мимических мышц, миокимия век. Наблюдается вертикальный и горизонтальный нистагм, саккады (однонаправленные движения глаз) с повышенной/пониженной амплитудой.
Болезнь Мачадо-Джозефа II тип дебютирует в период от 20 до 40 лет. Проявляется симптомами мозжечковой атаксии: абазией, гипер- и дисметрией, нарушением равновесия, дизартрией. Типично сочетание мозжечковой симптоматики с пирамидными и экстрапирамидными проявлениями, встречающимися при типе I. Офтальмоплегия и фасцикуляции наблюдаются гораздо реже, чем при болезни Мачадо-Джозефа I типа.
Болезнь Мачадо-Джозефа III тип представляет собой комбинацию мозжечковой атаксии и амиотрофий. Имеет наиболее позднее начало — после 40-летнего возраста. На фоне мозжечковых симптомов наблюдаются диффузные мышечные атрофии, сопровождающиеся гипотонией и слабостью, утратой сухожильных рефлексов. Отличительной особенностью выступает наличие расстройств всех видов чувствительности по дистальному типу, свидетельствующее о полиневропатии. Экзофтальм и лицевые фасцикуляции встречаются по различным данным у 20-50% пациентов с этой формой заболевания. Дегенерация кортикоспинальных трактов и поражение экстрапирамидной системы не характерны.
Диагностика болезни Мачадо-Джозефа
Большая вариабельность количества повторов триплета ЦАГ, наблюдаемая даже в пределах одной семьи, обуславливает значительный полиморфизм клинических проявлений болезни Мачадо-Джозефа, влекущий за собой существенные диагностические трудности. Распространенным является наличие различных типов заболевания у кровных родственников, особенно, если речь идет о разных поколениях. Описаны казуистические случаи, когда паркинсонизм выступал ведущим и единственным проявлением болезни. Таким образом, ключевым моментом в диагностике болезни Мачадо-Джозефа выступает консультация генетика, подробное исследование генеалогического древа с осмотром как можно большего числа родственников больного, проведение ДНК-диагностики.
С точки зрения невролога важным является выявление специфических отличий синдрома паркинсонизма, типичных для болезни Мачадо-Джозефа. Отсутствуют патогномоничные для болезни Паркинсона постуральные расстройства и тремор покоя, а неустойчивость в положении стоя и при ходьбе связана с статико-локомоторной атаксией. Паркинсонизм оказывается устойчивым к действию препаратов леводопы, хотя в начальных стадиях болезни может наблюдаться эффект в виде уменьшения мышечной ригидности.
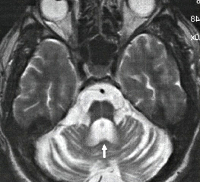
Первичная неврологическая диагностика (Эхо-ЭГ, ЭЭГ, РЭГ) не дает специфичных признаков, ее результаты могут быть в пределах нормы. КТ и МРТ головного мозга выявляет дегенерацию червя мозжечка и покрышки моста. Типичным признаком является выраженное расширение IV желудочка на фоне относительной сохранности мозжечковой коры. Дифференцируют болезнь Мачадо-Джозефа от других видов спиноцеребеллярных дегенерации, болезни Галлервордена-Шпатца, оливопонтоцеребеллярной дегенерации, атаксии Фридрейха, бокового амиотрофического склероза, атаксии Пьера-Мари, прогрессивного супрануклеарного паралича.
Лечение и прогноз болезни Мачадо-Джозефа
Эффективная терапия пока не найдена. Проводится симптоматическое лечение. При синдроме паркинсонизма показаны агонисты дофамина ( прамипексол, пирибедил), может применяться амантадин. Для снятия спастики назначаются фармпрепараты с миорелаксирующим действием (толперизон, баклофен). При гиперкинезах рекомендованы производные вальпроевой к-ты или бензодиазепины (клоназепам).
К сожалению, во многих случаях симптоматическая терапия оказывается не способной остановить прогрессирование болезни Мачадо-Джозефа. Наблюдается неуклонное усугубление симптоматики, приводящее к гибели пациента. Продолжительность жизни после дебюта заболевания составляет от 10 до 20 лет и зависит от клинического типа патологии. Наиболее скоротечным вариантом является болезнь Мачадо-Джозефа I типа. Профилактика заключается в проведении медико-генетического консультирования и пренатальной диагностики в отягощенных семьях; недопущении рождения ребенка, имеющего соответствующую генетическую мутацию.
Болезнь Мачадо-Джозефа
Болезнь Мачадо-Джозефа — довольно редкое неврологическое расстройство, проявляющееся в отсутствии мышечного контроля, что со временем при ненадлежащем лечении приводит к постепенному вырождению заднего мозга и гибели пациента.
Диагностика осуществляется посредством оценки клинических проявлений патологии как у самого больного, так и у его ближних родственников, проведении КТ и МРТ пациенту, а также оценки копии триплета ЦАГ.
К сожалению, для постановки правильного диагноза обойтись исключительно визитом к врачу не получится, так как только комплексная диагностика может выявить заболевание даже на начальной стадии, что предоставит возможность специалисту назначить своевременную терапию.
Синдром Мачадо-Джозефа может проявить первые признаки у людей с 10 до 70 лет — довольно широкий возрастной диапазон, во время которого заболевание проявляет себя. Вследствие мультисистемного поражения спинальных и церебральных структур, проявления патологического процесса могут быть самыми разнообразными, что очень часто становится причиной постановки неправильного диагноза.
В зависимости от выраженности синдромов и характерных жалоб пациентов, принято различать три типа патологии. Множество форм проявлений очень сильно затрудняет диагностические мероприятия. Диагностика может быть осуществлена при совместной работе генетиков и неврологов. Только комплексная диагностика, проведенная при помощи новейших диагностических методик, которая будет оцениваться различными специалистами, способна предоставить максимально развернутую информацию, на основании которой будет поставлен правильный диагноз.
Причины

Однако, с течением времени и по мере развития ДНК-исследований стало ясно, что главными причинами болезни выступает мутация генов, передаваемая по наследству аутосомно-доминантным путем.
Таким образом удалось выяснить, что заболевание имеет наследственный характер. Отклонения от нормы наблюдаются в 14 хромосоме и сводятся к экспансии комбинации «цитозин-аденин-гуанин». Количество повторов триплета ЦАГ очень сильно различается, в среднем показатели держатся в диапазоне от 62 до 84. Для сравнения: в норме эта цифра не должна быть выше 37. Чем данный показатель выше, тем раньше возникает болезнь у человека.
У больных возникает апоптоз нейронов в коре головного мозга, дегенеративные процессы красного и зубчатого ядер, моторных ядер ЧМ-нервов. Поражение зон мозга приводит к возникновению целого ряда признаков, которые по мере развития патологии и отсутствия соответствующего лечения начинают тревожить больного. Специалисты сходятся во мнении, что от момента возникновения патологии до проявления первых ее симптомов проходит от 3 до 6 месяцев, но многое зависит также от индивидуальных особенностей организма – у одних больных патология может проявиться значительно раньше, у других – позже.
Клинические варианты патологии

Со временем развиваются патологические рефлексы, клонус стоп. Больные начинают испытывать трудности при передвижении, походка становится неуклюжей, скованной, при этом человек ходит с широко расставленными ногами. Очень часто такие пациенты сильно шатаются во время ходьбы. Нередко у больных смещаются глазные яблоки вперед, возникают значительные фасцикулярные сокращения языка, мимических мышц, глазных век. Имеют место быть непроизвольные движения глаз высокой частоты.
Патология второго типа возникает чаще всего с 20 до 40 лет. Симптомы заболевания проявляются в мозжечковой атаксии: возникает дизартрия, больной не способен сохранять равновесие, появляется абазия. Характерной комбинации мозжечковых и пирамидных признаков, но второй тип имеет некую схожесть с первым типом болезни.
Патология третьего типа выражается в комбинации амиотрофий и мозжечковой атаксии. Данный тип заболевания возникает довольно поздно – как правило, только после 40 лет. У больных появляется мышечная атрофия, которая проявляется сильной слабостью и полной потерей сухожильных рефлексов. Особенностью данного типа болезни является наличие всех видов расстройств чувствительности по дистальному типу. Дегенеративные изменения в кортикоспинальных трактах и поражение экстрапирамидной системы не наблюдается.
Диагностика

Известны случаи, когда только одно из проявлений позволяло заподозрить наличие болезни у разных людей, имеющих между собой родственную связь. Одним из важнейших моментов в диагностике заболевания является консультация генетика, который осуществляет исследование генеалогического древа, учитывая большое количество родственников, а также проводя ДНК-исследование.
Немаловажным является и посещение невролога. Врач проведет первичный осмотр, по результатам которого выявит отличия болезни от других заболеваний.
К сожалению, в некоторых случаях осмотр у невролога не позволяет выявить характерные признаки заболевания из-за стертой клинической картины, поэтому врач может только заподозрить патологию, но поставить такой диагноз без более подробного обследования не получится. Пациентов с подозрениями на данный недуг в обязательном порядке направляют на КТ и МРТ, а после чего врач-рентгенолог определит наличие изменений в головном мозге. Важно понимать, что только обследование, проведенное на современных аппаратах, предоставит возможность врачам дать оценку возникшим изменениям в структуре головного мозга, на основании которых будет поставлен правильный диагноз.
Лечение и прогноз
Однако, полного выздоровления не наступает даже при правильной терапевтической тактике. Если имеет место быть синдром паркинсонизма, назначают агонисты дофамина, иногда пациентам показано применение амантадина. С целью снятия спастики выписываются лекарственные препараты с миорелаксирующим действием.
Как уже говорилось выше, почти всегда даже хорошее лечение не сможет остановить дальнейшее развитие заболевания, поэтому с течением времени у больных появляются новые симптомы патологии, что в конечном итоге приводит к смерти. Согласно официальным статистическим данным, после выявления заболевания до гибели больного проходит от 10 до 20 лет.
Продолжительность жизни имеет прямую связь с типом заболевания. Неблагоприятный прогноз имеет первый тип Масадо-Джозефа, больные с таким диагнозом, как правило, не живут дольше 10 лет после начала прогрессирования патологии.
Профилактические мероприятия сводятся к проведению пренатальной диагностики, а также в получении консультации у генетиков. Если у ближайших родственников был диагностирован синдром Мачадо-Джозефа, важно со всей ответственностью подходить к планированию и рождению ребенка, так как генная мутация может передаться по наследству. Многие генетики сходятся во мнении, что очень важно не допускать рождение ребенка, у которого имеется характерная генетическая мутация.
Болезнь Мачадо – Джозефа (MJD), также известен как Азорская болезнь Мачадо – Джозефа, Болезнь Мачадо, Болезнь Иосифа или спиноцеребеллярная атаксия 3 типа (SCA3), является редким аутосомно-доминантно унаследованный нейродегенеративный болезнь, вызывающая прогрессирующее мозжечок атаксия, [1] [2] что приводит к отсутствию мышечный контроль и координация из верхний и нижние конечности. [3] Симптомы вызваны генетическим мутация что приводит к увеличению количества аномальных тринуклеотидных повторов «CAG» в ATXN3 ген [1] что приводит к аномальной форме белка атаксин что вызывает дегенерацию клеток в задний мозг. [3] Из-за некоторых симптомов, таких как неуклюжесть и жесткость, MJD обычно принимают за пьянство или болезнь Паркинсона.
Содержание
Симптомы
Симптомами MJD являются нарушения памяти, [4] спастичность, трудности с речью и глотанием, слабость в руках и ногах, неуклюжесть, частое мочеиспускание и непроизвольные движения глаз. Симптомы могут начаться в раннем подростковом возрасте и со временем ухудшаются. В конце концов, MJD приводит к параличу; однако интеллектуальные функции обычно остаются прежними. [ нужна цитата ]
Генетика
Флорес и Сан-Мигель являются очагами болезни Мачадо – Джозефа в Азорские острова. [5]
Болезнь Мачадо Джозефа имеет множественное происхождение, поскольку SCA3 происходит от гаплотипа четырех разных источников, а не от одного происхождения на Азорских островах. Япония, Бразилия и Франция все они были эффектами основателя в областях с SCA3. [6]
В Китаймутация, вызывающая SCA типа 3, произошла от 8000 до 17000 лет назад. [11]
В Японии самая старая причинная мутация произошла около 5774 +/- 1116 лет назад. [12]
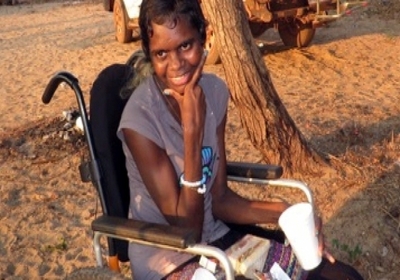
Среди австралийских аборигенов мутация-основатель, по-видимому, произошла около 7000 лет назад. Поскольку эта мутация характерна для других семей, живущих в Азии, вполне вероятно, что она была импортирована в Австралию. [13]
MJD затронул азорцев, и у японцев были общие гаплотипы, в то время как у азорцев также были гаплотипы двух разных источников. [14]
Патофизиология
В мосты (сооружение, расположенное на мозговой ствол) является одной из областей, затронутых MJD. В полосатое тело (область мозга, связанная с балансом и движением) также поражена этим заболеванием, что может объяснить как основные двигательные проблемы, вызываемые MJD: сжатие и скручивание конечностей, так и резкие, нерегулярные движения. [16]
В пораженных клетках этот белок накапливается и собирает внутриядерные тельца включения. Предполагается, что эти нерастворимые агрегаты нарушают нормальную активность ядра и вызывают дегенерацию и гибель клетки. [ нужна цитата ]
Диагностика
MJD можно диагностировать, распознав симптомы болезни и взяв семейный анамнез. Врачи задают пациентам вопросы о типах симптомов, которые были у родственников с заболеванием, о прогрессировании и резкости симптомов, а также о возрасте начала заболевания у членов семьи. [ нужна цитата ]
Пресимптоматический диагноз MJD может быть установлен с помощью генетического теста. [17] Прямое обнаружение генетической мутации, ответственной за MJD, доступно с 1995 года. [18] Генетическое тестирование проверяет количество повторов CAG в кодирующей области гена MJD / ATXN3 на хромосоме 14. Тест покажет положительный результат на MJD, если эта область содержит 61-87 повторов, в отличие от 12-44 повторов, обнаруженных у здоровых людей. лиц. Ограничение этого теста заключается в том, что если количество повторов CAG у испытуемого человека находится между нормальным и патогенным диапазоном (45-60 повторов), то тест не может предсказать, будут ли у человека симптомы MJD. [17]
Классификация
Есть пять подтипов MJD. [1] которые характеризуются возрастом начала и диапазоном симптомов. Подтипы иллюстрируют широкий спектр симптомов, которые могут испытывать пациенты. [1] Однако отнесение людей к конкретному подтипу заболевания имеет ограниченное клиническое значение. [1]
лечение
Нет лекарства от болезни Мачадо-Джозефа. Однако для некоторых симптомов доступны методы лечения. [1] [3] Например, спастичность можно уменьшить с помощью спазмолитических препаратов, таких как баклофен. Симптомы паркинсонизма можно лечить с помощью леводопа терапия. Призменные очки могут уменьшить диплопические симптомы. [3] Физиотерапия/Физиотерапия и / или трудотерапия может помочь пациентам, выписав средства передвижения повысить независимость пациентов, обеспечивая тренировка походки, и прописывать упражнения для поддержания подвижности различных суставов и общего состояния здоровья, чтобы снизить вероятность падений или травм в результате падений. Ходунки и инвалидные коляски могут очень помочь пациенту в повседневных задачах. Некоторые пациенты будут испытывать трудности с речь и глотание, поэтому Речевой патолог может помочь пациентам улучшить свои коммуникативные способности и проблемы с глотанием. [3]
Прогноз
Ожидаемая продолжительность жизни пациентов с тяжелыми формами MJD составляет около 35 лет. Те, у кого легкие формы, имеют нормальную продолжительность жизни. Причиной смерти тех, кто умирает рано, часто является аспирационная пневмония. [3]
История
Заболевание впервые было выявлено в 1972 году. [19]
В отличие от многих других заболеваний, болезнь Мачадо – Джозефа не названа в честь исследователей. Он назван в честь двух мужчин («Уильям Мачадо» и «Антон Джозеф»), которые были патриархами семей, в которых изначально было описано состояние. [20] Самый высокий показатель распространенности этого заболевания в Австралии. Грут Эйландт где 5% населения в настоящее время имеют симптомы или находятся в группе риска, [21] за которым следует азорский остров Флорес где примерно 1 из 140 человек в популяции имеет диагноз MJD. [22]
Известные случаи
Бразильский комик, актер и телеведущий Гильерме Карам была диагностирована болезнь Мачадо – Иосифа, унаследованная от матери, как и его брат и сестра. [23] Он умер 7 июля 2016 года. [24] В видео на Facebook через несколько дней после смерти Карама бразильский деятель, журналист и телеведущий, Арнальдо Дюран публично признал свою болезнь Мачадо-Джозеф. Бразильская пресса уделила огромное внимание обоим случаям. [25]
Этическое соображение
Специалисты по этике использовали болезнь Мачадо – Джозефа как парадигматическую болезнь, чтобы обсудить права сообщества пациентов контролировать «право собственности» на свое заболевание, особенно когда речь идет об исследованиях генетического тестирования. [26] Кроме того, поскольку в настоящее время не существует клинического вмешательства для предотвращения появления симптомов заболевания, существует дискуссия о том, следует ли людям проходить тестирование или нет. [18] Преимущества тестирования MJD включают уменьшение беспокойства и неуверенности, а также способность планировать будущее. К некоторым недостаткам можно отнести ожидание отрицательных результатов и трудности человека в адаптации к этому результату. [ нужна цитата ]
Этнографический пример изучения некоторых социальных и этических последствий жизни с болезнью Мачадо – Джозефа см. В João Biehl’s Vita: Жизнь в зоне отказа от общества (Беркли: Калифорнийский университет Press, 2006).