Масло кыст аль хинди что это
Можно ли вылечить рак
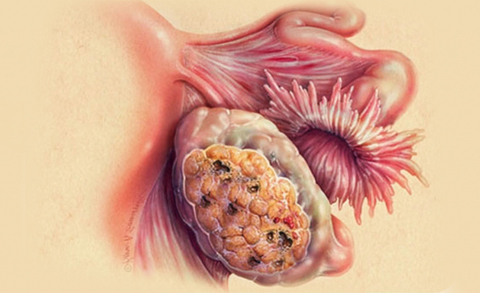
Злокачественная опухоль — крайне серьезное заболевание, требующее немедленного медицинского вмешательства. Однако на современном уровне развития науки такой диагноз еще не означает окончательного приговора.
Сегодня раковые опухоли поддаются лечению. Его эффективность не всегда хорошо предсказуема, но это лишь подтверждает тот факт, что даже если вам поставили угрожающий жизни диагноз, ни в коем случае нельзя опускать руки! Вполне возможно, что именно в вашей ситуации какой-то из методов лечения даст выраженный результат и поможет победить эту опасную патологию.
Как можно вылечить рак
На настоящий момент медицина имеет три крупные группы лечебных методик. Их можно применять как по отдельности, так и в различных сочетаниях:
1. Операционное вмешательство. Самый радикальный, но и самый эффективный способ лечения. Задача хирурга — как можно более полно удалить обнаруженные злокачественно перерожденные ткани.
К сожалению, сделать операцию получается не всегда. Например, если опухоль распространилась на слишком большую часть жизненно важного органа или уже появились отдаленные метастазы. В этом случае хирургическое вмешательство может быть признано нецелесообразным. Можно ли вылечить рак без операции? Теоретически — да. Но если врачи увидят, что при помощи лекарств получилось уничтожить метастазы, основной злокачественный очаг они все равно порекомендуют удалить хирургически. Повторимся: операция — самый эффективный способ избавления от опухоли.
2. Лечение препаратами. Сюда относится как традиционная химиотерапия, так и все новые наработки в области фармакологического лечения опухолей — иммунотерапия, таргетное лечение и др.
3. Воздействия ионизирующего излучения. Опухолевые клетки в силу быстрого метаболизма активнее поглощают радиацию. А следовательно, и намного быстрее погибают под ее влиянием. Именно это и лежит в основе лечения злокачественных новообразований лучевой терапией.
Хотите мы вам перезвоним?
Какие бывают стадии рака
Упрощенная классификация злокачественных новообразований предполагает разделение процесса развития опухоли на пять стадий:
Стадия 0
Так называемый рак на месте. Самый ранний этап развития опухоли, когда измененных клеток еще совсем мало, и они находятся только лишь в слизистой оболочке органа. Вылечить такое заболевание можно быстро и легко, попросту убрав это скопление клеток. Но проблема в том, что обнаружить опухоль на нулевой стадии практически невозможно, так как невооруженным глазом (а чаще всего и без специальных гистологических исследований!) она не видна.
Стадия I
Это начальный этап клинического процесса, когда злокачественно перерожденные клетки только образовали очаг. В этот момент вылечить опухоль также совсем несложно — поможет простая операция по удалению такого очага. Однако и на данном этапе найти опухоль и даже заподозрить ее существование очень непросто. При этом, здесь уже вполне работают скриниговые обследования (ранняя диагностика). Проходя их с определенной периодичностью, вы существенно повышаете свои шансы на раннее обнаружение опухоли, а значит, и на полное избавление от нее.
Стадия II
На данном этапе опухоль начинает разрастаться, но пока не выходит за пределы одного органа. Однако уже на этой стадии могут появляться вторичные опухолевые очаги в ближайших лимфатических узлах. Клинические проявления здесь пока либо отсутствуют, либо выражены слабо.
Стадия III
Новообразование прорастает в соседние органы и поражает большинство лимфатических узлов, расположенных в этой области. У пациента появляется выраженная симптоматика, которая заставляет его обратиться к врачу. Можно ли вылечить III стадию рака — зависит от вида опухоли. Но если вовремя прооперировать пациента, а потом провести интенсивную химио- или лучевую терапию, шансы на полное излечение довольно высоки.
Стадия IV
В эту стадию онкологическое заболевание переходит тогда, когда начинает давать метастазы в отдаленные органы и ткани. Это самая серьезная степень развития опухоли, на которой хирургическое лечение не всегда оказывается целесообразным. Можно ли вылечить онкологию на 4 стадии — сложный вопрос, ответ на который зависит от большого количества индивидуальных особенностей каждого клинического случая. Тем не менее шансы есть даже при наличии отдаленных метастазов.
Важно сказать, что вышеприведенная классификация по стадиям весьма условна. Дело в том, что опухоли разных органов, происходящие из разных типов клеток, могут иметь отличающееся клиническое течение, динамику развития, а следовательно, нести разную угрозу жизни пациента. Так, например, опухоль мозга уже на условной II стадии может привести к летальному исходу. А на вопрос, можно ли полностью вылечить рак IV стадии предстательной железы, положительный ответ можно дать с вероятностью около 30%.
Именно поэтому специалисты-онкологи используют более сложную, но и более объективную классификацию по системе TNM. Здесь каждая опухоль рассматривается индивидуально и описывается тремя основными параметрами с цифровыми индексами:
Соответственно, каждая опухоль может быть кодирована специфическим шифром. Например: T2N1M0 — новообразование имеет довольно большой размер, находится в пределах одного органа, уже поразило ближайшие лимфоузлы, но еще не дало метастазов. Такая опухоль примерно соответствует второй стадии по упрощенной классификации.
Каковы прогнозы выживаемости на разных стадиях
Здесь невозможно привести цифры, которые обладали бы хоть каким-то универсальным значением. Разброс, зависящий от типа опухоли, ее молекулярно-генетических характеристик и других индивидуальных особенностей, слишком велик. На вопрос «можно ли вылечить рак IV стадии с метастазами», ответ будет положительным. Но с тем учетом, что для каждого пациента вероятность излечения сильно отличается.
Однозначно можно сказать только одно — чем выше стадия развития опухоли, тем хуже прогноз. И если на стадии «0» или «I» почти для всех видов рака выживаемость составляет 90-100%, то на стадии IV она обычно не превышает 5-7%. Хотя эти значения могут сильно отличаться. По данным Американского онкологического общества, пятилетняя выживаемость при IV стадии опухоли составляет для рака:
Итак, главный вывод данной статьи — тот факт, что рак излечим, а шансы победить его есть на любой стадии развития. Конкретный ответ на вопрос «можно ли вылечить рак III или IV стадии» зависит от множества параметров клинического случая. Но чем раньше будет выявлена опухоль, тем выше вероятность от нее избавиться. А значит самым эффективным способом увеличить эту вероятность будет периодическое прохождение скрининговых профилактических обследований.
Восстановление легких после коронавируса
Восстанавливаются ли легкие после COVID-19? Да. Но нужно не пропустить сроки реабилитации и серьёзно отнестись к рекомендациям врача.
Новая коронавирусная инфекция, вызванная SARS-CoV-2, недостаточно изучена, однако ясно, что она наносит вред всем органам и тканям человека. Вирус проникает в организм через слизистые оболочки носа, глаз, глотки. Первые симптомы появляются на 2-14 день. Обычно это повышение температуры выше 37.5 градусов Цельсия, насморк, потеря обоняния, сухой кашель, послабление стула, слабость и головная боль. На 6–10 сутки от момента появления первых симптомов могут начать беспокоить одышка, боль в груди, усиление кашля. Это тревожные симптомы, говорящие о поражении легких и требующие проведения дополнительного обследования: компьютерной томографии легких, измерения насыщения крови кислородом (сатурации).
Легкие после COVID-19
Попадая в организм человека через слизистые оболочки дыхательных путей SARS-CoV-2 вызывает мощнейшую воспалительную реакцию. Активируются иммунные клетки, вырабатывается колоссальное количество воспалительных веществ (воспалительных цитокинов). Интенсивность этой реакции скорее всего обусловлена генетически. Именно интенсивностью воспалительной реакции и определяется тяжесть поражения легочной ткани по данным исследований. В легочной ткани поражение при COVID-19 обусловлено как поражением самих альвеол (в которых происходит газообмен и кровь насыщается кислородом из воздуха) нашими собственными иммунными клетками так и поражением легочных сосудов, оплетающих альвеолы. Степень поражения легких можно определить при помощи КТ (компьютерной томографии).
Таблица 1. Поражение лёгких при COVID-19
Процент поражения легочной ткани
Поражена часть лёгкого. Небольшое затруднение дыхания.
Гинеколог рассказала, как можно вылечить эрозию без прижигания
Наверное, каждая девушка слышала про эрозию шейки матки. Это заболевание является одним из самых распространенных в гинекологии.
Часто женщина даже и не знает, что у нее какие-либо патологии шейки матки, поскольку никаких явных симптомов эрозия не вызывает. Обнаружить ее можно только при проведении такого исследования как кольпоскопия. Что это такое и почему она нужна каждой современной девушке рассказывает врач-гинеколог Бакшанская Инесса Владимировна.
Инесса Владимировна, по каким симптомам Вы понимаете, что пациентке необходима кольпоскопия?
Все зависит от цитологического анализа мазка. Если результат показывает наличие воспаления, то кольпоскопия показана. Хотя девушка ни на что особо не жалуется, а при осмотре зеркалом шейка кажется чистой.
Вообще кольпоскопию желательно делать ежегодно, и женщинам с эрозией, и женщинам без показаний.
Как проходит кольпоскопия?
Кольпоскопия делается во время стандартного осмотра на кресле. Сначала при помощи кольпоскопа шейка смотрится под увеличением. Затем участки окрашиваются слабым раствором уксусной кислоты, смотрим как слизистая реагирует. Далее наносится проба люголем (йодом). Если окрашивание показывает настораживающую картину, то необходимо проведение биопсии и планирование дальнейшего лечения.
Также необходимо обследоваться на вирус папилломы человека (ВПЧ), и инфекции передаваемые половым путем. Результаты этих обследований очень важны для дальнейшей тактики лечения. Наличие ВПЧ увеличивает риск развития рака шейки матки.
Не вреден ли уксус?
Вы упомянули эрозию шейки матки. Об этом заболевании множество противоречивой информации: нужно ли лечить, как лечить?
Не лечить эрозию можно только в одном случае: девушке нет 25 лет, и при этом эрозия не осложненная (не воспаленная). Если же цитология показывает воспалительный процесс, то лечение необходимо. Будет ли это деструкция (прижигание) или, например, плазмолифтинг, решается в конкретном случае.
Почему гинекологи раньше не трогали эрозию у не рожавших женщин? Потому что было неизвестно, как прижигание скажется на раскрытии шейки матки во время родов. Но сегодня для «прижигания» мы применяем один из самых щадящих методов – радиоволновой, он не оставляет рубцов на шейке, поэтому показан для нерожавших девушек.
Но, хочу обратить внимание женщин с не осложненной эрозией! Вам необходимо крайне внимательно следить за своим здоровьем: очаг имеет свойство расти, углубляться. Главное, не допустить развития дисплазии и предраковых состояний.
Нет, совсем наоборот. Плазмолифтинг или PRP-терапия метод не деструктивный, а восстанавливающий. Когда плазма попадает под кожу – запускается процесс биологических реакций, происходит регенерация слизистой оболочки шейки матки. Необходимо от 3-4 сеансов, и можно увидеть, как эрозия затягивается.
В отличие от других процедур, плазмолифтинг действует на орган в целом, помогая значительно ускорить не только время лечения эрозии, но и полностью восстановить слизистую оболочку и поврежденные соседние ткани.
Существуют 2 основных методики: микроинъекции в шейку матки, либо постановка тампонов с плазмой на определенное время.
Помимо лечебного эффекта, плазмолифтинг повышает тонус мышц тазового дня, уменьшает послеродовые стрии, устраняет дискомфорт в интимной жизни.
Масло кыст аль хинди что это
Кафедра акушерства и гинекологии, неонатологии, анестезиологии и реаниматологии, ФГБУ «Ивановский научно-исследовательский институт материнства и детства им. В.Н. Городкова» Минздрава России (дир. — д.м.н. А.И. Малышкина), Иваново, Россия
ФГБУ «Ивановский научно-исследовательский институт материнства и детства им. В.Н. Городкова» Минздрава России, Иваново, Россия
ФГБУ «Ивановский научно-исследовательский институт материнства и детства им. В.Н. Городкова» Минздрава России, Иваново, Россия
ФГБУ «Ивановский научно-исследовательский институт материнства и детства им. В.Н. Городкова» Минздрава России
ФГБУ «Ивановский научно-исследовательский институт материнства и детства им. В.Н. Городкова» Минздрава России, Иваново, Россия
Инфекция шейки матки, ассоциированная с 52, 58 и 59-м типами вируса папилломы человека
Журнал: Российский вестник акушера-гинеколога. 2015;15(5): 10-14
Парейшвили В. В., Вахромеев А. П., Ситникова О. Г., Назаров С. Б., Кузьменко Г. Н. Инфекция шейки матки, ассоциированная с 52, 58 и 59-м типами вируса папилломы человека. Российский вестник акушера-гинеколога. 2015;15(5):10-14.
Pareishvili V V, Vakhromeev A P, Sitnikova O G, Nazarov S B, Kuzmenko G N. Cervical infection associated with human papillomavirus types 52, 58, and 59. Russian Bulletin of Obstetrician-Gynecologist. 2015;15(5):10-14.
https://doi.org/10.17116/rosakush20151544-9
Кафедра акушерства и гинекологии, неонатологии, анестезиологии и реаниматологии, ФГБУ «Ивановский научно-исследовательский институт материнства и детства им. В.Н. Городкова» Минздрава России (дир. — д.м.н. А.И. Малышкина), Иваново, Россия
Цель исследования — определение интенсивности свободнорадикальных процессов и антиоксидантной активности у беременных с недифференцированной дисплазией соединительной ткани. Материал и методы. Основную группу составили 60 беременных, которые были обследованы в сроки беременности 22, 36 и 40 нед с недифференцированной дисплазией соединительной ткани. В контрольную группу включены 30 соматически здоровых беременных с физиологическим течением беременности. Изучено функциональное состояние плацентарной системы при помощи ультразвукового исследования и допплерометрии, реактивность сердечно-сосудистой системы плода с помощью кардиотокографа. Свободнорадикальное окисление и антиоксидантную активность определяли методом индуцированной хемолюминесценции. Результаты. Установлено, что синдром недифференцированной дисплазии соединительной ткани во время беременности сопровождается развитием окислительного стресса и повышением антиоксидантной активности. Заключение. Недифференцированная дисплазия соединительной ткани, имеющая генерализованный характер ее поражения с вовлечением в патологический процесс репродуктивной системы, отражается на течении беременности и родов. Результаты хемолюминесцентного анализа свидетельствуют о высокой концентрации свободных радикалов, развитии окислительного стресса, повышении антиоксидантной активности в организме женщин с недифференцированной дисплазией соединительной ткани, что диктует необходимость дальнейших исследований для определения комплекса диагностических и профилактических мер при недифференцированной дисплазии соединительной ткани и беременности. Авторы информируют об отсутствии конфликта интересов.
Кафедра акушерства и гинекологии, неонатологии, анестезиологии и реаниматологии, ФГБУ «Ивановский научно-исследовательский институт материнства и детства им. В.Н. Городкова» Минздрава России (дир. — д.м.н. А.И. Малышкина), Иваново, Россия
ФГБУ «Ивановский научно-исследовательский институт материнства и детства им. В.Н. Городкова» Минздрава России, Иваново, Россия
ФГБУ «Ивановский научно-исследовательский институт материнства и детства им. В.Н. Городкова» Минздрава России, Иваново, Россия
ФГБУ «Ивановский научно-исследовательский институт материнства и детства им. В.Н. Городкова» Минздрава России
ФГБУ «Ивановский научно-исследовательский институт материнства и детства им. В.Н. Городкова» Минздрава России, Иваново, Россия
Высокая распространенность папилломавирусной инфекции (ПВИ), ее доказанная роль в развитии злокачественных новообразований половых органов свидетельствуют об актуальности данной проблемы. В настоящее время известно более 150 типов вируса папилломы человека (ВПЧ), 40 из которых вызывают заболевания аногенитальной области. По степени канцерогенного риска согласно классификации IARC (International Agency for Research on Cancer), в 2012 г. выделено три группы ВПЧ: канцерогенные — 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58 и 59-й (1-я группа), вероятно канцерогенные — 26, 30, 34, 53, 66, 67, 68, 70, 73, 82, 69, 85 и 97-й (2-я группа: 2А, 2В), неканцерогенные — 6, 11-й и др. (3-я группа). Все типы подразделены на определенные филогенетические группы. Наибольший клинический интерес представляет филогенетическая группа α, к которой относятся следующие типы ВПЧ высокого онкогенного риска (ВПЧ ВР): α5 (ВПЧ 51), α6 (ВПЧ 56), α7 (ВПЧ 18, ВПЧ 39, ВПЧ 45, ВПЧ 59), α9 (ВПЧ 16, ВПЧ 31, ВПЧ 33, ВПЧ 35, ВПЧ 52, ВПЧ 58) [1, 2]. Разделение по группам важно для динамического наблюдения за вирусной инфекцией и более точного прогнозирования ее развития, так как разные типы ВПЧ обладают разным онкогенным потенциалом, а также способностью к персистенции [3, 4].
Известно, что распространенность различных генотипов ВПЧ, как в разных регионах мира, так и в России варьирует. В настоящее время условно выделяют «европейские» (16, 18, 31, 33, 45-й и т. д.) и «азиатские» типы ВПЧ (52, 58, 59, 65-й и др.). ВПЧ 52-го и 58-го типов принадлежат к филогенетической группе α9, ВПЧ 59-го типа относятся к группе α7 (обе группы являются наиболее вирулентными для эпителия шейки матки), и данные типы вирусов представляют большой клинический интерес [5]. Следует отметить, что ВПЧ 52-го и 58-го типов 20 лет назад встречались крайне редко либо не встречались вообще, в то время как в настоящее время их доля составляет от 5,7 до 30,8% [6]. Установлено, что риск развития плоскоклеточной карциномы по классификации IARC выше для ВПЧ 52-го и 58-го типов, 59-го типа — 1,08, риск развития аденокарциномы выше для ВПЧ 59-го типа.
По данным метаанализа 2012 г., включающего 437 исследований, получены следующие данные: для ВПЧ 52-го типа общая инфицированность составила 8%, число случаев выявления ВПЧ 52-го типа при CIN I составило 13,8%, при CIN II — 16,4%, CIN III — 10,2%, при инвазивном раке — 3,5%. Общая распространенность ВПЧ 58-го типа составила 6,3%, при CIN I — 9,6%, CIN II — 12%, CIN III — 9%, при инвазивном раке — 4,4%. ВПЧ 59-го типа имеет распространенность 3,1%, при CIN I выявление составило 5%, CIN II — 4,7%, CIN III — 2,2% при инвазивном раке — 1,3% [7]. По данным литературы, существуют разноречивые показатели распространенности «азиатских» типов ВПЧ при раке шейки матки (РШМ). Так, распространенность ВПЧ 52-го при инвазивном составляет от 2,2 до 27% [8—15], ВПЧ 58-го типа обнаруживали от 1,6 до 28,5% [5, 8, 10, 11, 13, 16, 17], ВПЧ 59-го типа — в 0,5—2,2% случаев [11, 12].
Изменение эпидемиологической ситуации в отношении ВПЧ наряду с изменением в последние годы структуры CIN [1, 6, 18, 19] диктует необходимость продолжения изучения распространенности и роли типов ВПЧ, обладающих высоким онкогенным потенциалом, при CIN. Данные по исследованию частоты выявления «азиатских» типов ВПЧ ВР, включая 52-й и 58-й типы, их роли в развитии предраковых заболеваний шейки матки в популяции женского населения России немногочисленны. Отечественными авторами показано, что 52 и 58-й типы ВПЧ являются причиной аномальной цитологии в 22,4% [20].
Цель исследования — определить особенности течения цервикальной ПВИ, ассоциированной с 52, 58 и 59-м типами ВПЧ.
Материал и методы
В проспективное исследование в результате целенаправленного отбора включены 84 пациентки в возрасте 18—58 лет с цервикальной, обусловленной 52, 58 и 59-м типами ВПЧ, обследованные на специализированном приеме по патологии шейки матки женской консультации Омска. Средний возраст инфицированных пациенток составил 29,9±1,0 года (медиана и интерквартильный размах — 27 (23,0—32,5 года). Критерии включения в исследование: возраст от 18 до 60 лет, позитивный цервикальный ВПЧ-тест на наличие 52, 58 и 59-го типов, информированное согласие пациентки. Критерии исключения: беременность и лактация, отказ от участия в исследовании.
Комплексная диагностика включала жидкостную цитологию (Bethesda, 2001); кольпоскопическое исследование; гистологическое исследование цервикальных биоптатов и эндоцервикальных образцов и расширенный скрининг для дифференциального выявления ДНК ВПЧ, включая определение ВПЧ ВР 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58 и 59-го типов методом полимеразной цепной реакции (ПЦР) в режиме реального времени (тест-система РеалБест ДНК ВПЧ ВКР генотип) [1]. При трактовке вирусной нагрузки ВПЧ учитывали порог клинической значимости — 3 lg на 10 5 клеток, порог прогрессии (более 5 lg на 10 5 клеток) [21].
Статистический анализ данных проводился с применением пакета Statistica 6, возможностей MS Excel. Во всех процедурах статистического анализа критический уровень значимости р принимался равным 0,05. Проверка нормальности распределения производилась с использованием критерия Шапиро—Уилки, проверка гипотез о равенстве генеральных дисперсий — с помощью F-критерия Фишера. Средние выборочные значения количественных признаков приведены в тексте в виде M±SE, где M — среднее выборочное, SE — стандартная ошибка среднего. При распределении значений в ряду, отличном от нормального, указывались медиана (P 0,5), 25-й перцентиль (P 0,25) и 75-й перцентиль (P 0,75). При анализе таблиц сопряженности оценивались значения информационной статистики Кульбака (статистика 2I).
Результаты
В возрасте моложе 35 лет (включительно) были 79,8±4,4% пациенток группы наблюдения. Распределение инфицирования шейки матки 52, 58 и 59-м типами ВПЧ в зависимости от возраста было следующим: ранний репродуктивный возраст (18—25 лет) — 33 пациентки, средний (26—35 лет) — 34, старше 36 лет — 17.
Проведен анализ частоты ВПЧ-ассоциированных поражений шейки матки, которые подразделяют на клиническую (экзофитная кондилома), латентную (отсутствие клинических, морфологических изменений при обнаружении ДНК ВПЧ), субклиническую форму (невидимые невооруженным глазом, бессимптомные, выявляются только при кольпоскопии и/или морфологически), CIN I—III степени и РШМ [1]. Случаев клинической формы ПВИ не наблюдалось. Среди инфицированных женщин наблюдались пациентки с CIN (46—54,8%), относительно латентной формой инфекции без клинических ее проявлений (12—14,3%), субклинической формой инфекции (24—28,6%) и РШМ (2—2,4%).
В зависимости от тяжести гистологически верифицированного предрака CIN I установлена в 51,2%, CIN II — в 32,5%, CIN III — в 16,3% наблюдений.
При анализе частоты форм ПВИ, ассоциированной с изучаемыми типами в зависимости от возраста обращало внимание отсутствие существенных различий при латентной форме во всех возрастных группах (р>0,05) (табл. 1). В свою очередь при наличии цервикальной патологии наглядно проявляется влияние возрастного фактора. Так, субклиническая форма ПВИ доминировала у пациенток раннего репродуктивного возраста по сравнению с таковой у пациенток 26—35 лет (р=0,05), у которых отмечено преобладание CIN (р=0,02). Не установлено существенных различий по степени тяжести CIN (I—III cтепени) в зависимости от возраста. Два случая РШМ, ассоциированного с 58-м типом ВПЧ, наблюдались в группе женщин старше 36 лет. Установлена прямая слабой силы, статистически значимая корреляция формы ПВИ и возраста (r S =+0,21; p=0,0517).

При изучении характера инфицирования (моно-, сочетанное) установлено, что инфицирование шейки матки с участием одного из изучаемых типов ВПЧ наблюдалось у 37 (44%) пациенток: 52-й тип — у 19, 58-й тип — у 13, 59-й тип — у 5 (табл. 2). У 44 (52,4%) женщин наблюдалось сочетание с другими типами ВПЧ ВР 16, 18, 31, 33, 35, 39, 45, 51 и 56-м (наиболее часто встречались 16, 31 и 56-й типы), в трех случаях отмечено сочетание двух из 52, 58 и 59-го типов.

Особое внимание было уделено моноинфекции изучаемых типов ВПЧ. Среди 37 женщин, у которых был выявлен один из типов (52, 58, 59-й), распределение форм заболевания было следующим: латентная — у 5 больных, субклиническая — у 12, CIN — у 19, рак — у 1. Цервикальная неоплазия (CIN и РШМ) составила при моноинфекции 20 (54%) случаев, при сочетанной форме — 28 (59,6%) случаев, что не имело статистически значимых различий (р=0,3973). Частота CIN при моноинфекции 52-го типа — 6 наблюдений из 19 данного типа, при моноинфекции ВПЧ 58-го типа — 10 из 13, при моноинфекции ВПЧ 59-го типа — 3 из 5 наблюдений, РШМ (1 случай) — при моноинфекции ВПЧ 58-го типа (рис. 1).

Проведена оценка вирусной нагрузки ВПЧ 52, 58 и 59-го типов среди 84 инфицированных женщин (включая моно- и сочетанное инфицирование) (табл. 3). В 30 случаях ее уровень был ниже порога клинической значимости, в 30 случаях вирусная нагрузка ВПЧ 52, 58 и 59-го типов была в пределах от 3 до 5 lg на 10 5 клеток, в 33 случаях вирусная нагрузка была выше порога прогрессии. Превышение порога прогрессии варьировало в диапазоне 25—46,7% в зависимости от типа ВПЧ (рис. 2).


При анализе взаимосвязи клинических форм ПВИ и уровня вирусной нагрузки установлено двукратное превышение случаев c нагрузкой, превышающей 5 lg на 10 5 клеток, у женщин с CIN: 25 против 10 (менее 3 lg на 10 5 клеток) и 11 (от 3 до 5 lg на 10 5 клеток) случаев, p=0,0091 (табл. 4).

В случае моноинфекции латентная форма не сопровождалась нагрузкой выше порога прогрессии, субклиническая форма протекала на фоне превышения порога прогрессии в 1 случае против остальных 11, в то время как ЦИН и РШМ — в 13 против 7 случаев с меньшей вирусной нагрузкой (табл. 5). Установлено наличие статистически значимой связи между тяжестью формы ПВИ и уровнем вирусной нагрузки 52, 58 и 59-го типов (2I=16,29; p 
Согласно данным исследований, основанных на большом клиническом материале, среди различных возрастных групп повышение уровня вирусной нагрузки увеличивает тяжесть поражения шейки матки ВПЧ [5, 20, 22—24]. Согласно исследованию G. Shen и соавт. [25], отмечена положительная корреляция между уровнем вирусной нагрузки и степенью поражения шейки матки. Полученные нами данные доказывают влияние вирусной нагрузки для 52, 58 и 59-го типов ВПЧ на прогрессирование цервикальной неоплазии.
Выводы
1. Среди когорты женщин с папилломавирусной инфекцией шейки матки, ассоциированной с 52, 58 и 59-м типами ВПЧ, значительная доля женщин моложе 35 лет (79,8%).
2. Установлен возрастзависимый характер частоты субклинической формы инфекции и цервикальной неоплазии у инфицированных женщин.
3. Папилломавирусная инфекция, ассоциированная с 52, 58 и 59-м типами ВПЧ, сопровождалась наличием CIN и рака шейки матки в 57,1% случаев.
4. Высокая частота цервикальной неоплазии при моноинфекции (54%), сопоставимая с ее частотой при сочетании с другими типами ВПЧ ВР (59,6%; р>0,05), а также взаимосвязь тяжести поражения с уровнем вирусной нагрузки подтверждают высокий риск формирования предрака и рака шейки матки при наличии моноинфекции 52, 58 и 59-го типов ВПЧ.