Местный фибринолиз что это такое
Фибринолиз
Содержание
Внутренний и внешний путь активизации
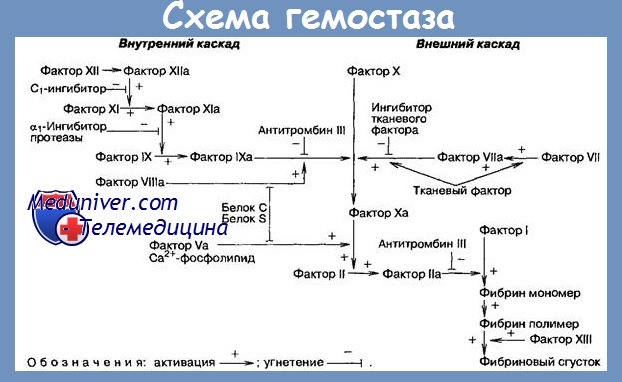
Фибринолиз, как и процесс свертывания крови, протекает по внешнему или внутреннему механизму. Внешний путь активации осуществляется при неотъемлемом участии тканевых активаторов, синтезирующихся преимущественно в эндотелии сосудов. К данным активаторам относят тканевый активатор плазминогена (ТАП) и урокиназу.
Внутренний механизм активации осуществляется благодаря плазменным активаторам и активаторами форменных элементов крови — лейкоцитов, тромбоцитов и эритроцитов. Внутренний механизм активации разделяют на на Хагеман-зависимый и Хагеман-независимый. Хагеман-зависимый фибринолиз происходит под влиянием фактора XIIа свертывания крови, калликреина, которые вызывают превращение плазминогена в плазмин. Хагеман-независимый фибринолиз происходит наиболее быстро. Его основным назначением является очищение сосудистого русла от нестабилизированного фибрина, который образуется в процессе внутрисосудистого свертывания крови.
Ингибирование фибринолиза
Фибринолитическая активность крови во многом определяется именно соотношением ингибиторов и активаторов процесса фибринолиза.
В плазме крови находятся также ингибиторы фибринолиза, подавляющие его. Одним из важнейших таких ингибиторов являются α2-антиплазмин, который вызывает связывание плазмина, трипсина, калликреина, урокиназы, тканевой активатор плазминогена. Таким образом препятствуя процессу фибринолиза на его ранних и на поздних стадиях. Сильным ингибитором плазмина является также α1-протеазный ингибитор. Также фибринолиз тормозится альфа2-макроглобулином, C1-протеазным ингибитором,и целым рядом ингибиторов активатора плазминогена, вырабатываемых в эндотелии, а также фибробластами, макрофагами и моноцитами.
Регуляция фибринолиза
Между процессами свертывания крови и фибринолизом в организме поддерживается равновесие.
Усиление фибринолиза обусловлено повышением тонуса симпатической нервной системы и поступлением в кровь адреналина и норадреналина. Это вызывает активацию фактора Хагемана, что запускает внешний и внутренний механизма продукции протромбиназы, а также стимулирует Хагеман-зависимый фибринолиз. Из эндотелия также происходит выделение тканевого активатора плазминогена и урокиназы, стимулирующих процесс фибринолиза.
При повышении тонуса парасимпатической нервной системы наблюдаются также ускорение свертывания крови и стимуляция процесса фибринолиза.
Основным эфферентным регулятором процессов свертывания крови и фибринолиза является сосудистая стенка.
Литература
См. также
Система фибринолиза. Общая информация
Фибринолитическая или плазминовая система – ферментная система, вызывающая асимметричное расщепление фибрина/фибриногена на более мелкие фрагменты.
В норме в крови обнаруживается спонтанная фибринолитическая активность. Она значительно колеблется даже у одного и того же индивидуума, в зависимости от его психического состояния, питания, времени суток и т.п.
Активация плазминогена заключается в ограниченном протеолизе одной АргВал-связи. Образовавшийся плазмин способен воздействовать на молекулу плазминогена и отщеплять от N-концевой области полипептид. Существует два пути превращения неактивного плазминогена в активный плазмин – внешний (вне сосудистого русла) и внутренний (в сосудистом русле).
Внешняя активация фибринолиза осуществляется в основном синтезируемыми в сосудистом эндотелии белковыми активаторами тканевого типа. Идентичные или очень близкие к ним активаторы содержатся во многих тканях и жидкостях организма, но из эндотелия они легче всего поступают в кровь. Их интенсивный выброс происходит при всех видах закупорки сосудов, в т. ч. и при сжатии сосудов манжеткой тонометра, при физических нагрузках, под влиянием вазоактивных веществ и лекарственных препаратов. Мощные активаторы плазминогена содержатся также в клетках крови – эритроцитах, тромбоцитах, лейкоцитах. Кроме того, гранулоциты и макрофаги могут секретировать внутриклеточные киназы, которые сами по себе (то есть без участия плазмина) расщепляют фибрин.
Внутренняя активация сложнее внешней. Плазминопластин переводит плазминоген в плазмин; однако, в крови этот активатор встречается только в виде предшественника проплазминопластина. Превращение проактиватора происходит под действием лизокиназы, которая синтезируется эндотеилоцитами.
Активный плазмин вызывает последовательное асимметричное расщепление фибриногена/фибрина. Вначале от их α- и β-цепей отщепляются низкомолекулярные фрагменты, а в плазме остается крупномолекулярный фрагмент Х, который еще сохраняет способность свертываться под воздействием тромбина. Затем плазмин расщепляет фрагмент Х на фрагменты Y и D, а фрагмент Y – на D и Е. Фрагменты Х и Y представляют собой “ранние” или растворимые фибрин-мономерные комплексы, а фрагменты D и Е – “поздние” и выявляются в виде D-диметров или D-тримеров.
Наиболее важным ингибитором фибринолиза является 2-антиплазмин. Он быстро инактивирует свободный плазмин. Ингибитор активатора плазминогена 1 типа (Plasminogen Activator Inhibitor type 1 – PAI-1) образует комплекс с тканевым активатором плазминогена и тем самым тормозит процесс фибринолиза. Тромбомодулин, находящийся на поверхности эндотелия, в комплексе с тромбином активирует прокарбоксипептидазу Y до активируемого тромбином ингибитора фибринолиза (Thrombin Activated Fibrinolysis Inhibitor – TAFI), который тормозит фибринолитическую активность.
Местный фибринолиз что это такое
Клиника фибринолитического синдрома. С клинической точки зрения, геморрагический синдром может принимать различные аспекты: эпистаксис, крупные экхимозы с контуром географической карты, гастроинтестинальные кровотечения, геморрагии на местах инъекций или пункций, геморрагии после хирургических вмешательств. Вначале эти явления имеют умеренный характер; с течением времени они станивятся все более тяжелыми, так как к ним присоединяются различные недостатки гемостаза, вызываемые самим развитием фибринолитического процесса; в конце концов геморрагический синдром становится таким тяжелым, что ставит в опасность жизнь больного.
Патофизиология фибринолитического синдрома. Нормальное действие механизма фибринолиза обеспечивается динамическим равновесием между активаторами и ингибиторами. Всякий раз когда преобладают активаторы, нарушение равновесия проявляется клинически как фибринолитический синдром; чем больше несоответствие, тем суровее клинический аспект.
Фибринолиз может выступать как самостоятельное расстройство (первичное) или как последствие простой или диссеминированной внутрисосудистой коагуляции (вторичное). Первичный фибринолиз может происходить по поводу роста активаторов плазминогена (спонтанный) или введения вциркуляцию активаторов для лизирования известных тромбов (терапевтически).
Во всех случаях результатом является высвобождение плазмина, который, благодаря своему литическому действию на фибрин, фибриноген, Ф. V, Ф. VIII вызывает геморрагический синдром, описанный в разделе симптоматологии.
Первичный фибринолиз бывает крайне редко (5%); вторичный фибринолиз встречается гораздо чаще.
Лабораторное исследование для диагностики фибринолитического синдрома. Результаты лабораторных тестов представляют большое разнообразие в зависимости от момента когда они производятся и от типа фибринолиза больного (первичного или вторичного). Ниже мы остановимся на тестах первичного фибринолиза, так как вторичный фибринолиз будет представлен в связи с синдромом ДВС.
Т.Н., РТТ и T.Q. могут быть слегка удлиненными (F.D.P. интерферирует с функцией тромбоцитов и с активностью тромбина, а плазма лизирует Ф. V и VIII). Сгустки проб маленькие (мало фибриногена). TLCE значительно сокращен; чем он короче, тем тяжелее синдром. Тест Аструпа (с пластинками фибрина) позволяет выделять каузальный агент фибринолиза: лизокиназа, активатор, плазмин. TEG представляет характерную трассу, вида теннисной ракеты. Тест выявления FDP позитивный (со степенями от + до + + + +).
Дозировка фибриногена дает тем более низкие цифры, чем сильнее фибринолиз. Остальные тесты на гемостаз и коагуляцию дают нормальные результаты.
Положительный клинический диагноз фибринолитического синдрома основывается на следующем: позднее появление кровотечения, картообразный контур экхимозов, кровотечения на месте инъекций и пункций, маленький и хрупкий сгусток, который высвобождает большое количество эритроцитов (когда синдром тяжелый — кровь теряет способность коагулироваться!).
Лабораторные исследования показывают почти нормальные тесты на коагуляцию наряду с позитивными тестами на фибринолиз, что позволяет ставить несомненный диагноз. Дифференциальная диагностика производится по отношению к остальным геморрагическим диатезам. Обстоятельства, при которых возникают кровотечения и лабораторные результаты выясняют неоспоримо диагноз.
Течение и осложнения фибринолитического синдрома. Фибринолитический синдром может иметь очень разнообразную эволюцию. В рамках такой эволюции хронический и острый фибринолитические синдромы находятся на двух крайностей.
Хронический синдром имеет доброкачественную эволюцию и без осложнений. Он может обостряться по поводу хирургического вмешательства, произведенного без антифибринолитической защиты.
Лечение фибринолитического синдрома относится к острому синдрому и преследует цель прекращения геморрагического синдрома. В качестве эффективных средств можно использовать:
а) Антифибринолитические, которые пресекают механизм фибринолиза; этого можно добиться двумя способами:
1) Антиплазминовое действие: блокирование плазмина, которое осуществляют антиплазмины или протеазовые ингибиторы, двух типов: ингибитор Kunitz, изготовляемый из поджелудочной железы и выпускаемый в продажу под названием Iniprol и ингибитор Frey, изготовляемый из околоушной слюнной железы и выпускаемый в продажу под названием Trasylol (первый в десять раз более активный чем второй).
2) Антиактивирующее действие: блокирование активации плазминогена в плазмин, которое осуществляют синтетические вещества двух типов: с линейной молекулой (ЕАСА) и циклической молекулой (АМСНА) (последнее в 7 раз более активное чем первое).
б) Субституционные: инъецируемый фибриноген и лиофилизированная антигемофилическая плазма, оба содержащие факторы коагуляции, которые в процессе гиперфибринолиза были лизированы в плазме больного и которые мы замещаем при помощи перфузии.
Схема лечения фибринолитического синдрома: мы начинаем с применения Trasylol 1 000 000 Ед в виде медленной перфузии в течение 24 часов. Через час после начала перфузии Trasylol-ом, инъецируется медленно в.в. ЕАСА в дозе 0,3 г/кг веса тела/день, разделенной на 4 приема (по 1 через 6 часов).
Спустя 2 часа от первой инъекции ЕАСА, инъецируется в.в. фибриноген 2 г и продолжается перфузия одного флакона лиофилизированной антигемофилической плазмы. Обычно за 24 часа эффект лечения оказывается благоприятным, так что его следует прервать; если состояние больного требует этого, мы повторяем на следующий день то же лечение. (Внимание! при вторичном фибринолизе все вышеуказанное лечение должно предшествоваться введением гепарина: 40 000 Ед/день, по 10 000 Ед в.в., через 6 часов в течение 2—3 дней).
Антифибринолитическое лечение при ДВС применяется только если во время гепаринового лечения возникает известная степень фибринолиза, требующего такое лечение.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Хагеман-зависимый фибринолиз
Описание
Фибринолиз — часть системы гемостаза (свертывающей системы в организме), которая обеспечивает процесс разрушения (лизиса) уже сформированных кровяных сгустков. Являясь важной защитной реакцией, фибринолиз предотвращает закупорку кровеносных сосудов фибриновыми сгустками. Кроме того, фибринолиз ведет к реканализации сосудов после остановки кровотечения.
Активация фибринолиза осуществляется по внешнему пути и внутреннему пути.
Внешний механизм активации фибринолиза осуществляется при участии тканевых активаторов, синтезирующихся, главным образом, в эндотелии сосудов. К ним относятся тканевый активатор плазминогена и урокиназа. Урокиназа образуется в юкстагломерулярном аппарате почки.
Внутренний механизм активации фибринолиза осуществляется плазменными активаторами, а также активаторами лейкоцитов, тромбоцитов и эритроцитов. Внутренний путь делится на Хагеман-зависимый и Хагеман-независимый.
Хагеман-зависимый фибринолиз протекает под влиянием факторов XIIа, калликреина, которые переводят плазминоген в плазмин. В основе метода оценки Хагеман-зависимого фибринолиза лежит активация фактора XII путем добавления к исследуемой плазме каолина. Инкубация плазмы с каолином приводит к активации фактора XII и компонентов калликреин-кининовой системы, запускающих внутренний (плазменный) механизм фибринолиза. Метод позволяет оценить состояние внутреннего механизма фибринолиза (ХПа-зависимого), в котором участвуют компоненты калликреин-кининовой системы.
Фибринолитическая активность определяется по времени лизиса сгустков эуглобулиновой фракции под действием плазмина активированного фактором XIIa. Удлинение времени лизиса свидетельствует о депрессии внутреннего механизма фибринолиза, связанного чаще всего с дефицитом или истощением плазменного прекалликреина, ВМК и/или плазминогена, с дефицитом фактора XII. Такое истощение внутреннего механизма фибринолиза наблюдается при заболеваниях, сопровождающихся тромботическими или тромбогеморрагическими синдромами, при системных васкулитах.
Хагеман-зависимый фибринолиз вследствие истощения или нарушения активации плазминогена резко ослаблен у больных крупозной пневмонией, особенно осложненной инфекционно-токсическим шоком и ДВС-синдромом, у больных тромбозом вен нижних конечностей.
Активность Хагеман-зависимого фибринолиза можно определять для диагностики тромбозов сосудов макро- и микроциркуляции.
Хагеман-независимый фибринолиз осуществляется быстрее. Его основное назначение сводится к очищению сосудистого русла от нестабилизированного фибрина, образующегося в процессе внутрисосудистого свертывания крови.
Если пациент принимает лекарственные препараты, следует проконсультироваться с врачом по поводу целесообразности проведения исследования на фоне приёма препаратов или возможности его отмены перед исследованием, длительность отмены определяется периодом выведения препарата из крови.
Интерпретация результатов
Единицы измерения: мин.
Нормальное время: 4–12 мин (зависит от возраста и пола).
Нарушение гемостаза
Общие сведения
Причины нарушения гемостаза:
ДВС-синдром. Распостраненный вид патологии гемостаза. Свертываемость крови нарушается из-за массивного освобождения из тканей тромбопластических веществ. Божет протекать бессимптомно.
Нарушение гемостаза (коагулопатия). Нарушение функций свертывающей и противосвертывающей систем крови. Патологическое состояние организма. Возможно выделить иммунные, приобретённые и генетические формы коагулопатий.
Тромботический синдром (тромбофилия). Характеризуется неадекватной коагуляцией крови и тромбообразованием, ведущими к ишемии тканей и органов.
Гипокоагуляционно-геморрагическое состояние. Сопровождается патологическим процессом уменьшения свёртываемости крови.
Классификация нарушения гемостаза:
наследственный или приобретенный;
гипокоагулятивный (понижение свертываемости крови) или гиперкоагулятивный (повышение свертываемости крови);
локальный (тромбоз) или глобальный (ДВС-синдром).
Пониженная свертываемость крови
Пониженная свертываемость крови может проявляться повышенной кровоточивостью, повторными кровотечениями, кровоизлияниями, которые возникают даже при незначительных травмах. Тромбоцитарно-сосудистый гемостаз нарушается при количественных и качественных изменениях тромбоцитов (тромбоцитопениях и тромбоцитопатиях), а также поражениях сосудистой стенки. ромбоцитопенией называется уменьшение содержания тромбоцитов в крови ниже нормы. Однако спонтанные кровотечения возникают лишь при снижении их числа меньше 30 Г/л. Под тромбоцитопатиями понимают качественную неполноценность и дисфункцию тромбоцитов при нормальном или пониженном их содержании.
Причины пониженной свертываемости крови:
Иммунные реакции (вирусы, препараты);
Дефецит цианокобаламина и фолиевой кислоты;
Действие токсических препаратов;
Гормональные нарушения (гипотиреоз);
Геморрагический синдром
Геморрагический синдром характеризуется состоянием повышенной кровоточивости и нарушениями в одном из звеньев свертывающей систеы крови. Может быть как острым, так и хроническим заболеванием.
Характерные симтомы:
сыпь в виде мелких точек;
пятна диаметром до 3 мм (петехии);
синяки на коже и слизистых оболочках (экхзимозы);
Экхимозы это не просто синяки, а характерные признаки кровоизлияния в кожу или слизистую оболочку. Если обнаружены вышеуказанные признаки, важно провести лабораторную диагностику. По ней станут видны показатели снижения количества тромбоцитов и удлинение времени самого кровотечения.
Болезнь Виллебранда
Болезнь Виллебранда является врожденным дефицитом фактора Виллебранда (ФВ), который приводит к дисфункции тромбоцитов. Обычно характеризуется кровоточивостью легкой степени. Также отмечается увеличение времени кровотечения, нормальное количество тромбоцитов и, возможно, небольшое увеличение частичного тромбопластинового времени. Диагноз базируется на низком уровне антигена фактора Виллебранда и отклонении от нормы активности ристоцетинового кофактора. Лечение включает контроль за кровоточивостью с заместительной терапией
Симптомы болезни Виллебранда:
склонность к подкожным кровоизлияниям;
длительная кровоточивость небольших порезов;
продолжительные менструации (в некоторых случаях);
аномальная кровоточивость после хирургического вмешательства.
Тромбоцетопения при нарушении гемостаза
Тромбоцитопения характеризируется снижением количества тромбоцитов и сопровождается повышенной кровоточивостью и проблемами с обстановкой кровотечений. Может сопровождать любые гематологические заболевания, как один из основных симптомов.
В качестве самостоятельного заболевания иногда диагностируется как болезнь Верльгофа. Основными причинами тромбоцетопении является нарушение продукции тромбоцитов, а также их повышенное разрушение. Также среди возможных причин возникновения выделяют инфекционные и эпидимологические:
острые проявления герпесовой инфекции;
Нарушение гемостаза и развитие кровоточивости при тромбоцитопении обусловлено следующими механизмами:
повышение проницаемости микрососудов для эротроцитов и других составных частей крови;
ломкость сосудов из-за дистрофии стенки;
уменьшение адгезивно-агрегационной функции тромбоцитов;
нарушение реакции освобождения тромбоцитарных факторов свертывания крови;
меньшением ретракции сгустка в результате снижения активности сократительного белка тромбоцитов.
Коагуляционный гемостаз
активизация фибринолитической системы;
увеличение эндогенных антикоагулянтов;
Антикоагулянты тормозят появление нитей фибрина; они препятствуют тромбообразованию, способствуют прекращению роста уже возникших тромбов, усиливают воздействие на тромбы эндогенных фибринолитических ферментов.
Причины нарушения I фазы свертывания крови
Причины нарушения образования тромбопластина могут быть следующими:
снижение продукции факторов (IX, X) при патологии печени;
образование антител при лейкозе;
передозировка антикогулянтом гепарином;
генетические дефекты синтеза VIII, IX и XI факторов.
Причины нарушения II фазы свертывания крови
Причины нарушений образования тромбина: