Метаболически активная ткань что это
Материалы конгрессов и конференций
X РОССИЙСКИЙ ОНКОЛОГИЧЕСКИЙ КОНГРЕСС
ПЭТ В ОНКОЛОГИЧЕСКОЙ КЛИНИКЕ
А.М. Гранов, Л.А. Тютин, Н.А. Костеников, Д.В. Рыжкова, М.С. Тлостанова,
А.А. Станжевский, Д.Б. Фрейдман, А.А. Балабанова
Центральный научно-исследовательский рентгенорадиологический институт Росздрава, Санкт-Петербург
Онкологические заболевания относятся к числу наиболее распространенных среди населения экономически развитых стран и занимают лидирующее положение по показателям смертности. Так, в США ежегодно регистрируются около 1,5 млн. случаев злокачественных опухолей и более 560 тыс. больных в год умирает. Хорошо известно, что исход онкологических заболеваний во многом зависит от своевременной диагностики и объективной оценки эффективности проводимого лечения. Однако, несмотря на внедрение в клиническую практику высокоинформативных методов диагностики (УЗИ, СКТ, МРТ и др.), большая часть больных поступает в медицинские центры уже с запущенными стадиями заболевания, а адекватность проводимых лечебных мероприятий своевременно не оценивается. В связи с этим дальнейшее совершенствование методов диагностики является весьма актуальным. По мнению специалистов, наиболее перспективным в этом отношении может быть всестороннее изучение и внедрение в клиническую практику позитронной эмиссионной томографии (ПЭТ), позволяющей получать уникальную информацию о метаболизме и перфузии нормальных и патологически измененных тканей на клеточно-молекулярном уровне. Эти данные могут иметь решающее значение для диагностики и дифференциальной диагностики злокачественных опухолей на ранних этапах их развития. Кроме того, с помощью ПЭТ удается своевременно установить изменения, происходящие в опухоли под влиянием лекарственной и лучевой терапии, а также выявить признаки продолженного роста или рецидива новообразования. Однако имеющиеся в литературе данные свидетельствуют о том, что многие аспекты использования ПЭТ в онкологии изучены недостаточно. В настоящее время весьма противоречивым является вопрос об эффективности ПЭТ при различных опухолях. Так, согласно данным систематизированного анализа возможностей ПЭТ в онкологии III всеобщей конференцией врачей ФРГ признана недоказанной эффективность использования этого метода при раке щитовидной железы, пищевода, опухолях костей и мягких тканей, рецидиве и оценке эффективности лечения рака молочной железы, феохромацитоме, опухолях головы и шеи, низкодифференцированной лимфоме Ходжкина. Однако в ряде других публикаций имеются сведения об успешном применении ПЭТ при большинстве из указанных онкологических заболеваний. Очевидно, что использование ПЭТ в онкологической клинике, по существу, находится в начале своего пути. Широкому внедрению метода должно предшествовать полное, всестороннее изучение его диагностических возможностей с применением различных технологий исследования и специфических туморотропных препаратов.
В настоящем сообщении нами обобщен коллективный 9-летний опыт применения ПЭТ при обследовании больных онкологического профиля.
Всего обследованы более 5000 пациентов, которым выполнены 7220 исследований. При этом опухоли различных локализаций выявлены у 2045 больных. Распределение онкологических больных в зависимости от нозологической формы опухолевого заболевания представлено в табл. 1.
Таблица 1.
Распределение онкологических больных по диагнозу.
| Нозологическая форма | Число обследованных больных | |
|---|---|---|
| Количество | % | |
| Объемные образования головного мозга | 542 | 26,5 |
| Рак молочной железы | 192 | 9,4 |
| Злокачественные опухоли печени | 381 | 18,6 |
| Рак поджелудочной железы | 240 | 11,7 |
| Лимфопролиферативные заболевания | 128 | 6,3 |
| Рак легкого | 117 | 5,7 |
| Герминогенные опухоли | 82 | 4 |
| Рак предстательной железы | 53 | 2,6 |
| Колоректальный рак | 119 | 5,8 |
| Меланома | 67 | 3,3 |
| Прочие | 124 | 6,1 |
| Всего | 2045 | 100 |
ПЭТ в нейроонкологии. Всего обследованы 542 больных с объемными образованиями головного мозга. Основную группу составили пациенты с опухолями глиального ряда (преимущественно злокачественными), метастатическим поражением головного мозга и менингиомами. Результаты ПЭТ больных со злокачественными новообразованиями головного мозга представлены в табл. 2 и 3.
Таблица 2.
КДН, полученные при ПЭТ с различными РФП у больных со злокачественными новообразованиями головного мозга.
Таблица 3.
Информативность ПЭТ с различными РФП при диагностике злокачественных новообразований головного мозга.
| Название методики | Чувствительность (%) | Специфичность (%) | Диагностическая точность (%) |
|---|---|---|---|
| ПЭТ с 18 F-ФДГ (n=385) | 82,2 | 99,6 | 94,8 |
| ПЭТ с 11 C-БН (n=159) | 94,1 | 82,4 | 88,7 |
| ПЭТ с 11 C-метионином (n=33) | 84,6 | 65,0 | 72,7 |
| ПЭТ с 18 F-ФДГ и 11 C-БН (n=36) | 96,0 | 100,0 | 97,2 |
Рак молочной железы (РМЖ). ПЭТ с 18 F-ФДГ выполнена 192 больным раком молочной железы. В 141 случае исследование проводилось до операционного вмешательства. При этом в 21 случае ПЭТ одним и тем же больным проводилась дважды: до начала и после завершения неоадъювантной химиотерапии. Кроме того, 51 больной ПЭТ с 18 F-ФДГ проведена после удаления первичного очага с целью определения регионарных и отдаленных метастазов.
Таблица 4.
Диагностические показатели ПЭТ с 18 F-ФДГ у пациенток в основной и контрольной клинических группах.
| Клиническая группа | Количество пациенток | Характер накопления РФП | SUVmax | SUVmean |
|---|---|---|---|---|
| Фиброзно-кистозная мастопатия | 55 | Диффузно-неравномерное | 1,50±0,08 | 1,12±0,03 |
| Рак молочной железы | 139 | Очаговое | 3,71±0,21 | 2,33±0,08 |
Во всех случаях для злокачественной опухоли было характерно повышенное накопление РФП в зоне поражения. Визуализировать злокачественное новообразование не удалось лишь в 3 случаях в связи с крайне малыми размерами первичного очага (ниже разрешающей способности метода). Ложноположительное заключение сделано в 1 случае при наличии у пациентки с фиброзно-кистозной мастопатией воспалительного процесса. Чувствительность, специфичность и диагностическая точность ПЭТ с 18 F-ФДГ при РМЖ составила 97,8%, 98,2% и 98,0%, а при поражении регионарных лимфоузлов – 92,0%, 100% и 97,8% соответственно.
Рак поджелудочной железы (РПЖ). Распределение обследованных больных по диагнозу представлено в табл. 5.
Таблица 5.
Распределение больных с объемными образованиями поджелудочной железы по диагнозу.
| Характер патологии | Количество больных | |
|---|---|---|
| n | % | |
| Рак поджелудочной железы | 150 | 62,5 |
| Хронический псевдотуморозный панкреатит в стадии ремиссии | 81 | 33,7 |
| Хронический псевдотуморозный панкреатит в стадии обострения | 9 | 3,8 |
| Всего | 240 | 100,0 |
Первичные опухоли печени и метастазы. Нами было обследован 381 пациент с первичными опухолями печени и метастазами. Контрольную группу составили 65 пациентов с нормальной паренхимой печени и доброкачественными новообразованиями. Распределение больных в зависимости от морфологического типа поражения и метаболической активности злокачественной опухоли представлено в табл. 6.
Таблица 6.
Распределение больных в зависимости от морфологического типа поражения и метаболической активности злокачественной опухоли.
| Морфологический тип опухоли | Количество больных | SUVмакс | SUVср | |
|---|---|---|---|---|
| n | % | |||
| Холангиоцеллюлярный рак | 31 | 8,1 | 3,00±0,15 | 2,05±0,09 |
| Гепатоцеллюлярный рак | 54 | 14,2 | 2,22±0,25 | 1,63±0,13 |
| Метастатическое поражение печени | 296 | 77,7 | 4,76±0,21 | 2,86±0,11 |
| Всего | 381 | 100 | ||
В 189 из 192 случаев злокачественного поражения паренхимы печени нами были получены истинноположительные результаты. Ложноположительные данные определялись у 2 пациентов с локальным нарушением перфузии печени. Таким образом, чувствительность, специфичность и диагностическая точность метода составили 98,4%, 96,9% и 98,0% соответственно.
Таблица 7.
Распределение больных лимфопролиферативными заболеваниями в зависимости от метаболического ответа опухоли на проводимое лечение (n=54).
| Выраженность метаболического ответа | Количество больных | SUVмакс до лечения | SUVмакс после лечения | SUVср до лечения | SUVср после лечения | |
|---|---|---|---|---|---|---|
| n | % | |||||
| Полная метаболическая ремиссия | 28 | 51,8 | 3,00±0,15 | Отсутствие накопления | 2,22±0,25 | Отсутствие накопления |
| Частичная метаболическая ремиссия | 14 | 25,9 | 4,76±0,21 | 4,1±0,18 | 2,31±0,15 | 2,10±0,10 |
| Стабилизация процесса | 8 | 14,9 | 3,93±0,25 | 3,89±0,27 | 2,67±0,21 | 2,56±0,19 |
| Прогрессирование заболевания | 4 | 7,4 | 3,84±0,16 | 5,1±0,19 | 2,93±0,18 | 3,11±0,17 |
Таким образом, представленные данные свидетельствуют о том, что ПЭТ является высокоинформативным методом диагностики большинства наиболее социально значимых злокачественных новообразований, в т.ч. на ранних стадиях их развития, и, как правило, позволяет установить истинные размеры, распространенность и степень злокачественности опухолевого поражения, а также объективно оценить эффективность проводимого лечения. Вместе с тем, накопленный опыт показал относительно низкие диагностические возможности ПЭТ с 18 F-ФДГ при некоторых опухолях головы и шеи, раке почки, предстательной железы (выявление первичного опухолевого узла), раке мочевого пузыря и др. Мировой клинический опыт по использованию для диагностики специфических туморотропных РФП, в силу целого ряда причин, крайне ограничен. До настоящего времени не решен вопрос об оптимальных сроках выполнения контрольных исследований при лечении различных онкологических заболеваний. Требует совершенствования и технология проведения ПЭТ сканирования. Другими словами, очевидно, что диагностические возможности ПЭТ еще далеко не исчерпаны. На базе проводимых исследований эффективность метода должна быть существенно повышена.
Метаболически активная ткань что это
Актуальность проблемы. В настоящее время большинство онкобольных нуждаются в комбинированном лечении [4,6]. Наблюдаемые у ряда больных неудачи побудили в последнее время шире прибегать к выбору тактики лечения в зависимости от оценки распространенности процесса [3]. Происходит постоянная оптимизация методов для оценки распространения заболевания у пациентов с опухолями пищевода и желудка. Компьютерная томография (КT) представляет стандарт в определении инвазии опухоли. КТ является неинвазивным и наименее дорогостоящим из доступных методов, но имеет серьезные ограничения в плане точной постановки диагноза [5]. Позитронно-эмиссионная томография (ПЭТ) также является неинвазивным, но предоставляет качественно иную информацию по сравнению с КТ, благодаря своей функции участия в метаболическом процессе опухоли, а не только определяя размер опухоли [1]. Многие исследователи показали, что снижение метаболической активности, измеренной значением стандартизированного накопления (SUV) на ПЭТ/КТ, в результате терапии является прогностически значимым критерием [7,9,10]. Следует отметить, что ПЭТ/КТ изображения были изучены у ограниченного количества больных и, согласно другим исследованиям, прогностическая ценность является сомнительной [8,11]. Тем не менее данные ПЭТ/КТ при злокачественных опухолях верхних отделов желудочно-кишечного тракта не были подтверждены [2] и требуют дальнейшего изучения.
Цель работы: выявить зависимость коэффициента максимального поглощения радиофармпрепарата18F-ФДГ от следующих характеристик опухолевого процесса – глубины инвазии опухолевого процесса, гистологической структуры опухоли и степени дифференцировки злокачественной опухоли.
Материалы и методы исследования. В исследование были включены 56 больных с установленным диагнозом или подозрением на злокачественную опухоль верхних отделов желудочно-кишечного тракта, в возрасте от 29 до 89 лет, проходивших обследование на базе отделения радиоизотопной диагностики АО «Республиканского диагностического центра» г. Астана в период с 2010 по 2012 г. Основными критериями включения в исследование явились: наличие или подозрение на злокачественную опухоль желудка или пищевода; проведение позитронно-эмиссионной томографии, совмещенной с компьютерной томографией. Локализация патологического процесса в пищеводе отмечена у 16 больных (28,5%), локализация в желудке – у 40 больных (71,5%). Всем больным проведено ПЭТ/КТ исследование на базе Республиканского Диагностического Центра г. Астана. Позитронно-эмиссионный томограф, совмещенный с 16-срезовым компьютерным томографом GeminiGXL 16 фирмы Philips производства 2008 года. Для проведения ПЭТ/КТ исследования на базе РДЦ создан производственный комплекс, включающий циклотрон «Cyclone 18/9» для производства короткоживущих изотопов, радиохимическая лаборатория для производства радиофармпрепаратов. При проведении ПЭТ/КТ использовался радиофармацевтический препарат «Фтордезоксиглюкоза, 18F, раствор для внутривенного введения». Вводимая доза препарата зависела от площади поверхности тела исследуемого человека. Поверхность тела рассчитывалась по номограмме, исходя из веса и роста больного. Диагностическая доза препарата составляла 220 МБк на 1 м2 поверхности тела пациента; как правило, использовали 300–550 МБк на одно исследование. Препарат вводился внутривенно медленно в объеме 5,0–10,0 мл.
Результаты и их обсуждение. Нами проведен анализ показателя SUVmax в первичной опухоли и определена зависимость коэффициента SUVmax в зависимости от основных характеристик онкологического процесса, таких как глубина инвазии опухолевого процесса, гистологическая структура и дифференцировка опухоли.
Накопление фармпрепарата в первичной опухоли у больных со злокачественными новообразованиями верхних отделов желудочно-кишечного тракта варьировало от 2,1 до 13, в среднем составило 6,25±2,26.
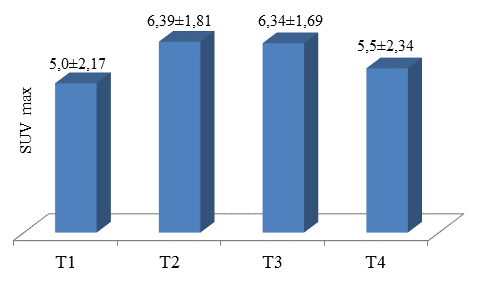
Зависимость максимального накопления радиоизотопа глюкозы от глубины инвазии опухолевого процесса в стенку органа представлена на рисунке 1.
Рисунок 1. Коэффициент SUVmax в зависимости от глубины инвазии опухолевого процесса
Как видно из представленной диаграммы, максимальное накопление радиофармпрепарата не зависело от глубины инвазии стенки органа опухолевым процессом. Наибольшие показатели накопления радиофармпрепарата в первичной опухоли отмечены при прорастании мышечного (Т2, n=27) и серозного (Т3, n=21) слоев. Наиболее низкие показатели отмечены при поражении только слизистого слоя (Т1, n=3) и при прорастании в соседние органы (Т4, n=5). Полученные данные не имели статистически значимых различий (p=0,41).
Проведен анализ содержания радиофармпрепарата ФДГ 18F в зависимости от протяженности поражения органа. Полученные данные представлены в таблице 1.
Таблица 1. Коэффициент SUVmax в зависимости от протяженности поражения органа
Метастатическое поражение шейных лимфатических узлов
Шейные лимфатические узлы являются частым местом метастазирования злокачественных опухолей, первичный очаг которых располагается в области головы и шеи. К ним, например, относятся плоскоклеточный рак верхних отделов дыхательных путей, а также метастазы рака слюнных желез и щитовидной железы.
Наиболее распространенным клиническим признаком является увеличивающееся образование шеи, которое обычно обнаруживается пациентом или его врачом. При подозрении на метастатическое поражения лимфатических узлов шеи для диагностики и определения наилучшей тактики лечения потребуется осмотр врачом-онкологом, инструментальные методы и биопсия.
Иногда новообразования вне области головы и шеи могут неожиданно метастазировать в шейные лимфатические узлы, что требует особенно тщательной диагностики для выявления первичного очага.
Лечение будет зависеть от типа и локализации первичной опухоли, которая распространилась в лимфатические узлы шеи, и, скорее всего, будет включать в себя комбинацию хирургического вмешательства, лучевой терапии и/или химиотерапии.
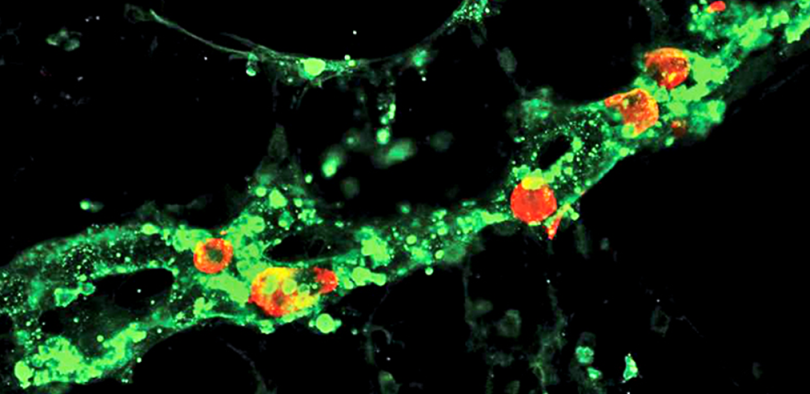
Иммунофлюоресцентная визуализация метастатических клеток меланомы (красные) внутри лимфатических сосудов (зеленые). Масштабная линейка: 100 мкм
(Science Advances/Michael Detmar Group ©)
Из чего состоит лимфатическая система шеи
Лимфатическая система шеи включает в себя сосуды и узлы.
Лимфатические капилляры — это тонкостенные структуры, состоящие из одного слоя эндотелиальных клеток. Они находятся во всех тканях организма и, объединяясь друг с другом, способствуют оттоку лимфатической жидкости в более крупные лимфатические сосуды.
Стенка лимфатических сосудов состоит из трех слоев: внутреннего слоя эндотелиальных клеток, среднего мышечного слоя и внешнего слоя соединительной ткани. В лимфатических сосудах гораздо больше клапанов, чем в венозных, при этом циркуляция лимфы полностью зависит от сжатия сосудов окружающими мышцами. Лимфатические сосуды дренируют лимфу в лимфатические узлы.
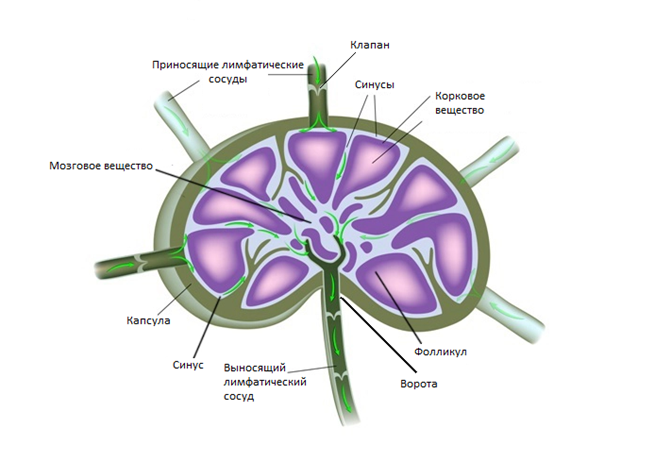
В среднем на каждой стороне шеи расположено до 75 лимфатических узлов. Снаружи узел покрывает капсула, под которой располагается субкапсулярные синусы – место куда попадает лимфатическая жидкость из приносящих лимфатических сосудов. Жидкость проходит сквозь ткань лимфатического узла, которая состоит из коркового и мозгового вещества, а затем выходит через ворота лимфатического узла и попадает в отводящие лимфатические сосуды. В итоге лимфа попадает в венозную систему в месте соустья внутренней яремной и подключичной вены.
Анатомическая структура лимфатического узла (Alila Medical Media/ Shutterstock ©)
Классификация лимфатических узлов шеи
На данный момент во всем мире рекомендована к использованию классификация Американского объединенного комитета по раку (American Joint Committee on Cancer (AJCC)) 8 издания от 2018 года:
Уровни лимфатических узлов шеи (Tenese Winslow LLC ©)
Диагностика
Осмотр
При пальпации шеи врач обращает внимание на расположение, размер, плотность и подвижность каждого узла. Особое внимание уделяется узлам, которые кажутся фиксированными к подлежащим сосудисто-нервным структурам и внутренним органам. Описание каждого узла становится важной частью медицинской документации, которая в дальнейшем может использоваться для оценки эффекта лечения.
Лучевые методы
Преимуществами УЗИ перед другими методами визуализации являются цена, скорость исследования и низкая лучевая нагрузка на пациента.
Ультразвуковыми признаками метастатического поражения лимфатических узлов может быть образование сферической формы, нарушение структуры, нечеткие границы, наличие центрального некроза и др.
Поскольку не всегда по УЗИ можно с уверенностью сказать является лимфатический узел пораженным или нет, иногда одновременно выполняют тонкоигольную аспирационную биопсию под ультразвуковым контролем с последующим цитологическим исследованием материала из этого узла. Результат цитологического исследования зависит от навыков врача УЗИ и качества образца (т.е. наличия достаточного количества репрезентативных клеток).
С появлением систем высокого разрешения и специальных контрастных веществ КТ позволяет обнаруживать лимфатические узлы, которые могли быть пропущены при иных методах диагностики.
Ценность МРТ – превосходная детализация мягких тканей. МРТ превосходит КТ в качестве предпочтительного исследования при оценке ряда новообразований головы и шеи, таких как основание языка и слюнные железы. Размер, наличие нескольких увеличенных узлов и центральный некроз – критерии, общие для протоколов исследования КТ и МРТ.
Этот новый метод визуализации все чаще используется для определения стадии опухолей головы и шеи. Метод основан на поглощении 2-фтор-2-дезокси-D-глюкозы (ФДГ) метаболически активными тканями. Исследование также может быть объединено с КТ, чтобы улучшить разрешение получаемого изображения и более точно определить расположение образования.
Биопсия
Биопсия — это удаление небольшого кусочка ткани для исследования под микроскопом или для тестирования в лаборатории на предмет наличия признаков злокачественности. В подавляющем большинстве случаев проводится тонкоигольная аспирационная биопсия. Врач, выполняющий биопсию, может использовать УЗИ или КТ для выполнения процедуры. Иногда тонкоигольная аспирационная биопсия не позволяет поставить окончательный диагноз, и требуются другие виды биопсии, такие как трепан-биопсия или эксцизионная биопсия.
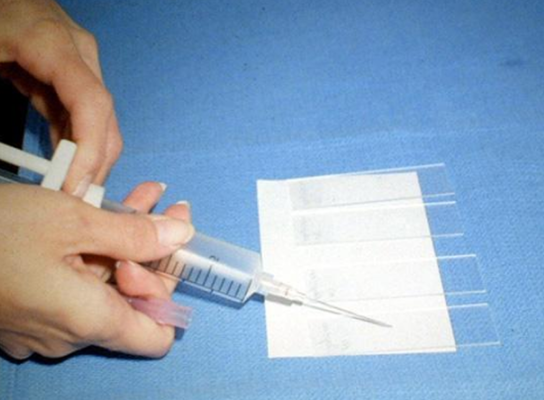 | 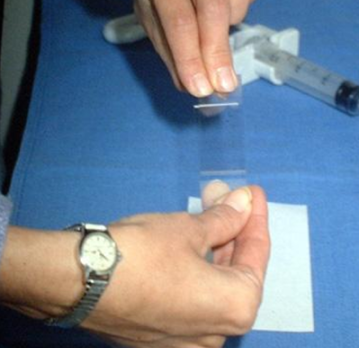 |
| Процесс приготовления предметных стекол для цитологического исследования. Материалом служит содержимое шприца после выполнения тонкоигольной аспирационной биопсии | |
План лечения
После определения диагноза и проведения всех диагностических исследований врач порекомендует оптимальный для пациента курс лечения. В конечном итоге лечение метастатического поражения лимфатических узлов зависит от типа и локализации первичной опухоли.
Существует три различных варианта лечения, которые могут быть использованы отдельно или в комбинации:
Хирургическое лечение
Хирургическое лечение обычно включает удаление лимфатических узлов шеи (лимфодиссекция) и последующее гистологическое исследование для точного определения стадии, так как это может существенно повлиять на дальнейшую тактику лечения. Хоть и не всегда, но чаще всего лимфодиссекция выполняется одновременно с удалением первичной опухоли.
Существуют различные виды лимфодиссекций:
Лучевая терапия
Лучевая терапия может быть назначена в качестве самостоятельного метода лечения в послеоперационном периоде, чтобы снизить вероятность рецидива либо в комбинации с химиотерапией в качестве самостоятельного или адъювантного лечения. Обычно адъювантная лучевая терапия необходима, если по результатам гистологического исследования обнаруживается несколько пораженных лимфатических узлов.
Химиотерапия
Химиотерапия обычно добавляется к лучевой терапии в качестве самостоятельного или адъювантного (послеоперационного) лечения. В некоторых случаях может использоваться индукционная химиотерапия с целью уменьшения объема образования и последующего хирургического вмешательства.
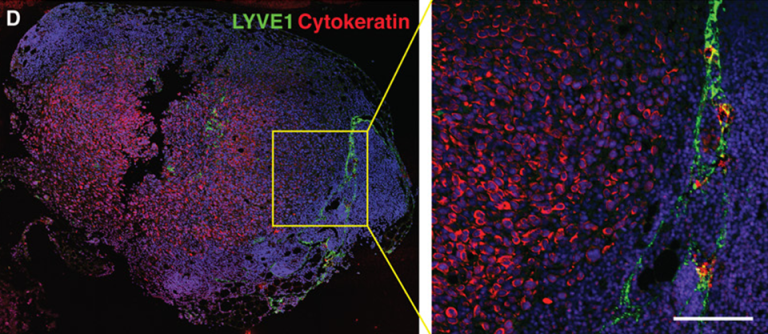
Иммунофлюоресцентная визуализация метастатически пораженного лимфатического узла с окраской на Цитокератин (красный) – маркер характерный для опухолевых клеток эпителиального происхождения. Масштабная линейка: 50 мкм
(Science Advances/Michael Detmar Group ©)
Прогноз
Метастазы в лимфатические узлы шеи могут возникать при онкологических заболеваниях различных локализаций, поэтому давать прогностические оценки для этой группы пациентов следует только после выявления первичной опухоли.
Факторы, влияющие на прогноз:
Наблюдение после лечения
Пациенты должны регулярно посещать своего специалиста по опухолям головы и шеи для оценки состояния на предмет любых признаков рецидива заболевания.
Стандартный график наблюдения
В первые 1–2 года осмотр и сбор жалоб рекомендуется проводить каждые 3–6 месяца, на сроке 3–5 лет – один раз в 6–12 месяцев. После 5 лет с момента операции посещать врача необходимо один раз в год или при появлении жалоб. У пациентов с высоким риском рецидива перерыв между обследованиями может быть сокращен.
Список литературы:
Авторская публикация:
Амиров Николай Сергеевич
Клинический ординатор НМИЦ онкологии им. Н.Н. Петрова
Под научной редакцией:
Раджабова З.А.
Заведующий отделением опухолей головы и шеи
НМИЦ онкологии им. Н.Н. Петрова,
врач-онколог, научный сотрудник, кандидат медицинских наук, доцент