Метаплазия пилорическая что это
Метаплазия пилорическая что это
Определенные состояния связаны с повышенным риском развития рака желудка. К ним относят: пернициозную анемию, аденоматозные полипы, кишечную метаплазию, а также предшествующие хирургические вмешательства на желудке и, что особо важно с учетом количества больных, хронический гастрит, связанный с инфекцией Н. pylori.
Целесообразность эндоскопического скрининга в настоящее время не доказана, отчасти это связано с небольшой долей положительных результатов среди обследуемых пациентов, а отчасти с тем, что дисплазия или метаплазия не всегда переходят в злокачественный процесс.
Особая разновидность кишечной метаплазии — кишечная метаплазия III типа, характеризующаяся неполной клеточной дифференцировкой и секрецией сульфомуцина — наиболее тесно связана с развитием рака.
Однако скрининговое обследование этих больных проводиться не может до тех пор, пока не будут разработаны новые гистохимические или иммунологические методы исследования, так как используемый способ окраски слишком токсичен.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Современная стратегия ведения пациента с предраковыми заболеваниями желудка

Представлен обзор, обобщающий существующие международные рекомендации по ведению пациентов с атрофическим гастритом, кишечной метаплазией и дисплазией желудка. Показано, что пациенты с хроническим атрофическим гастритом или кишечной метаплазией имеют повы
The review summarize existing international recommendations for managing patients with atrophic gastritis, intestinal metaplasia and gastric dysplasia. It is shown that patients with chronic anthropic gastritis or intestinal metaplasia have an increased risk of stomach adenocarcinoma development. Helicobacter pylori eradication tends to relieve indications of chronic nonatrophic gastritis and can lead to partial regression of atrophic gastritis, and reduces the risk of stomach cancer development.
Несмотря на успехи в области диагностики и лечения, рак желудка остается серьезной проблемой в мировом масштабе, занимая шестое место по уровню заболеваемости и второе — в структуре смертности от онкологических заболеваний [1–2]. Самые высокие показатели отмечаются в странах Восточной и Центральной Азии, Латинской Америке, самые низкие — в Северной Америке. В Восточной Азии заболеваемость раком желудка составляет 32,1 на 100 000 у мужчин, 13,2 — у женщин, в Южной Корее — 57,8 и 23,5 на 100 000, в Японии 40,7 и 16,0 на 100 000 для мужчин и женщин соответственно [1–2]. Наименьшая заболеваемость наблюдается в Северной Америке и большинстве районов Африки. Так, в Соединенных Штатах Америки (5,5 на 100 000 у мужчин; 2,8 — у женщин) [1]. Россия относится к странам с умеренным риском рака желудка, наряду с Португалией, Сингапуром, Эстонией. По итогам 2018 г., согласно российской статистике, в структуре общей заболеваемости удельный вес опухолей желудка достигал 20,4 на 100 000 населения у мужчин и 8,8 — у женщин [3]. Улучшение эпидемиологической ситуации по раку желудка наблюдается, как правило, в странах, где разработаны профилактические мероприятия, высокий уровень осведомленности населения и длительное время существуют национальные программы скрининга и ведения пациентов с предраковыми заболеваниями [4].
Цель представленного обзора — обобщение существующих международных рекомендаций по ведению пациентов с атрофическим гастритом, кишечной метаплазией и дисплазией желудка.
В 2012 г. Европейским обществом гастроинтестинальной эндоскопии (ESGE), Европейской группой по изучению Helicobacter и микробиоты (EHMSG), Европейским обществом патологов (ESP) и Португальским обществом гастроинтестинальной эндоскопии (SPED) были разработаны первые международные рекомендации по лечению предраковых состояний и изменений желудка (MAPS I). В 2019 г. опубликована обновленная версия рекомендаций под названием MAPS II [4]. Данные рекомендации были представлены на рассмотрение в разных странах.
Различные формы рака имеют свои специфические характеристики, знание которых позволит оптимизировать диагностику рака желудка на ранних стадиях. Подавляющее большинство раков желудка — аденокарциномы (АК, около 90%), которые происходят из желез слизистой оболочки желудка. Аденокарциномы желудка (АКЖ) подразделяют на кардиальные и некардиальные. Выделяют два основных гистологических типа некардиальных АКЖ: диффузные и кишечные. Кардиальной формой рака желудка является некардиальная аденокарцинома кишечного типа (90% АКЖ). Последняя имеет строение опухоли, сходное с картиной рака кишки. Для них характерны отчетливые железистые структуры, состоящие из высокодифференцированного цилиндрического эпителия с развитой щеточной каемкой. Диффузный тип опухоли представлен слабо организованными группами или одиночными клетками с большим содержанием муцина (перстневидные клетки) и характеризуется диффузным инфильтративным ростом. Возможен смешанный тип — в опухоли присутствуют участки кишечного и диффузного типа [5]. Дифференцированный тип чаще встречается у пожилых мужчин и развивается медленно, тогда как диффузный тип чаще встречается у женщин более молодого возраста и имеет худший прогноз [5].
Обзор представленных рекомендаций не распространяется на наследственный/семейный диффузный рак желудка, для которого разработаны специальные рекомендации [6].
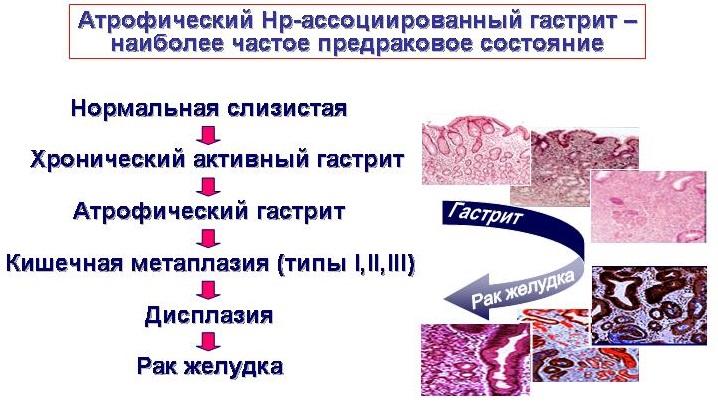
Аденокарцинома желудка кишечного типа представляет собой окончательный исход последовательности «воспаление — атрофия — метаплазия — дисплазия — карцинома», известной как каскад Корреа [7–11].
Рекомендация 1 (MAPS II). Пациенты с хроническим атрофическим гастритом или кишечной метаплазией подвержены риску развития аденокарциномы желудка (высокий уровень доказательности) [4].
Хронический атрофический гастрит и кишечную метаплазию (КМ) рассматривают как предраковые состояния, поскольку они сами по себе связаны с риском развития рака желудка и на их фоне возможно развитие дисплазии и аденокарциномы [7–11].
Рекомендация 2 (MAPS II). Гистологически подтвержденная кишечная метаплазия — наиболее надежный маркер атрофии слизистой оболочки желудка (высокий уровень доказательности) [4].
Рекомендация 3 (MAPS II). Необходимо выявлять пациентов с гастритом на поздних стадиях, т. е. с атрофией и (или) кишечной метаплазией, слизистой оболочки как антрального отдела желудка, так и тела желудка, поскольку считается, что они подвержены более высокому риску развития аденокарциномы желудка (умеренный уровень доказательности, сильная рекомендация).
Рекомендация 4 (MAPS II). Дисплазию тяжелой степени и инвазивную карциному следует рассматривать как исходы, которые необходимо предотвратить при лечении пациентов с хроническим атрофическим гастритом или кишечной метаплазией (умеренный уровень доказательности, сильная рекомендация).
Рекомендация 5 (MAPS II). У пациентов с эндоскопически определяемыми патологическими изменениями, указывающими на дисплазию легкой или тяжелой степени или карциному, следует определить стадию заболевания и начать лечение (высокий уровень доказательности, сильная рекомендация).
Рекомендация 6 (MAPS II). Эндоскопия высокого разрешения в сочетании с хромоэндоскопией более эффективна, чем эндоскопия высокого разрешения в белом свете, при диагностике предраковых состояний желудка и неопластических поражений на ранней стадии (высокий уровень доказательности).
Рекомендация 7 (MAPS II). При наличии возможности и после надлежащего обучения для диагностики предраковых состояний желудка следует применять виртуальную хромоэндоскопию с увеличением или без увеличения изображения, что позволяет выполнять контролируемую биопсию на участках атрофических и метапластических изменений, а также обеспечивает выявление неопластических поражений (умеренный уровень доказательности, сильная рекомендация).
Рекомендация 8 (MAPS II). Для надлежащего определения стадии предраковых состояний желудка первая диагностическая эндоскопия верхнего отдела желудочно-кишечного тракта должна включать взятие биопсийных образцов из желудка для определения наличия инфекции Helicobacter pylori и выявления атрофического гастрита на поздних стадиях (умеренный уровень доказательности, сильная рекомендация) [4].
Рекомендация 9 (MAPS II). Следует выполнить биопсию как минимум на двух топографических участках (по малой и большой кривизне, как в антральном отделе желудка, так и в теле желудка). Следует дополнительно выполнить биопсию видимых предполагаемых неопластических поражений (умеренный уровень доказательности, сильная рекомендация) [4].
Рекомендация 10 (MAPS II). Для выявления пациентов с гастритом на поздних стадиях можно использовать системы гистопатологического определения стадии заболевания (например, оперативную систему оценки гастрита (OLGA) и оперативную систему оценки гастрита, основанную на кишечной метаплазии (OLGIM)). Стадии III и IV могут указывать на пациентов, подверженных более высокому риску развития рака желудка [12].
Следует рассмотреть возможность выполнения дополнительной биопсии из угла желудка (умеренный уровень доказательности, слабая рекомендация). Данный подход позволяет обеспечить максимальную степень выявления пациентов с предраковыми состояниями, в особенности в случаях, когда применение хромоэндоскопии для прицельной биопсии невозможно [4].
В случае выявления патологического изменения и результатов эндоскопической оценки, указывающих на наличие дисплазии, рекомендуется проводить резекцию патологического участка без дополнительной биопсии [4].
При наличии возможности для диагностики предраковых состояний желудка следует применять виртуальную хромоэндоскопию с увеличением или без увеличения изображения, что позволяет выполнять контролируемую биопсию на участках атрофических и метапластических изменений, а также обеспечивает выявление неопластических поражений. Эндоскопия высокого разрешения в сочетании с хромоэндоскопией более эффективна, чем эндоскопия высокого разрешения в белом свете, при диагностике предраковых состояний желудка и неопластических поражений на ранней стадии. Если при такой эндоскопии высокого разрешения не выявлены патологические изменения, рекомендуется выполнить биопсию для определения стадии гастрита (если ее не выполняли ранее) и эндоскопическое наблюдение в течение от 6 месяцев (при дисплазии тяжелой степени) до 12 месяцев (при дисплазии легкой степени) [4].
Дисплазия желудка представляет собой предпоследнюю стадию последовательности желудочного канцерогенеза. Ее определяют как гистологически подтвержденные неопластические изменения эпителия без признаков тканевой инвазии, что указывает на непосредственное неопластическое предраковое изменение [13]. Всемирная организация здравоохранения подтвердила классификацию дисплазии/интраэпителиальной неоплазии [14]:
Диагноз «неопределенная дисплазия/неоплазия» не следует изначально рассматривать как безобидный, несмотря на то, что у большинства пациентов прогноз будет благоприятным. В действительности в одном из исследований было установлено, что 26,8% резецированных поражений, классифицированных как неопределенная дисплазия/неоплазия по результатам биопсии перед резекцией, фактически представляли собой неопластические поражения (5,0% — аденома и 21,8% — ранний рак желудка) [15].
Следует помнить, что даже дисплазия легкой степени может представлять собой злокачественное новообразование [16].
В случае видимых патологических изменений одной эндоскопической биопсии недостаточно для диагностики злокачественного новообразования, при наличии любого эндоскопически определяемого патологического изменения с любыми неопластическими изменениями необходимо производить его эндоскопическую резекцию[4].
Рекомендуется проверка гистологических препаратов и немедленная (в кратчайшие возможные сроки) повторная оценка с применением эндоскопии высокого разрешения и хромоэндоскопии [4].
При отсутствии эндоскопически определяемых патологических изменений у пациентов с дисплазией рекомендуется выполнять немедленную повторную оценку с применением эндоскопии высокого разрешения и хромоэндоскопии (виртуальной или с применением красителя) [4].
Пациентам с неопределенной дисплазией, дисплазией, как и с карциномой, диагностированными на основании результатов неприцельной биопсии, необходимо дообследование и лечение только в клиниках, специализирующихся на диагностике и эндоскопическом лечении рака желудка [4].
Неинвазивные методы диагностики предраковых изменений слизистой оболочки желудка
Низкий уровень пепсиногена I в сыворотке крови и (или) низкое соотношение пепсиногена I/II позволяет выявлять пациентов с атрофическим гастритом на поздних стадиях. У таких пациентов рекомендуется выполнять эндоскопию, в особенности при отрицательном результате серологического теста на H. pylori. В качестве предельных значений указывается уровень пепсиногена I
* ФГБОУ ВО МГМСУ им. А. И. Евдокимова Минздрава России, Москва
** ФГБОУ ВО ОмГМУ МЗ РФ, Омск
*** МЦ ЦБ РФ, Москва
**** ФГБОУ ВО СибГМУ Минздрава России, Томск
# ФГБОУ ВО КубГМУ Минздрава России, Краснодар
## ГБУЗ ГБ № 3 г. Сочи Минздрава КК, Сочи
### ИГМАПО — филиал ФГОУ ДПО РМАНПО Минздрава России, Иркутск
#### ФГБОУ ВО КрасГМУ им. проф. В. Ф. Войно-Ясенецкого Минздрава России, Красноярск
@ ФГБОУ ВО УрГМУ Минздрава России, Екатеринбург
@@ ФГБОУ ВО Южно-Уральский ГМУ Минздрава России, Челябинск
Современная стратегия по ведению пациента с предраковыми заболеваниями желудка/ Л. Б. Лазебник, Е. А. Лялюкова, Г. В. Белова, И. В. Долгалёв, Н. В. Корочанская, В. К. Косёнок, А. С. Лялюкова, Е. В. Онучина, М. М. Петрова, Л. В. Прохорова, А. С. Сарсенбаева
Для цитирования: Лечащий врач № 9/2019; Номера страниц в выпуске: 60-64
Теги: хронический атрофический гастрит, кишечная метаплазия, аденокарцинома желудка
Особенности атрофических и дисрегенераторных изменений слизистой оболочки желудка у больных хроническим атрофическим гастритом различных возрастных групп
Клиника госпитальной терапии Военно-медицинской академии имени С.М. Кирова
Интерес исследователей к раннему раку желудка в значительной мере обусловлен тем, что он является своеобразной «переходной» формой между предраковыми изменениями слизистой оболочки желудка и развитым раком желудка, и его изучение позволяет точнее понять морфогенез опухоли и обосновать методы своевременной диагностики и профилактики [8].
Как показали исследования P. Correa, формирование интестинального рака желудка закономерно протекает через ряд последовательных дискретных морфологических стадий: неатрофический гастрит, атрофический гастрит, метаплазия эпителия кишечного типа, прогрессирующая дисплазия и рак insitu, завершающийся инвазивным раком (каскад Корреа). Указанный процесс охватывает обычно период от 20 до 30 лет [11].
Диагноз заболевания верифицировали на основании характерных жалоб, анамнеза, результатов объективного обследования, данных лабораторных и инструментальных исследований. Решающими в постановке окончательного диагноза были данные эзофагогастродуоденоскопии и морфологического исследования слизистой оболочки желудка.
В процессе эндоскопического исследования визуально оценивали наличие, выраженность, распространенность и локализацию воспалительной реакции, очагов атрофии. При воспалительных изменениях слизистой оболочки желудка наблюдали пятнистую гиперемию, отек, подслизистые кровоизлияния, гиперплазию складок. При атрофическом процессе наблюдали бледность, истонченность, повышенную ранимость, сглаженность слизистой оболочки в теле и антральном отделе желудка, просвечивание сосудов.
Прицельные биоптаты слизистой оболочки желудка, полученные при эндоскопическом исследовании, фиксировали в 10% растворе нейтрального формалина, обезвоживали, заливали в парафин, срезы толщиной в 5 мкм окрашивали гематоксилином и эозином и методом ШИК-реакции. Патоморфологические изменения слизистой оболочки желудка оценивали в соответствии с международной классификацией хронического гастрита (Dixon M. Et al., 1996). Оценку выраженности атрофического процесса, кишечной метаплазии и клеточной инфильтрации стромы слизистой оболочки проводили в соответствии с дополнениями к Сиднейской классификации.
Результаты. В работах различных авторов [3, 9, 10] неоднократно указывалась ценность эндоскопического метода исследования в возможности выполнения биопсии с последующим гистологическим исследованием полученного материала. Диагноз “хронический гастрит” должен быть исключительно клинико-морфологическим, а при постановке окончательного диагноза необходимо, прежде всего, ориентироваться на результаты гистологического анализа, поскольку данные эндоскопического и морфологического исследований нередко могут не совпадать. Однако часто в повседневной клинической практике врачи ориентируются только на данные эндоскопического исследования.
В нашем исследовании также проводился анализ эндоскопических и морфологических признаков атрофии слизистой оболочки желудка.
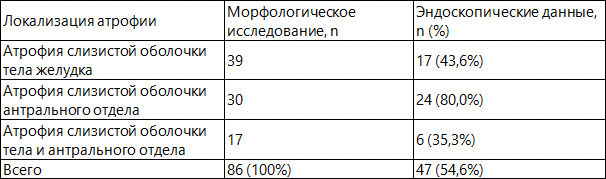
Данные по выявлению атрофических изменений слизистой оболочки желудка, полученные в процессе эндоскопического исследования, в сравнении с морфологическими данными представлены в табл. 1.
Таблица 1. Сравнительная оценка морфологических и эндоскопических данных в диагностике атрофии слизистой оболочки желудка.
Согласно полученным данным, можно утверждать, что при диагностике атрофических изменений слизистой оболочки желудка у больных хроническим гастритом в процессе эндоскопического исследования и морфологического анализа их результаты совпадают лишь в 54,6% случаев. Примерно у половины больных атрофические изменения слизистой оболочки желудка, выявленные морфологическим методом, остаются недоступными для адекватной эндоскопической оценки, что обосновывает необходимость гистологической верификации «гастритического» процесса.
Кишечная метаплазия, дисплазия слизистой желудка
Часто приходят на прием пациенты, которым было проведено эндоскопическое исследование желудка и в заключении специалист пишет: «хронический гастрит, кишечная метаплазия». Если о хроническом гастрите наши пациенты наслышаны, то кишечная метаплазия вызывает тревогу и мысли о злокачественном поражении желудка. Так ли это?
Термин «хронический гастрит» обозначает хроническое воспаление желудка, но речь идет не обо всей стенке желудка, а только слизистой оболочке, в которой наряду с воспалительными и атрофическими процессами развивается нарушение обновления клеток слизистой желудка, что является важным признаком гастрита и может определять прогноз хронического гастрита.
О слизистой желудка подробнее
Слизистой желудка свойственно постоянное клеточное обновление. При любых повреждениях слизистой желудка активизируется регенерация, что приводит к восстановлению структуры слизистой. Свидетельством нарушения клеточного обновления при хроническом гастрите служат характерные для него изменения слизистой, нарушение фаз клеточного обновления, которые хорошо известны морфологам и определяются как нарушения морфологической перестройки слизистой оболочки желудка в виде кишечной метаплазии и дисплазии слизистой.
Поэтому при проведении эндоскопического исследования необходимо провести множественные биопсии слизистой желудка, чтобы подтвердить диагноз хронического гастрита, при котором может наблюдаться качественное нарушение регенерации (восстановления) клеток и замещение их несвойственными для желудка или его отделов клетками, т.е. речь идет о замещении желудочного эпителия кишечным. Метаплазия (от греческого «образование, формирование) — стойкое замещение клеток одного типа на клетки другого типа при сохранении видовой принадлежности ткани.
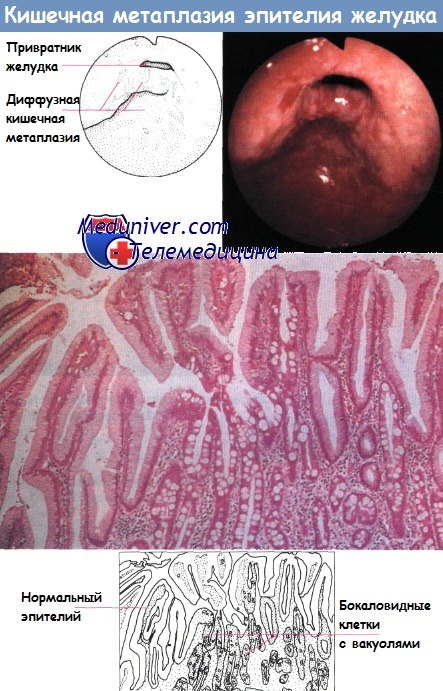
Что представляет собой кишечная метаплазия
Кишечная метаплазия была описана более ста лет назад, и до настоящего времени она изучается, главным образом, из-за возможной связи с раком желудка. Кишечная метаплазия встречается достаточно часто. В пожилом возрасте ее находят и у практически здоровых людей, но особенно часто при атрофическом гастрите почти в 100%. При язвах желудка – в 81%. При язвах 12-перстной кишки – 47%. Рак желудка занимает 4 место в структуре онкологических заболеваний.
Уровень пепсиногенов в крови является маркером хронического атрофического гастрита и риска развития рака желудка. Поэтому проведение определения по анализу крови уровня пепсиногенов и хеликобактерной инфекции улучшает выявление хронического атрофического гастрита и рака желудка.
При подозрении у пациента хронического атрофического гастрита (по результатам гастропанели) показано проведение гастродуоденоскопии с множественной биопсией слизистой желудка. Гистологическое подтверждение кишечной метаплазии является наиболее надежным маркером атрофии слизистой оболочки желудка. Пациенты, у которых диагностирован хронический атрофический гастрит с кишечной метаплазией, находятся в группе риска по развитию рака желудка (аденокарциномы желудка).
Факторами риска кишечной метаплазии могут быть:
Кишечная метаплазия — типы
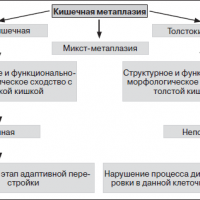
В настоящее время различают два типа метаплазии – полную, напоминающую слизистую тонкой кишки, метаплазия 1 типа и неполную, напоминающую слизистую толстой кишки, метаплазия 2 типа.
Полная кишечная метаплазия
Она встречается наиболее часто при хронических гастритах. Тонкокишечный эпителий, образующий участки метаплазии, вообще мало склонен к малигнизации (раковому перерождению). Широко известным фактором является большая редкость рака тонкой кишки. Поэтому полную кишечную метаплазию не относят к предраковым изменениям слизистой. Если наблюдаются проявления хронического гастрита, то динамическое наблюдение и проведение гастродуодкерскопии проводится через 3-5 лет.
В питании показано употреблять продукты, обладающие обволакивающими свойствами — рисовый отвар, кисель, фрукты в запеченном виде, джемы на пектинах, из трав – семя льна.
Неполная кишечная метаплазия
Напоминает слизистую толстой кишки и выявляется у 11% больных всеми доброкачественными заболеваниями желудка, но при раке желудка она наблюдается в 94% случаев. Неполная кишечная метаплазия показала более высокую специфичность этого признака изменения слизистой желудка к раку, но низкая чувствительность (38%) говорит об ограниченном значении ее как показателя прогноза развития рака кишечного типа. Важным фактором при этом имеет большая площадь замещения нормального желудочного эпителия кишечным.
Известна связь хронического атрофического гастрита, кишечной метаплазии и хеликобактер пилори, при которых ликвидация хеликобактера способна предотвратить развитие и прогрессирование атрофии, а также возможно обратное развитие атрофии слизистой желудка. Наличие же кишечной метаплазии является признаком хеликобактерного гастрита. Пациенты с неполной кишечной метаплазией наблюдаются динамически ежегодно.
Неполная кишечная метаплазия слизистой желудка часто переходит в следующую стадию перестройки слизистой – дисплазию метаплазированного эпителия.
Морфологическая диагностика болезней желудка
Дисплазия метаплазированного эпителия – диагноз морфологический. О ней можно говорить при наличии клеточной атипии и нарушении структуры клеток слизистой оболочки желудка. В зависимости от выраженности этих изменений выделяют 3 степени дисплазии:
Понятие дисплазии было предложено для обозначения предраковых изменений, формирования групп повышенного риска для наблюдения и превентивного лечения. Исследования развития дисплазий показали, что у больных с дисплазией 2 степени в 4-8% найдено прогрессирование в дисплазию 3 степени.
Наблюдение больных дисплазией 1 и 2 степени
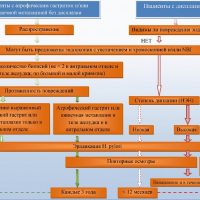
При выявлении в биоптатах слизистой желудка признаков тяжелой дисплазии следует провести множественные повторные биопсии через 6-12 месяцев, так как тяжелая дисплазия чаще свидетельствует не о том, что у больного может возникнуть рак, а о том, что он уже есть. И если даже рак еще не обнаружен, то таким больным рекомендуется хирургическое лечение — хирургическая или эндоскопическая резекция из-за высокой вероятности развития аденокарциномы (рака желудка). У 25% дисплазия высокой степени может спрогрессировать до аденокарциномы в течение года.
Иначе просто динамическое наблюдение даже с множеством биопсий при эндоскопии при подтверждении тяжелой дисплазии слизистой желудка может закончиться тем, что будет упущено время для диагностики раннего рака желудка и своевременного лечения и выздоровления.
Лечение больных дисплазией 3 степени
У пациентов, у которых выявлен хронический атрофический гастрит с дисплазией, которая связана со штаммами хеликобактер пилори высокой вирулентности, повышенный риск развития рака желудка. Эрадикация хеликобактер пилори может привести к регрессу атрофических процессов в желудке и снижению риска рака желудка. При дисплазии требуется эрадикация хеликобактер пилори, ритмичное питание, защита слизистой желудка от повреждения ее лекарственными средствами.
Если при обследовании выявлен низкий уровень пепсиногена I и низкое соотношение пепсиноген I/пепсиноген II, это уже серьезная стадия атрофического гастрита/ Рекомендуется гастродуоденоскопия с множественной биопсией, даже в тех случаях, если серологический тест (определение антител в сыворотке крови) на хеликобактер пилори не выявил инфекцию в желудке.
Морфологами в биоптатах слизистой оболочки желудка по новой системе стадирования атрофического гастрита (OLGA) cумммируются показатели атрофии в теле и антральном отделе желудка с определением баллов в каждом биоптате. III и IV стадии выраженности атрофического гастрита по этой системе свидетельствует о высокой реальности развития рака желудка
Кишечная метаплазия – будьте бдительны!
В заключении хочу привести слова проф. Аруина Л.И., опытного и знающего морфолога, который сказал: «хронический гастрит и рак желудка разделяет дистанция огромного размера, а дисплазия и рак желудка живут в одной квартире».
Будьте внимательны к своему здоровью, вовремя проводите обследования, задавайте вопросы доктору, следуйте его рекомендациям. Здоровья вам!