Метопролол сукцинат и метопролол в чем отличие
Метопролол сукцинат и метопролол в чем отличие
Ю.Б. Белоусов, М.В. Леонова, О.А. Манешина, А.В. Соколов, И.Ф. Тищенкова
Метопролола сукцинат и тартрат: влияет ли соль на эффективность препарата?
Стремление повысить эффективность и безопасность лечения метопрололом сердечно-сосудистых заболеваний привело к разработке пролонгированных форм препарата. Освещаются основные этапы их создания, приводятся сравнительные данные фармакокинетических параметров различных лекарственных форм метопролола. Вопрос о влиянии соли в составе препаратов метопролола на эффективность лечения остается предметом научных дискуссий. Было показано, что соли обеспечивают разную фармакокинетику и изменяют скорость всасывания препарата в кровь, а эффективность лекарственного средства обусловлена плазменной концентрацией метопролола. Использование ретардных технологий с длительным высвобождением лекарственного вещества позволяет модифицировать фармакокинетический профиль метопролола тартрата и нивелировать роль соли. Это создает значительные перспективы для дальнейших исследований в области ретардных технологий с целью повышения эффективности медикаментозного лечения и улучшения контроля за течением сердечно-сосудистых заболеваний.
Создание новых лекарственных средств (ЛС) требует колоссальных финансовых затрат и сопряжено с высоким экономическим риском, что ограничивает долговременные инвестиции в этой области. Альтернативой на пути усовершенствования медикаментозной терапии становится разработка новых лекарственных форм с различными системами доставки лекарственного вещества на основе уже известных препаратов. Усовершенствование технологий по производству новых лекарственных форм возможно лишь за счет модификации фармакокинетических параметров ЛС, таких как скорость выделения лекарственного вещества из таблетки, длительность нахождения его в определенной зоне желудочно–кишечного тракта (ЖКТ), место всасывания и метаболизма. Фармакодинамические характеристики лекарственного вещества изменить невозможно, т. к. они зависят только от химического строения его молекулы, которое, как известно, при любых модификациях лекарственной формы не изменяется.
Применение новых лекарственных форм, как правило, способствует повышению эффективности и переносимости лечения, снижению риска развития побочных эффектов и за счет уменьшения кратности приема ЛС повышает приверженность (комплаенс) пациентов проводимой терапии.
Пролонгированные формы ЛС
Эффективность пролонгированных форм ЛС достигается за счет изменения фармакокинетического профиля, что обеспечивает более стабильную концентрацию препарата в течение 24–часового интервала с увеличением показателя минимальной концентрации (Сmin) и возрастанием минимального эффекта (Emin) в интервале дозирования [1]. Показатель максимальной концентрации (Cmax) препарата в крови для таких лекарственных форм имеет меньшее значение, что сопряжено с уменьшением максимального эффекта (Emax). Это делает прием новых лекарственных форм более безопасным, что очень актуально у особых категорий больных [2]. Однократный режим дозирования удобен для пациентов, а особая структура таблетки, состоящей из отдельных защищенных гранул, позволяет делить ее на необходимые дозы.
Первые технологии ретард (retardo – препятствующий, замедляющий) появились в 1970–1980–х гг., когда возникла необходимость в лекарственных формах, обеспечивающих длительное равномерное выделение ЛС в просвет ЖКТ, что предупреждает развитие побочных эффектов, возникающих при использовании ЛС с быстрым всасыванием и высокими пиковыми концентрациями [3, 4]. Равномерное выделение лекарственного вещества, помещенного в капсулу в виде раствора, за счет осмотического градиента легло в основу технологии осмотического насоса OROS (Oral Osmotic). Позже была разработана технология Геоматрикс (Geomatrix, Skye Pharma), основанная на послойном покрытии таблетки и создании вокруг нее барьера из высоковязкой гидроксипропилметилцеллюлозы. В центре такой таблетки находится активное вещество (вещества), покрытое одним или более слоями полимера, контролирующего скорость диффузии лекарства. Во время растворения таблетки набухающий барьер утолщается, но не разрушается, тогда как разрушающийся барьер, постепенно распадаясь, открывает внутреннее ядро таблетки, что приводит к контролируемому выделению действующего вещества.
Следующим этапом на пути создания пролонгированных лекарственных форм стала сфероидальная система для орального применения (SODAS, Elan) с использованием частиц с контролируемым выходом лекарства. Шарообразные частицы диаметром 1–2 мм, содержащие действующее лекарственное вещество, покрыты специфичным для данного лекарства полимером и обеспечивают его контролируемый выход. Выделение активного вещества начинается, когда полимер растворяется, жидкость входит в ядро сферы, растворяет его, после чего лекарство начинает диффундировать [5]. В настоящее время известны различные модификации технологий ретард (табл. 1).
Интерес к пролонгированным формам ЛС с усовершенствованной системой доставки лекарственных веществ вновь повысился после того, как стало известно, что ретардные формы препаратов способны не только повышать эффективность лечения, но и самостоятельно осваивать новые нозологические ниши.
Лекарственные формы метопролола
Метопролол – селективный блокатор бета1–адренорецепторов без внутренней симпатомиметической активности со слабым мембраностабилизирующим действием, принадлежит к группе жирорастворимых бета–адреноблокаторов [6]. Вследствие низкой растворимости в воде в состав лекарственных препаратов метопролол входит в виде соли. Обычные таблетированные формы метопролола с немедленным высвобождением (IR – Immediate Release) содержат его хорошо растворимый тартрат (растворимость в воде > 700 мг/мл при 37 °С), в то время как формы метопролола с замедленным (SR – Sustained Release) и контролируемым высвобождением (CR – Controlled Release) – менее растворимые соли (фумарат и сукцинат соответственно с растворимостью в воде
Стремление повысить эффективность и безопасность лечения метопрололом пациентов с сердечно–сосудистыми заболеваниями привело к разработке пролонгированных форм препарата. Первоначально были произведены две лекарственные формы с использованием технологии матричных полимеров, которые содержали метопролола тартрат в дозе 200 мг (таблетки Slow Lopresor ® и Betalok Durules ® ). Матрикс, покрывающий таблетки, был инертен в пищеварительном соке, но полностью распадался под действием кишечной перистальтики с высвобождением активного вещества [10, 11].
Исследования лекарственных форм метопролола с замедленным высвобождением (SR) лекарственного вещества показали, что, несмотря на модификацию ряда фармакокинетических характеристик, требования, которым должна отвечать идеальная ретардная технология препарата, так и не были достигнуты. Установлено, что плато концентрации метопролола в плазме на стадии равновесной концентрации может и не образоваться. Кроме того, оставались достаточно высокими колебания между значениями Cmax и Cmin (“пик–спад”), что является показателем флюктуации препарата [9, 10].
Следующим этапом на пути разработки новых лекарственных форм с усовершенствованной системой доставки лекарственного вещества стала технология CR/XL ZOK (Controlled Release/Extended Release, Zero–Order–Kinetics) с использованием метопролола сукцината. Таблетка метопролола сукцината CR/XL (Беталок ЗОК, AstraZeneca, Швеция) содержит спрессованные сферические гранулы препарата, окутанные этилцеллюлозной полимерной мембраной, контролирующей высвобождение лекарства из гранул. После приема внутрь таблетка распадается на отдельные гранулы, каждая из которых действует как диффузная камера, обеспечивая относительно постоянную скорость высвобождения препарата в течение 20 часов независимо от рН пищеварительного сока и других физиологических показателей. Таблетка в 100 мг содержит 95 мг метопролола сукцината, который по активности эквивалентен 100 мг метопролола тартрата [1, 11, 12].
Сравнение фармакокинетических параметров, полученных на стадии равновесной концентрации при применении метопролола сукцината CR/XL в дозе 50–400 мг/сут однократно и метопролола тартрата в форме таблеток IR в различных режимах дозирования выявило четкие различия в показателях максимальной концентрации (Сmax), минимальной концентрации(Cmin), площади под кривой зависимости концентрации от времени (AUC – Area Under Curve) и флюктуации (табл. 2) [7].
Показано, что значение Сmax значительно ниже при применении метопролола CR/XL, чем метопролола IR, причем разница в величине Сmax двух препаратов была максимальной при их применении в дозах 50 мг и 100 мг, а наименьшей – при назначении суточной дозы 400 мг. Величина Cmin была значительно выше для CR/XL формы в дозах 50 и 100 мг, равнозначной – в дозе 200 мг и ниже – в дозах 300–400 мг, чем для IR формы [13]. Показатель флюктуации препарата определяли как разность между Сmax и Cmin препарата в крови по отношению к AUC в интервале дозирования [8].
Максимальная разница в показателях флюктуации наблюдалась при применении 50 мг обеих форм метопролола однократно в сутки. При увеличении кратности приема препарата в IR форме с увеличением суточной дозы до 400 мг различия исчезали. Коэффициент флюктуации для формы с контролируемым высвобождением оставался стабильно низким при однократном приеме различных доз препарата (см. рисунок) [8, 13].
Cогласно данным Guppy M. (2004), перед всасыванием соль метопролола растворяется, а свободный метопролол становится активным ингредиентом. Если это утверждение верно, то соль не должна влиять на фармакокинетику и фармакодинамику препарата и различия в эффективности лекарственных форм объясняются особенностями ретардных технологий.
В большинстве исследований, которые проводились на раннем этапе изучения этой проблемы, использовали метопролола тартрат. Применение именно этой соли позволило продемонстрировать способность метопролола снижать смертность больных артериальной гипертензией (АГ) и инфарктом миокарда (ИМ). Позже появились метопролола сукцинат и метопролола фумарат [14]. Вид соли определяет различия в фармакокинетике и скорости поступления метопролола в кровь. Однако эффективность препарата обусловлена плазменной концентрацией метопролола. Поэтому разработка ретардных технологий позволяет, по сути, нивелировать эффект соли.
Исследования, проведенные на здоровых добровольцах, показали, что применение ретардной технологии OROS с использованием метопролола фумарата (лекарственной формы метопролола – ER/OROS) обеспечивает достижение относительно стабильных плазменных концентраций ЛС при однократном ежедневном приеме [15, 16]. Биологическую эквивалентность метопролола ER/ZOK и метопролола ER/OROS доказали Sandberg А. и соавт. (1993) [17].
Подтверждением приоритетного значения концентрации метопролола в крови в реализации его клинических эффектов являются результаты многочисленных крупных клинических исследований метопролола и огромный опыт его длительного применения для лечения сердечно–сосудистых заболеваний. Так, согласно результатам исследования Herlitz J. и соавт. (1999) влияния метопролола сукцината и тартрата на уровень смертности больных, перенесших ИМ, метопролол независимо от состава соли снижал смертность после ИМ на 34 % (р
Сравнительное изучение нового препарата метопролола тартрата пролонгированного действия – эгилока ретард и оригинального препарата метопролола сукцината – беталока зок у больных мягкой и умеренной артериальной гипертонией
Материалы и методы. В исследовании участвовало 30 человек – 11 мужчин и 19 женщин, страдающих мягкой и умеренной артериальной гипертонией (АГ). Исследование было рандомизированным, открытым, перекрестным. Перед началом исследования всем пациентам отменялась ранее используемая гипотензивная терапия на 10-14 дней. Каждый из пациентов поочередно проходил 6-недельное лечение Эгилоком ретард (ЭР) и Беталоком ЗОК (БЗ) в дозе 50-100 мг. После отмены предшествующей антигипертензивной терапии пациенту назначалось лечение БЗ или ЭР (по таблице рандомизации) в дозе 50 мг. Препараты принимались один раз в сутки. Терапию первым рандомизационным препаратом завершили 29 человек, вторым – 25 пациентов. Через две недели оценивалась эффективность терапии по достижению целевого уровня АД (
Результаты исследования. После 6-недельного лечения ЭР и БЗ средний уровень систолического АД снизился на 15,7 и 15,2 мм рт ст, диастолического АД снизился на 8,0 и 4,5 мм рт ст, ЧСС – на 4,1 и 4,3 уд. в мин. соответственно. Различия между гипотензивным и брадикардитическим эффектом исследуемых препаратов статистически не значимы. Целевого уровня АД при терапии обоими ББ удалось до- стичь приблизительно в половине случаев – у 48% больных, получавших БЗ и у 56% пациентов, принимавших ЭР. Большее число побочных эффектов было зарегистрировано во время лечения БЗ (р=0,003). Большинство побочных реакций не носило серьезного характера, а по субъективной оценке пациентов переносимость препаратов не отличалась.
Заключение. По результатам исследования новый препарат метопролола тартрата пролонгированного действия – Эгилок ретард при назначении в течение 6 нед пациентам с мягкой и умеренной артериальной гипертонией в виде монотерапии не отличается по эффективности и безопасности от оригинального препарата метопролола сукцината пролонгированного действия – Беталока ЗОК.
Ключевые слова: метопролол тартрат, метопролол сукцинат, артериальная гипертония, антигипертензивная терапия.
Aim. To study efficiency and safety of new drug of long acting metoprolol tartrate, “Egilok retard” (ER) in patients with mild to moderate arterial hypertension (AH) in comparison with the original drug of metoprolol succinat, “Betaloc ZOK” (BZ), possibility of reaching target blood pressure (BP) level with treatment with each drug.
Material and methods. 30 patients (11 men and 19 women) with mild to moderate AH took part in randomized, open, cross over study. Previous antihypertensive treatment had been canceled for all the patients 10-14 days before the study started. Each patient by turns was treated during 6 weeks with ER and BZ 50-100 mg daily. After cancellation of the previous antihypertensive therapy, BZ and ER were prescribed (according to the randomization table) in dose 50 mg daily. Drugs were taken once per day. 29 patients completed therapy with the first drug of randomization, 25 patients – with the second. After 2 weeks efficiency of treatment was assessed by target BP level achievement (
Results. After 6-week treatment with ER and BZ average level of systolic BP reduced by 15,7 and 15,2 mmHg, of diastolic BP – by 8,0 and 4,5 mmHg, heart rate – by 4,1 and 4,3 beat/min respectively. Differences between antihypertensive and heart rate lowering effect of the studied drugs were not significant. Target BP level with treatment with both drugs was reached in approximately half cases – in 48% of BZ patients, and in 56% of ER patients. Biger number of side effects was registered in BZ treatment (p=0,03). Most side effects were not severe and according to the patient assessment tolerance of both drugs didn’t differ.
Conclusion. Results of the study show that in patients with mild to moderate AH 6-week monotherapy with new drug of long acting metoprolol tartrate, ER, does not differ on efficacy and safety from original drug of long acting metoprolol succinate, BZ.
Key words: metoprolol tartrate, metoprolol succinate, arterial hypertension, antihypertensive therapy
Rational Pharmacother. Card. 2005;3:35-40
Бета-адреноблокаторы (БАБ) занимают одно из ведущих мест в терапии больных с сердечно-сосудистыми заболеваниями. Эти препараты используются в клинике с начала 60-х годов, причем их роль в лечении сердечно-сосудистых заболеваний оказалась столь значительной, что в 1988 г. ученые, принимавшие участие в создании БАБ, были награждены Нобелевской премией [1]. БАБ входят в состав основных групп антигипертензивных препаратов [2,3]. Одним из наиболее известных БАБ является метопролол [4]. В ряде крупных рандомизированных многоцентровых исследований были подтверждены положительные эффекты метопролола у больных артериальной гипертонией, ишемической болезнью сердца [2,3,5]. С целью достижения стабильной блокады бета1-адренорецепторов был разработан препарат метопролола сукцинат пролонгированного действия – MS-CR/XL. Именно эта форма метопролола доказала свои преимущества при лечении пациентов с хронической сердечной недостаточностью в исследованиях MERIT-HF, RESOLVED (Metoprolol study) [5,6].
Несмотря на очевидную положительную роль БАБ в лечении больных c сердечно- сосудистой патологией, практические врачи неохотно назначают эти препараты, а если и назначают их, то обычно используют недостаточные дозы. Неактивность врачей в отношении терапии БАБ приводит к тому, что многие больные не получают той пользы от лечения, которую оно могло бы дать. Кроме того, при наличии большого выбора современных препаратов из этой группы продолжают широко использовать устаревшие БАБ или БАБ с недостаточной доказательной базой. Известно, например, что назначение метопролола в России составляет около 4% от всех назначений БАБ (в Германии – 35%), при этом наиболее часто назначаются препараты, действующим веществом в которых является метопролола тартрат с немедленным высвобождением активного вещества (MT-IR) [7].
В последнее время в качестве альтернативы препаратам метопролола сукцината созданы новые лекарственные формы метопролола тартрата, обеспечивающие устойчивый пролонгированный эффект препаратов с этим действующим веществом.
Задачей настоящего исследования было сравнительное изучение нового препарата метопролола тартрата пролонгированного действия – ЭГИЛОКА РЕТАРД (ЭР) (EGIS, Венгрия) и оригинального препарата метопролола сукцината – БЕТАЛОКА ЗОК (БЗ) (Аstra Zeneca, Великобритания).
Материалы и методы
Протокол открытого, рандомизированного, перекрестного, сравнительного исследования был одобрен Этическим комитетом ГНИЦ ПМ. Каждый больной давал письменное информированное согласие на участие в исследовании.
Для исследования были отобраны пациенты с мягкой и умеренной артериальной гипертонией (АГ): 140
Всего в исследование было включено 30 больных (11 мужчин и 19 женщин) в возрасте от 42 до 78 лет, средний возраст составил 62,7 года. Длительность диагностированной АГ колебалась от 2 лет до 31 года и составила в среднем 10 лет. На ЭКГ у 5 пациентов, перенесших инфаркт миокарда, регистрировались признаки рубцовых изменений, у 2 больных определялась АВ-блокада I степени, у 1 пациента была зарегистрирована желудочковая экстрасистолия.
Во время визита к врачу проводились измерения АД и ЧСС, через 24 ч после последнего приема препарата, до приема очередной дозы БАБ. Контроль артериального давления (АД) (в положении пациента сидя, трижды с интервалом в 2 мин) и ЧСС проводили исходно (до лечения), а также через 2 и 6 недель терапии каждым препаратом. Через 2 недели лечения первой дозой БАБ и через 6 недель терапии препаратом метопролола проводилась регистрация побочных эффектов и определялась приверженность лечению.
После 6 недель лечения первый препарат отменяли на 10-14 дней (в зависимости от используемой дозы метопролола).
При каждом визите всем пациентам регистрировалась ЭКГ.
Гипотензивный эффект препаратов оценивали по результатам измерения АД (изменение от базового уровня после 6-недельного курса терапии). Препарат считали эффективным, если регистрировалось снижение АД ниже уровня 140/90 мм рт.ст.
При обработке результатов исследования использовался пакет статистических программ STATISTICA 6.0. Для оценки полученных данных применялись как стандартные методы описательной статистики (вычисление средних, средних квадратичных отклонений), так и известные критерии значимости (парный t-критерий Стьюдента, χ2 и др.).
Результаты представлены в виде М+σ (М – среднее, σ – среднее квадратичное отклонение). Различия расценивались как статистически значимые при р
Результаты исследования
Из 30 человек, принимавших участие в исследовании, полностью оба курса лечения завершили 25 человек.
Лечение первым препаратом завершили 29 человек. Во второй этап исследования было включено 28 человек, из которых полностью закончили лечение 25 человек, 5 человек выбыли на разных этапах исследования вследствие наличия у них побочных явлений. Возможная связь нежелательных явлений с приемом препаратов была зафиксирована лечащими врачами у 4 больных.
Лечение БЗ было назначено 30 пациентам (по таблице рандомизации), 6-недельное лечение препаратом метопролола сукцината завершили 29 человек. Два пациента, прошедших терапию БЗ, в результате развившихся во время лечения нежелательных явлений отказались принять дальнейшее участие в исследовании и терапию ЭР не получали, однако у одного из этих больных побочный эффект был зафиксирован в конце 6-й недели БЗ, лечение которым он завершил.
Терапия ЭР была назначена 28 пациентам (2 выбыли на этапе лечения первым препаратом). Еще 3 человека выбыли из-за побочных эффектов и нежелательных явлений на фоне лечения ЭР.
Таким образом, 6-недельную терапию ЭР прошли 25 человек, а БЗ – 29 пациентов с артериальной гипертонией.
В результате рандомизации было сформировано 2 группы пациентов, в одной из которых первым получаемым препаратом был ЭР, а в другой – БЗ. Статистически значимых отличий по основным параметрам на начало исследования между группами выявлено не было, поэтому результаты анализировались суммарно, без учета последовательности назначения препарата.
Оба исследуемых препарата оказывали выраженный гипотензивный эффект. Причем ЭР в среднем вызывал несколько большее снижение ДАД, однако статистически значимых различий между препаратами по влиянию на уровень САД и ДАД выявлено не было (рис.1).
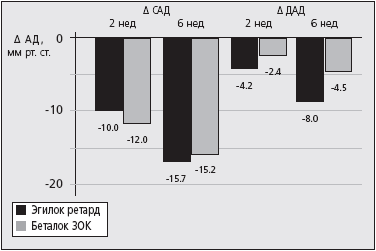
Рис.1. Изменение показателей САД и ДАД в результате терапии (Δ САД и Δ ДАД).
Также не обнаружено статистически значимого различия между исследуемыми препаратами по влиянию на ЧСС (рис. 2).
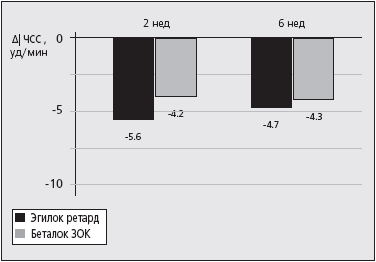
Рис. 2. Изменение ЧСС через 2 и 6 недель лечения каждым препаратом (Δ ЧСС).
На серии ЭКГ, зарегистрированных на каждом визите, новых патологических изменений и статистически значимого отклонения определяемых параметров (длительности интервалов QT, QTc, PR, комплекса QRS, а также ЧСС) выявлено не было.
Распределение пациентов в зависимости от суточной дозы метопролола было одинаковым для исследуемых препаратов (табл.1).
Таблица 1.
Распределение пациентов в зависимости от получаемой дозы метопролола
| Число больных | ||
|---|---|---|
| Доза | Эгилок ретард | Беталок ЗОК |
| 50 мг/сут | 12 | 13 |
| 100 мгсут | 16 | 17 |
| Всего | 28 | 30 |
В ряде случаев удвоение дозы препарата было невозможно из-за развившихся уже при применении 50 мг/сут метопролола побочных эффектов. В остальных случаях дозы препаратов были удвоены. Только у 1 пациентки оба препарата вызывали синусовую брадикардию с ЧСС
Целевой уровень АД (
Таблица 2.
Оценка эффективности препаратов (по визитам)
| Препарат | Пациенты, достигшие целевого АД | Больные, не достигшие целевого АД | |
| визит 2 нед | визит 6 нед | ||
| Эгилок ретард (n=25) | 6 (24%) | +8 (32%) (всего 14 (56%)) | 11 (44%) |
| Беталок ЗОК (n=29) | 8 (28%) | +6 (21%) (всего 14 (49%)) | 15 (51%) |
Таблица 3.
Побочные эффекты Эгилока ретард и Беталока ЗОК
| Побочный эффект | Эгилок ретард | Беталок ЗОК |
| Кашель | 0 | 1 |
| Аллергический дерматит | 1 * | 1 |
| Головокружение | 0 | 1 |
| Головная боль | 1 | 1 |
| Боль в эпигастрии | 0 | 1 * |
| Дискомфорт в правом подреберье | 0 | 1 * |
| Нарушение стула | 1 | 0 |
| Тошнота | 1 * | 0 |
| Синусовая брадикардия (с клинической симптоматикой) | 1 | 1 |
| Всего случаев | 5 | 7 |
| * Побочные эффекты, приведшие к выбыванию пациентов из исследования. | ||
При анализе согласованности побочных реакций на препараты метопролола критерий χ 2 превысил критическое значение, соответствующий уровню значимости р 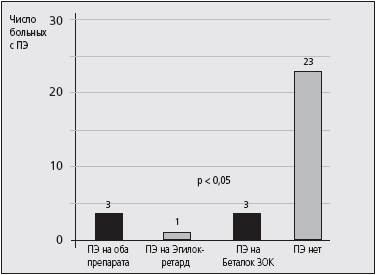
Рис. 3. Побочные эффекты (ПЭ) при лечении бета-адреноблокаторами.
Однако в большинстве случаев побочные эффекты не носили характера серьезных, после отмены препаратов метопролола проходили самостоятельно и не требовали назначения дополнительной терапии.
На фоне терапии ЭР было зарегистрировано серьезное нежелательное явление – повторный острый инфаркт миокарда у пациентки, страдающей гипертонической болезнью III стадии, II степени, риск осложнений – очень высокий. Однако, по-видимому, данное нежелательное явление не было связано с проводимой терапией и обусловлено течением конкурирующего основного заболевания на фоне недостаточно эффективной гипотензивной монотерапии.
Данные врачебной клинической и субъективной оценки эффективности и переносимости ЭР и БЗ продемонстрированы на рис. 4 и 5. Выявлено, что при одинаковой хорошей субъективной переносимости препаратов, пациентами и врачами отмечена несколько лучшая гипотензивная эффективность ЭР по сравнению с действием БЗ.
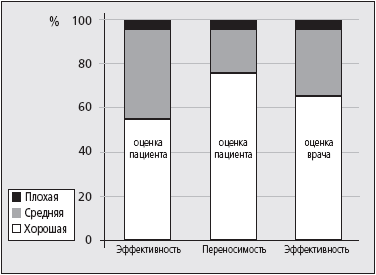 | 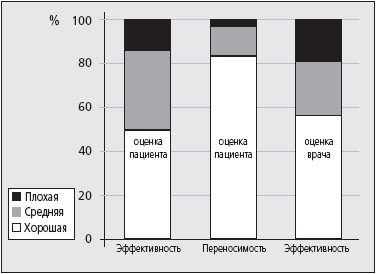 |
| Рис. 4. Оценка эффективности и переносимости Эгилока-ретард пациентами и врачами. | Рис. 5. Оценка эффективности и переносимости Беталока ЗОК пациентами и врачами. |
Обсуждение
В настоящее время метопролол является одним из наиболее изученных селективных БАБ [4]. В России зарегистрированы препараты, действующим веществом которых является одна из солей метопролола: метопролола тартрат или метопролола сукцинат.
Различие между двумя солями метопролола заключается в неодинаковой скорости всасывания в кишечнике: метопролол сукцинат в отличие от тартрата всасывается медленнее, что позволяет назначать препараты с данной солью метопролола 1 раз в день. Это позволило незначительно уменьшить дозу действующего вещества в БЗ, о чем указано в аннотации к препарату: 1 таблетка БЗ 50 или 100 мг содержит соответственно 47,5 и 95 мг метопролола сукцината, что эквивалентно 50 и 100 мг метопролола тартрата [8].
Очевидные преимущества метопролола сукцината пролонгированного действия (метопролол CR/LX) были доказаны при сердечной недостаточности [4,5,9] и, кроме того, при изучении антиатеросклеротического эффекта метопролола на фоне гиполипидемической терапии в исследовании ELVA [11]. Оригинальным препаратом метопролола сукцината пролонгированного действия, зарегистрированным в России, является «Беталок ЗОК».
Недавно была создана новая лекарственная форма метопролола тартрата пролонгированного действия – «Эгилок ретард» (ЭР). Оригинальный матрикс таблеток ЭР обеспечивает замедленное высвобождение метопролола и стабильную концентрацию препарата в плазме в течение суток, что позволяет сократить кратность приема препаратов до 1 раза в день [12]. Результаты, подтверждающие высокую эффективность и безопасность ЭР у пациентов с мягкой и умеренной АГ, были получены в многоцентровом проспективном исследовании ProlongER, проводившемся на Украине [12]. По данным ProlongER, при лечении ЭР снижение офисного систолического АД составило 32 мм рт. ст., диастолического АД – 18 мм рт. ст., а ЧСС – на 18 ударов в минуту. Более скромные результаты, полученные в нашем исследовании, могут объясняться меньшими дозами БАБ (50-100 мг/сут), так как в программе ProlongER ЭР применялся в дозе 25-300 мг/сут. Достижение целевого уровня АД в ProlongER по данным офисного измерения и суточного мониторирования АД было достигнуто в 93,6 и 85% случаев соответственно. Это значительно превышает показатели, продемонстрированные в нашем исследовании, и может быть объяснено более высокими дозами ЭР, а также добавлением к терапии БАБ гидрохолортиазида в 30% случаев.
Результаты данного исследования, продемонстрировавшие, что целевого уровня АД удается достичь у 48 и 56% пациентов на фоне терапии Беталоком ЗОК и Эгилоком ретард соответственно, согласуются с данными крупных исследований, в которых использовался метопролола тартрат 14. Следует учитывать, что средняя доза метопролола в международных трайлах составляла 100-150 мг/сут.
Заключение
Таким образом, новый препарат метопролола тартрата пролонгированного действия – Эгилок ретард при назначении в течение 6 нед пациентам с мягкой и умеренной артериальной гипертонией в виде монотерапии не отличается по эффективности и безопасности от оригинального препарата метопролола сукцината пролонгированного действия – Беталока ЗОК. При подборе гипотензивного лечения следует учитывать, что у больных мягкой и умеренной артериальной гипертонией эффективность монотерапии препаратами группы бета-адреноблокаторов дозозависима и позволяет достичь целевого уровня АД приблизительно в 50-60% случаев.