Между чем образуется водородная связь
Водородная связь.
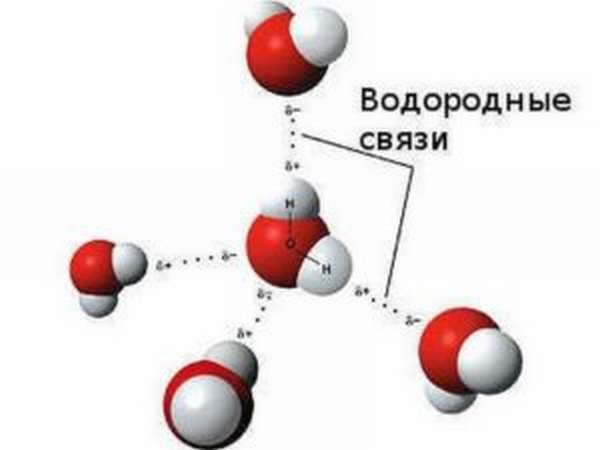
Водородная связь – связь между положительно заряженным атомом водорода одной молекулы и отрицательно заряженным атомом другой молекулы.
Механизм возникновения водородной связи – частично электростатический и частично донорно-акцепторный.
Характерной чертой водородной связи является расстояние между атомом водорода и другим атомом, её образующим. Оно должно быть меньше, чем сумма радиусов этих атомов.
Водородная связь подразделяется:
1. Межмолекулярная водородная связь образуется между молекулами веществ, в состав которых входят водород и сильно электроотрицательный элемент – фтор, кислород, азот, хлор, сера. Сильно смещенная общая электронная пара от водорода к атому отрицательно заряженного элемента, при этом положительный заряд водорода сконцентрирован в малом объеме, приводит взаимодействие протона с неподеленной электронной парой другого атома или иона, обобществляя её.
Водородную связь обозначают точками, указывая, что она намного слабее ковалентной связи (примерно в 15-20 раз).
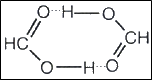
Межмолекулярная водородная связь: две молекулы воды и две молекулы уксусной кислоты с образованием циклической структуры
2. Внутримолекулярная водородная связь присутствует в многоатомных спиртах, углеводах, белках и других органических веществах.
Молекула салициловой кислоты.
Вещества с водородной связь имеют молекулярные кристаллические решетки, в узлах которой находятся молекулы.
Примеры: вода в виде льда, йод, хлор, бром, «сухой лёд» (твердый диоксид углерода), твёрдый аммиак, а также твёрдые органические вещества (метан, бензол, фенол, нафталин, белки и т.д.).
Физические свойства веществ с водородной связью.
Водородная связь обеспечивает низкомолекулярным веществам способность быть при обычных условиях в жидком агрегатном состоянии (этанол, метанол, вода) или сжижающимися газами (аммиак, фтороводород).
Более высокая температура кипения воды (100 о С) по сравнению с водородными соединениями элементов подгруппы кислорода (Н2S, Н2Sе, Н2Те), так как затрачивается дополнительная энергия на разрушение водородных связей.
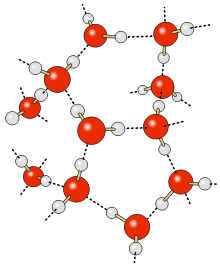
Также при плавлении воды её плотность возрастает. Это объясняется тем, что в структуре льда каждый атом кислорода связан через атомы водорода с четырьмя другими атомами кислорода других молекул воды. В результате образуется рыхлая «ажурная» структура.
Водородная связь
Межмолекулярные взаимодействия
Ориентационные силы притяжения возникают между полярными молекулами (диполь-диполь взаимодействие). Эти силы возникают между полярными молекулами. Индукционные взаимодействия — это взаимодействие между полярной молекулой и неполярной. Неполярная молекула поляризуется из-за действия полярной, что и порождает дополнительное электростатическое притяжение.
Особый вид межмолекулярного взаимодействия — водородные связи.
Водородные связи — это межмолекулярные (или внутримолекулярные) химические связи, возникающие между молекулами, в которых есть сильно полярные ковалентные связи — H-F, H-O или H-N. Если в молекуле есть такие связи, то между молекулами будут возникать дополнительные силы притяжения.
Механизм образования водородной связи частично электростатический, а частично — донорно–акцепторный. При этом донором электронной пары выступают атом сильно электроотрицательного элемента (F, O, N), а акцептором — атомы водорода, соединенные с этими атомами. Для водородной связи характерны направленность в пространстве и насыщаемость.
Водородные связи возникают между следующими веществами:
Водородная связь оказывает влияние на физические и химические свойства веществ. Так, дополнительное притяжение между молекулами затрудняет кипение веществ. У веществ с водородными связями наблюдается аномальное повышение тепературы кипения.
Химическая водородная связь: примеры
Водород простейший химический элемент во Вселенной. Его атом состоит всего из одного протона в ядре и одного электрона. Несмотря на свою физическую и химическую простоту, водород является основным элементом мироздания, благодаря ему горят и светятся звезды, наша планета покрыта водой, а сложнейшие органические соединения дали начало самому удивительному явлению во Вселенной жизни….
Особенности вещества
В природе встретить водород в составе других элементов таблицы Менделеева можно повсюду. Самым ярким примером такого соединения является такое вещество, как вода.
Водород имеет три изотопа:
Водородная связь характерна и присутствует в большинстве органических соединений. Соединяясь с хлором, водород образует хлорную кислоту, с кислородом воду, с азотом аммиак. Данные явления, обнаруженные в конце 19 века, были открыты русскими химиками М. Ильинским и Н. Бекетовым.
Ученые установили, что содержащая водород группа атомов чаще всего образует стабильные объединения с заряженным отрицательно атомом, который может входить в состав той или ной молекулы (не исключено, что даже в ту же самую). Данная дополнительная сцепка называется водородной связью.
Природа явления
Дадим определение водородной связи (в.с.). Это взаимодействие между отрицательно заряженными частицами молекул, реализованным атомом водорода.
Если чертой обозначить связь ковалентного типа, а тремя точками водородную, то символически можно отобразить в.с. между молекулами А и В таким образом: 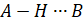
Природу данного межатомного явления понять довольно просто. Атом Н несет положительные заряды δ+, если он встречает на своем пути заряженный отрицательно и обладающий зарядом δ−, то вступает с ним в электростатический контакт.
Важно! Чаще всего в.с. заметно слабее по сравнению с ковалентными. Однако они намного крепче, чем стандартное молекулярное притяжение частиц, свойственное твердым и жидким телам.
Ковалентность
Несмотря на то, что в.с. может протекать в рамках двух частиц пары совершенно разных молекул, водородная химическая не является молекулярной связью. Свойство направления и насыщения одно из качеств в.с., которое делает ее очень похожей на ковалентную. Отметим, что во многих теориях, в.с. считается видом ковалентной связи и это совершенно никак не влияет на результаты, поэтому можно считать данное мнение корректным. Более того, сама природа в.с. очень близка к ковалентной.
Это можно легко продемонстрировать при помощи традиционных химических методов, рассчитывающих орбитали внутри молекул. В этом исчислении она будет представлять собой трехцентровые двухэлектронные связи. В очередной раз это доказывает, что отнесение ВС к разновидности ковалентной не несет ничего антинаучного.

Процесс образования
Каков способ образования. Образуются водородные связи между электроотрицательными атомами, один из которых имеет свободную электронную пару.
Самым убедительным признаком в.с. является дистанция между атомом Н и вторым атомом. Все дело в том, что дистанция между атомами меньше, чем сумма двух атомарных радиусов. Не смотря на часто встречающуюся асимметрию (когда в 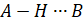
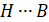
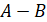
Да, асимметрия в в.с. встречается часто, однако существуют и симметричные конструкции, например HF. Угол между первым и вторым атомом в системе 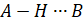
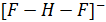
Соединение частиц через водород найдено в большом количестве различных соединений. Химическая связь часто возникает между фтором, азотом и кислородом, так как последние являются самыми электроотрицательными элементами. Редко обнаруживается между хлором, серой и прочими элементами, не являющимися металлами.
Важно! Азот и кислород основа жизни, эти элементы содержатся в особо высокой концентрации в углеводах, белках и нуклеиновой кислоте. Если бы между этими веществами не было прочного контакта через атом Н, жизнь на Земле была бы невозможна.
Межмолекулярная водородная связь разновидность образования крепкой структуры, связывающей через атом Н одну молекулу с другой. Ярким примером является муравьиная кислота. Она представляет собой молекулу, состоящую из двух или более простых молекул (димер).
Внутримолекулярная ВС разновидность, при которой атом Н является связующим звеном в рамках одной молекулы.
То же самое относится к фтороводороду, который находится в газообразном состоянии. Он содержит такие полимерные структуры, которые могут состоять из четырех простых молекул НF, объединенных друг с другом через водород.
Примеры водородной межмолекулярной конструкции искать не приходится: растворимость глюкозы, фруктозы, сахарозы в водном растворе объясняются именно при помощи водорода и его соединительным свойствам. Молекулярные структуры живых организмов (молекула ДНК, например) содержат миллионы сложных конструкций, связанных водородом.
Функция соединений
Насколько важна социальная роль данных связей. Рассмотрим несколько веществ, которые существуют благодаря водородному соединению. Мы будем сравнивать эти молекулы с водой. Чтобы наши размышления были честными, мы будем выбирать для сравнения исключительно неметаллы. Эти вещества называются халькогеноводородами.
Внимание! Если бы не было в.с., а кислород не обладал настолько цепкими качествами, при существующем климате на Земле не существовало бы воды в жидком состоянии. Такая высокая температура кипения непосредственное следствие водородной связи.
Сцепление атомов кислорода с водородом показано на следующем изображении.
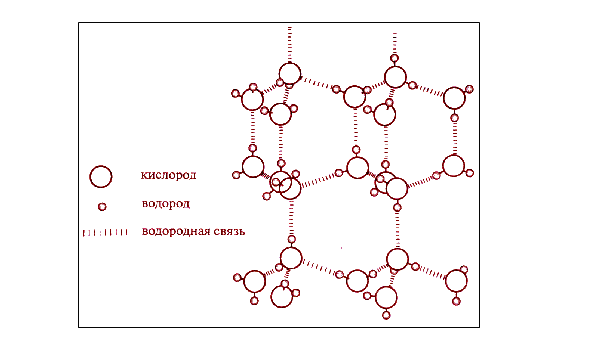
Но на этом удивительные свойства воды не заканчиваются. Следует также помнить о ее плавлении. И снова водородная связь именно из-за нее при плавлении плотность начинает расти. При таянии льда, каждое десятое водородное соединение разрушается, из-за чего молекулы воды приближаются друг к другу.
Типы и свойства водородной связи.
Водородная связь. Самоподготовка к ЕГЭ и ЦТ по химии
Вывод
Образования водородной связи влияют на кислотность веществ. К примеру, плавиковая кислота НF является достаточно слабой. При этом другие галогеноводородные кислоты довольно сильны. Причина этого в том, что Н соединен сразу с двумя атомами F, а это не дает им возможности отцепиться. Именно благодаря этому, НF- единственная кислота, образующая кислую соль NaHF2.
Водородная связь
Водородная связь — форма ассоциации между электроотрицательным атомом и атомом водорода H, связанным ковалентно с другим электроотрицательным атомом. В качестве электроотрицательных атомов могут выступать N, O или F. Водородные связи могут быть межмолекулярными или внутримолекулярными. [1]
Содержание
Природа
Часто водородную связь рассматривают как электростатическое взаимодействие, усиленное небольшим размером водорода, которое разрешает близость взаимодействующих диполей. Тогда об этом говорят как о разновидности донорно-акцепторной связи, невалентном взаимодействии между атомом водорода H, ковалентно связанным с атомом A группы A-H молекулы RA-H и электроотрицательным атомом B другой молекулы (или функциональной группы той же молекулы) BR’. Результатом таких взаимодействий являются комплексы RA-H•••BR’ различной степени стабильности, в которых атом водорода выступает в роли «моста», связывающего фрагменты RA и BR’.
История
Свойства
Энергия водородной связи значительно меньше энергии обычной ковалентной связи (не превышает 40 кДж/моль). Однако этой энергии достаточно, чтобы вызвать ассоциацию молекул, то есть их объединение в димеры или полимеры. Именно ассоциация молекул служит причиной аномально высоких температур плавления и кипения таких веществ, как фтороводород, вода, аммиак.
Связь этого типа, хотя и слабее ионной и ковалентной связей, тем не менее играет очень важную роль во внутри- и межмолекулярных взаимодействиях. Водородные связи во многом обусловливают физические свойства воды и многих органических жидкостей (спирты, карбоновые кислоты, амиды карбоновых кислот, сложные эфиры).
Прочность водородной связи (энтальпия образования комплекса) зависит от полярности комплекса и колеблется от
6 кДж/моль для комплексов молекул галогеноводородов с инертными газами до 160 кДж/моль для ион-молекулярных комплексов (AHB) ± ; так, для комплекса (H2O•H•OH2) + образованного H2O и H3O + — 132 кДж/моль в газовой фазе.
В воде
Механизм Гротгуса
Аномально высокая теплоёмкость воды, а также теплопроводность многоатомных спиртов обеспечивается многочисленными водородными связями. Одна молекула воды может образовать до четырёх классических водородных связей с соседями (с учётом бифуркатных Н-связей до 5-6).
Водородные связи повышают температуру кипения, вязкость и поверхностное натяжение жидкостей. Водородные связи ответственны за многие другие уникальные свойства воды.
Водные кластеры
Согласно современным представлениям, наличие водородных связей между молекулами воды приводит к возникновению так называемых водных кластеров или комплексов. Простейшим примером такого кластера может служить димер воды:
В нуклеиновых кислотах и белках
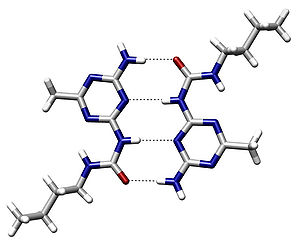
Водородная связь в значительной мере определяет свойства и таких биологически важных веществ, как белки и нуклеиновые кислоты. В частности, элементы вторичной структуры (например, α-спирали, β-складки) и третичной структуры в молекулах белков, РНК и ДНК стабилизированы водородными связями. В этих макромолекулах, водородные связи сцепляют части той же самой макромолекулы, заставляя её сворачиваться в определенную форму. Например, двойная спиральная структура ДНК, определяется в значительной степени наличием водородных связей, сцепляющих пары нуклеотидов, которые связывают одну комплементарную нить с другой.
В полимерах
Много полимеров усилены водородными связями в их главных цепях. Среди синтетических полимеров самый известный пример — нейлон, где водородные связи играют главную роль в кристаллизации материала. Водородные связи также важны в структуре полученных искусственно полимеров (например, целлюлозы) и в многих различных формах в природе, таких как древесина, хлопок и лён.
См. также
Примечания
Литература
Полезное
Смотреть что такое «Водородная связь» в других словарях:
ВОДОРОДНАЯ СВЯЗЬ — ВОДОРОДНАЯ СВЯЗЬ, ХИМИЧЕСКАЯ связь, образующаяся между некоторыми молекулами, содержащими водород. Атом водорода должен быть связан с электроотрицательным (отталкивающим электроны) атомом; связь возникает между положительным зарядом атома… … Научно-технический энциклопедический словарь
ВОДОРОДНАЯ СВЯЗЬ — тип связи, промежуточный между ковалентной химической связью и невалентным межат. вз ствием и осуществляющийся с участием атома водорода, расположенного либо между молекулами, либо между атомами внутри молекулы. Примером межмолекулярной В. с. явл … Физическая энциклопедия
ВОДОРОДНАЯ СВЯЗЬ — вид химической связи типа А Н. А ; образуется в результате взаимодействия атома водорода, связанного ковалентной связью с электроотрицательным атомом А (N, O, S и др.), и неподеленной парой электронов другого атома А (обычно O, N). Атомы А и А… … Большой Энциклопедический словарь
водородная связь — – особый вид трехцентровой химической связи X H. Y, в которой центральный атом водорода, соединенный ковалентной связью с электроотрицательным атомом X (C, N, O, S) образует дополнительную связь с атомом Y (N, O, S), имеющим направленную вдоль… … Химические термины
водородная связь — — [http://www.dunwoodypress.com/148/PDF/Biotech Eng Rus.pdf] Тематики биотехнологии EN hydrogen bond … Справочник технического переводчика
водородная связь — Термин водородная связь Термин на английском hydrogen bond Синонимы Аббревиатуры H bond Связанные термины клатрат, когезия, протеомика, супрамолекулярная химия, нанодиапазон, межмолекулярное взаимодействие Определение притяжение между ковалентно… … Энциклопедический словарь нанотехнологий
водородная связь — вид химической связи типа А Н. А ; образуется в результате взаимодействия атома водорода, связанного ковалентной связью с электроотрицательным атомом A (N, O, S и др.), и неподелённой парой электронов другого атома А (обычно О, N). Атомы А и А… … Энциклопедический словарь
Водородная связь — вид химического взаимодействия атомов в молекулах, отличающийся тем, что существенное участие в нём принимает атом водорода (Н), уже связанный ковалентной связью с другим атомом (А). Группа А Н выступает донором протона (акцептором… … Большая советская энциклопедия
ВОДОРОДНАЯ СВЯЗЬ — невалентное взаимод. между группой АН одной молекулы (RAH) и атомом В другой (BR ). В результате этого взаимод. образуется устойчивый комплекс RAH. BR с межмолекулярной B.C., в к ром атом водорода играет роль мостика, соединяющего фрагменты RA и … Химическая энциклопедия
водородная связь — hydrogen bond водородная связь. Cлабое электростатическое взаимодействие между атомами водорода, связанными с атомами кислорода либо азота; В.с. слабее ковалентной связи; В.с. играет важную роль в образовании структур высшего порядка у… … Молекулярная биология и генетика. Толковый словарь.
Между чем образуется водородная связь
Ключевые слова конспекта: Водородная химическая связь: меж- и внутримолекулярная. Значение водородной связи в природе и жизни человека.
Молекулы электронейтральны, однако и между ними могут возникнуть силы взаимного притяжения, получившие название вандервальсова взаимодействия в честь голландского учёного, лауреата Нобелевской премии Йоханнеса Дидерика Ван-дер-Ваальса. Причиной такого притяжения является электромагнитное взаимодействие электронов и ядер одной молекулы с электронами и ядрами другой. Межмолекулярные связи значительно менее прочные, чем химические. Однако именно они приводят к тому, что вещества молекулярного строения могут существовать в конденсированном, т. е. жидком или твёрдом, состоянии.
Силы Ван-дер-Ваальса — предмет изучения физики. Однако к межмолекулярному взаимодействию относят и водородную связь, которая имеет большое значение в химии и биологии.
Энергия водородной связи составляет всего лишь 4—40 кДж/моль, т. е. соответствует энергетической характеристике межмолекулярных сил. Поэтому её можно рассматривать как частный случай вандерваальсовых сил взаимодействия. Несмотря на низкие энергетические характеристики, а может быть именно благодаря им, водородная связь — основа организации и функционирования живой материи на нашей планете.
| Водородная связь образуется между атомом водорода, связанным ковалентной связью с электроотрицательным атомом одной молекулы и атомами фтора, кислорода, азота другой молекулы, имеющими неподелённые электронные пары. |
Это определение справедливо для межмолекулярной водородной связи.
В молекуле воды — два атома водорода и две неподелённые электронные пары. Следовательно, каждая молекула способна к образованию не одной, а четырёх водородных связей. Образуется своеобразный пространственный каркас, скрепляющий между собой множество молекул воды.
Водородная связь может возникать между атомами водорода и атомами неметаллов с высокой электроотрицательностью (фтора, кислорода, азота), обладающих неподелёнными парами электронов.
Водородная связь примерно в 10 раз слабее, чем ковалентная полярная, однако она сцепляет молекулы воды друг с другом. В результате вода приобретает аномальные свойства, которые позволяют считать её самым удивительным веществом на Земле.
Например, для того чтобы оторвать одну молекулу воды от другой, требуется затратить некоторое количество энергии. Если бы водородных связей не было, вода закипала бы при температуре –80 °С, а замерзала бы при –100 °С. В таком случае наша Земля превратилась бы в безжизненную пустыню: все реки, моря и океаны выкипели бы, а на небе не было бы ни облачка, ни тучки.
Плотность воды тоже аномальна. В твёрдом агрегатном состоянии (лёд) молекулы воды «упакованы» так, что между ними остаётся много «пустого места». Поэтому плотность льда меньше, чем плотность воды, и лёд плавает на её поверхности. Благодаря этому аномальному свойству даже при самых сильных морозах температура воды на глубине подо льдом не опускается ниже +4 °С. Именно при такой температуре плотность воды самая большая, а потому лёд легче воды и в ней не тонет. Это позволяет глубоким водоёмам не промерзать зимой до дна, что спасает жизнь водным обитателям.
Удивительная красота и многообразие снежинок — также результат работы водородных связей.
Благодаря водородным связям вещества с низкими относительными молекулярными массами ассоциированы в жидкости, например, первые члены гомологических рядов предельных одноатомных спиртов и карбоновых кислот. Эти вещества, как и некоторые многоатомные спирты (этиленгликоль, глицерин), благодаря водородным связям неограниченно растворимы в воде:
Водородная связь способствует лёгкому переходу некоторых веществ (например, аммиака, фтороводорода) из газообразного состояния в жидкое и обратно:
Это свойство аммиака позволяет использовать его в качестве хладагента в промышленных холодильных установках.
Рассмотрим ещё одну разновидность водородной связи, которая играет большую роль в организации структур таких важнейших биополимеров, как белки и нуклеиновые кислоты. Так как эта связь возникает внутри полимерных молекул, она называется внутримолекулярная водородная связь. Именно эта связь определяет вторичную структуру белка и двойную спираль ДНК.
Разрушение вторичной структуры белка приводит к его денатурации.
Каждая половинка двойной спирали представляет собой полимер, построенный из четырёх видов нуклеотидов, — полинуклеотид. Строгий порядок расположения остатков нуклеотидов одной цепи ДНК напротив нуклеотидов другой формируется именно за счёт водородных связей по принципу комплементарности: между остатками аденинового (А) и тиминового (Т) нуклеотидов — две водородные связи, между цитозиновым (Ц) и гуаниновым (Г) — три водородные связи.
Водородные связи играют важную роль в процессе передачи наследственной информации. При самоудвоении ДНК водородные связи материнской молекулы разрываются и синтезируются две новые цепи полинуклеотидов, в соответствии с принципом комлементарности. В итоге возникают две новые молекулы ДНК, в каждой из которых одна цепь была взята из материнской ДНК, а вторая, комплементарная ей, была выстроена заново.
Водородные связи — основа соблюдения строгой программы синтеза мРНК и затем соответствующего белка. Следовательно, без водородных связей невозможно было бы существование белковых организмов на нашей планете.
За открытие структуры двойной спирали дезоксирибонуклеиновой кислоты (ДНК) американские биологи Джеймс Уотсон и Фрэнсис Крик были удостоены Нобелевской премии.
Конспект урока по химии «Водородная химическая связь». В учебных целях использованы цитаты из пособия «Химия. 11 класс : учеб, для общеобразоват. организаций : базовый уровень / О. С. Габриелян, И. Г. Остроумов, С. А. Сладков. — М. : Просвещение». Выберите дальнейшее действие: