Миастенический криз что это
Миастенический криз что это
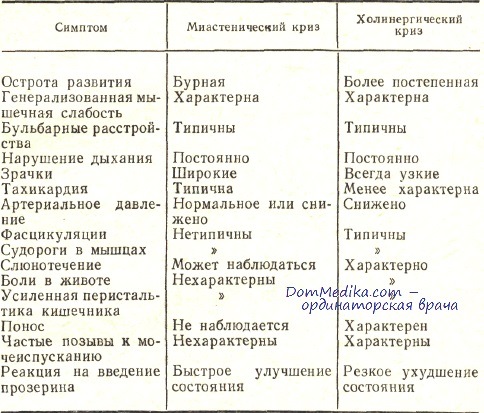
Наиболее опасным, угрожающим жизни состоянием при миастении являются кризы — миастенический и холинергический.
Миастенический криз при миастении обычно связан с ухудшением нервно-мышечной передачи. Это может быть обусловлено изменением функционального состояния синаптического аппарата под влиянием разных факторов: недомогания, лихорадочного состояния, менструации, переутомления и т. д. или уменьшения по той или иной причине дозы АХЭП. Основная опасность — ухудшение бульбарных функций, вплоть до афагии, а также слабость дыхательной мускулатуры с нарастанием дыхательной недостаточности. На догоспитальном этапе необходимо немедленное подкожное или даже внутривенное введение 0,05 % раствора прозерина; через 30 мин прозерин вводится повторно подкожно; обязательно внутривенное введение метилпреднизолона — до 1,5—2 г или преднизолона 1,5-2 мг/кг.
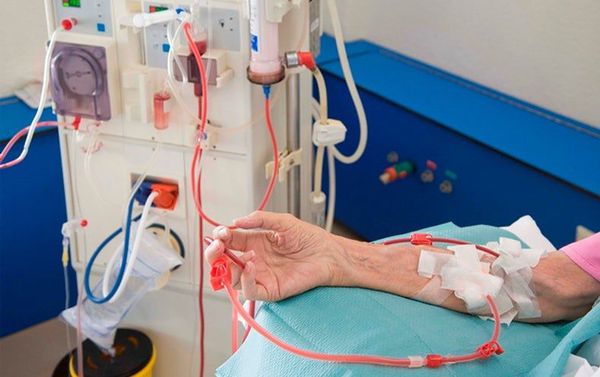
Больные с осложнениями миастении госпитализируются в центры нервно-мышечной патологии или реанимационные, нейрореанимационные отделения, либо отделения интенсивной терапии, где обычно им проводится плазмаферез, а при необходимости и возможности (препарат очень дорог!) — внутривенно вводится иммуноглобулин G — 0,4 мг/кг, по показаниям применяется ИВЛ.
Холинергический криз при миастении связан с передозировкой антихолинэстеразных препаратов, в результате чего возникают симптомы мускари-новой и никотиновой интоксикации: фасцикуляции мышц, птоз, гиперсекреция слюны, потливость, бледность, брадикардия, боли в животе, понос. АХЭП немедленно временно отменяются. В угрожающей ситуации внутривенно медленно вводится 0,5—1,0 мл 0,1 % раствора атропина. Больные доставляются в указанные выше отделения, где им по показаниям назначается ИВЛ, проводится плазмаферез.
Миастения
Симптомы
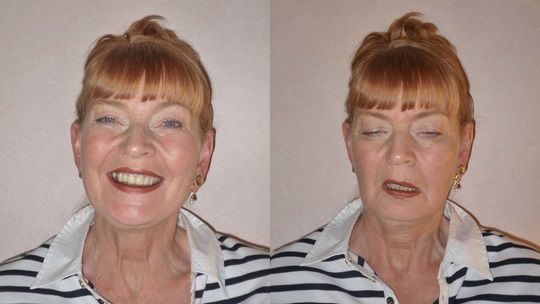
Мышечная слабость вызванная миастенией увеличивается в больных мышцах при повторных нагрузках на эти мышцы. Так как симптомы обычно уменьшаются после отдыха, мышечная слабость может появляться и исчезать. Симптомы миастении прогрессируют с течением времени и, как правило, наибольшего пика достигают через несколько лет после дебюта заболевания. Несмотря на то, что миастения может поразить любые из поперечно-полосатых мышц, определенные группы мышц вовлекаются в процесс чаще, чем другие.
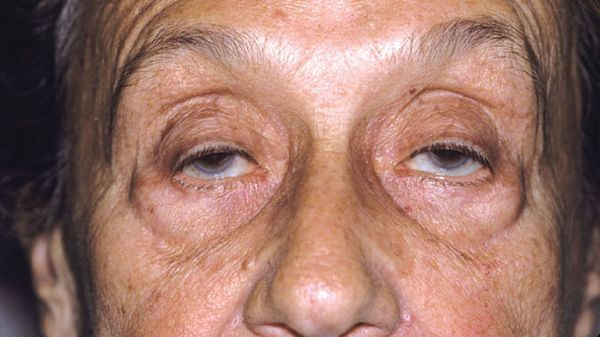
Глазные мышцы
У более чем половины пациентов, у которых развилась миастения, первые симптомы связаны со зрением:
Примерно у 15 процентов пациентов с миастенией, первые симптомы затрагивают мышцы лица, и гортани что будет проявляться:
Мышцы конечностей и шеи
Причины
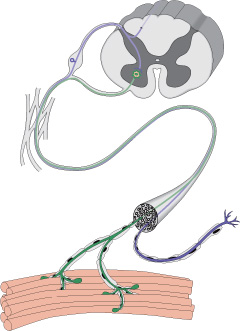
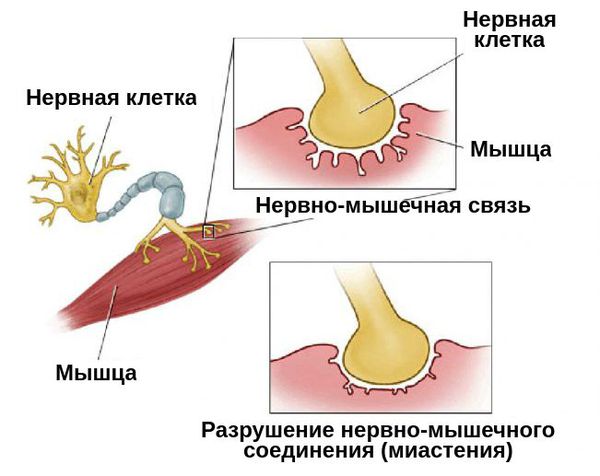
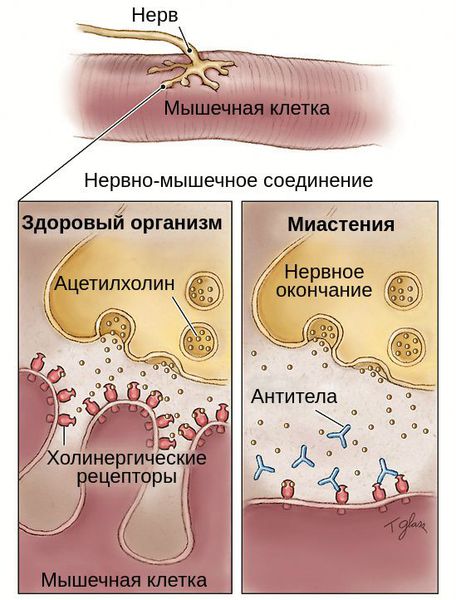
Нервы передают импульсы мышцам с помощью выброса химических веществ, называемых нейротрансмиттерами, которые попадают точно в рецепторы на мышечных клетках. При миастении, иммунная система вырабатывает антитела, которые блокируют или уничтожают много мышечных рецепторов нейротрансмиттера ацетилхолина. С уменьшением количества действующих рецепторов, мышцы получают меньше нервных сигналов, в результате это приводит к мышечной слабости.
Факторы, которые могут ухудшить течение миастении
Осложнения
Осложнения миастения обычно поддаются лечению, но некоторые из них могут быть опасны для жизни.
Миастенический криз
Миастенический криз является угрожающим жизни состоянием, которое возникает, когда мышцы, которые контролируют дыхание, становятся слишком слабыми для выполнения своих функций. В таких случаях требуется неотложная помощь для обеспечения дыхания и с использованием аппаратного дыхания. Медикаментозное лечение и фильтрация крови помогают пациентов выйти из миастенического криза и тогда они могут дышать самостоятельно
Опухоли тимуса
У приблизительно 15 процентов пациентов с миастенией отмечается наличие опухоли в вилочковой железы. Большинство этих опухолей доброкачественные.
Другие нарушения
У пациентов с наличием миастении, также нередко встречаются следующие проблемы:
Диагностика
Прежде всего, при подозрение на миастению пациента направляют на консультацию невролога. Врача-невролога могут интересовать подробное описание симптомов, наличие в анамнезе приема лекарств (дозировок), связь симптомов с физическими нагрузками. Врач-невролог проведет изучение неврологического статуса (рефлекторную активность, мышечную силу, мышечный тонус, координацию, зрение и осязание).
Основным признаком того, что указывает на возможность миастении, является слабость мышц, которая регрессирует после отдыха. Тесты, которые могут помочь подтвердить диагноз могут включать:
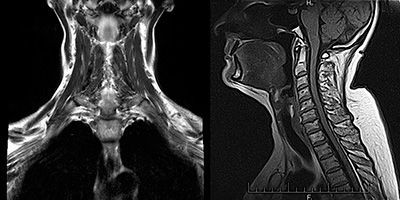
КТ или МРТ может быть назначено для исключения опухоли вилочковой железы.
Лечение
Врачи используют различные методы лечения, по отдельности или в комбинации, чтобы уменьшить симптомы миастении.
Лекарственные препараты
Хирургическое лечение
У 15 процентов людей, у которых есть миастения, также отмечается наличие опухоли в вилочковой железе. В таких случаях рекомендуется оперативное лечение и удаление опухоли.
Для пациентов с миастенией, у которых нет опухоли в вилочковой железе, удаление железы является достаточно спорным методом лечения.
Хирургическое вмешательство не рекомендуется большинством врачей, если:
Образ жизни
Использование материалов допускается при указании активной гиперссылки на постоянную страницу статьи.
Кризы при миастении
Кризы при миастении – это состояния острой декомпенсации патологии в виде пароксизмального нарушения витальных функций. Резкое усиление мышечной слабости сопровождается угнетением дыхания, бульбарными, сердечно-сосудистыми расстройствами. Чаще всего кризы сочетают в себе признаки миастенического и холинергического вариантов, что придает им более тяжелое течение. В диагностике используют клинические, лабораторные методы, электронейромиографию, КТ и МРТ органов грудной клетки. Неотложные состояния требуют ИВЛ, медикаментозной терапии, экстракорпоральной детоксикации, решения вопроса о хирургической коррекции.
МКБ-10
Общие сведения
Кризы при миастении достаточно редки – в общей популяции регистрируется 50–400 случаев на 1 млн. населения. На протяжении жизни их испытывают 10–45% пациентов с мышечной слабостью, особенно в первые два года болезни. Ежегодный риск возникновения кризов находится в пределах 2–3%. Декомпенсация миастении может наступить в любом возрасте, но значительно чаще встречается среди людей 18–40 лет. В гендерной структуре пароксизмальных состояний практически пятикратное преимущество принадлежит женщинам репродуктивного периода. В пожилом возрасте существенно возрастает показатель распространенности среди мужчин, выравнивая соотношение с женщинами.
Причины кризов
Осложненное течение характерно для приобретенной генерализованной миастении или локальных форм, за исключением глазной. Хотя некоторые авторы указывают на роль наследственной предрасположенности, но врожденные варианты болезни крайне редко сопровождаются кризами. Возникновение тяжелой декомпенсации связано с рядом внешних и внутренних факторов. Значимыми триггерами выступают следующие состояния:
Вероятность тяжелого пароксизмального течения увеличивается у пожилых людей с сопутствующей соматической патологией (гипертонической, ишемической болезнью), при травмах. Провоцирующим фактором могут стать тяжелые стрессовые ситуации, интенсивные физические нагрузки, перегревание. В группу риска попадают лица в возрасте до 18 и старше 60 лет, с ранней генерализацией миастении, длительно принимавшие антихолинэстеразные препараты. Более половины кризов ассоциируют с неправильным ведением пациентов, но в трети случаев явную причину определить не удается.
Патогенез
Основой патогенеза кризов при миастении является массивная аутоиммунная агрессия против структур мионеврального синапса. Патологический процесс сопровождается образованием антител к ацетилхолиновым рецепторам, белкам постсинаптической мембраны (MuSK, LRP4), что приводит к комплемент-связанной деструкции и резкому уменьшению их количества. В результате не происходит генерации потенциала действия на постсинаптической мембране, что проявляется курареподобным блоком нервно-мышечной проводимости.
Особый механизм развития присущ холинергическому кризу. Генез моторных и вегетативных расстройств связан с гиперполяризацией постсинаптических мембран, вызванной чрезмерным количеством ацетилхолина. Как результат, снижается чувствительность незатронутых аутоиммунным процессом никотиновых и мускариновых рецепторов. Во всех случаях появление криза обусловлено передозировкой антихолинэстеразных препаратов. Кроме мышечной слабости, он характеризуется комплексом холинергических эффектов.
Дыхательные расстройства во время кризов обусловлены феноменом генерализации мышечного утомления, распространяющегося на области, испытывающие функциональную нагрузку. Респираторные расстройства при осложненном течении патологии связаны со слабостью скелетной мускулатуры: диафрагмы, межреберий, брюшного пресса. Не последнюю роль в этом процессе играют нарушение функции надгортанника, накопление слизи в дыхательных путях при недостаточности кашлевого толчка.
Классификация
Согласно классификации миастении по степени тяжести, кризы относят к V классу, когда дыхательные и бульбарные нарушения достигают такого уровня, что без искусственной вентиляции легких и зондового питания не обойтись. Разделение же самих пароксизмов достаточно условно, поскольку один быстро переходит в другой. В практической неврологии выделяют следующие кризы:
Существует три типа дыхательных расстройств при декомпенсированной миастении – скелетно-мышечный, бульбарный, смешанный. Первый характеризуется поражением мышц грудной клетки и диафрагмы. Бульбарный вариант предполагает парез надгортанника и западение языка с развитием асфиксии. У большинства пациентов оба типа развиваются одновременно.
Симптомы кризов при миастении
Декомпенсация болезни возникает внезапно (за 12–48 часов), сопровождается резким ухудшением жизненно важных функций из-за прогрессирующей мышечной слабости. Иногда наблюдается подострое развитие, когда симптомы нарастают в течение 3–14 дней. У пятой части пациентов кризы являются первым проявлением миастении, что обычно наблюдается при ее поздней манифестации. Склонность к повторному развитию пароксизмов свидетельствует о крайне тяжелом течении основного заболевания.
Миастенический и холинергический кризы имеют ряд общих признаков, к которым относят нарастающую слабость скелетной и бульбарной мускулатуры, глазодвигательные нарушения, гипомимию. Наиболее грозный симптом – дыхательные нарушения, представляющие прямую угрозу жизни пациента. Оба варианта характеризуются психомоторным возбуждением с беспокойством, страхом, спутанностью сознания, обусловленными нарастающей гипоксией головного мозга.
Миастенический криз
Помимо описанных симптомов, миастенический криз сопровождается вегетативной дисфункцией – гипергидрозом, гиперсаливацией, бледностью и цианозом кожных покровов. Он развивается постепенно, так как необходимо время на вовлечение вспомогательной мускулатуры. Пациент принимает вынужденную позу – полусидя, держась за спинку кровати для фиксации плечевого пояса. При генерализованном приступе усиливаются общая слабость, птоз, ограничивается подвижность глазных яблок. Бульбарные нарушения сочетаются с расстройствами дыхания и деятельности сердца.
Одним из вариантов проявления парциального кардиального миастенического криза становятся приступы, схожие со стенокардическими: пациент ощущает дискомфорт в области сердца, перебои в его работе. Объективно выявляют гипотонию, тахикардию. Пароксизм обычно возникает в ночное время, проходит после приема антихолинэстеразных препаратов. Парциальные дыхательные кризы развиваются по бульбарному или спинальному типу с нарастанием слабости в соответствующих группах мышц.
Холинергический криз
Характеризуется парадоксальным снижением мышечной силы в ответ на введение антихолинэстеразных средств. В клинической картине присутствуют отчетливо выраженные мускариновый и никотиновый эффекты. Первый проявляется усилением секреции слюны и бронхиальной слизи, повышенной потливостью, сужением зрачков. Возникают абдоминальные боли, диспепсические явления (тошнота, рвота, понос), брадикардия. Активация никотиновых рецепторов сопровождается мышечными фасцикуляциями, судорогами.
Смешанный криз
Учитывая быструю трансформацию кризов при миастении, их разграничение затруднено, поэтому чаще констатируют смешанный вариант. Он сопровождается несостоятельностью бульбарных и дыхательных мышц при незначительном снижении силы в конечностях. Сопутствующие нарушения туловищной локализации остаются чувствительны к анитихолинэстеразным препаратам. Но в сочетании с холинергическими симптомами такой криз представляет существенную опасность для пациента.
Осложнения
Кризы угрожают остановкой дыхания и сердечно-сосудистой недостаточностью, повышающими летальность при миастении вдвое. У трети пациентов пароксизмы имеют тенденцию к рецидивированию. При миастеническом кризе возрастает риск экстубационной дыхательной недостаточности, частота которой составляет 27%. Поражение бульбарных мышц ведет к развитию аспирационных состояний (пневмонии, синдрома Мендельсона).
Распространенными осложнениями кризов являются различные инфекции – бронхолегочные, мочевыводящих путей, колит, сепсис. В состоянии декомпенсации пациенты подвергаются повышенному риску сосудистых осложнений, включая тромбоз глубоких вен, острый инфаркт миокарда, аритмии. Существует несколько сообщений о возникновении у пациентов стресс-индуцированной кардиомиопатии (синдрома такоцубо).
Диагностика
Важной задачей для врача-невролога является ранняя диагностика дыхательных нарушений с выявлением риска кризового течения миастении. Тяжесть процесса устанавливается по международной классификации, шкале мышечной силы. Клиническими критериями являются прогрессирующая мышечная слабость, дисфагия, респираторный дистресс (одышка, тахипноэ, вовлечение вспомогательных мышц). Для выявления факторов декомпенсации применяются методы лабораторного и инструментального контроля:
Дифференцировать кризы при миастении необходимо с другими тяжелыми состояниями, сопровождающимися респираторными расстройствами. В списке вероятных заболеваний могут присутствовать синдром Ламберта-Итона, ботулизм, полиомиелит. Необходимо учитывать врожденные миастенические состояния, острые нарушения мозгового кровообращения, синдром Гийена-Барре и прочие нарушения со схожей симптоматикой.
Лечение кризов при миастении
Консервативное лечение
Резкая декомпенсация мышечной слабости – это жизнеугрожающее состояние, требующее оказания ургентной помощи. Все пациенты поступают в отделение реанимации и интенсивной терапии, где проводится восстановление дыхания и сердечной деятельности. В терапии кризов практикуется последовательный междисциплинарный подход, включающий общие и патогенетические (специфические) мероприятия консервативной коррекции.
Купирование дыхательной недостаточности проводится путем санации ротоглотки и трахеобронхиального дерева, интубации трахеи, перевода пациента на ИВЛ. Объем респираторной поддержки определяется тяжестью нарушений. Одновременно отменяют препараты антихолинэстеразного ряда и другие, усугубляющие проведение нервных импульсов. К мероприятиям общего характера относят выявление и устранение инфекционных осложнений, профилактику тромбозов. Специфическое лечение при кризах включает:
В комплексной терапии используются различные средства симптоматической и вспомогательной коррекции, действие которых направлено на усиление выработки ацетилхолина, улучшение мышечной функции, подавление побочных эффектов патогенетического лечения. Используются метаболические средства (метионин, глутаминовая кислота, витамины), препараты кальция, адаптогены. Профилактику кортикостероид-ассоциированного остеопороза осуществляют ретаболилом, фторидом натрия.
Хирургическое лечение
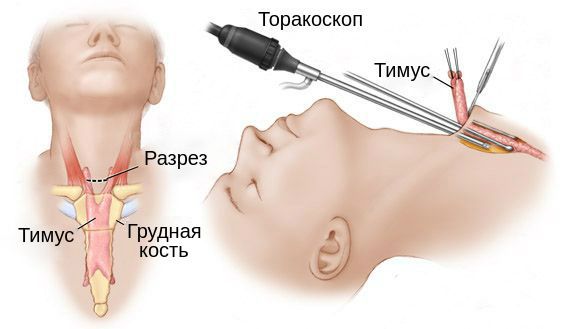
Своевременное удаление тимуса (тимэктомия) оказывает превентивный эффект – уменьшает частоту и тяжесть кризов при миастении, особенно при ранней декомпенсации. В послеоперационном периоде у 6–22% пациентов отмечаются рецидивы тяжелых пароксизмов, но риск отрицательных последствий снижается при использовании малоинвазивных техник: цервикотомии, частичной стернотомии, торакоскопии под видеоконтролем. Пациенты с тяжелыми бульбарными расстройствами нуждаются в трахеостомии.
Экспериментальное лечение
Для лечения кризов при миастении предлагают использовать другие иммуносупрессивные препараты – азатиоприн, мофетила микофенолат, циклоспорин. Их рассматривают в качестве альтернативы кортикостероидам при наличии противопоказаний или неадекватного терапевтического ответа. Но в силу отсроченного действия эти препараты обладают ограниченным применением. При злокачественном течении болезни отмечена эффективность моноклональных антител (ритуксимаба).
Прогноз и профилактика
Как распознать миастению? Все о диагностике и лечении
Миастения – это болезнь, которая характеризуется нарушением нервно-мышечной передачи (то есть нарушением процесса сокращения мышцы, возникающим в ответ на импульс, идущий по нервному волокну). Причиной миастении зачастую является аутоиммунный процесс, в результате которого в организме вырабатываются антитела к структурам нервно-мышечного синапса. Согласно статистике, миастения встречается у каждого 5-го из 100 тысяч человек. Это хроническое заболевание с острым или постепенным началом. Основным проявлением является преходящая мышечная слабость, так же может возникать птоз (опущение) верхних век, нарушение глотания, «гнусавость» голоса. В тяжелых случаях и при прогрессировании заболевания может возникнуть слабость дыхательных мышц, вплоть до остановки дыхания.
Опасный недуг быстро прогрессирует, клинические проявления могут утихать и вновь обостряться. Диагностируют патологическую мышечную утомляемость чаще у женщин, чем у мужчин, много реже у детей. Средний возраст пациентов от 15 до 45 лет, таким образом, максимальное количество случаев регистрируется у самой активной части населения.
О причинах
В настоящее время причины развития миастении изучены не до конца. Иногда нельзя однозначно сказать, почему у того или иного пациента возникло заболевание. Принято считать, что весомую роль играют следующие факторы:
При появлении злокачественных новообразований в яичниках, в органах дыхания или в молочных железах говорят о миастеническом синдроме Ламберта-Итона. Мышечная слабость, иногда принимаемая за миастению, возникает при болезни Шарко-Мари, при дерматомиозите (разрушении соединительной ткани), различных формах миопатий, синдроме БАС (боковой амиотрофический склероз) и многих других патологиях.
Сложность диагностики состоит в том, что у пациентов с миастенией в начале заболевания может не быть каких-либо четких жалоб и симптоматики. При нейровизуализации (КТ или МРТ) нет значимых отклонений в структурах центральной нервной системы. Только у 30% заболевших тимус увеличивается, либо в нем выявляются новообразования. Мышцы при осмотре так же никак не изменены, патология может выявляться только при микроскопическом исследовании.
Классификация
Врожденная миастения может быть обусловлена генетическими мутациями. Так же плод может получить антитела к рецепторам постсинаптической мембраны от матери, в этом случае речь идет о неонатальной миастении.
Приобретенная миастения может развиться у пациентов любого возраста. Данный диагноз ставят подросткам, молодым людям и пенсионерам. Наиболее часто недуг встречается в активном возрасте, от 20 до 30 лет. Причины могут быть внешними (инфекционные агенты) и внутренними (хронические заболевания, наследственность).
Условно, по распространенности мышечной слабости, миастения подразделяется на следующие виды:
Данное деление относительно, так как при углубленном исследовании чаще всего выявляется поражение всех мышц, но клинические проявления миастении могут возникать только в отдельных группах мышц определенной локализации.
По характеру течения различают:
Симптомы
Клинические проявления миастении зависят от формы заболевания.
Симптомы, характерные для генерализованной формы:
Симптомы, характерные для глазной формы:
Сложность диагностики миастении связана с тем, что вышеперечисленные симптомы могут появляться и пропадать. Наиболее выражено они проявляются, когда человек занимается спортом, длительно читает или работает за компьютером. То есть в те моменты, когда поперечнополосатые мышцы задействованы больше всего. Ведь даже поддержание определенной позы или чтение требуют постоянного напряжения определенных групп мышц.
При отсутствии адекватного лечения существует риск не только инвалидизации, но и смерти. В то время, когда уровень развития медицины не позволял проводить длительную искусственную вентиляцию легких, от миастении умирали 8 из 10 заболевших. При обнаружении тревожных симптомов миастении, необходимо записаться на прием к неврологу. При необходимости специалист направит на обследование и подберет эффективную терапию.
Диагностика
Врач-невролог ставит диагноз миастения на основе жалоб, данных анамнеза, осмотра и исследований. Специалист сравнивает жалобы пациента с симптомами, характерными для этой болезни. Для подтверждения диагноза проводят диагностические исследования.
Электронейромиография при миастении является «золотым стандартом» и обязательным исследованием. Используется специальный режим ЭНМГ – «декремент-тест». При проведении обследования с помощью электрической стимуляции исследуемую мышцу заставляют сокращаться с высокой частотой. В результате при миастении или миастеническом синдроме регистрируется уменьшение интенсивности мышечного сокращения.
Прозериновая проба. Выполняется самостоятельно или после проведения декремент-теста. Прозерин — вещество, улучшающее нервно-мышечную передачу. Подкожно вводится небольшое его количество, через 30 минут после этого пациент вновь осматривается врачом или проводится повторная ЭНМГ. Проба считается положительной, если отмечается клиническое улучшение или позитивная динамика при выполнении декремент-теста.
Лабораторная диагностика. Анализ крови на содержание специфических антител к рецепторам, мышцам. Антитела выявляются далеко не во всех случаях миастении.
Как правило, этих методов в сочетании с консультацией невролога бывает достаточно для установления диагноза.
Во время осмотра врач может провести пробы на повышенную мышечную утомляемость. Сначала на определенную группу мышц дается нагрузка, затем оценивается их состояние. При глазной форме миастении нагружают глазодвигательные мышцы, для этого больного просят в течение 30 секунд смотреть в одну точку. При жалобах на патологическую усталость мышц шеи, пациента укладывают на спину и просят держать голову поднятой в течение 1 минуты. При слабости в ногах, больному нужно сделать несколько приседаний либо походить на носочках. Для определения степени утомляемости мышц кисти и предплечья, человека просят несколько раз интенсивно согнуть и разогнуть кисть.
Что такое миастения? Причины возникновения, диагностику и методы лечения разберем в статье доктора Попович Анны Мироновны, невролога со стажем в 33 года.
Определение болезни. Причины заболевания
Считается, что эта болезнь впервые была описана британским учёным-медиком Томасом Уиллисом в 1672 году, а первое доказательство её аутоиммунной природы появилось спустя более 200 лет.
Миастения — это хроническое аутоиммунное заболевание с прогрессирующим течением. Оно связано с разрушением рецепторов, которые участвуют в передаче нервных импульсов. При миастении эти рецепторы атакуются антителами, в результате чего нервно-мышечная передача нарушается.
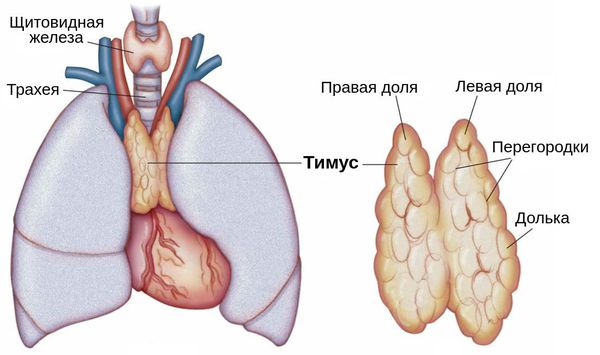
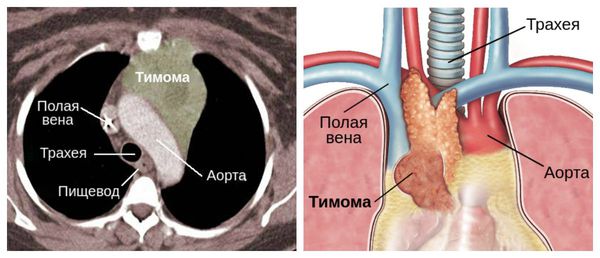
Также причиной миастении может стать патология тимуса (вилочковой железы) — главного органа иммунной системы. В частности её развитие может быть связано с тимомой — группой опухолей вилочковой железы. В 30 % случаях он и являются злокачественными.
Провоцирующими факторами развития миастении являются:
Симптомы миастении
В целом симптомы миастении яркие и многообразные. Они зависят от формы патологии:
Патогенез миастении
Патогенез миастении до конца не выяснен. Но известно, что в развитии патологической утомляемости мышц главную роль играют аутоантитела. Они блокируют постсинаптические холинергические рецепторы нервно-мышечных соединений. В результате этой блокады развиваются структурные изменения и часть рецепторов гибнет.
Также на развитие миастении влияет вилочковая железа. При нарушении её функции в организме начинают синтезироваться антитела к холинергическим рецепторам, что в дальнейшем ведёт к развитию миастении.
Имеются данные о возможной роли персистирующей (постоянной хронической) инфекции вилочковой железы. Например, при миастении выявлено повышение титра комплемент-связывающих антител к цитомегаловирусу. У больных, которым проводилось лечение стероидами или тимэктомия (операция по удалению вилочковой железы), этот признак отсутствовал.
Классификация и стадии развития миастении
Миастения делится на генерализованные и локальные формы.
К локальным формам относятся :
К генерализованным формам относятся:
Последнюю форму генерализованной миастении можно разделить по стадиям:
Также миастению можно разделить по характеру течения. Выделяют:
Осложнения миастении
К наиболее значимым осложнениям миастении относятся холинергический и миастенический криз.
Чаще всего причинами возникновения миастенического криза становятся:
Отдельно стоит сказать о тимоме, при которой риск миастенического криза увеличивается в два раза.
Также существует ряд лекарственных препаратов, провоцирующих развитие осложнений миастении. К ним относятся:
Особенное внимание при подозрении на миастению следует уделять жалобам ребёнка, так как он не всегда может правильно сформулировать их. Это приводит к поздней диагностике заболевания и нарушению дыхания.
Диагностика миастении
При сборе анамнеза (истории болезни) следует обращать внимание:
При физикальном обследовании необходимо обращать внимание на птоз век, бульбарные расстройства (проблемы, связанные с глотанием пищи) и быструю мышечную утомляемость во время и после физической нагрузки.
Так как в большинстве случаев патогенез миастении связан с выработкой антител к холинергическим рецепторам, для подтверждения клинического диагноза достаточно выполнить иммунологический тест — анализ крови на наличие антител. В случае отрицательного результата могут потребоваться дополнительные методы диагностики.
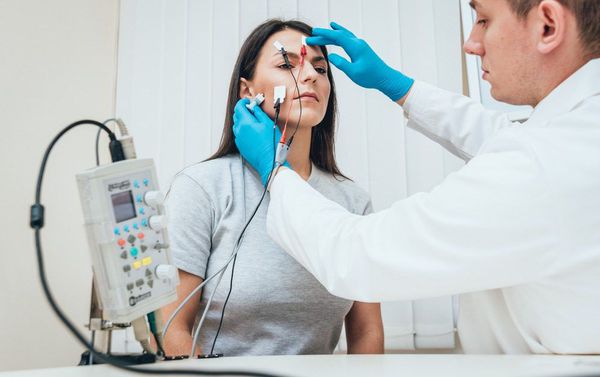
Наиболее современным и решающим методом диагностики при подозрении на миастению является электронейромиография (ЭНМГ) с проведением декремент-теста (исследования нервно-мышечной передачи). Для выполнения теста на области поражённых мышц фиксируются специальные электроды, через которые к мышцам ритмично поступают электрические импульсы. Получаемые мышечные ответы отображаются на нейромиографе в виде графика амплитуд.
Заподозрить миастению позволяет постепенное снижение амплитуд мышечной реакции более чем на 10 % от изначального мышечного ответа. Чтобы убедиться в диагнозе, после текста пациенту подкожно вводят прозерин 0,05 % и снова выполняют тестирование. В случае миастении данный препарат временно устранит нарушение нервно-мышечной передачи, тем самым увеличит амплитуду мышечных ответов.
Дифференциальная диагностика
Миастению необходимо отличать от следующих заболеваний:
Миастенические синдромы также возникают при:
Особое внимание следует уделять дифференциальной диагностике между холинергическим и миастеническим кризом. Первый тип криза встречается всего лишь у 3 % больных и начинается медленнее, чем миастенический криз. Он всегда связан с передозировкой антихолинэстеразными препаратами. В течение суток или более у пациента нарастает слабость и утомляемость, он не выдерживает прежнего интервала между приёмами данных средств, мышечная сила в ответ на стандартную или увеличенную дозу препарата снижается даже без предшествующей физической нагрузки.
Важное диагностическое значение при определении типа криза имеет прозериновая проба : пациенту подкожно вводят 2 мл 0,05 % прозерина. В течение 30 минут после введения препарата при холинергическом кризе отмечается уменьшение мышечной слабости, тогда как при миастеническом кризе мышечная сила увеличивается.
Лечение миастении
Методы лечения миастении делятся на две группы:
К средствам медикаментозного лечения относятся: антихолинэстеразные препараты, анаболические стероиды, АКТГ (адренокортикотропный гормон) и кортикостероиды. Как правило, применяется только один препарат, так как использование нескольких средств чревато холинергическим кризом.
Для лечения миастении также применяется внутривенное ведение иммуноглобулинов G 5 % и 10 %. Они быстро, но временно улучшают течение заболевания. Так как использование высоких доз человеческих иммуноглобулинов способно подавлять иммунные процессы, иммуноглобулины G позволяют снижать выработку антител к холинергическим рецепторам.
Прогноз. Профилактика
Миастения является достаточно тяжёлым заболеванием. Если пациент вовремя не обратится к врачу и диагноз не будет установлен, то возможен быстрый переход болезни в генерализованую форму и миастенический криз с летальным исходом.
При своевременной постановке диагноза и правильно подобранном лечении возможно наступление ремиссии. При нарушении режима приёма препаратов, после перенесённых инфекций, черепно-мозговых травм и стрессов возможно развитие миастенических кризов с острой дыхательной недостаточностью, нередко приводящих к гибели.
Пациентам с миастенией необходимо ограничить приём препаратов магния, миорелаксантов, петлевых диуретиков, D пеницилламина, нейролептиков, транквилизаторов, хинина, аминогликозидов, фторхинолонов, Стрептомицина, Арбидола и Дексаметазона. Данные средства способствуют развитию миастенических симптомов и усиливают слабость скелетных мышц, т. е. ведут к прогрессированию заболевания.
Больным миастенией следует избегать стрессов, интенсивных физических нагрузок, длительного нахождения на солнце, т. к. это может привести к усугублению дисфункции иммунитета и ухудшению состояния. Особое внимание следует уделять возрастной группе до 18 и старше 60 лет, которые длительно принимают антихолинэстеразные препараты.