Миелодепрессивное действие что это
Начальные проявления недостаточности кровоснабжения мозга (лечение, профилактика, трудоспособность)
Проблема профилактики и лечения ранних форм сосудистых заболеваний мозга имеет большое социальное и экономическое значение. Они не только являются серьезным фактором риска развития мозгового инсульта — одной из ведущих причин инвалидизации и смертности на
Л. С. Манвелов, кандидат медицинских наук
В. Е. Смирнов, доктор медицинских наук, профессор
НИИ неврологии РАМН, Москва
Диагноз «начальные проявления недостаточности кровоснабжения мозга» (НПНКМ) устанавливается в соответствии с «Классификацией сосудистых поражений головного и спинного мозга», разработанной НИИ неврологии РАМН [4], если у больного с признаками общего сосудистого заболевания (вегетососудистая дистония, артериальная гипертония (АГ), атеросклероз) имеются жалобы на головную боль, головокружение, шум в голове, нарушение памяти, снижение работоспособности. Причем основанием для данного диагноза может быть только сочетание двух и более из пяти перечисленных жалоб, которые должны отмечаться не реже одного раза в неделю на протяжении не менее трех последних месяцев
Проблема профилактики и лечения ранних форм сосудистых заболеваний мозга имеет большое социальное и экономическое значение. Они не только являются серьезным фактором риска развития мозгового инсульта — одной из ведущих причин инвалидизации и смертности населения, но и сами по себе существенно ухудшают качество жизни, а нередко и снижают трудоспособность.
Вторичная профилактика, в проведении которой нуждаются больные начальными проявлениями недостаточности кровоснабжения мозга (НПНКМ), включает мероприятия по предупреждению как обострений основных сердечно-сосудистых заболеваний, так и сосудистых поражений мозга.
Лечебно-профилактические мероприятия при НПНКМ можно схематично разделить на следующие виды: режим труда, отдыха и питания; лечебная физкультура; дието-, физио- и психотерапия; медикаментозное лечение и профилактика. Чаще всего назначают диету № 10 с учетом антропометрических данных, результатов исследования особенностей обмена.
Терапию больных НПНКМ следует проводить по трем основным направлениям:
У больных НПНКМ на ранних стадиях формирования основного сосудистого заболевания для компенсации состояния иногда бывает достаточно рационального трудоустройства, соблюдения режима труда, отдыха и питания, отказа от курения и злоупотребления алкоголем, использование средств, повышающих физиологические защитные силы организма. При выраженных формах заболевания необходима комплексная терапия с широким использованием медикаментозных средств.
Следует проводить терапию, направленную на ликвидацию очагов инфекции: одонтогенной; хронических тонзиллита, гайморита, пневмонии, холецистита и др. Больные сахарным диабетом должны получать адекватное противодиабетическое лечение.
Если лечение проводится нерегулярно, то риск развития острых нарушений мозгового кровообращения, а также дисциркуляторной энцефалопатии значительно увеличивается. Так, по нашим данным, основанным на семилетнем проспективном наблюдении 160 больных АГ с НПНКМ (мужчины 40-49 лет), преходящие нарушения мозгового кровообращения (ПНМК) развивались в 2,6, а мозговой инсульт — в 3,5 раза чаще у не лечившихся или лечившихся нерегулярно, чем у лечившихся регулярно и соблюдавших врачебные рекомендации.
Медикаментозные методы лечения и профилактики обострений основного сосудистого заболевания
Вегетососудистая дистония. Терапия проводится в соответствии с принципами деления вегетативных расстройств по симпатикотоническим и ваготоническим проявлениям.
При повышенном симпатическом тонусе рекомендуют диету с ограничением белков и жиров, теплые ванны, углекислые ванны. Применяют центральные и периферические адренолитики, ганглиоблокаторы. Назначают альфа-адреноблокаторы: пирроксан, редергин, дигидроэрготамин, и бета-адреноблокаторы: анаприлин, атенолол, тенормин, обладающие сосудорасширяющим и гипотензивным действием.
В случаях недостаточности симпатического тонуса показаны диета, богатая белками; солевые и радоновые ванны, прохладный душ. Эффективны препараты, стимулирующие центральную нервную систему: кофеин, фенамин, эфедрин и др. Улучшают симпатическую активность настойки лимонника по 25-30 капель в день, пантокрина — 30-40 капель, женьшеня — 25-30 капель, заманихи — 30-40 капель, препараты кальция (лактат или глюконат по 0,5 г три раза в день); аскорбиновая кислота — 0,5-1,0 г три раза; метионин — 0,25-0,5 г два-три раза в день.
При повышении парасимпатической активности рекомендуют малокалорийную, но богатую белками диету, хвойные ванны (36оС). Используют средства, повышающие тонус симпатической системы. Применяют препараты белладонны, антигистаминные, витамин В6.
При слабости парасимпатической системы положительный эффект оказывают: пища, богатая углеводами; кофе; крепкий чай; сульфидные ванны низкой температуры (35оС). Повышают парасимпатический тонус холиномиметические препараты, ингибиторы холинэстеразы: прозерин по 0,015 г внутрь и по 1 мл 0,05%-ного раствора в инъекциях, местинон по 0,06 г., препараты калия: хлорид калия, оротат калия, панангин. Иногда применяют малые дозы инсулина.
Разделение синдрома вегетососудистой дистонии по характеру проявлений (преобладание симпатической или парасимпатической активности) не всегда возможно. Поэтому в практике нашли широкое применение препараты, воздействующие на оба периферических отдела вегетативной нервной системы, обладающие как адрено-, так и холиномиметической активностью: беллоид, белласпон, препараты эрготамина.
Артериальная гипертония. Лечебно-профилактические мероприятия при АГ прежде всего должны быть направлены на устранение или коррекцию факторов риска, способствующих развитию заболевания, таких как психоэмоциональные перенапряжения, курение, злоупотребление алкоголем, избыточная масса тела, малоподвижный образ жизни, сахарный диабет.
Необходимо ограничить употребление поваренной соли до 4-6 г в сутки (1/2 чайной ложки), а при тяжелой АГ — даже до 3-4 г.
В настоящее время для медикаментозного лечения АГ наиболее эффективными считаются пять классов гипотензивных препаратов: бета-блокаторы, ингибиторы ангиотензин-превращающего фермента (АПФ), диуретики, антагонисты кальция и альфа-блокаторы. В докладе Комитета экспертов ВОЗ даны рекомендации по выбору первоначального препарата для лечения АГ, представленные в табл.
Эффективны комплексные гипотензивные средства: бринальдикс, адельфан-эзидрекс, трирезид К и др. Однако они обладают побочными негативными действиями своих ингредиентов: резерпина, тиазидовых диуретиков и гидралазинов. Эти средства можно применять в период обострения АГ, но в дальнейшем необходимо подобрать индивидуальную схему поддерживающего лечения. Терапию при злокачественной форме АГ нужно начинать в стационаре.
Не следует многократно повышать дозу первоначально действенного препарата, если он перестает надежно контролировать уровень АД. Если назначенное лекарство оказалось малоэффективным, его нужно заменить. Лучше добавить небольшие дозы другого гипотензивного средства, чем увеличивать дозу первого. Эффективность лечения повышается при использовании следующих комбинаций препаратов:
Если у больных с умеренной и тяжелой АГ АД не снижается в течение месяца комбинированного лечения двумя или тремя препаратами, ее принято считать резистентной. Причины резистентности весьма разнообразны: нерегулярный прием лекарств, назначение недостаточно высоких доз, неэффективная комбинация препаратов, прием прессорных средств, увеличение плазмы крови, наличие симптоматической гипертонии, избыточное потребление поваренной соли и алкоголя. Известен эффект «белого халата» (повышение АД у больного в присутствии врача или медицинской сестры), который может создать впечатление резистентности. Наиболее серьезными причинами резистентности к терапии являются увеличение плазмы крови в ответ на снижение АД, заболевания почек и побочные действия лекарств. У ряда больных резистентной гипертонией положительный эффект дают применение петлевых диуретиков, комбинации ингибиторов АПФ и антагонистов кальция.
Считается, что гипотензивный эффект достигнут при стойком снижении АД у больных мягкой АГ (140-179/90-104 мм рт. ст.) до нормального или пограничного уровня (ниже 160/95 мм рт. ст.), а при умеренной и выраженной АГ (180/105 мм рт. ст. и выше) — на 10-15% от исходных показателей. Резкое снижение АД при атеросклеротическом поражении магистральных сосудов головы, которое встречается у 1/3 больных АГ, может ухудшить кровоснабжение мозга.
После подбора терапии больного приглашают на осмотры до тех пор, пока не будет достигнуто адекватное снижение АД. Это позволяет убедиться, что АД удерживается на оптимальном уровне, а факторы риска находятся под контролем. Постепенное и осторожное снижение АД существенно уменьшает побочные явления и осложнения гипотензивной терапии.
При достижении стабильного снижения АД больного следует приглашать на повторные осмотры с интервалом 3-6 мес. Гипотензивная терапия, как правило, проводится неопределенно долго. Однако после длительного адекватного контроля уровня АД допускается осторожное снижение дозы или отмена одного из комбинируемых препаратов, особенно у лиц, строго придерживающихся рекомендаций по немедикаментозному лечению.
Атеросклероз. Для лечения больных атеросклерозом необходимо прежде всего выявить высокий уровень холестерина сыворотки крови (ХС) и провести мероприятия по его коррекции.
Основные препараты, используемые при лечении больных НПНКМ
Особая роль принадлежит средствам, обладающим сочетанным действием на кровоснабжение и метаболизм мозга, а также на центральную гемодинамику и реологические свойства крови. Применяют кавинтон (винпоцетин) по 0,005 г; циннаризин (стугерон) — 0,025 г; ксантинола никотинат (теоникол, компламин) — 0,15 г; пармидин (ангинин) — 0,25-0,5 г; сермион — 0,005-0,03 г; танакан — 0,04 г — три-четыре раза в день.
В случаях повышения тонуса мозговых сосудов при спастическом типе РЭГ рекомендуют спазмолитические и вазоактивные средства. Целесообразно назначение эуфиллина по 0,15 г три раза в день. В результате, как правило, улучшается общее состояние больных, уменьшаются или проходят головные боли, головокружение, отмечаются положительные изменения реографических и допплеросонографических показателей. Больным с неустойчивым тонусом сосудов назначают беллоид, белласпон, грандаксин. При гипотонии сосудов мозга и признаках венозной недостаточности рекомендуют стимулирующие препараты: элеутерококк, заманиху, корневище левзеи, пантокрин, дуплекс, женьшень, настойку китайского лимонника, алоэ — и венотонизирующие: троксевазин, эскузан, анавенол, венорутон.
В связи с тем что сосудистому заболеванию мозга нередко предшествуют или к нему присоединяются нарушения сердечной деятельности, больным по показаниям назначают средства, улучшающие коронарный кровоток, противоаритмические, сердечные гликозиды. При функциональных расстройствах сердечной деятельности у больных НПНКМ благоприятное действие оказывает боярышник в виде жидкого экстракта по 20-30 капель четыре раза в день.
В настоящее время из средств, положительно влияющих на реологические свойства свертывающей и противосвертывающей системы крови, лучше всего изучен и наиболее широко применяется аспирин. В качестве основного недостатка этого препарата отмечается раздражающее действие на желудочно-кишечный тракт. Поэтому его рекомендуют принимать однократно в суточном количестве не более 1 мг на 1 кг веса. С этой целью применяют также трентал по 0,1 г, дипиридамол — 0,25 г и метиндол — 0,025 г три раза в день. Кроме того, указанные средства предупреждают дестабилизацию клеточных мембран нейронов при ишемии мозга, подавляют отек и набухание эндотелия, увеличивают приток крови к мозгу, облегчают венозное кровообращение и оказывают спазмолитическое действие, что в результате определяет их эффективность для вторичной профилактики и лечения сосудистых заболеваний мозга. Антиагрегантным действием обладает и ряд других препаратов: папаверин, но-шпа, альфа- и бета-адренергические блокаторы и др.
При нарушениях памяти, внимания, для повышения психической и двигательной активности рекомендуется лечение ноотропилом (пирацетамом) по 0,4 г, энцефаболом (пиридитолом) по 0,1 г, аминалоном по 0,25-0,5 г два-четыре раза в день, инъекциями церебролизина по 5,0 мл внутривенно или внутримышечно и другими средствами подобного действия.
При наличии проявлений неврозоподобного синдрома назначают транквилизаторы: хлозепид (элениум, напотон) по 0,005-0,01 г три-четыре раза, сибазон (седуксен, реланиум) — 0,005 г один-два раза, феназепам — 0,00025-0,0005 г и мезапам (рудотель) — 0,005 г два-три раза в день; седативные средства: препараты валерианы, пустырника, настойку пиона и др.
Из методов физической терапии чаще всего используется электрофорез лекарственных средств по рефлекторно-сегментарному (воротниковому) трансорбитальному методу Бургиньона, а также по общей методике воздействия как обычным, так и биполярным способом. Отмечены благоприятные результаты при лечении электрофорезом 10%-ного раствора ацетилсалициловой кислоты и 7,5-10%-ного раствора оротата калия из среды 40-50%-ного универсального растворителя — димексида по методике общего воздействия: продольно на позвоночник с наложением электродов на воротниковую, межлопаточную и пояснично-крестцовую области — на курс 8-12 процедур.
Новым методом лечения является электрофоретическое введение стугерона в форме трансцеребрального рефлекторного йонофореза 0,5%-ного его раствора. У больных с цефалгиями перед этим целесообразно провести три-четыре процедуры эндоназального электрофореза 0,1%-ного раствора дигидроэрготамина.
Для больных с нарушениями венозного оттока предложен метод трансцеребрального электрофореза 5%-ного раствора троксевазина. Комбинированное применение электрофоретического и перорального введения стугерона и троксевазина позволяет воздействовать на все звенья сосудистой системы мозга: артериальный тонус, микроциркуляцию и венозный отток.
При головных болях, вегетативных нарушениях применяется электрофорез йода по методу воротникового воздействия, а при невротических состояниях и гипостении — электрофорез новокаина. Биполярный электрофорез йода и новокаина рекомендуют при неврастеническом синдроме, наклонности к головокружениям, болях в области сердца. При нарушениях сна, повышенной общей возбудимости используют электрофорез брома и йода, диазепама или магния по методике Вермеля, электросон. Положительное воздействие оказывает электрофорез далларгина на рефлексогенные зоны С-4 — T-2 и T-8 — L-2.
Следует подчеркнуть, что лекарственная терапия имеет ряд ограничений: побочные действия, аллергические реакции, привыкание к препаратам, снижение их эффективности при длительном применении. Кроме того, нужно учитывать возможность полной нечувствительности больных к тому или иному препарату. Поэтому большое значение имеет использование немедикаментозных методов лечения.
Немедикаментозные методы профилактики и лечения при НПНКМ
В комплекс лечения включают диетотерапию, активный двигательный режим, утреннюю гигиеническую гимнастику, лечебную физкультуру, плавание в бассейне, спортивные игры. При избыточной массе тела проводят подводный душ-массаж. При сопутствующем остеохондрозе шейного отдела позвоночника — массаж воротниковой зоны.
Успешно применяются воздействие переменным низкочастотным магнитным полем, синусоидальные модулированные токи на рефлексогенные зоны и мышечные группы шейной, воротниковой и поясной областей, верхних и нижних конечностей с учетом суточных биоритмов.
В практическое здравоохранение все шире внедряются методы рефлексотерапии: иглоукалывание, прижигание, электроакупунктура, воздействие лазерным излучением. У больных НПНКМ в результате лечения этими методами значительно улучшается общее состояние, уменьшаются или исчезают субъективные нарушения, отмечается положительная динамика показателей РЭГ и ЭЭГ, что объясняется нормализующим влиянием рефлексотерапии на обменные процессы, повышением физического и психического тонуса, устранением вегетососудистых нарушений. При повышенном тонусе церебральных вен рекомендуют курс СВЧ-облучения (8-12 сеансов) на рефлексогенные зоны и точки акупунктуры.
Как универсальный компонент патогенетической терапии при сосудистых заболеваниях нервной системы рассматривают гипербарическую оксигенацию, которая позволяет добиться стабилизации патологического процесса, сократить сроки лечения и улучшить прогноз. В процессе баротерапии улучшаются общее состояние больных, сон, память, уменьшаются явления астенизации, психоэмоциональные нарушения, головные боли, головокружения, вегетативные расстройства.
Стойкий клинический эффект и длительные ремиссии наблюдались у больных НПНКМ, получавших комплексное лечение с включением гипербарической оксигенации, иглорефлексотерапии и лечебной физкультуры.
Рекомендуют широкое использование бальнеотерапии.
Как в качестве самостоятельного метода, так и в комплексе с другими видами физиотерапии и лекарственными средствами применяется гидроаэроионотерапия. Целесообразно использовать оксигенотерапию в виде кислородных коктейлей, что оказывает общее стимулирующее действие и улучшает функциональное состояние нервной системы. Сочетание аэроионотерапии и оксигенотерапии дает больший клинический эффект: улучшаются самочувствие, память, исчезают головные боли, уменьшаются вестибулярные и эмоционально-волевые нарушения. Эти методы лечения можно использовать не только в стационаре, но и в поликлинике.
Предложен способ тренирующей терапии прерывистым гипоксическим воздействием: ингаляцией воздушно-азотной смеси, содержащей 10% кислорода.
При неврозоподобном синдроме, который выявляется у значительного числа больных НПНКМ, рекомендуется психотерапия. Ее важнейшими задачами являются выработка у больных правильного отношения к заболеванию, адекватной психологической адаптации к окружающей среде, повышение эффективности медицинской и социальной реабилитации. Психотерапия предполагает активное участие больного во всех ее этапах и должна начинаться уже с первого приема. В случаях выраженного проявления церебрастении успешно применяется гипнотерапия. Эффективно использование аутогенной тренировки. Наилучшие результаты достигаются при сочетанном лечении транквилизаторами и антидепрессантами с психотерапией и аутогенной тренировкой.
Большое значение имеет комплексная поэтапная терапия больных НПНКМ, которая включает лечение в стационаре, санаторно-курортное лечение и амбулаторно-поликлиническое наблюдение. Санаторно-курортное лечение наиболее целесообразно проводить в санаториях сердечно-сосудистого или общего типа, не меняя климатического пояса, поскольку из-за снижения адаптационных возможностей больные НПНКМ значительное время тратят на акклиматизацию, что укорачивает период активного лечения, снижает стойкость его эффекта, а в некоторых случаях даже ухудшает состояние.
Основным лечащим и диспансерным врачом у больных НПНКМ должен быть участковый (цеховый) врач-терапевт. На невропатолога возлагаются обязанности консультанта этих пациентов. Диспансерное наблюдение и курсовое лечение, продолжительность которого составляет 1-2 месяца, должны осуществляться не реже двух раз в год (обычно весной и осенью).
Трудоспособность
Больные НПНКМ, как правило, трудоспособны. Однако иногда они нуждаются в облегченных условиях труда, которые рекомендует ВКК: освобождение от ночных смен, дополнительных нагрузок, коррекция режима труда. Больные направляются на ВТЭК в случаях, когда условия работы противопоказаны им по состоянию здоровья. Они не могут трудиться в кессоне, при измененном атмосферном давлении, в горячих цехах (сталевар, кузнец, термист, повар), при постоянном значительном психоэмоциональном или физическом перенапряжении. Если перевод на другую работу связан со снижением квалификации, то устанавливается III группа инвалидности.
Миелодиспластический синдром
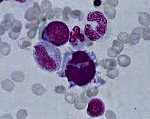
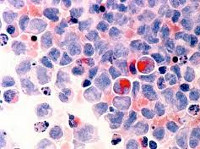
Миелодиспластический синдром относится к группе гематологических заболеваний, при которых нарушается нормальная работа органов кроветворения и изменяются основные показатели крови. Выявляется чаще у лиц трудоспособного возраста, у детей встречается редко. Особую актуальность для современной медицины миелодиспластический синдром приобрел, потому что он повышает риск развития лейкоза.
Виды миелодиспластического синдрома
В зависимости от факторов, которые послужили причиной развития заболевания, выделяют два основных вида миелодиспластического синдрома.
Существует более подробная классификация миелодиспластического синдрома, которая разработана экспертами ВОЗ. Она учитывает количество бластов в периферической крови, степень дисплазии костного мозга и общие показатели крови. В этой классификации выделяется форма миелодиспластического синдрома, которая ассоциирована с делецией длинного плеча 5-й хромосомы. Медико-генетический центр «Геномед» имеет необходимое оборудование для того, чтобы выявить данную мутацию.
Заболевание характеризуется нарушением кроветворения, поэтому клиническая картина будет зависеть от степени выраженности этих нарушений. Обычно для миелодиспластического синдрома характерны следующие проявления:
Если миелодиспластический синдром протекает в мягкой форме, то первые признаки могут появиться нескоро, а степень их выраженности обычно слабая. Длительное скрытое течение и стертая симптоматика не вызывает у пациентов настороженности и не заставляет обращаться за медицинской помощью, поэтому заболевание часто выявляется случайно.
Для того чтобы достоверно подтвердить миелодиспластический синдром, необходимо пройти комплексное гематологическое обследование, в которое включаются:
Хромосомные нарушения выявляются у 75 % больных, поэтому дополнительно назначается генетическое исследование.
Лечение миелодиспластического синдрома
План лечения составляется согласно тяжести заболевания и степени выраженности изменений в показателях крови. Если у пациента не выявляется анемия, геморрагические проявления и сопутствующие осложнения, то лечение в таких случаях не проводится, но необходимость в регулярном контроле и наблюдении сохраняется. Если же нарушения выражены существенно, выявлен высокий риск развития лейкоза, то назначается терапия, направленная на подавление иммунных реакций, возможна химиотерапия, регулярные переливания крови и ее компонентов, в тяжелых случаях пересадка костного мозга.
Продолжительность жизни пациентов с миелодиспластическим синдромом зависит от клинических проявлений и успешности лечения. В лучшем случае она составляет 10 лет и более, а в самых худших – меньше года.
Обзор таблеток от повышенного давления нового поколения
Частое повышение показателей артериального давления (АД) – причина развития серьезных заболеваний (инсульт, инфаркт миокарда и пр.). Гипертоническая болезнь в России диагностируется у каждого третьего человека преклонного возраста. Для борьбы с гипертонией многим пациентам приходится принимать препараты на протяжении всей жизни, чтобы исключить осложнения.
Современные фармакологические компании предлагают большой выбор лекарственных средств, эффективных при гипертонии. Если не знаете, как выбрать таблетки от повышенного давления, ознакомьтесь с рейтингом, представленным ниже. В ТОП вошли лучшие медикаменты с учетом эффективности, стоимости и отзывов.
Классификация препаратов от повышенного давления
Причины гипертонии
Когда нужно вызвать врача на дом при повышении давления?
Общепринятые показатели АД – 120/80. Параметры могут незначительно варьировать в зависимости от времени суток, физической активности и возраста человека.
Таблица – Показатели артериального давления и рекомендации
Миелодиспластический синдром
Миелодиспластический синдром – группа гематологических заболеваний, при которых наблюдаются цитопения, диспластические изменения костного мозга и высокий риск возникновения острого лейкоза. Характерные симптомы отсутствуют, выявляются признаки анемии, нейтропении и тромбоцитопении. Диагноз устанавливается с учетом данных лабораторных анализов: полного анализа периферической крови, гистологического и цитологического исследования биоптата и аспирата костного мозга и т. д. Дифференциальный диагноз может представлять значительные затруднения. Лечение – переливание компонентов крови, химиотерапия, иммуносупрессивная терапия, пересадка костного мозга.
Общие сведения
Миелодиспластический синдром – группа заболеваний и состояний с нарушениями миелоидного кроветворения и высоким риском развития острого лейкоза. Вероятность развития увеличивается с возрастом, в 80% случаев данный синдром диагностируется у людей старше 60 лет. Мужчины страдают несколько чаще женщин. У детей миелодиспластический синдром практически не встречается. В последние десятилетия гематологи отмечают увеличение заболеваемости среди лиц трудоспособного возраста. Предполагается, что причиной «омоложения» болезни могло стать существенное ухудшение экологической обстановки.
До недавнего времени лечение миелодиспластического синдрома было только симптоматическим. Сегодня специалисты разрабатывают новые методы терапии, однако эффективное лечение этой группы болезней все еще остается одной из самых сложных проблем современной гематологии. Пока прогноз при миелодиспластическом синдроме, в основном, зависит от особенностей течения болезни, наличия или отсутствия осложнений. Лечение осуществляют специалисты в сфере онкологии и гематологии.
Причины и классификация миелодиспластического синдрома
С учетом причин развития различают два типа миелодиспластического синдрома: первичный (идиопатический) и вторичный. Идиопатический вариант выявляется в 80-90% случаев, диагностируется преимущественно у пациентов старше 60 лет. Причины возникновения установить не удается. В числе факторов риска первичного миелодиспластического синдрома – курение, повышенный уровень радиации при выполнении профессиональных обязанностей или проживании в неблагоприятной экологической зоне, частый контакт с бензином, пестицидами и органическими растворителям, некоторые наследственные и врожденные заболевания (нейрофиброматоз, анемия Фанкони, синдром Дауна).
Вторичный вариант миелодиспластического синдрома наблюдается в 10-20% случаев, может возникать в любом возрасте. Причиной развития становится химиотерапия или радиотерапия по поводу какого-то онкологического заболевания. В число лекарственных средств с доказанной способностью вызывать миелодиспластический синдром включают циклофосфан, подофиллотоксины, антрациклины (доксорубицин) и ингибиторы топоизомеразы (иринотекан, топотекан). Вторичный вариант отличается более высокой резистентностью к лечению, более высоким риском развития острого лейкоза и более неблагоприятным прогнозом.
В современной редакции классификации ВОЗ различают следующие типы миелодиспластического синдрома:
Симптомы миелодиспластического синдрома
Клиническая симптоматика определяется степенью нарушений миелопоэза. При мягко протекающих расстройствах возможно длительное бессимптомное или стертое течение. Из-за слабой выраженности клинических проявлений некоторые больные не обращаются к врачам, и миелодиспластический синдром обнаруживается во время проведения очередного медицинского осмотра. При преобладании анемии наблюдаются слабость, одышка, плохая переносимость физических нагрузок, бледность кожных покровов, головокружения и обморочные состояния.
При миелодиспластическом синдроме с тромбоцитопенией возникает повышенная кровоточивость, отмечаются десневые и носовые кровотечения, на коже появляются петехии. Возможны подкожные кровоизлияния и меноррагии. Миелодиспластический синдром с выраженными нейтропенией и агранулоцитозом проявляется частыми простудами, стоматитом, синуситом или стрептодермией. В тяжелых случаях возможно развитие пневмонии или сепсиса. Инфекционные заболевания нередко вызываются грибками, вирусами или условно-патогенными микробами. У каждого пятого пациента с миелодиспластическим синдромом выявляется увеличение лимфоузлов, селезенки и печени.
Диагностика миелодиспластического синдрома
При исследовании костного мозга количество клеток обычно нормальное либо повышенное. Уже на ранних стадиях обнаруживаются признаки дизэритропоэза. Количество бластов зависит от формы миелодиспластического синдрома, может быть нормальным либо увеличенным. В последующем наблюдаются дисгранулоцитопоэз и дисмегакариоцитопоэз. У некоторых больных признаки дисплазии костного мозга выражены очень слабо. В процессе цитогенетического исследования у ¾ больных выявляются хромосомные нарушения. Дифференциальный диагноз миелодиспластического синдрома проводят с В12-дефицитной анемией, фолиево-дефицитной анемией, апластической анемией, острым миелолейкозом и другими острыми лейкозами.
Лечение и прогноз при миелодиспластическом синдроме
Тактика лечения определяется выраженностью клинической симптоматики и лабораторных изменений. При отсутствии явных признаков анемии, геморрагического синдрома и инфекционных осложнений осуществляется наблюдение. При миелодиспластическом синдроме с выраженной анемией, тромбоцитопенией и нейтропенией, а также при высоком риске возникновения острого лейкоза назначают сопроводительную терапию, химиотерапию и иммуносупрессивную терапию. При необходимости осуществляют пересадку костного мозга.
Сопроводительная терапия является самым распространенным методом лечения миелодиспластического синдрома. Предусматривает внутривенные инфузии компонентов крови. При длительном применении может провоцировать повышение уровня железа, влекущее за собой нарушения деятельности жизненно важных органов, поэтому переливания гемокомпонентов производят при одновременном приеме хелаторов (лекарственных средств, связывающих железо и способствующих его выведению).
Иммуносупрессоры эффективны при лечении миелодиспластического синдрома с отсутствием хромосомных аномалий, наличием гена HLA-DR15 и гипоклеточном костном мозге. Химиотерапию применяют при невозможности трансплантации костного мозга. Высокие дозы препаратов используют при трансформации миелодиспластического синдрома в острый лейкоз, а также при рефрактерных анемиях с избытком бластов при нормоклеточном и гиперклеточном костном мозге, низкие – при невозможности пересадки костного мозга. Наряду с перечисленными средствами пациентам назначают гипометилирующие средства (азацитидин). Наиболее надежным способом достижения полноценной длительной ремиссии является трансплантация костного мозга.
Прогноз зависит от типа миелодиспластического синдрома, количества хромосомных аномалий, необходимости в регулярных переливаниях компонентов крови, выраженности клинических проявлений и наличия осложнений. Различают 5 групп риска. Средняя выживаемость больных миелодиспластическим синдромом, входящих в группу с самым низким уровнем риска, составляет более 11 лет; с самым высоким – около 8 месяцев. Вероятность отторжения костного мозга после трансплантации – около 10%.