Микроделеции не обнаружено что это значит
Что такое микроделеционные синдромы?
Статья опубликована: 2018-12-06
Рейтинг: 5 из 5
Беременность и рождение ребенка счастливое и долгожданное время для каждого родителя. Всем нам хочется иметь крепкого и здорового малыша. Будущие родители часто говорят: “Без разницы мальчик или девочка, главное, чтобы здоровый был.” Это действительно так. Могу с уверенностью говорить, как мать.
Но иногда выходит не так, как хотелось бы. Сейчас мы поговорим о микроделеционных синдромах или микроделециях. Это заболевание относится к разряду генетических и лечению не подлежит. Но, в отличие от синдромов Дауна, Патау и Эдвардса, совместимо с нормальными условиями жизни. Причем жизни до старости. Это не приговор для ребенка!
Немного науки. У всех нас есть 23 пары хромом, которые достались нам от родителей. По 23 хромосомы от каждого родителя. Хромосомы состоят из участков — локусов. Может так произойти, что какой-то участок в хромосоме может отсутствовать, как говорят генетики, выпадает. Выпадение этого участка и приводит к микроделеционным синдромам. Термин происходит от латинского “deletio” — уничтожение.
Причины. Как правило причины появления микролелеций носят генетический наследственный характер. Это наследственное заболевание передается от родителей к ребенку. Встречались случаи, когда у родителей не было выраженных признаков делеций в хромосоме, но ребенок все равно рождался больным. Это происходило из-за того, что у бабушек, дедушек, прабабушек и прадедушек был этот синдром. Поэтом рекомендуется выяснять карту наследственных заболеваний на несколько поколений.
Другими причинами появления такого синдрома могут быть:
Последствия. В результате таких хромосомных отклонений рождаются дети несколько отличающиеся по внешнему виду. Но некоторые делеции могут и вовсе не иметь вешних признаков. Например, делеция локуса AZF, приводящая к полному или частичному мужскому бесплодию.
В общем такие люди живут долго, социальны и самостоятельны. Однако у них велика вероятность вновь произвести потомство с аномалией в хромосомах, возможно уже с более негативными последствиями.
Методы диагностики. Диагностировать микроделеционный синдром можно у взрослого человека, проведя ДНК анализ на хромосомные отклонения. Для этого достаточно сдать 20мл крови из вены. У плода тоже можно выявить такие отклонения, причем на ранних стадиях беременности. ДНК тест проводится по крови матери, без вмешательства в утробу. Это полностью устраняет риски каких-либо осложнений беременности. Подобный анализ называется пренатальным неинвазивгым тестом или НИПТ тестом. Он возможен уде с 7-9 ой недели беременности.
Генетический центр ДТЛ проводит все виды неинвазивных тестов на хромосомные отклонения. Мы сотрудничаем с ведущими ДНК лабораториями во всем мире: США, Канада, Кипр, Германия.
Анализ микроделеций AZF локуса Y хромосомы у мужчин c бесплодием
В современном мире бесплодие представляет собой важную медико-социальную проблему, затрагивающую демографические основы общества. Бесплодием страдают около 15% супружеских пар, при этом, неуклонно растет доля мужского фактора и по данным Европейской ассоциации урологов она в настоящее время составляет около 50% [1]. Приблизительно у 5% мужчин репродуктивного возраста имеются различные количественные и качественные изменения спермы. Около 1/3 случаев мужского бесплодия относят к так называемому идиопатическому типу бесплодия, большинство случаев которого может быть обусловлено генетическими факторами, такими как различные нарушения хромосом или мутации в ответственных за сперматогенез генах [2,3].
Результаты многочисленных исследований, посвященных изучению роли генетических факторов в этиологии бесплодия, убедительно доказывают ведущее место данных факторов в структуре нарушений репродуктивной функции как у мужчин, так и у женщин [4,5]. Так, генетические факторы обуславливают, по крайней мере, 30-50% всех случаев тяжелых форм бесплодия у мужчин. Помимо аномалий кариотипа наиболее частой генетической причиной бесплодия у мужчин являются делеции Y-хромосомы, захватывающие локус AZF. Распространенность данной мутации среди мужчин с выраженными отклонениями в показателях спермограммы широко варьирует в различных популяциях и составляет в среднем 7,6% [6,7].
Делеции AZF-локуса связаны с различной степенью нарушения сперматогенеза от умеренного снижения его активности (гипосперматогенез) или блока сперматогенеза до практически полного отсутствия половых клеток в семенных канальцах – Сертоли клеточный синдром (СКС) [4-6, 8-12].
Азооспермия и олигозооспермия тяжелой степени являются одними из наиболее тяжелых форм нарушения сперматогенеза и составляют 10-20% и 15-20%, соответственно, от всех нарушений репродуктивной функции у мужчин при измененных показателях спермограммы. С помощью имеющихся в настоящее время методов цитогенетической и молекулярно-генетической диагностики макро- и микроделеции Y-хромосомы, захватывающие локус AZF, удается обнаружить у 10-15% мужчин с азооспермией и у 5-10% мужчин с олигозооспермией тяжелой степени [5-8,11-15].
Впервые роль делеций локуса Yq11 в этиологии нарушения сперматогенеза и бесплодия у мужчин была показана в 1976 г. L. Tiepolo и O. Zuffardi [16]. Дальнейшие цитогенетические и молекулярно-генетические исследования позволили с помощью STS-технологии (sequencetagged sites) построить детальную карту Y-хромосомы, включающую 43 делеционных интервала [17]. Было подтверждено наличие в дистальной части длинного плеча Yхромосомы локуса AZF, делеции которого ответственны за нарушение сперматогенеза. В 1996 г. P.H. Vogt и соавт. на основе полученных данных о локализации и размере делеций, выявленных у 26 мужчин, предложили выделить в локусе Yq11.21-q11.23 три неперекрывающихся субрегиона: AZFa, AZFb и AZFc [18].
Целью нашего исследования явилось уточнение структуры и определение роли генетических нарушений при бесплодии.
МАТЕРИАЛЫ И МЕТОДЫ
За период с 2017 по 2018 гг. было обследовано 63 пациента с первичным бесплодием. На основании результатов спермиологического исследования мужчин с бесплодием разделили на 2 группы: группу с азооспермией и контрольную группу (табл. 1). В группу с азооспермией были включены 63 пациента, контрольную группу составили 30 здоровых (фертильных) мужчин.
Обследование, проведенное пациентам, включало общеклиническое, общее и специальное андрологическое исследование, сперматологическое (стандартное спермиологическое исследование, в некоторых случаях – гистологическое исследование биоптата яичка), молекулярно-генетическое исследование (анализ микроделеций Y-хромосомы).
Спермиологический анализ эякулята выполняли по стандартной методике, рекомендованной ВОЗ [19]. Гистологическое исследование биоптата яичка проводилось путем цитогистологического анализа [9].
Полимеразную цепную реакцию (ПЦР) выполняли на программируемом термоциклере МС2 производства фирмы «ДНК-технология» (Россия) с использованием Taq-полимераз.
Анализ микроделеций локуса AZF был проведен в соответствии с руководством по молекулярной диагностике микроделеций Y-хромосомы [12]. Для обнаружения делеций применяли мультиплексную амплификацию (МПА), предложенную в данном руководстве в собственной модификации. На первом этапе анализа выполняли детектирование делеций в трех субрегионах AZF.
РЕЗУЛЬТАТЫ
Среди 63 обследованных мужчин кыргызов с бесплодием делеции локуса AZF были обнаружены у 7 (11,1%) пациентов (табл. 1). Делеции Y-хромосомы были выявлены только у пациентов с азооспермией. Ни одной Y-делеции не было обнаружено у фертильных мужчин контрольной группы. Чаще всего делеции располагались в AZFc-субрегионе (57,1% делеций Y-хромосомы) (табл. 2). Микроделеции субрегиона AZFb были выявлены только у двух пациентов (28,6 % случаев от всех обнаруженных делеций локуса AZF) и у одного пациента выявлена микроделеция AZFa+b+c – субрегиона (14,3% случаев).
Таблица 1. Частота делеций локуса AZF в обследованных группах мужчин
| № | Группы пациентов | Количество обследованных мужчин | Число обнаруженных делеций AZF- локуса |
|---|---|---|---|
| 1 | Пациенты с азооспермией | 63 | 7 (11,1%) |
| 2 | Контрольная группа | 30 | 0 (0%) |
Таблица 2. Количество обнаруженных микроделеций AZF локуса длинного плеча Y-хромосомы
Спермиологическая и гистологическая картина, обнаруженная нами у мужчин с делециями локуса AZF, выявляла различную степень нарушений сперматогенеза. У обоих пациентов с микроделециями AZFbсубрегиона отмечали азооспермию. Гистологическое исследование биоптата яичка, проведенное у одного из них, позволило выявить синдром клеток Сертоли. По результатам молекулярного анализа у этих пациентов область делеции захватывала маркер sY1197 субрегиона AZFb. У мужчин с делециями субрегиона AZFc сперматозоиды отсутствовали (азооспермия). При анализе гистопрепаратов биоптата яичка, выполненного у двух из этих пациентов, было установлено, что у одного из них половые клетки отсутствовали в большинстве семенных канальцев.
ОБСУЖДЕНИЕ
Частота обнаружения микроделеций Y-хромосомы среди мужчин с бесплодием значительно варьирует в различных исследованиях (от 1% до 35%) [7,8,10,20]. Широкий разброс частот выявляемости делеций обусловлен влиянием ряда факторов, среди которых наибольшее значение имеют критерии отбора пациентов для проведения микроделеционного анализа. В среднем выявлено наличие делеций локуса AZF у 7,5% мужчин с бесплодием, при этом наибольшая частота делеций отмечена среди мужчин с идиопатической азооспермией (18%) или тяжелой олигозооспермией неясного генеза (14,3%) [9]. Количество делеций, выявленных по результатам нашего исследования, в общем аналогично частоте встречаемости делеций отдельных субрегионов или захватывающих несколько регионов, а также аналогично средней частоте встречаемости микроделеций в азиатских популяциях [20]. При этом соотношение между различными типами выявленных нами делеций в целом отражает структуру делеционных нарушений в локусе AZF у мужчин с бесплодием.
При делециях, захватывающих субрегионы AZFb и AZFc, у мужчин выявляются азооспермия и СКС. Определение зависимости степени нарушения сперматогенеза от размера и локализации делеций может иметь прогностическое значение для возможного получения сперматозоидов, пригодных для проведения ICSI (Intra Cytoplasmic Sperm Injection) – инъекцией сперматозоида в цитоплазму ооцита [5,8,11]. Наличие делеций, захватывающих субрегионы AZFa или AZFb, указывает на невозможность получения зрелых половых клеток, а у пациентов с делециями AZFc при биопсии яичка примерно в 50-70 % случаев удается получить зрелые сперматозоиды [5,11].
ЗАКЛЮЧЕНИЕ
Результаты многочисленных исследований микроделеций Y-хромосомы у мужчин с бесплодием, а также оценка роли генов локуса AZF в дифференцировке и развитии мужских половых клеток убедительно свидетельствуют о высокой значимости генов Y-хромосомы в контроле сперматогенеза у человека. У специалистов в области генетики, андрологии, репродуктивной медицины произошло осознание того, что азооспермия является одной из наиболее распространенных причин бесплодия у мужчин, и исследование микроделеций Y-хромосомы широко вошло в практику. Молекулярно-генетический анализ Y-хромосомы на наличие классических микроделеций должен быть рекомендован всем мужчинам с азооспермией или олигозооспермией тяжелой степени.
Исследование микроделеций AZF локуса Y-хромосомы у мужчин с тяжелой формой олигозооспермии и азооспермии позволяет установить генетическую причину нарушения сперматогенеза и является важным диагностическим и прогностическим критерием, определяющим рациональную тактику лечения, выбор метода преодоления бесплодия, а также прогнозировать вероятность получения сперматозоидов для проведения экстракорпорального оплодотворения, в частности интрацитоплазматической инъекции сперматозоида в ооцит.
ЛИТЕРАТУРА
Статья опубликована в журнале»Экспериментальная и клиническая урология» №2 2018, стр.90-93
Что такое микроделеционные синдромы и их виды?
Статья опубликована: 2018-12-29
Рейтинг: 4 из 5
У здорового человека должно быть ровно 46 хромосом. Хромосомы находятся в парах, образуя 23 пары. Отклонение от нормы вызывает тяжелые заболевания порой не совместимые с жизнью. А если ребенок выживает, то становится инвалидом и доживает лет до 35-40. К таким серьёзным отклонениям относятся, например, синдром Дауна, Патау, Эдвардса.
Виды делеций
Тем не менее количество хромосом может быть в норме, но сама структура нарушается. Такие синдромы называются микроделециями. Делеция – это в переводе с латинского уничтожение, то есть в хромосоме отсутствует участок. Такое явление имеет место при разрыве или при неравном кроссинговере. Существуют разные виды делеций:
Виды микроделеционных синдромов
Подобного рода аномалии встречаются редко. Намного реже чет трисомии или моносомии. Люди с делециями могут вести достаточно социальный образ жизни и даже иметь своих детей. К основным видам подобных аномалий относятся:
Подобные аномалии можно диагностировать еще на ранних сроках беременности. На 9-ой неделе при помощи неинвазивного пренатального теста возможно выявить микроделеционные синдромы с точностью до 99,99%.
Что такое делеция, структурные хромосомные мутации?
Статья опубликована: 2018-12-25
Рейтинг: 5 из 5
Геном человека устроен таким образом, что для нормальной жизни у нас должно быть ровно 23 пары хромосом. Хромосомы существуют именно парно, потому что одна хромосома в паре приходит от мамы, а другая от папы. Нарушение в числе хромосом приводит к тяжелым заболеваниям, например, синдрому Дауна. Однако, количество хромосом может быть в норме, но все равно человек имеет аномалии в развитии, которые не совместимы с нормальной и долгой жизнью.
Дело в том, что могут быть отклонение в самой структуре хромосомы. Из хромосомы выпадают участки. Такое явление называется делецией. Делеция происходит от лат. deletio что значит уничтожение. Такая аномалия может возникать в результате неравного кроссинговера или при разрыве хромосомы.
Признаки делеционного синдрома
Делеции или микроделеции могут вообще внешне не проявляться. Человек может всю жизнь прожить с этим синдромом и не знать о его существовании. Заболевание может обнаружится, например, когда возникнет необходимость завести ребенка, но попытки будут безуспешными.
Существуют делеции с явно выраженными внешними признаками:
Причины появления делециий
Существует несколько причин, при которых возможно развитие делеционного синдрома:
Диагностика синдромов
Выявить наличие делеций возможно на ранних сроках беременности. Уже на 9-ой недели по венозной крови матери можно провести ДНК анализ и диагностировать заболевание. Такое генетическое исследование называется неинвазивный пренатальный ДНК тест. Тест проводится без направления врача, т. к. не имеет противопоказаний и побочных эффектов.
Генетический центр “ДТЛ” выполняет НИПТ тесты уже более 4 лет. В сотрудничестве с ведущими мировыми лабораториями в области пренатальной диагностики нами проведено уже болен 1000 подобных исследований.
Микроделеционные синдромы
Организм человека состоит из огромного количества клеток. Они в свою очередь объединяются в более крупные единицы – ткани и органы. Из последних строятся системы органов, а и из них и получается организм. И на всех уровнях постоянно идут различные взаимодействия и сложные биохимические реакции. Чтобы все это гармонично развивалось из оплодотворенной яйцеклетки и слаженно функционировало, требуется специальная схема работы для всех уровней. Ее роль в организме выполняет организованная генетическая информация.
Именно на наследственный материал возлагается задача по сохранению данных об общем облике человека, особенностях строения отдельных органов, принципах регуляции при помощи гормонов, и даже того, каким образом должны собираться белки. Все данные записываются в виде последовательности структурных единиц – нуклеотидов. Они подобно буквам алфавита формируют группы-слова, выполняющие определенные функции. Каждая группа называется геном. Все вместе они формируют молекулу ДНК. Если посмотреть на уровень выше, то можно заметить, что весь наследственный материал в виде цепочек дезоксирибонуклеиновой кислоты сконцентрирован в особых образованиях, которые называются хромосомами.
Их у человека в норме насчитывается 23 пары. В каждой паре информация хранится в двух копиях. Это необходимо для того, чтобы при передаче генетической информации каждая дочерняя клетка получила свою копию. Одна пара хромосом отличается от остальных и отвечает за вопросы определения пола. Если в ней имеются две одинаковые большие хромосомы (ХХ вариант), то организм относится к женскому полу. Если же имеется одна большая и одна малая хромосома, то речь идет о мужском поле (XY вариант). Эти две отличающиеся от прочих хромосомы называются половыми. Оставшиеся 22 пары встречаются во всех организмах независимо от пола. Их называют аутосомами.
Аномалии генетического материала
Наследственный материал состоит из огромного количества нуклеотидов, формирующих гены. При этом в каждом гене последовательность нуклеотидов строго определена, поскольку должна кодировать определенный белок. Кроме того, сами гены при формировании хромосом также выстраиваются в фиксированном порядке. Благодаря сохранению этого порядка организм может функционировать, а ученые – быстро и точно указывать друг другу, про какой ген идет речь.
В идеальном случае система работает без малейших сбоев, а генетическая информация всегда передается в неизменном виде. Однако на практике большое число структурных единиц и постоянное воздействие различных факторов (например, ионизирующего излучения) приводит к тому, что время от времени возникают различные аномалии. В частности, отдельные участки последовательности ДНК могут быть скопированы на новое место. В таком случае говорят о дупликации. Если же вместо создания новой копии была перемещена часть исходной цепочки, то модификация называется транслокацией. Кроме того, иногда часть последовательности просто теряется, удаляется из генетического материала. В таком случае изменение называется делецией.
Поскольку взаимодействия в организме оттачивались в течение многих тысячелетий эволюционного развития, получилась очень слаженная система. И аномалии, даже самые небольшие, могут вызвать нарушение баланса. В таком случае в организме развивается то или иное нарушение. Если при этом причина находится на уровне генов, то говорят о генных болезнях. Если была утрачена или наоборот получена лишняя копия хромосомы, то такие нарушения называются хромосомными заболеваниями.
Что такое микроделеционный синдром?
Самые незначительные изменения (они же мутации) называются точечными. Их появление влияет на считанные единицы генов. В некоторых случаях нарушение относится вообще к одному единственному гену. Однако если он обеспечивал выработку важного белка, последствия для всего организма могут быть очень серьезными. Подобные патологические изменения относятся к группе микроделеционных синдромов.
Каждое такое заболевание обусловлено небольшим изменением генетического материала, которое происходит в строго определенном месте. Точный механизм возникновения подобных нарушений на сегодняшний день не установлен, что не мешает ученым заниматься исследованием их воздействия на организм.
Так, было выяснено, что развитие синдрома в таком случае может происходить несколькими различными вариантами. В частности, ряд заболеваний характеризуется участием онкогенов. В других случаях на воздействие непосредственно самой делеции накладывается эффект хромосомного импринтинга и возможные однородительские дисомии.
Частота возникновения большей части микроделеционных синдромов крайне невелика: порядка 1 случая на 50-100 тысяч новорожденных. Набор клинических признаков обычно выражается отчетливо. Для того чтобы поставить диагноз, бывает достаточно лишь совокупности симптомов. Однако при таком подходе невозможно точно прогнозировать здоровье потомков, поэтому зачастую наряду с проверкой обычных признаков производится молекулярно-генетическая диагностика пробанда и его родственников (обычно родители, в некоторых случаях также требуется анализ генотипа братьев, сестер, теть, дядь и так далее).
Патологические проявления сильно отличаются. В частности, их проявление определяется тем, насколько большой участок генетического материала был утрачен в результате делеции. Кроме того, в ряде случаев играет роль то, от кого из родителей была получена мутация (влияние хромосомного импринтинга). Хорошей иллюстрацией последней ситуации является пара синдромов Прадера-Вилли и Ангельмана. Они оба обусловлены наличием делеции в 15 хромосоме. Однако из-за различного механизма действия при передаче от разных родителей клиническая картина этих заболеваний значительно отличается.
Позитивное влияние некоторых делеций на жизнеспособность
Небольшие изменения делеционного характера могут существенно повлиять на выживание организма. К примеру, утрата гена, кодирующего белок CCR5-δ32, становится причиной невосприимчивости к вирусу иммунодефицита человека. Ученые предполагают, что эта мутация впервые появилась около 2,5 тысячелетий назад и с течением времени распространилась по территории Европы.
Имеющееся на сегодняшний день распределение отличается неравномерностью. Согласно статистическим данным, около 10% жителей европейских стран устойчиво к ВИЧ. Вместе с тем в скандинавских государствах этот показатель достигает 14-15 процентов. Русские и финны демонстрируют 16-процентный уровень устойчивости. В то же время для Сардинии частота равняется скромным 4 процентам.
Ряд ученых выдвинул гипотезу, что подобное распространение определяется прошедшими в средневековый период эпидемиями бубонной чумы. Вероятно, мутация в гене вызывает повышенную сопротивляемость этому заболеванию. Поэтому на территории тех стран, где прошлась «черная смерть», выжило больше людей с этим генотипом.
Влияние делеций на способность к оплодотворению
Делеции, происходящие в обычных хромосомах (аутосомах) могут в некоторых случаях быть компенсированы нормальной копией гена. Однако когда речь заходит о половых хромосомах, особенно об Y-хромосоме, ситуация меняется.
Прежде всего необходимо отметить, что локализованные на ней гены не имеют второго экземпляра. При нормальном количестве хромосом в наборе Y-хромосома оказывается крайне уязвимой. В сочетании с малым количеством генов это приводит к серьезным последствиям каждого изменения. Особый интерес представляют мутации, касающиеся AZF-локуса и SRY гена.
Аномалии гена SRY (Sex-determining Region Y)
Ген SRY, как следует из его названия, отвечает за крайне важную функцию. Именно его наличие в хромосомном наборе запускает процесс формирования организма по мужскому фенотипу и стимулирует развитие соответствующих половых органов.
Наличие даже небольшой делеции в этом гене нарушает механизм дифференцировки пола. В результате при нормальном кариотипе 46XY зародыш начинает развиваться как женский организм. По этой причине на ген SRY приходится наибольшее число мутаций, связанных с неразвитостью гонад. Кроме того, изменения этого гена вызывают инверсию пола.
Аномалии AZF-локуса
На Y-хромосоме также имеется особый участок, который контролирует процесс выработки сперматозоидов. Именно от этого зависит, насколько эффективным будет сперматогенез. Кроме того, состояние этого участка сказывается на свойствах сперматозоидов, таких как общее количество в эякуляте, способность двигаться, наличие структурных изменений и способность к оплодотворению. Только при наличии хорошо сформированных подвижных сперматозоидов мужской генетический материал может быть доставлен до яйцеклетки. Иными словами, о состоянии этого небольшого участка генетического кода зависит способность мужчины иметь детей.
При наличии в AZF-локусе аномалий процесс выработки сперматозоидов нарушается. В результате могут развиться азооспермия и олигозооспермия. При этих патологиях в эякуляте либо совсем не содержится сперматозоидов, либо их число сильно снижено.
Сам AZF локус делится на три части со специфическими задачами. Они именуются путем добавления индекса: AZFa, AZFb и AZFc. Возникшая делеция может удалять фрагмент отдельной части, либо ее целиком, либо захватывать сразу два региона. При полном удалении AZF развивается тяжелое поражение сперматогенеза. Частичные делеции могут проявляться по-разному. При этом на степень проявления патологии влияют размеры утраченного фрагмента и его расположение в локусе. Поэтому для прогностических целей крайне важно знать, в каком месте произошла делеция. Кроме того, эта информация может использоваться для правильного планирования семьи и проведения экстракорпорального оплодотворения.
Если при делеции был удален весь локус или любой из регионов с индексами a/b, то у мужчины не могут быть получены жизнеспособные сперматозоиды. Если делецию можно описать формулой AZFb/AZFb+, то развивается азооспермия из-за тяжелых нарушений процесса формирования сперматозоидов.
Делеции участка AZFc приводят к проявлению патологических симптомов различной степени тяжести. В том числе возможно развитие олигоспермии, которая в принципе допускает зачатие. В 50-70 процентах от общего числа подобных случаев возможно получение сперматозоидов для дальнейшего использования в методах искусственного оплодотворения. Частичная делеция региона AZFс может выражаться в форме различных нарушений от нормозооспермии до азооспермии.
Все делеции в AZF-локусе, вызывающие ту или иную патологическую ситуацию, являются причинами мужского бесплодия. Определение мутации возможно путем гистологического анализа семенной жидкости. При этом необходима остановка созревания сперматозоидов или обнаружение незрелых сперматозоидов. Для получения точных данных о делециях в AZF-локусе используется ПЦР 6 маркеров, которые относятся к отдельным участкам локуса.
Синдром Ангельмана
При синдроме Ангельмана развивается характерный набор патологических изменений. В частности, отмечается задержка психологического развития, сопровождающаяся проблемами со сном, частыми хаотическими движениям (больше руками), постоянными улыбками и смехом.
Патология развивается при отсутствии некоторых генов, расположенных на 15 хромосоме. При этом обязательным условием является передача мутантной копии гена от матери. Если поврежденная хромосома будет унаследована от отца, то разовьется синдром Прадера-Вилли. Кариотип обычно нормальный (46XX и 46XY для девочек и мальчиков соответственно). Различные независимые исследования указывают на связь болезни с геном UBE3A, который в норме обеспечивает выработку ферментного компонента в сложной системе деградации белков.
Частота появление синдрома составляет примерно 1 случай на 10-20 тысяч новорожденных (показатели отличаются у различных ученых).
Характерными особенностями больных с синдромом Ангельмана являются следующие признаки:
· проблемы с питанием, начинающиеся еще во время грудного вскармливания, поскольку дети плохо набирают вес (распространенность признака порядка 75 процентов);
· заторможенное развитие навыков общей моторики, то есть дети позже других начинают сидеть и ходить;
· для всех детей характерны нарушения речевого развития;
· больные обычно понимают больше, чем в состоянии выразить при помощи ограниченного словарного запаса;
· часто заболевание сопровождается дефицитом внимания и гиперактивностью;
· проблемы с обучением в обычной школе;
· у 80% заболевших развивается эпилепсия, сопровождающаяся заметными на электроэнцефалографии нарушениями; ученые полагают, что заболевание эпилепсией носит вторичный (симптоматический) характер.
· выполнение необычных движений, к которым относятся произвольные хаотические движения конечностями, мелкий тремор;
· возникновение приступов смеха при отсутствии видимых причин;
· характерная ходьба на негнущихся ногах, из-за которой возникло сравнение с марионетками;
· уменьшенная по сравнению со средними размерами голова, часто с уплощенным затылком;
· в некоторых случаях встречаются своеобразные запоминающиеся черты лица – широкий рот с редко расположенными зубами, выдвинутый вперед подбородок с выпущенным наружу языком;
· различные нарушения сна;
· примерно в 40 процентах случаев развивается косоглазие;
· порядка 10% больных также страдает от искривления позвоночника;
· высокие температуры воспринимаются с повышенной чувствительностью;
· наибольшего комфорта обычно достигают в воде (к примеру, в ванной)
Как правило, синдром определяется при помощи методов молекулярно-генетической диагностики по 15 хромосоме. Показанием к проведению тестирования для новорожденного является пониженный мышечный тонус (гипотонус), заметное отставание в развитии речи и мелкой моторики. Кроме того, на заболевание могут указывать мелкий тремор, порывистые беспорядочные движения, передвижение на негнущихся ногах.
Анализ может проводиться через флуоресцентную гибридизацию in situ, метилированием ДНК в области 15q11-q13. Также можно проверить мутации в импринтинговом центре и в гене UBE3A.
Поскольку заболевание обусловлено генетическим нарушением, адекватного и действенного способа лечения для него не имеется. Выполнение лечебных мероприятий, таких, как массаж для больных с гипотонусом, позволяет повысить качество жизни.
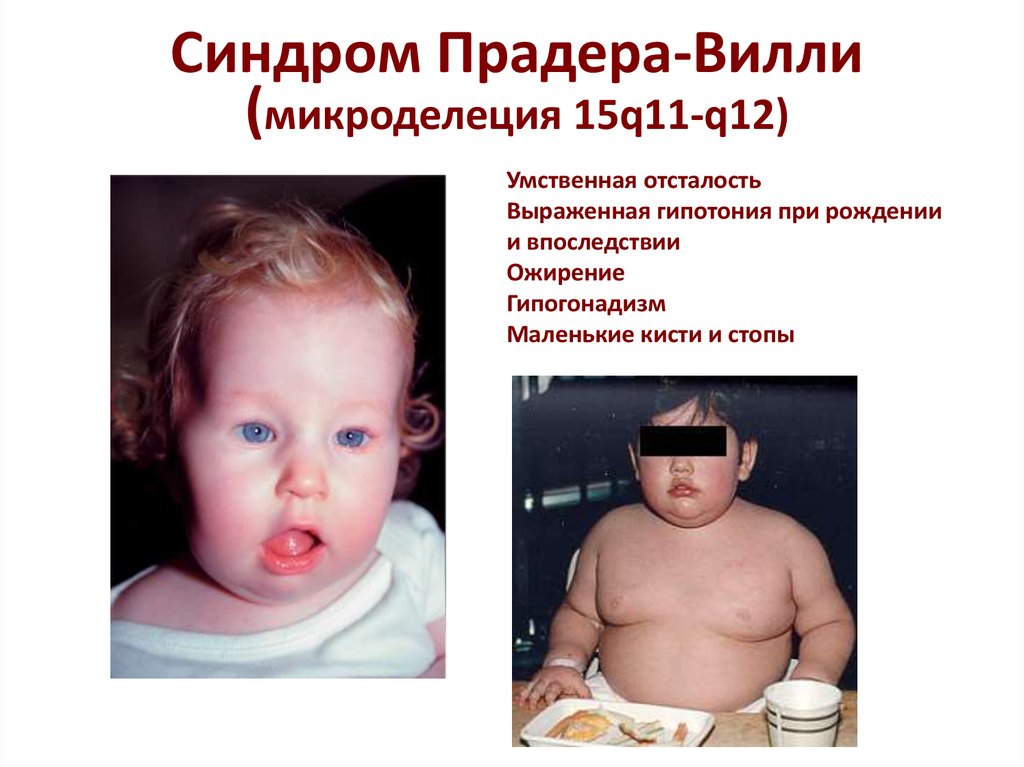
Синдром Прадера-Вилли
Это заболевание определяется той же самой генетической мутацией, что и для синдрома Ангельмана. Отличие состоит в том, что при этом нарушение наследственного материала получается со стороны отца. Кариотип соответствует нормальному (46XX или 46XY). По распространенности (1 случай на 12-15 тысяч новорожденных) примерно совпадает с распространенностью синдрома Ангельмана.
Характерными признаками синдрома Прадера-Вилли являются следующие симптомы:
· в пренатальный период малая подвижность плода;
· часто встречается неверное положение плода;
· возможна дисплазия тазобедреных суставов;
· к двум годам может проявиться склонность много есть (больше нормы), что приводит к ожирению;
· низкий мышечный тонус (гипотонус), сочетающийся с нарушенной координацией движений;
· стопы и кисти обычно маленькие, кроме того характерен невысокий рост;
· формирование косоглазия и сколиоза;
· отмечают повышенную сонливость;
· плотность костей находится на более низком уровне, чем у здоровых людей;
· слюна густая, обычно состояние зубов плохое;
· недостаточная функция половых желез, вызывающая в итоге бесплодие;
· позднее по сравнению со сверстниками половое созревание;
· больные позже учатся говорить, отстают в психическом развитии;
· внешние признаки включают выраженную переносицу, узкий и высокий лоб, миндалевидную форму глаз, узкие губы.
В большинстве случаев у человека с мутацией насчитывается от одного до пяти признаков заболевания.
Диагностика заболевания проводится путем молекулярно-генетического тестирования, на которое направляются дети с пониженным мышечным тонусом. Зачастую вместо верного диагноза определяется более распространенный «синдром Дауна». Опытный генетик, достаточно часто встречающийся с проявлениями синдрома Прадера-Вилли способен диагностировать его по комплексу внешних признаков.
Синдром лиссэнцефалии Миллера — Дикера
При синдроме лиссэенцефалии Миллера – Дикера причиной патологических изменений является делеция некоторых генов в локусе 17p13. При этом больше всего страдает центральная нервная система. Наряду с лиссенцефалией (сглаживание находящихся на поверхности мозга извилин из-за нарушения деятельности гена PAFAH1B1) отмечается сокращение числа кортикальных слоев. Если в норме их насчитывается 6 штук, то у больных можно обнаружить только 4. Сопутствующими признаками является заметное изменение форм лица. Кроме того, больные медленно растут. Попытки интеграции в общество осложняются множественными патологиями сердца, желудочно-кишечного тракта, почек. Если при заболевании происходит делеция гена 14-3-3 эпсилон, то синдром проявляется значительно тяжелее.
Аниридия
При аниридии нарушается нормальное строение глаза: в органе зрения отсутствует радужная оболочка. Кроме того, часто развиваются сопутствующие патологические изменения, такие как макулярная гипоплазия и гипоплазия зрительного нерва, изменения роговицы, катаракта. Острота зрения заметно падает, попытки коррекции не приносят существенных результатов. Развивается светобоязнь и горизонтальный нистагм. В некоторых случаях отмечается появление врожденной глаукомы.
Причиной заболевания является нарушение функционирования гена PAX6 из короткого плеча 11 хромосомы. Кодируемый им белок приводит к запуску ряда процессов, которые управляют процессом правильного формирования органов зрения и ряда других структур. Примечательно, что ген очень консервативен: отличие форм PAX6 у человека и данио рерио составляет менее 5%, несмотря на расхождение эволюционных линий примерно 400 млн лет назад.
Заболевание относится к группе аутосомно-доминантных патологий. В случае гомозиготности по мутантной копии гена PAX6 негативный эффект на организм возрастает, что вызывает множественные нарушения в работе органов зрения. Кроме того, поражается ЦНС, что приводит к летальному исходу.
Лечение направлено на сглаживание симптомов. Для визуальной имитации зрачка рекомендуется использовать специальным образом окрашенные линзы. Возможно восстановление зрачка путем реконструктивной пластической операции.
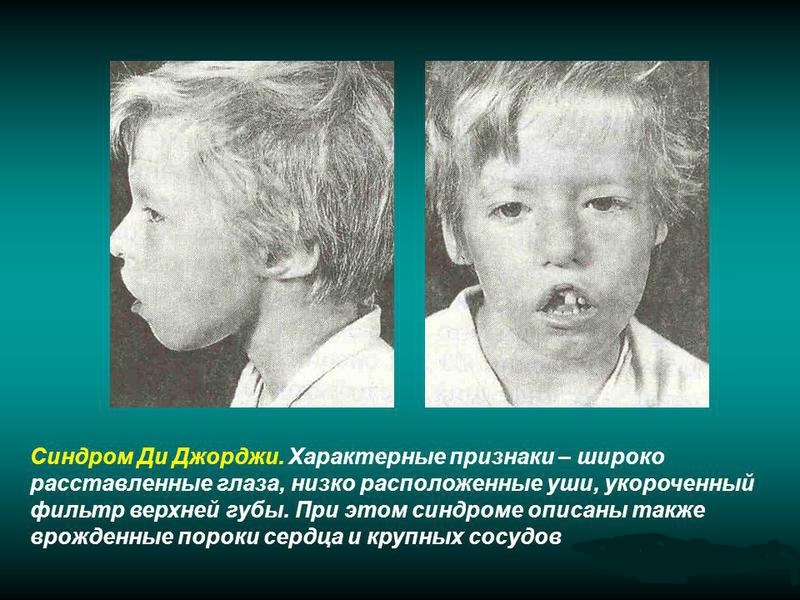
Синдром Ди Джорджи
При синдроме Ди Джорджи у больных отмечается наличие врожденной формы аплазии паращитовидных желез и тимуса. Является разновидностью идиопатического изолированного гипопаратиреоза. Встречается достаточно редко.
При этом заболевании патологические изменения касаются околощитовидных (паращитовидных) желез, у которых отмечается дисгенез или агенезия. Вилочковая железа (тимус) отсутствует от рождения. В результате сочетания таких патологий происходит резкое снижение числа Т-лимфоцитов, формируется иммунологическая недостаточность. Кроме того, этот синдром сопровождается формированием врожденных аномалий крупных сосудов.
Заболевание является аутосомным и определяется наличие мутации в 22 хромосоме. В большинстве случаев причиной является спорадическая делеция 22q11 (реже микроделеция 22q11.2). Наследование происходит по доминантному принципу, с полом не связано. Некоторые авторы не соглашаются с такой характеристикой и приводят аргументы в пользу аутосомно-рецессивного типа, обладающего различной эспрессивностью.
Для заболевания характерно нарушение процесса эмбриогенеза 3-4 жаберных карманов, что приводит к нарушению закладки вилочковой железы и паращитовидных желез.
В клинике наиболее постоянными симптомами являются кандидомикоз и гипопаратиреоз, довольно часто сопровождающиеся нарушением процесса формирования рта, носа и ушей.
Тимус из-за нарушения развития в эмбриональном периоде остается неразвитым. Эпителий тимуса не обеспечивает нормального процесса развития Т-клеток. В итоге формируется специфическая форма иммунодефицита, при которой ослабляется гуморальный иммунный ответ и ответ на клеточном уровне. Если у ребенка имеется подобное патологическое нарушение иммунитета, то он будет обладать повышенной чувствительностью к инфекциям бактериального, вирусного и грибкового происхождения.
Синдром может протекать в форме генетически обусловленного отсутствия паращитовидных желез или изолированной недостаточности околощитовидных желез – в сопровождении гипокальциемических судорог, которые начинаются от рождения. Иммунологическая недостаточность приводит к появлению различных инфекционных заболеваний. Как правило, совокупность симптомов вызывает сердечную недостаточность. Кроме того, летальный исход вызывают инфекционные болезни.
Диагностика синдрома предполагает выявление типичных для синдрома патологий: искажения формы лица и черепа, наличие иммунологической недостаточности, аплазии тимуса, дисгенезии или агенезии паращитовидных желез. Ярче всего при заболевании проявляются кандидомикоз и гипопаратиреоз.
Ретинобластома
Ретинобластомой называют злокачественную опухоль сетчатки глаза. Процесс развития начинается обычно в детском возрасте, причем исходным материалом являются ткани эмбрионального происхождения. Пиковая фаза приходится на двухлетний возраст.
Практически все известные случаи выявляются в течение первых 5 лет жизни.
Причиной заболевания в большинстве случаев является мутация в генетическом материале. При этом необходимо наличие генетической обусловленности за счет наличия мутантной версии гена Rb, полученной по наследству. Вторая мутация, вызывающая появление опухоли, происходит в ретинобласте.
Существует небольшая вероятность, что у родителей, которые переболели ретинобластомой, могут родиться дети с отсутствием патологического изменения.
Отмечаются односторонние и двусторонние случаи ретинобластомы. По статистике для двусторонней формы вероятность наследственного происхождения заметно выше.
Симптомы заболевания включают боль в глазах, свечение зрачка, а также потерю зрения. Выявить их у маленького ребенка очень и очень трудно.
Диагностика обычно проходит в форме обследования под наркозом с применением УЗИ, КТ и МРТ. Достаточно распространенным приемом является биопсия красного костного мозга и спинномозговая пункция. По тяжести симптомов выделяется 5 групп.
Существует два эффективных метода лечения. При криотерапии и фотокоагуляции остается возможность сохранить и зрение, и сам глаз. Осложнения при их использовании возникают редко. Тем не менее, если возникнет рецидив, лечение потребуется повторить в той же форме. Обычно криотерапия используется в случаях, когда поврежден передний отдел сетчатки. Для заднего отдела более предпочтительным вариантом представляется фотокоагуляция.
Важность своевременной диагностики, в том числе пренатальной
Несмотря на минимальные изменения в генетическом материале, микроделеционные заболевания оказываются не менее опасными для здоровья человека, чем масштабные изменения. Поэтому важно вовремя определить наличие потенциально опасных мутаций. Благодаря пренатальной диагностике родители еще до момента родов могут убедиться, что у ребенка отсутствуют тяжелые генетические патологии. Постоянное совершенствование методов диагностики делает эти методы проверки все более эффективными и доступными.