Микроскопический колит что это
Микроскопический колит и синдром раздраженной кишки с диареей: трудности дифференциального диагноза
Микроскопический колит (МК) представляет собой особую форму хронических воспалительных заболеваний кишечника, для которой характерны особые изменения в толстой кишке.
Относительно гистологических изменений выделяют лимфоцитарный колит (наличие значительной инфильтрации слизистой толстой кишки интраэпителиальными лимфоцитами при сохраненной архитектонике слизистой) и коллагеновый колит (утолщение базальной мембраны за счет депозитов коллагена в ней). Доминирующим, а часто и единственным клиническим проявлением у таких больных является диарея без патологических примесей.
Первое описание микроскопического колита было сделано Lindstrom и Freeman в 1976 году, что позволило разграничить данную патологию с инфекционными и заболеваниями кишечника. С тех пор данных о МК получено мало, заболевание продолжает оставаться малоизученным, а причины его возникновения и прогрессирования до конца не выяснены. Возможно, это связано с невысокой распространенностью МК (103, 00 на 100 000 человек, M. Storr et al. Microscopic Colitis: Epidemiology, Pathophysiology, Diagnosis and Current Management—An Update 2013. ISRN Gastroenterol. 2013).
На сегодня разработаны методы терапии, которые позволяют если не излечивать таких больных, то улучшать качество их жизни. В клинической практике одним из самых частых заболеваний, при котором наблюдается диарея без патологических примесей, является синдром раздраженной кишки (СРК). Таким образов, практикующие врачи нередко сталкиваются с необходимостью дифференциального диагноза в случае выявления подобной диареи. Для уточнения и описания различий между МК и СРК во Франции проведено масштабное мультицентровое исследование.
Цели и методы
Целью данного проспективного исследования являлось описание характеристик когорты пациентов с МК и сравнение их с пациентами с СРК с диареей. Проводилось данное исследование в 26 медицинских центрах во Франции. Критериями включение были: диарея без патологических примесей как минимум 3 раза в день, продолжительность заболевания более 3 недель и отсутствие органической патологии при колоноскопии. При этом каждому пациенту выполнялись биопсии из области слепой кишки и всех отделов толстой кишки при колоноскопии, а также проводилась эзофагогастродуоденоскопия с взятием биопсийного материала из желудка и двенадцатиперстной кишки.
Диагноз «лимфоцитарный колит» устанавливался на основании обнаружения более 20% интраэпителиальных лимфоцитов слизистой толстой кишки и «коллагеновый колит» на основании утолщения базальной мембраны более чем 10 микрон за счет депозитов коллагена. Полученные данные были статистически обработаны и сравнены друг с другом.
Результаты
Из включенных в исследование 433 человек, у 129 обнаруживался МК (лимфоцитарный колит у 87 и коллагеновый колит у 42 больных), у 278 исследуемых диагностирован СРК с диареей, вследствие чего они отнесены в контрольную группу. У 26 участников выявлена органическая патология. Диагностическая ценность биопсии была выше в поперечной кишке, при лимфоцитарном колите 96% и коллагеновом колите 98.5%, и ниже в прямой кишке, 83% и 78% соответственно. Прием лекарств отмечен у 53% пациентов с МК, связь с аутоиммунными заболеваниями выявлялась в 34% случаев.
При статистическом анализе существенная разница между группами больных с МК и СРК наблюдалась в таких характеристиках, как: средний возраст (61 г для МК vs. 47 лет для СРК, p
Микроскопический колит
Микроскопический колит (МК) представляет собой редкую форму воспалительного заболевания толстой кишки, для которой характерны особые изменения в толстой кишке.
Этиология заболевания неизвестна. Предполагают, что микроскопический колит развивается в результате взаимодействия нескольких факторов, среди которых определенное значение имеют

Диагноз микроскопического колита можно предположить при наличии водянистой диареи, продолжающейся свыше 4-х недель.
При эндоскопическом исследовании изменения слизистой оболочки обычно не выявляют. Для постановки точного диагноза необходимо проведение гистологического исследования кусочков (биоптатов) слизистой оболочки толстой кишки. На основании изучения гистологических препаратов выделяют лимфоцитарный колит (наличие значительной инфильтрации слизистой толстой кишки интраэпителиальными лимфоцитами при сохраненной архитектонике слизистой) и коллагеновый колит (утолщение базальной мембраны за счет депозитов коллагена в ней).
На сегодняшний день разработаны комплексные методы терапии, позволяющие значительно улучшать качество жизни больных с этим заболеванием. К качестве симптоматического лечения применяют препараты висмута, адсорбенты, антибиотики, топические глюкокортикостероиды.
В Московском клиническом научном центре им. А.С.Логинова лечение больных микроскопическим колитом осуществляется специалистами отдела патологии кишечника.
Не откладывайте свой визит к специалистам нашего Центра. Это поможет своевременно диагностировать заболевание и правильно выбрать тактику лечения. Врачи отдела патологии кишечника ГБУЗ МКНЦ имени А.С.Логинова всегда готовы Вам помочь.
Микроскопический колит: «невидимая болезнь кишечника»
Начнем с краткой истории болезни. Женщина 40 лет, обратилась к гастроэнтерологу клиники «Эксперт» с жалобами на боли в животе, водянистую диарею, неотложность позывов на дефекацию. Данные симптомы беспокоили ее в течение последних 2 лет, за которые пациентка сменила 3-х гастроэнтерологов. Диагноз не установлен, хотя предполагалась и целиакия, и болезнь Крона, и различные изменения кишечной микробиоты. Эти болезни не подтвердились, а колоноскопия (без биопсии!), выполненная трижды в течение 2 лет, не выявила опухолевых и воспалительных изменений в толстой и подвздошной кишке. Отмечался небольшой эффект от приема препаратов висмута и лоперамида.
Врач заподозрил было наличие у пациентки синдрома раздраженного кишечника (СРК), поскольку для этой болезни очень характерны боли в животе и диарея в отсутствии органической патологии кишечника. Однако при тщательном анализе жалоб выяснилось, что боли в животе и нарушения стула преимущественно ночные, вызывающие пробуждение. Такие симптомы обычно заставляются сомневаться в диагнозе СРК и направить диагностический поиск в другую стороны. В частности, на исключение микроскопического колита.
Микроскопический колит (МК) ― хроническое воспалительное заболевание кишечника, которое характеризуется типичной симптоматикой и наличием иммунного воспаления в биоптатах толстой кишки. Это заболевание что называется «не на слуху», однако оно не такое уж редкое: распространенность его достигает 119 случаев на 100 тыс.населения, а заболеваемость (количество новых случаев болезни) в среднем составляет 11,4 на 100 тыс. населения в год. Несмотря на то, что для МК в основном характерен возраст старше 60 лет, примерно в 25% случаев болезнь диагностируется у лиц до 45 лет. МК в детском возрасте встречается, но скорее в виде исключения. Чаще болеют женщины: 52-86% случаев МК у лиц женского пола, женский пол в целом повышает риск развития заболевания в 2,5 и более раз.
В настоящее время термином МК принято обозначать два отдельных заболевания: коллагенозный колит (КК) и лимфоцитарный колит (ЛК). Среди двух разновидностей микроскопического колита КК встречается значительно чаще ― в 2/3 случаев.
Факторы риска развития микроскопического колита
Как уже говорилось выше одним из факторов риска возникновения МК является женский пол. Риск также увеличивается с возрастом: чем он больше, чем вероятность возникновения заболевания выше (для лиц старше 65 лет риск повышается в 5,25 раз).
Прием некоторых лекарственных препаратов ассоциирован с повышенным риском развития МК: ингибиторов протонной помпы (особенно лансопразола), нестероидных противовоспалительных препаратов, статинов, антидепрессантов из группы ингибиторов обратного захвата серотонина, лизиноприла, карбамазепина и ряда других.
Табакокурение ― еще один известный фактор риска, повышающий вероятность возникновения МК в 2,1 раза, при этом курильщики характеризуются более ранним возрастом дебюта болезни (на 10 и более лет).
Причины и механизмы возникновения микроскопического колита
Причины возникновения заболевания до конца не ясны. В настоящее время признается, что МК ― это мультифакторная болезнь с генетической предрасположенностью и участием иммунной системы с развитием воспалительной реакции в ответ на кишечное содержимое.
В настоящее время не описан конкретный ген, ответственный за развитие МК, скорее всего речь идет о комбинации нескольких генетических маркеров. Описаны семейные случаи заболевания, однако нет обязательной передачи МК по наследству.
Клинические проявления (прежде всего водянистая диарея) обусловлены повышенной секрецией воды и электролитов в просвет толстой кишки. У пациентов преобладает секреторный тип диареи, который можно определить специальными исследованиями. Тот факт, что ограничение пищи уменьшает частоту стула у пациентов с МК, свидетельствует о возможном осмотическом компоненте диареи.
Клинические проявления (симптомы) микроскопического колита
Для МК характерны следующие симптомы:
1) Хроническая диарея с частым (5-15 раз в сутки) жидким, нередко водянистым стулом. Диарея обычно развивается постепенно, но в 40% случаев описано внезапное ее появление;
2) Императивность (срочность, неотложность) позывов на дефекацию, характерная для 70% больных;
3) Недержание стула, встречающееся нередко (до 40% случаев);
4) Ночные эпизоды нарушения стула, в т.ч. вызывающие пробуждение больного, характерны для половины лиц с МК;
5) Боли в животе у пациентов с активным МК наблюдаются в 50% случаев
6) Потеря массы тела (встречается у части пациентов из-за снижения потребления пищи и потери жидкости)
Дополнительными (но не обязательными) симптомами могут быть артриты и увеиты.
Лабораторно-инструментальные исследования при микроскопическом колите
Обычно лабораторные тесты не выявляют никаких специфических изменений, характерных только для МК. Тем не менее, у пациентов может отмечаться анемия легкой степени, несколько ускоренная скорость оседания эритроцитов, а также достаточно часто выявляются аутоантитела (антинуклеарные, антинейтрофильные, антитела к Saccharomyces cerevisiae, ревматоидный фактор), не являющиеся диагностическими методами для этой болезни.
Анализ кала на фекальный кальпротектин может быть повышен, однако в настоящее время использование этого «суррогатного» маркера воспаления для контроля обострения и ремиссии МК не рекомендуется. То же самое касается и других фекальных маркеров воспаления.
Колоноскопия обычно показывает нормальную картину слизистой толстой кишки, однако могут встречаться неспецифические изменения в виде отека, покраснения и «смазанности» сосудистого рисунка в разных отделах кишечника. Несмотря на то, что МК ― это болезнь только толстой кишки, при проведении колоноскопии обязателен осмотр подвздошной кишки для исключения других патологий.
Гистологическое исследование ― основной метод для подтверждения диагноза МК, а также для выделения его вида (лимфоцитарный или коллагенозный колит). Во время колоноскопии берутся биоптаты из правых и левых отделов толстой кишки с последующим их исследованием под микроскопом.
Основными гистологическим критериями лимфоцитарного колита при окраске гематоксилин-эозином являются:
Гистологическими признаками коллагенозного колита являются:
Европейские рекомендации по микроскопическому колиту (2020) выделяют также неполный ЛК и неполный КК.
Для неполного ЛК характерны описанные выше гистологические признаки, однако число МЭЛ составляет >10 и менее 20. Толщина субэпителиального коллагенового слоя при неполном КК превышает 5 мкм, но не достигает нужных 10 мкм.
Дифференциальный диагноз
МК следует дифференцировать с такими заболеваниями как болезнь Крона, целиакия, синдром раздраженного кишечника. Для болезни Крона характерны наличие эрозивно-язвенных поражений кишечника, часто повышены маркеры, отражающие наличие системного воспалительного процесса. Целиакия характеризуется наличием атрофическим изменений в тонкой кишке, толстая кишка не вовлечена. Синдром раздраженного кишечника похож по симптоматике на МК, однако наличие ночных симптомов (вызывающих пробуждение пациента) для него не типично.
У лиц с недавно возникшими симптомами следует обязательно исключить острую кишечную инфекцию, а также провести исследования для исключения лямблиоза, гельминтозов и других паразитарных инвазий, инфекции Clostridium (Clostridioides) difficile.
Подтвердить диагноз МК позволяет выявление типичных гистологических признаков в биоптате толстой кишке в сочетании с характерными симптомами.
Лечение микроскопического колита.
Цель лечения – достижение клинической ремиссии, которая определяется как частота стула менее 3 раз в сутки при отсутствии жидкого стула в течение как минимум одной недели. Еще одной целью является улучшение качества жизни пациента с МК.
I. Лечение активной болезни (стул 3 и более раз в сутки или водянистый стул ≥1 раза в день).
А. Общие рекомендации.
1. Отказ от употребления нестероидных противовоспалительных препаратов и (при возможности) от лекарственных средств. для которых установлена возможная связь с МК (см.раздел «Факторы риска»). Отмена терапии возможна только после обсуждения с профильным специалистом при сопоставлении пользы/риска.
2. Отказ от табакокурения.
Б. Симптоматическая терапия. Лоперамид может быть использован в качестве единственной терапии (при слабо выраженных симптомах МК) или в сочетании с базисными препаратами.
В. Базисная терапия.
1. Стероидные гормоны местного (будесонид) или системного (преднизолон, метилпреднизолон) действия.
2. Вспомогательные средства, включающие секвестранты желчных кислот (холестирамин) и препараты висмута. Обычно используются в дополнение к гормональной терапии при ее недостаточной эффективности или отдельно у лиц с непереносимостью стероидных гормонов. целесообразность применения холестирамина обусловлена нередким сочетанием МК с хологенной диареей. Что касается препаратов висмута, их эффективность до сих пор оспаривается, хотя имеются доказательства, что они влияют на частоту дефекаций, консистенцию стула, а также улучшают гистологическую картину слизистой толстой кишки.
3. Иммуносупрессоры (азатиоприн, меркаптопуин) могут быть использованы у лиц с редицидивом после отмены стероидоных гормонов.
4. Генно-инженерная биологическая терапия препаратами из группы ингибиторов фактора некроза опухоли альфа (инфликсимаб, адалимумаб и т.д.) может быть обсуждена у пациентов с тяжелым течением МК и неэффективностью стероидных гормонов.
5. Хирургическое лечение с удалением толстой кишки или наложением илеостомы (у возрастных лиц) может быть обсуждена у лиц с рефрактерным течением МК. При неэффективности базисной терапии следует еще раз пересмотреть диагноз.
II. Поддержание ремиссии МК.
Достижение клинической ремиссии заболевания не является основанием для прекращения терапии, пациенты с МК нередко требуют поддерживающей терапии. В качестве средств поддержания ремиссии рассматриваются топические стероидные гормоны (будесонид) и иммуносупрессоры.
Примечание: препараты 5-аминосалициловой кислоты (месалазин) и пробиотики не доказали своей эффективности в лечении МК.
Течение и прогноз микроскопического колита
МК это хроническое заболевание, для которого характерны периоды обострения и ремиссии. Ремиссия (т.е. неактивная болезнь) может наступить на фоне лечения или самостоятельно, однако отсутствие или прекращение терапии часто приводит к быстрым рецидивам (30-60%).
Несмотря на то, что формально МК относится к заболеваниям кишечника с хроническим воспалительным процессом, он не повышает риск развития рака толстой кишки. Частые рецидивы или наличие персистирующей симптоматики снижает качество жизни пациентов.
Микроскопический колит
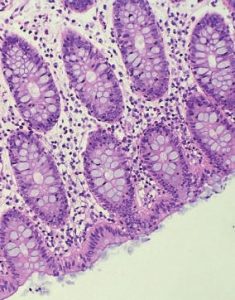
С 1984 года начались исследования в центрах Европы, которые показали увеличение случаев микроскопического колита. Распространенность его стала сопоставима с неспцифическим язвенным колитом и болезнью Крона. При наличии у пациентов хронической диареи наряду с классическими диагностическими признаками необходимо исключать микроскопический колит.
Считается, что это заболевание пожилых людей, чаще женщин, отягощенных различными аутоиммунными заболеваниями такими, как сахарный диабет, тиреоидит (заболевание щитовидной железы) и др.
Симптомы микроскопического колита
Основным клиническим проявлением заболевания является хронический понос без примесей крови, который может носить водянистый характер, приводить к ложным позывам на стул и недержанию кала. Количество дефекаций может быть от 3 и более раз, и в тяжелых случаях до 15 раз в сутки и чаще. Обращается внимание не на частоту стула, а его консистенцию (водянистый стул).
Другими симптомами могут быть боль в животе, дискомфорт, спазм, потеря в массе тела за счет поносов и ограничения приема пищи, что требует исключения целиакии. Клинические признаки наиболее выражены в период обострения заболевания и уменьшаются после лечения.
Микроскопический колит — это морфологический диагноз, гистологические изменения чаще встречаются в правой половине толстой кишки, но не исключаются и другие ее отделы, в связи с чем, при колоноскопии рекомендуется брать биопсию на всем протяжении всей толстой кишки. Различают две гистологические формы микроскопического колита: лимфоцитарный и коллагеновый колит.
Факторы риска микроскопического колита
Микроскопический колит. Лечение
Лечение ставит основной своей целью достижение клинической ремиссии и улучшение качества жизни пациента.
До назначения лекарственной терапии следует отказаться от лекарств, которые, возможно, могут стать причиной микроскопического колита. Уже этот отказ может привести к исчезновению клинических признаков диареи.
Медикаментозное лечение микроскопического колита является трудной клинической задачей. На основании имеющихся в настоящее время доказательств, Европейской группой по изучению микроскопического колита предложен алгоритм ведения пациента с данной болезнью.
При легком течении болезни назначаются антидиарейные средства, такие как лоперамид, который может применяться в виде монотерапии или в сочетании с другими видами лечения.
При активной форме заболевания лечение начинается с применения местного кортикостероида – Буденофалька, который не обладает системным действием и превосходит по своему действию гормоны типа преднизолона. Продолжительность курса 6-8 недель, по 3 мг принимать 2-3 раза в день за 30 минут до еды. Эффект наблюдается через 2-4 недели и далее постепенно препарат отменяется. Пациентам, которые ответили на лечение, возможно назначать короткие курсы или пролонгированное лечение низкими дозами препарата.
При средней тяжести обострения заболевания, если нет эффекта от приема буденофалька, применяются препараты висмута, лоперамид, холестероламин в виде комбинированного лечения или монотерапии.
В процессе разработки и изучения находятся применение биологических препаратов (инфликсимаба), азатиопринна, метотрексата и др.
Таким образом, научные исследования показывают, что микроскопический колит становится распространенным заболеванием. У всех больных при наличии хронической диареи при проведении колоноскопии должна быть взята биопсия для гистологического исследования для подтверждения или исключения микроскопического колита, особенно у пожилых людей. У каждого конкретного больного необходимо провести анализ возможных провоцирующих факторов – лекарственные препараты, инфекции, режим питания, состояние гормонального фона.
Другие уточненные неинфекционные гастроэнтериты и колиты (K52.8)
Версия: Справочник заболеваний MedElement
Общая информация
Краткое описание
2. Эозинофильный колит:
— изолированный эозинофильный колит (проктоколит);
— эозинофильный гастроэнтероколит.
Термином «микроскопические колиты» (МК) обозначают особую форму хронических воспалительных заболеваний кишечника, при которой наблюдается синдром диареи, при этом в слизистой оболочке толстой кишки больных определяются признаки воспаления.
Период протекания
Период протекания более 4 недель
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Этиология и патогенез
В качестве возможных триггерных механизмов развития болезни рассматривают курение и влияние лекарственных веществ.
Эозинофильный колит
Этиология неизвестна. Ранее большое значение в его развитии придавали пищевой аллергии, однако она играет роль менее чем у 20% больных. Часто у них отмечается повышенная концентрация IgE в плазме натощак; прием пищи-аллергена вызывает боль в животе, понос и подъем концентрации IgE. В основном уровень иммуноглобулинов при эозинофильном колите остается в норме, не выявляют каких-либо отклонений и реакция бласттрансформации лимфоцитов, определение уровня комплемента и числа лимфоцитов. Таким образом, возможны два варианта болезни: IgE-зависимый и IgE-независимый.
Эпидемиология
Признак распространенности: Крайне редко
Факторы и группы риска
5. Кишечные инфекции Clostridium difficile, Yersinia enterocolitica, Campylobacter jejuni.
6. Гиперпродукция желчи.
Эозинофильный колит
Клиническая картина
Клинические критерии диагностики
Cимптомы, течение
Микроскопический колит
Признаки
Лимфоцитарный колит
Коллагеновый колит
Длительность диареи (лет)
Средний возраст (лет)
Нормальная эндоскопическая картина
Нормальная рентгенологическая картина
Увеличение содержания межэпителиальных лимфоцитов
Различия
Отношение женщин и мужчин
Частота обнаружения аутоантител
Расширение субэпителиального слоя коллагена
Эозинофильный колит
Симптомы разнообразны и зависят от локализации, степени поражения, возраста. Все проявления сводятся к определенной группе признаков:
— лихорадка (редко);
— потеря веса;
— рвота, тошнота;
— боли в животе, спазмы, вздутие живота;
— кровь в стуле в небольших количествах (редко);
— пальпируемое образование в животе (иногда);
— диарея;
— нарушения сна.
В зависимости от того, какой слой стенки поражен сильнее, выделяют 3 основных клинических варианта течения заболевания:
Диагностика
Микроскопический колит
Программа обследования включает:
Биопсия. Следует брать биоптаты из слизистой оболочки не только сигмовидной ободочной кишки, но и из проксимальных отделов толстой кишки, поскольку именно в указанных отделах выявляются гистологические изменения, свойственные лимфоцитарному колиту.
Эозинофильный колит
Диагностика складывается из:
— тщательно собранного анамнеза (семейный анамнез, связь с приемом пищи);
— выявления сопутствующей аллергической патологии;
— клинической диагностики колита (гастроэнтероколита, проктоколита);
— тестов (клинических и аллергологических);
— инструментальные методы исследования (эндоскопия, биопсия) применяются редко, т.к. диагноз может быть установлен в большинстве случаев клинически.
Тесты
1. Элиминационные диагностические диеты. Простейшим типом элиминационной диеты является исключение из рациона «подозреваемых продуктов» на срок 2-4 недели или дольше. Продолжительность диагностической элиминационной диеты может быть уменьшена до 3-5 дней у детей с ранним клиническим ответом (исчезновением симптомов). При отсутствии подозреваемых аллергенов из рациона исключаются теоретически наиболее значимые пищевые аллергены.
3. Пищевая провокация.
Выбор метода. Двойная слепая, плацебо-контролируемая, оральная провокация с использованием вероятного антигена является идеальным методом для подтверждения развития побочных реакций на пищевые белки, однако такой подход редко используется в клинической практике.
Не слепой метод провокации (когда врач и пациент знают о приеме в пищу потенциального аллергена) может быть использован только в том случае, если симптомы могут быть оценены врачом и пациентом объективно. Использование двойного слепого, плацебо-контролируемого теста возможно, если симптомы по мнению врача являются лишь субъективными.
Информированное согласие. В любом случае пищевая провокация должна выполняться с согласия пациента, т.к. возможны различные реакции со стороны других органов и систем. Эпизоды анафилаксии в анамнезе являются относительным противопоказанием к проведению провокации.
Начальная доза, например, молока должна быть заведомо ниже тех доз, которые могут вызвать реакцию, и должна увеличиваться поэтапно до 100 мл. Сроки появления реакции могут разниться от нескольких часов до нескольких дней. Среднее время между поступлением аллергена и началом проявления отсроченных клинических симптомов составило 13,3 дней (диапазон 4-26 дней). Сильно отсроченные проявления, включая внекишечные (дерматит и пр.), были отмечены лишь у небольшой группы пациентов.
Подготовка: предварительное проведение эффективной элиминационной диеты или достаточно длительное спонтанное уменьшение/исчезновение симптомов.
Оценка результатов. Пищевая провокация была принята в качестве стандартного критерия для диагностики пищевой непереносимости при любом механизме ее развития. Тест считается положительным, если симптомы исчезают после полной элиминации патогенного агента из пищи или если симптомы повторяются в течение 48 часов после провокации. Реакция должна быть воспроизводимой.
Конкретные клинические картины:
1. Энтероколитический синдром:
— Prick-test и RAST, как правило, отрицательны;
— стул, как правило, содержит скрытую кровь, нейтрофилы и эозинофилы;
— при биопсии тощей кишки выявляется атрофия ворсинок и инфильтрация лимфоцитами, эозинофилами и тучными клетками.
2. Колит и проктоколит:
— в анализе кала, как правило, обнаруживаются нейтрофилы;
— эозинофилы могут отсутствовать;
— результаты колоноскопии представлены ниже.
Лабораторная диагностика
Эозинофильный колит
При обследовании могут отмечаться анемия, гипопротеинемия, снижение содержания витаминов и микроэлементов, изменение показателей пробы с D-ксилозой.
У 60%-80% пациентов выявляется эозинофилия.
Исследование кала на эозинофилы. Выявление эозинофилов в кале является важным ключом к диагностике аллергического колита. Однако после обострения в кале могут преобладать лимфоциты и нейтрофилы с небольшим количеством эозинофилов. В кале иногда удается обнаружить кристаллы Шарко-Лейдена.
Дифференциальный диагноз
Дифференциальную диагностику микроскопического колита следует проводить с синдромом раздраженного кишечника, целиакией, болезнью Крона, неспецифическим язвенным колитом, гипотиреозом. Исключают инфекционные колиты, лямблиоз, ишемический колит. Выясняют, употреблял ли больной слабительные препараты.
При дифференциальной диагностике эозинофильного гастроэнтерита и колита требуется исключение заболеваний, протекающих с эозинофилией и аналогичной гистологической картиной (болезнь Крона, коллагенозы, злокачественные новообразования, паразитарные инвазии). Наибольшие трудности представляет дифференциация эозинофильного гастроэнтерита с болезнью Крона, лимфомой кишечника и узелковым периартериитом.
Осложнения
— анемия;
— обезвоживание;
— гиповитаминозы.
Лечение
Микроскопический колит
Общие положения
Лечение направлено на снижение воспаления и симптомов диареи и по сути является эмпирическим (метод «проб и ошибок»), так как каждый случай индивидуален. При адекватно подобранной терапии, большинством симптомов можно управлять. Однако когда лечение заканчивается, симптомы обычно появляются вновь. Большинству пациентов, следовательно, необходимо постоянное лечение чтобы контролировать симптомы. Случаются спонтанные длительные ремиссии.
Поскольку единого мнения по терапии микроскопического колита не существует, ниже приводятся различные мнения.
Диета
1. Конкретных диет не существует. Пищевые продукты, содержащие кофеин, или лактоза должны быть исключены из рациона, так как они стимулируют секрецию жидкости в толстой кишке. Если пациент не в состоянии переваривать жиры, низкое содержание жиров в рационе может быть полезным. Следует избегать приема НПВП (ибупрофен и пр.), так как исследования показали, что они могут быть связаны с коллагеновым колитом. Однако прием парацетамола (ацетаминофен) является допустимым.
Лекарственные препараты
Субсалицилат висмута назначается для лечения коллагеновых колитов курсом 8 недель, в среднем по 8 таблеток в сутки. Эффективность препарата имеет доказательства в исследованиях.
Мезаламин (асакол) также может быть эффективным для лечения хронической диареи, связанной с коллагеновым колитом. Назначается курсом до 6 месяцев. Некоторыми авторами он рассматривается как «препарат первой линии».
Холестирамин чаще всего назначают для лечения высокого уровня холестерина в крови, но этот препарат также может быть использован для уменьшения диареи в случаях коллагенового колита. Холистирамин выпускается в виде порошка, который смешивается с водой. Как правило, препарат применяют в низкой дозе от 1/2 до 1 пакетика в день. Отмечается достаточно хороший эффект холистирамина в низких дозах, чтобы остановить эпизоды водянистой диареи, особенно те, которые возникают после еды. В более высоких дозах холестирамин может вызвать запор (в этих случаях требуется снижение дозы). Кроме того холестирамин может уменьшить всасывание других препаратов, принятых с ним в одно и тоже время. Дополнительной выгодой от лечения может быть снижение холестерина в крови.
Не существует никаких доказательств эффективности других методов лечения, таких как: экстракт босвеллии пильчатой (индийское ладанное дерево), пробиотиков и прочих препаратов и веществ.
Терапия антибактериальными препаратами не оправдала надежд в связи с быстрым возвращением симптомов и высоким риском побочных эффектов.
Один из возможных алгоритмов терапии выглядит следующим образом:
— Первая линия терапии: лоперамид (имодиум) или дифоксилат/атропин (lomotil) для легкой диареи.
— Вторая линия терапии: висмут субсалицилат 2-3 табл. 3-4 раза в день, в течение 1-2 месяцев (эффективно у 90% больных); мезаламин 3 г/сутки в течение 8 недель или холестирамин (особенно, если нарушение всасывания желчных кислот подтверждено документально) при средней дозе до 8 г/сутки при умеренной клинике.
— Третья линия терапии. Если пациент по-прежнему не отвечает на терапию или если у пациента клинически более тяжелый колит, рекомендуется 6-недельный курс будесонида в минимальной эффективной дозе (обычно 9 мг каждое утро) или 2-недельный курс высоких доз преднизолона (60-80 мг/сутки). Курсы будесонида предпочтительнее вследствие меньшего побочного эффекта. Рецидивы, возникающие после прекращения приема будесонида, обычно лечатся возобновлением приема этого же лекарства.
Более длинные курсы преднизолона (до 2 месяцев) могут быть необходимы у некоторых пациентов, рефрактерных к терапии, но рецидивы встречаются и после ее прекращения.
— Четвертая линия. В некоторых упорных случаях может быть эффективен азатиоприн (около 2 г/кг/сутки) или 6-меркаптопурин, но ответ на такую терапию может возникать часто только через несколько месяцев. Метотрексат является альтернативным препаратом.
У пациентов, отвечавших на лечение, но испытывающих рецидивы, часто бывают эффективны ранее использованные и показавшие себя лекарства.


