Многоузловой эутиреоидный зоб 1 степени что
Диффузный эутиреоидный зоб
терапевт / Стаж: 18 лет
Дата публикации: 2019-03-27
гинеколог / Стаж: 27 лет
Поскольку продуцирование гормонов щитовидной железой не нарушается, то заболеванию дали ещё одно название —диффузный нетоксический зоб, который превышает допустимую норму размеров щитовидной железы, которая у мужчин составляет 25 мл, а у женщин — 18 мл.
При частоте заболевания в регионе проводимых обследований среди детей младшего и среднего школьного возраста превышающей 5% зоб считают эндемическим. Диффузный эутиреоидный зоб является патологией молодой части населения и развивается он до 20-летнего возраста в более чем 50% случаях, при этом поражая женщин в 2-3 раза чаще, чем мужчин, особенно в периоды повышенной потребности организма в йоде — во время полового созревания, вынашивания ребенка и кормления его грудью.
Диффузный нетоксический зоб преимущественно развивается на фоне йододефицита, когда щитовидная железа претерпевает компенсаторную гиперплазию для восполнения дефицита тиреоидных гормонов.
Напрямую на рост тканей щитовидной железы влияют аутокринные факторы, стимулирующие тиреоциты: фибробластный, эпидермальный и трансформирующий факторы роста.
Кроме недостаточного количества йода в рационе, ДЭЗ провоцирует прием специфических лекарственных препаратов, курение табака, наличиедлительного стрессового состояния и инфекционного заболевания, нерациональное питание с дефицитом жизненно важных микроэлементов, отвечающих за метаболизмйода, а также врожденные дефекты некоторых ферментов, возраст, пол и предрасположенность к заболеванию пациента.
Классификация диффузного эутиреоидного зоба
ДЭЗ в практической медицине наиболее часто классифицируется на базе макроскопических изменений щитовидной железы, точнее всего характеризуемых в процессе УЗИ щитовидки при расчёте ее объема и оценке размера узловых образований.
В эндокринологии выделены:
Исходя из этиологии заболевания, отмечают:
Согласно рекомендациям ВОЗ,степень выраженности зоба оценивается в процессе пальпирования по критериям:
Прогноз и профилактика диффузного эутиреоидного зоба
В большинстве случаев с помощью этиотропного лечения объем щитовидной железы удается нормализовать. У части пациентов на фоне ДЭЗ формируются узловые образования с функциональной автономией.
Пациенты с диффузным эутиреоидным зобом старше 45-50 лет должны находиться под динамическим наблюдением эндокринолога, ежегоднопроходить УЗИ щитовидной железы и контролировать уровень ТТГ.
Профилактика ДЭЗ бывает массовая и индивидуальная.
Массовая профилактика предполагает употребление в пищу йодированной соли, продуктов, насыщенных йодом, — морской капусты, морской рыбы и др. морепродуктов, грецких орехов, хурмы и прочих.
Индивидуальная профилактика представляет собой специальный приём препаратов йода лицами из групп риска развития диффузного эутиреоидного зоба: беременным, проживающим в обедненных йодом регионах, пациентам после операции щитовидной железы и др. Для профилактики спорадических случаев ДЭЗ необходимо ограничение и исключение струмогенных факторов.
Причины диффузного эутиреоидного зоба
Наиболее значимой причиной возникновения диффузного эутиреоидного зоба является недостаток йода, поступающего в организм с водой и пищей. Гиперплазия щитовидной железыв связи с этим —это защитная реакция организма, направленная на сохранение гомеостаза тиреоидных гормонов железы в условиях недопоступления йода извне, то естьщитовидная железа приспосабливается к условиям йодного дефицита.
Благодаря усилению активного захвата йода тиреоцитами начинается увеличенное синтезирование трийодтиронина, для продуцирования которого требуется только 3 атома йода.Кроме того, форсируется повторная переработка эндогенного йода, что умножает эффективность синтеза тиреоидных гормонов. Хотя адаптационные механизмы щитовидной железы регулируются и контролируются тиреотропным гормоном гипофиза (ТТГ), при диффузномнетоксичном зобе его повышение почти не заметно. Современные представления таковы, что при дефиците йода влияние ТТГ (тиреотропного гормона) на щитовидную железу также обусловлено аутокринными факторами роста.
На начальном этапе заболевания отслеживается компенсаторное увеличение тироцитов и вследствие этого развивается паренхиматозный зоб (характерный для детского и подросткового возраста), когда щитовидная железа состоит из множества мелких фолликулов, практически лишенных коллоида.
Больные пожилого возраста и пациентыс прооперированной железой страдают коллоидным зобом, морфологически представляющим собой ткань железы из крупных фолликулов, заполненных желеобразным веществом. Вследствие такого преобразования в тканях щитовидной железы прослеживается сбой процессов синтеза и распада тиреоглобулина, снижение степени его йодирования. Также наблюдается снижение продукций одтиронинов и йодлипидов.
Другими причинами развития диффузного эутиреоидного зоба считаются:
Симптомы диффузного эутиреоидного зоба
При отсутствии дисфункции щитовидной железы при диффузном эутиреоидном зобе клинические проявления практически не выявляются.
Иногда могут беспокоить:
Осложнения диффузного эутиреоидного и других форм зоба наблюдаются при существенной гипертрофии щитовидной железы и выражаются:
Довольно часто диффузный нетоксический переходит в узловой, эутиреоидный или токсический зоб.
Диагностика диффузного эутиреоидного зоба
Для диагностирования диффузного эутиреоидного зоба используются весьма простые методы, доступныев широкой клинической практике, когда достаточно:
Лечение диффузного эутиреоидного зоба
Лечение диффузной нетоксической формы зоба начинается, как правило, с определения степени гиперплазии щитовидной железы и причин её роста.
При подтверждении йододефицитной природы заболевания проводится монотерапия препаратами йода. Для уменьшения размера зоба и поддержания эутиреоза применяется заместительная терапия левотироксином (Эутирокс).
Зоб нулевой степени не требует активного лечения, достаточно только динамического наблюдения эндокринолога за состоянием щитовидной железы пациента с контролем уровня гормонов.
ДЭЗ первой степени с подтвержденной йодной недостаточностью у детей, подростков и молодых взрослых лечится препаратами йода (калия йодид в суточной дозировке до 200 мкг) в течение полугода, тогда чаще всего размеры железы нормализуются благодаря подавлению роста тироцитов.
При отсутствии положительных результатов в течение полугода для уменьшения размера железы и поддержания эутиреоза применяют заместительную терапию левотироксином (L-Т4).
Зобу второй степени требуется комбинированная терапия из 200 мкг йодсодержащего препаратами и 150 мкг гормона железы — левотироксина (Йодокомб, Йодотирокс, Левотироксин натрия с йодидом калия).
Когда зоб достиг больших размеров, или развились осложнения (компрессия, кровоизлияние), проводится оперативное лечение.
Альтернативным методом лечения диффузного эутиреоидного зоба служит терапия радиоактивным йодом-131, с помощью которой достигается уменьшение объема щитовидной железы на 40-50 % уже после однократного введения изотопа.
Любой из вариантов коррекции ДЭЗ предполагает дальнейшие профилактические мероприятия, одним из которых является использование йодированной соли при приготовлении пищи.
Введите ваши данные, и наши специалисты свяжутся с Вами, и бесплатно проконсультируют по волнующим вас вопросам.
Узловой зоб у взрослых
Общая информация
Краткое описание
Российская ассоциация эндокринологов
Год утверждения: 2016 (пересмотр каждые 3 года)
Нетоксический зоб — заболевание, характеризующееся диффузным или узловым увеличением щитовидной железы без нарушения ее функции.
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
• 2 степень — зоб четко виден при нормальном положении шеи.
Этиология и патогенез
Несомненно, что все реакции адаптации стимулируются и контролируются тиреотропным гормоном (ТТГ). Однако, как было показано во многих работах, уровень ТТГ при диффузном нетоксическом зобе (ДНЗ) не повышается. В ходе ряда исследований in vivo и in vitro были получены новые данные об ауторегуляции щитовидной железы йодом и аутокринными ростовыми факторами. По современным представлениям, повышение продукции ТТГ или повышение чувствительности к нему тиреоцитов имеет лишь второстепенное значение в патогенезе йододефицитного зоба. Основная роль при этом отводится аутокринным ростовым факторам, таким как инсулиноподобный ростовой фактор 1 типа, эпидермальный ростовой фактор и фактор роста фибробластов, которые в условиях снижения содержания йода в щитовидной железе оказывают мощное стимулирующее воздействие на тиреоциты. Экспериментально было показано, что при добавлении в культуру тиреоцитов калия йодида (КI) наблюдалось снижение ТТГ-индуцируемой цАМФ (циклический аденозинмонофосфат) — опосредованной экспрессии мРНК инсулиноподобным ростовым фактором 1 типа, с полным ее прекращением при значительном увеличении дозы калия йодида.
Хорошо известно, что йод сам по себе не только служит субстратом для синтеза тиреоидных гормонов, но и регулирует рост и функцию щитовидной железы. Пролиферация тиреоцитов находится в обратной зависимости от интратиреоидного содержания йода. Высокие дозы йода ингибируют поглощение йода, его органификацию, синтез и секрецию тиреоидных гормонов, поглощение глюкозы и аминокислот. Йод, поступая в тиреоцит, вступает во взаимодействие не только с тирозильными остатками в тиреоглобулине, но и с липидами. Образованные в результате этого соединения (йодолактоны и йодальдегиды) служат основными физиологическими блокаторами продукции аутокринных ростовых факторов. В щитовидной железе человека идентифицировано много различных йодолактонов, которые образуются за счет взаимодействия мембранных полиненасыщенных жирных кислот (арахидоновой, докозогексаеновой и др.) с йодом в присутствии лактопероксидазы и перекиси водорода.
Эпидемиология
Диагностика
Нетоксический зоб небольших размеров обычно протекает бессимптомно. Как правило, зоб — случайная находка.
В условиях умеренного и тяжелого йодного дефицита зоб может достигать больших размеров и явиться причиной развития компрессионного синдрома с появлением жалоб на затруднение дыхания и глотания, а также косметического дефекта шеи. На фоне узлового и многоузлового зоба в дальнейшем также может сформироваться функциональная автономия щитовидной железы, которая служит одной из основных причин развития тиреотоксикоза в йододефицитных регионах.
Важно отметить, что не всегда определяемые пальпаторно размеры ЩЖ совпадают с истинными, например, по причинам низкого расположения самой ЩЖ или загрудинного зоба. Пальпация ЩЖ должна сопровождаться пальпаторным исследованием шейных лимфатических узлов.
Уровень убедительности рекомендаций D. Уровень достоверности доказательств 4.
Наиболее специфичными признаками, позволяющими заподозрить метастатическое поражение лимфоузла, являются микрокальцинаты, кистозный компонент, периферическая васкуляризация, сходство ткани лимфоузла с тканью ЩЖ; менее специфичными – увеличение размеров, закругленность контуров, отсутствие ворот.
Комментарии: После пункции измененного лимфоузла игла промывается физиологическим раствором, пробирка с которым отправляется в лабораторию для определения тиреоглобулина или кальцитонина. Для метастатического поражения лимфоузлов характерна очень высокая концентрация этих гормонов в смыве из иглы (обычно более 1000 нг/мл или пг/мл).
Также показанием к проведению сканирования является эктопия щитовидной железы, которую обычно выявляют в раннем детском возрасте.
Эутиреоидный узловой коллоидный зоб
Зоб – стойкое увеличение щитовидной железы, не связанное с ее воспалением.
Коллоидный узловой зоб- это увеличение щитовидной железы за счет образования узлов, содержимым которых является коллоид (др.-греч. κόλλα — клей + εἶδος — вид; «клеевидные» – гомогенная масса, без содержания в ней тиреоидных клеток. По данным ВОЗ (Всемирной организации здравоохранения) в настоящее время более 200 млн человек во всём мире поражены эутиреоидным узловым зобом. Соотношение количества мужчин и женщин, у которых обнаружен коллоидный эутиреоидный узловой зоб, равен 1:8. Это заболевание возникает вследствие дефицита йода в детском и подростковом возрасте, также существует наследственная предрасположенность к развитию эутиреоидного зоба. Узловой коллоидный зоб может проявляться как нарушением функций щитовидной железы (гипотиреоз, или гипертиреоз), так и нарушением её структуры и размеров. Под нормальным размером щитовидной железы всегда следует иметь в виду истинный размер щитовидной железы (выраженный в мл или см 3 ), определённый с помощью УЗИ. ВОЗ выделяет следующие степени увеличения щитовидной железы: 1) 0 — зоба нет; 2) I — зоб небольших размеров; 3) II — зоб большой.
Термин «эутиреоидный узловой зоб» – понятие собирательное, включающее в себя следующую патологию щитовидной железы: коллоидные узлы (многоузловой зоб), аденому щитовидной железы, а также рак щитовидной железы. У пациентов с таким заболеванием не обнаруживают ни клинических, ни лабораторных признаков тиреотоксикоза (повышение уровня гормонов щитовидной железы) или гипотиреоза (снижение функций щитовидной железы).
Выделяют диффузную, узловую (многоузловую) и смешанную форму эутиреоидного коллоидного зоба. Диффузная форма более распространена в подростковом возрасте или при беременности, в то время как узловая форма — у лиц наиболее старшего возраста.
Многоузловой коллоидный эутиреоидный зоб
Клиническая картина складывается из жалоб пациента и данных объективного исследования.
Жалобы. Клиническая картина обычно бессимптомна, небольшие узлы можно выявить на диспансерном осмотре у врача, когда он «ощупывает» шею или во время УЗИ шеи. Однако при значительном увеличении размеров щитовидной железы более 50 мл могут появиться так называемые компрессионные симптомы, т.е. крупный зоб может приводить к затруднению дыхания или глотания вследствие сдавления пищевода или трахеи (эти симптомы следует отличать от невротического ощущения «кома в горле»). Иногда возникает местная болезненность вследствие кровоизлияния в узел.
Объективное исследование позволяет при осмотре выявить увеличение щитовидной железы различной степени выраженности, и это должно быть подтверждено данными инструментальных исследований (главным образом, УЗИ). При этом, осмотр щитовидной железы, являясь основным методом клинического исследования органа, не позволяет точно определить её объём и имеет лишь вспомогательное значение. В норме щитовидная железа пальпируется в большинстве случаев; у молодых девушек с тонкой шеей она может быть даже видна. Трудности могут возникать при обследовании мужчин с развитой шейной мускулатурой. Существуют характерные ультразвуковые признаки различных заболеваний, протекающих с узловым зобом, но их диагностическая чувствительность и специфичность не высока. Поэтому, при выявлении пальпируемого узлового образования и/или превышающего по данным УЗИ 1 см в диаметре, пациенту показано проведение пункционной тонкоигольной аспирационной биопсии (ПТАБ). Проведение ПТАБ при случайно выявленных образованиях меньшего размера целесообразно только при подозрении на злокачественную опухоль ЩЖ по данным УЗИ. Проведение ПТАБ необходимо под контролем УЗИ независимо от пальпаторных данных, что существенно увеличивает информативность исследования. В настоящее время ПТАБ является одним из самых эффективных методов дифференциальной диагностики доброкачественных и злокачественных поражений ЩЖ. Точность этого метода целиком зависит от квалификации специалистов, принимающих участие в выполнении манипуляции и цитологическом исследовании полученных пунктатов. ПТАБ наряду с определением уровня ТТГ крови используют в качестве первого диагностического метода у больных с выявленными узловыми образованиями в ЩЖ для получения цитологического диагноза и оценки уровня клинического подозрения о злокачественности. ПТАБ не имеет каких-либо существенных осложнений.
Лабораторная диагностика основана на определении уровня ТТГ. Если он находится в пределах нормы, то пониженную или повышенную функцию ЩЖ можно исключить. При отклонении от нормальных значений следует определять уровни свободных Т4 и Т3. При снижении уровня ТТГ после исключения диффузного токсического зоба регистрируют функциональную автономию щитовидной железы. Увеличение уровня ТТГ свидетельствует о развитии гипотиреоза.
Лечение
Подавляющее большинство узлового коллоидного зоба, без нарушения функции ЩЖ, имеет небольшой размер, не представляющий угрозу здоровью человека. Их патологическое значение для организма зачастую сомнительно. Особенно это касается мелких, случайно выявленных узлов. Следовательно, при выявлении узлового (многоузлового) коллоидного пролиферирующего зоба активное медикаментозное(при нормальных значениях уровня ТТГ, Т4 св.) и, тем более, инвазивное вмешательство (операция), в большинстве случаев, не показаны. Динамическое наблюдение таких пациентов подразумевает периодическую (1 раз в год) оценку функции ЩЖ и УЗИ.
Патологическое значение узлового коллоидного пролиферирующего зоба определяется:
Исходя из патологического значения, можно выделить следующие показания к хирургическому лечению узлового коллоидного зоба:
Оптимальный объем оперативного вмешательства должен основываться на характере морфологических изменений ЩЖ. Морфологически при узловом коллоидном зобе процесс узлообразования не ограничивается каким-нибудь определенным участком ЩЖ. Помимо видимых узлов в тиреоидной ткани существуют т.н. зобные изменения, что и служит морфологической основой для появления новых коллоидных узлов. Именно этот морфологических факт и объясняет высокую частоту рецидивов узлового коллоидного зоба после органосохраняющих операций и экономных резекций.
Сохранение или оставление большого участка тиреоидной ткани при удалении многоузлового коллоидного зоба с целью сохранить гормонпродуцирующую функцию ЩЖ неизбежно может привезти к рецидиву.
Оптимальный объем оперативного вмешательства при узловом коллоидном зобе и двухстороннем поражении обеих долей ЩЖ – тиреоидэктомия, при одностороннем поражении – гемитиреоидэктомия.
Традиционно такие операции выполняются «открытым» способом, т.е. доступ к щитовидной железе осуществляется через разрез на шее. После удаления щитовидной железы рана ушивается косметическим швом. В настоящее время в мире активно развиваются методики эндоскопических и видеоассистированных операций на щитовидной железе. Они позволяют достичь отличных косметических результатов, не оставляя рубцов на шее пациента.
В нашей клинике осуществляются методы традиционного доступа к щитовидной железе, а также видеоассистированные вмешательства из срединного шейного доступа и эндоскопические (без разрезов на шее).
Лечение эутиреоидного зоба
Опубликовано в журнале:
Клиницист № 3’2007
В.В. Фадеев
ФГУ Эндокринологический научный центр росмедтехнологий, Москва
Контакты: Валентин Викторович Фадеев walfad@nccom.ru В статье кратко суммированы современные представления о патогенетической терапии эутиреоидного зоба. Рассматриваются преимущества, недостатки и потенциальная эффективность монотерапии препаратами йода, супрессивной терапии препаратами левотироксина и комбинированной терапии препаратами йода и левотироксина. Описываются принципы послеоперационной профилактики рецидива зоба.
Ключевые слова: эутиреоидный зоб, левотироксин, препараты йода
Treatment for euthyroid goiter
V.V. Fadeyev
Endocrinology Research Center, Russian Medical Technology Agency The paper briefly summarizes the present views of pathogenetic therapy for euthyroid goiter. It considers the advantages, disadvantages, and potential efficiency of monotherapy with iodines, suppressive therapy with levothyroxine, and combined therapy with iodines and levothyroxine. The principles of postoperative prevention of recurrent goiter are described.
Key words: euthyroid goiter, levothyroxine, iodines.
Определение зоба
Зобом обозначается увеличение щитовидной железы (ЩЖ). В соответствии с принятыми на сегодняшний день нормативами увеличенным считается объем ЩЖ, измеренный при УЗИ, более 18 мл у женщин и 25 мл у мужчин [1]. Общепринятые клинически адаптированные референтные объемы ЩЖ для детей на сегодняшний день отсутствуют, поскольку предлагаемые ВОЗ нормативы, которые учитывают площадь поверхности тела ребенка, рекомендованы только для эпидемиологических исследований, в который распространенность зоба у детей рассматривается как косвенный показатель напряженности йодного дефицита.
Наиболее частым вариантом зоба является эутиреоидный зоб, т.е. протекающий на фоне нормальной функции ЩЖ. В ряде случаев эутиреоидный зоб обозначается термином «нетоксический», но такое определение использовать менее предпочтительно.
Этиология и патогенез эутиреоидного зоба
Наиболее частой причиной эутиреоидного зоба является дефицит йода, который определяется на всей территории России [1]. В эндемичных регионах с йодным дефицитом связано около 90—95% случаев увеличения ЩЖ; у детей — до 99%. Давид Марин впервые в начале ХХ века научно обосновал связь между йодным дефицитом и гиперпластическими процессами в ЩЖ. Он впервые обнаружил зависимость между объемом ЩЖ и содержанием в ней йода, а также описал гистологические изменения, характерные для эндемического зоба.
После того как была описана регуляция ЩЖ гипоталамо-гипофизарной системой, в частности отрицательная обратная связь между продукцией ТТГ и Т4, в экспериментах на животных было показано, что искусственно смоделированный тяжелейший йодный дефицит приводит к повышению уровня ТТГ и образованию зоба. В соответствии с этим была выдвинута теория, согласно которой ТТГ оказывает не только специфическое стимулирующее воздействие на ЩЖ, но и обусловливает ее увеличение, а сам ТТГ стал расцениваться как основной трофический стимулятор ЩЖ. Тем не менее по данным многих работ, у лиц, проживающих в регионах с нормальным йодным обеспечением, а также умеренным и легким дефицитом йода, уровень ТТГ существенно не отличается; он повышается лишь при тяжелейшем йодном дефиците, который встречается относительно редко. В связи с этим формирование зоба стали объяснять повышением чувствительности ЩЖ к эффектам ТТГ в условиях йодного дефицита. Вплоть до последних 20 лет эта концепция абсолютно доминировала и определяла основной подход к лечению зоба — супрессивную терапию препаратами левотироксина (L-Т4), направленную на подавление эндогенной продукции ТТГ. Уже первые проспективные и рандомизированные исследования показали, что использование для лечения йододефицитного зоба препаратов йода оказалось сопоставимо по эффективности, а с другой стороны, по сравнению с супрессивной терапией L-Т4, назначение препаратов йода приводило к значительно более стойкой стабилизации объем ЩЖ [2] (см. таблицу).
Таблица
Результаты клинических исследований, оценивающих различные схемы лечения эутиреоидного йододефицитного зоба
| Автор (год) | Пациенты | Дозы, мкг/сут | Уменьшение объема ЩЖ, % | |||||
|---|---|---|---|---|---|---|---|---|
| n | Возраст | L-T4 | KJ | L-T4 + KJ | L-T4 | KJ | L-T4 + KJ | |
| P. Schumm (1983) | 53 | 14—35 | 100 | 130 | 100 + 130 | 20 | 30 | |
| T. Olbricht (1985) | 39 | 18—63 | 100 | 500 | 28 | 22 | ||
| B. Leisner (1985) | 55 | 5—17 | 100 | 37 | ||||
| P. Pfannenstiel (1988) | 74 | 28,1±7,5 | 150 | 100 + 100 | 25 | 30 | ||
| G. Hintze (1989) | 166 | 30—60 | 150 | 400 | 75 + 200 | 32 | 38 | 38 |
| A. Hotze (1989) | 82 | 18—31 | 100 | 100 + 100 | 24 | 40 | ||
| D. Einenkel (1992) | 30 | 13—15 | 100 | 150 | 50 + 100 | 42 | 52 | 51 |
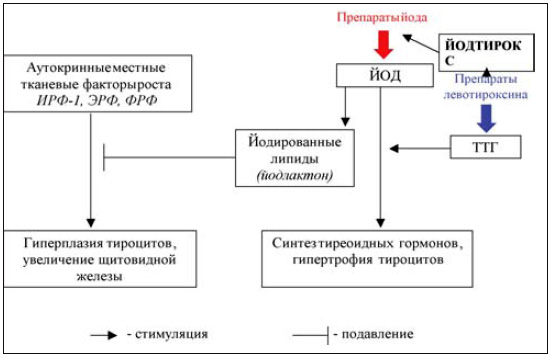
Кроме того, эту концепцию подтвердили результаты ряда исследований in vitro и in vivo, в которых были получены новые данные об ауторегуляции ЩЖ йодом и аутокринными ростовыми факторами (АРФ) [3]. По современным представлениям, повышение продукции ТТГ или повышение чувствительности к нему тироцитов не имеет первостепенного значения в патогенезе йододефицитного зоба (рис. 1). Основную роль в этом плане отводят АРФ, в частности, инсулиноподобному ростовому фактору 1-го типа (ИРФ-1), эпидермальному ростовому фактору (ЭРФ) и фактору роста фибробластов (ФРФ), которые в условиях снижения содержания йода в ЩЖ оказывают мощное стимулирующее воздействие на тироциты. Основным физиологическим блокатором продукции АРФ является йод, связанный с непредельными жирными кислотами (йодлактоны). В экспериментальных работах было показано, что аутокринная продукция тироцитами ИРФ-1 может быть полностью блокирована йодом [3]. Более того, рост изолированных интактных фолликулов ЩЖ, содержащих достаточное количество йода, не удается простимулировать введением ТТГ, а при блокаде рецепторов ИРФ-1 специфическими антителами ТТГ не способен оказать трофические эффекты на тироциты.
Рис. 1. Патогенез и лечение эутиреоидного зоба
Естественное течение йододефицитного зоба
Диффузный эутиреоидный зоб — самое частое, но при этом самое безобидное и легко излечимое заболевание ЩЖ. Сам по себе небольшой эутиреоидный зоб на момент постановки диагноза не несет никакой опасности. Опасность для здоровья человека диффузного эутиреоидного зоба определяется риском дальнейшего прогрессирования йододефицитной патологии ЩЖ. Первым этапом прогрессирования является диффузное увеличение ЩЖ без нарушения ее функции. В зависимости от выраженности йодного дефицита диффузный зоб может формироваться у 10—80% населения. Отдельные клетки ЩЖ оказываются более чувствительными к стимуляции АРФ, в результате чего получают преимущественный рост. Так формируется узловой и многоузловой эутиреоидный зоб. На очередном этапе описанные компенсаторные процессы приобретают патологическое значение. В отдельных активно делящихся тироцитах начинают запаздывать репаративные процессы, в результате чего накапливаются мутации, среди которых наибольшее клиническое значение имеют так называемые активирующие; в результате этих мутаций дочерние клетки приобретают способность автономно, т.е. вне регулирующих эффектов ТТГ, продуцировать тиреоидные гормоны. Конечным этапом естественного морфогенеза йододефицитного зоба является узловой и многоузловой токсический зоб [4]. Этот процесс занимает многие десятилетия, вследствие этого узловой и многоузловой эутиреоидный и токсический зоб наиболее часто встречается у лиц пожилого возраста. По данным многих эпидемиологических исследований, одной из наиболее серьезных проблем легкого и умеренного йодного дефицита является высокая заболеваемость многоузловым и узловым токсическим зобом в старшей возрастной группе.
Консервативное лечение йододефицитного зоба
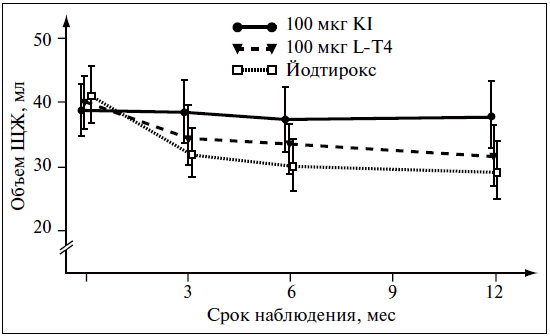
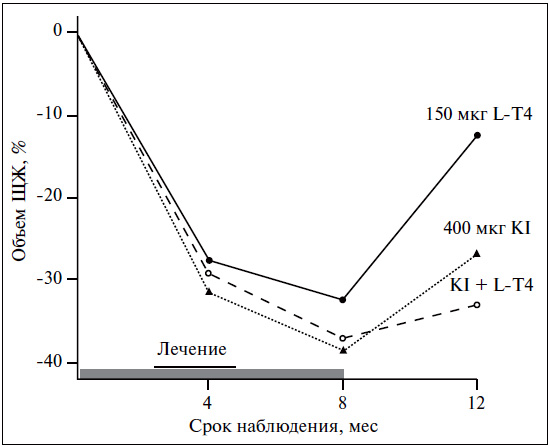
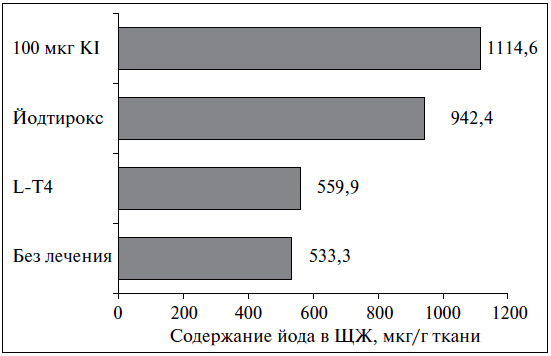
Супрессивная монотерапия препаратами L-Т4, по современным патогенетическим представлениям, не является лечением выбора при диффузном эутиреоидном зобе. На первом этапе лечения в большинстве случаев целесообразно назначение йодида калия в дозе 100-200 мкг в день (например, «Йодбаланс-100» и «Йодбаланс-200»). В контролируемых клинических исследованиях (см. таблицу) было показано, что на фоне терапии йодидом за первые 6 мес объем ЩЖ в среднем уменьшается на 30% (рис. 2). Основными преимуществами монотерапии препаратами йода являются ее этиотропный характер, безопасность, отсутствие необходимости в подборе дозы и в проведении частых гормональных исследований [5]. Супрессивная монотерапия препаратами L-Т4 («Эутирокс»), направленная на подавление продукции ТТГ (в пределах 0,1—0,4 мМЕ/л, что у взрослых, как правило, требует назначения около 100 мкг L-Т4), весьма эффективна и достаточно быстро обусловливает уменьшение объема ЩЖ (см. рис. 2), тем не менее после ее отмены зачастую происходит рецидив зоба (феномен рикошета; рис. 3). Это объясняется тем, что на фоне монотерапии L-T4 ЩЖ обедняется йодом, что показали исследования удаленной ткани ЩЖ у пациентов, получавших различные варианты лечения зоба (рис. 4).
На фоне терапии препаратами йода этого не происходит, в связи с чем эффект терапии остается стойким. Назначая терапию L-Т4, всегда следует помнить о том, что в организм вводится активный гормон, оказывающий воздействие на большинство органов и тканей, несмотря на то что это назначение делается с целью воздействия на одну только ЩЖ за счет подавления продукции ТТГ. В то же время йод в организме оказывает воздействие практически исключительно на ЩЖ и в физиологических дозах абсолютно безопасен.
Хорошо себя зарекомендовавшей в клинических исследованиях альтернативой монотерапии L-Т4 является комбинированное назначение йодида и L-T4. Наиболее просто ее проводить при помощи препаратов, одновременно содержащих оба компонента — и йод, и L-T4 в наиболее распространенных дозах. Например, «Йодтирокс» в одной таблетке содержит 100 мкг L-T4 и 100 мкг йодида калия. Такой препарат воздействует сразу на два основных патогенетических механизма развития зоба (см. рис. 1). Основными плюсами комбинированной терапии являются более быстрое достижение уменьшения объема ЩЖ (за счет L-Т4) и нивелировка феномена отмены L-Т4 (рецидив зоба) за счет йодида, который предотвращает снижение интратиреоидного содержания йода, возникающего при монотерапии L-Т4 (см. рис. 4).
Рис. 2. Динамика объема ЩЖ на фоне лечения зоба (P.M. Schumm, 1983)
Рис. 3. Динамика объема ЩЖ на фоне лечения зоба (G. Hintze, J. K?berling, 1992)
Рис. 4. Уровень интратиреоидного йода на фоне лечения зоба (H.J. R?her, 1986)
В принципе L-Т4 и йодид можно назначать и последовательно: в начале быстрое достижение регресса объема железы на фоне супрессивной терапии LТ4 с последующим добавлением 100-200 мкг йодида. Аргументом в пользу последовательного, а не одновременного назначения L-Т4 и йодида является тот факт, что супрессия ТТГ, которая развивается на фоне назначения L-Т4, подавляет транспорт вЩЖ йода (получается, что один компонент терапии как бы «мешает» другому). Тем не менее, по нашему мнению, этот феномен вряд ли имеет существенное клиническое значение, о чем свидетельствуют как экспериментальные работы, изучавшие интратиреоидное содержание йода на фоне различных вариантов терапии (см. рис. 4), так и клинические исследования, показавшие высокую и долгосрочную эффективность весьма популярных во многих странах фиксированных комбинаций L-Т4 и йодида.
Здесь хотелось бы заметить, что по данным многих клинических исследований, которые сравнивали эффективность терапии йодидом, L-Т4 и их комбинации, конечное уменьшение ЩЖ (в процентах от исходного объема) на фоне всех трех схем существенно не различалось (см. рис. 3). Как уже указывалось, отличался прогноз: с окончанием монотерапии L-Т4 очень часто развивался рецидив зоба [2, 5].
Таким образом, лечение эутиреоидного зоба может быть представлено в виде нескольких этапов. В начале большинству пациентов необходимо назначить монотерапию препаратами йода или комбинированную терапию препаратами йода и L-T4. Последняя, наряду с этим, может быть назначена при неэффективности монотерапии (рис. 5). При стойкой нормализации объема ЩЖ необходимо предпринять попытку возврата к монотерапии препаратами йода.
Рис. 5. Схема лечения эутиреоидного зоба
При обнаружении в ЩЖ одного или нескольких пальпируемых и/или превышающих 1 см в диаметре узловых образований пациенту показаны дополнительные исследования: пункционная биопсия «узла» и, в большинстве случаев (особенно, если речь идет о лицах старше 50 лет), сцинтиграфия ЩЖ с целью исключения функциональной автономии. В последнем случае назначение пациенту препаратов йода не показано, поскольку оно может вызвать декомпенсацию автономии с развитием тиреотоксикоза.
Есть ли ситуации, в которых более предпочтительно назначение монотерапии L-Т4? Вопрос, который часто обсуждается в этом контексте — безопасность назначения йодида в ситуации, когда данные обследования не позволяют исключить у пациента аутоиммунный тиреоидит (АИТ) как причину увеличения ЩЖ. Сразу хотелось бы оговориться, что в соответствии с рекомендациями практически всех без исключения эндокринологических сообществ сам по себе АИТ в фазе эутиреоза не является показанием к назначению какой-либо терапии. Вопрос о назначении супрессивной терапии может рассматриваться при АИТ в относительно редких ситуациях значительного увеличения ЩЖ (гигантский зоб Хашимото встречается весьма редко, и у большинства пациентов к этому времени уже имеется гипотиреоз, сам по себе требующий заместительной терапии). В целом нужно исходить из того, что в йододефицитных регионах случаи значительного увеличении ЩЖ без нарушения ее функции в подавляющем большинстве случаев связаны с эндемическим зобом. Последнему зачастую сопутствуют те изменения, которые описываются и при АИТ (умеренное повышение уровня антител к ЩЖ и снижение ее эхогенности), поэтому обнаружение последних, особенно порознь, не может быть основанием для постановки диагноза АИТ. Если диагноз АИТ представляется весьма вероятным (с абсолютной уверенностью об этом можно говорить только при наличии гипотиреоза) и при этом у пациента имеется небольшое увеличение ЩЖ на фоне эутиреоза, оптимальной тактикой, по нашему представлению, является динамическое наблюдение.
Особенности наблюдения пожилых пациентов
По мере увеличения возраста и длительности проживания в йододефицитном регионе возрастает объем автономно функционирующей и автономно пролиферирующей ткани ЩЖ. В связи с этим лечение зоба у пожилых пациентов, как правило, не будет столь эффективно, как у молодых. Как указывалось, среди лиц старше 50—60 лет высока распространенность узлового и многоузлового зоба и функциональной автономии ЩЖ. Это делает нецелесообразным назначение как препаратов йода, которые могу привести к декомпенсации автономии и развитию тиреотоксикоза, так и препаратов L-Т4, которые, с одной стороны, при функциональной и пролиферативной автономии малоэффективны, а с другой стороны, в тех дозах, от которых можно ожидать какого-то эффекта, небезопасны. Таким образом, у лиц старше 60 лет при зобе небольшого размера с узловыми изменениями или без них наиболее оправданной тактикой следует признать активное наблюдение, подразумевающее УЗИ и определение уровня ТТГ с интервалом в 1—2 года. Если все-таки принято решение о назначении лечения, нужно помнить о следующем:
Всем ли показано лечение?
В соответствии со сказанным выше очевидно, что не всем. Об этом наиболее явственно свидетельствует тот факт, что по данным аутопсий распространенность многоузлового зоба в соответствующей возрастной группе достигает 40% и более, при этом эутиреоидный зоб, за исключением казуистических случаев летального сдавления трахеи гигантским зобом, не является причиной смерти. В связи с этим влияние многоузлового эутиреоидного зоба небольшого размера на продолжительность и качество жизни весьма сомнительно, что и определяет наше отношение к его потенциально небезопасному активному лечению у пожилых людей.
При обнаружении зоба у молодых людей тактика, безусловно, должна быть более активной, что определяется потенциально большей эффективностью и безопасностью препаратов йода и супрессивной терапии L-T4. Тем не менее нужно помнить о том, что описанные выше методы лечения наиболее эффективны при общем увеличении объема ЩЖ (т.е. при диффузном и смешанном зобе), чего, к сожалению, нельзя сказать об узловом зобе. Последние рекомендации Американской тиреоидной ассоциации и Американской ассоциации клинических эндокринологов (AACE) по диагностике и лечению узлового зоба признают супрессивную терапию препаратами L-T4 неэффективной и потенциально небезопасной.
Ограничивается ли рекомендация о возможности активного наблюдения пациентов с эутиреоидным зобом без назначения каких-либо препаратов только пожилыми людьми? Конечно, нет. Если речь не идет о зобе большого размера, отсутствие нарушения функции ЩЖ позволяет динамически наблюдать и молодых пациентов. Особенно ценным такое динамическое наблюдение оказывается в ситуациях, когда нет полной уверенности в поставленном диагнозе. В любом случае, если нет нарушений функции ЩЖ, а при узловом зобе на основании тонкоигольной биопсии исключена опухоль, вопрос о назначении какой-либо терапии может быть безболезненно отложен.
Оперативное лечение и терапия радиоактивным 131 I
Если речь идет о диффузном эутиреоидном зобе, операция может быть показана лишь при его гигантском размере и/или при явлениях компрессии окружающих органов. В случае многоузлового и узлового зоба, в ситуациях, когда при помощи тонкоигольной биопсии исключена опухолевая природа этих образований, показанием для операции опять же является компрессионный синдром и/или косметический дефект. Как в том, так и в другом случае, а также в целом для лечения как токсического и эутиреоидного зоба серьезной альтернативой операции является терапия радиоактивным йодом. Последний метод, как известно, является лечением выбора при функциональной автономии ЩЖ, а также в большинстве случаев болезни Грейвса (диффузного токсического зоба). Наряду с этим в последние несколько десятилетий в мире накоплен большой опыт лечения при помощи радиоактивного 131 I эутиреоидного зоба. Метод позволяет неинвазивно буквально в течение нескольких месяцев достичь уменьшения объема ЩЖ на 30—50% даже после однократного введения изотопа. Появляется все больше данных об успешном лечении 131 I гигантского зоба с явлениями компрессии. Остается сожалеть, что этот эффективный, безопасный и дешевый метод лечения малодоступен в России.
Послеоперационная профилактика
Общая тенденция в хирургии ЩЖ в последние десятилетия во многих западных странах заключается в том, что если хирургическая операция на ЩЖ по поводу эутиреоидного зоба (не говоря уже про болезнь Грейвса и опухоли ЩЖ) вообще предпринимается, удаляется большая часть органа (тиреоидэктомия). Наряду с этим отсутствие в нашей стране единых подходов к оперативному лечению заболеваний ЩЖ приводит к тому, что эндокринологи сталкиваются с пациентами, которым в одинаковых клинических ситуациях выполняются совершенно разные по объему операции. Наибольшие возражения вызывают операции, подразумевающие удаление (энуклеацию) отдельных узловых образований, не может не тревожить и огромное количество необоснованных оперативных вмешательств по поводу банального узлового и многоузлового коллоидного зоба.
Разбирая принципы профилактического лечения после операций по поводу различных вариантов йододефицитного зоба, прежде всего следует отметить, что такая профилактика необходима. На это указывает тот факт, что риск послеоперационного рецидива зоба достаточно высок и варьирует от 20 до 80%. Лечение будет зависеть от объема предпринятого оперативного вмешательства, а точнее от объема тиреоидного остатка, который необходимо оценить при помощи УЗИ. Наиболее прост этот алгоритм в ситуации удаления большей части ЩЖ, которое приводит к развитию гипотиреоза: после того как заместительная доза L-Т4 подобрана, как правило, необходим лишь ежегодный контроль уровня ТТГ.
Если объем оставленной доли ЩЖ или суммарный объем тиреоидного остатка достаточен для поддержания эутиреоза (больше 8—10 мл), большинству пациентов показано назначение профилактической монотерапии йодидом в дозе 200 мкг/сут («Йодбаланс-200»). Если на фоне монотерапии йодидом по мере наблюдения со временем выявляется повышение уровня ТТГ (развивается субклинический гипотиреоз), лечение дополняется L-T4. Если объем оставленной после операции ткани ЩЖ не позволяет поддерживать эутиреоидное состояние, пациенту наиболее целесообразно назначить комбинированную терапию препаратами L-T4 и йода: LT4 в этом случае будет замещать дефицит тиреоидных гормонов, а йод способствовать профилактике рецидива узлового образования в оставленной ткани ЩЖ [2]. С этой целью удобно использовать фиксированные комбинации, содержащие в одной таблетке йодид и L-T4 («Йодтирокс»).
Литература