Мочевой пузырь спавшийся что
Чувство полного мочевого пузыря как симптом
Неприятное раздражающее ощущение полного мочевого пузыря и возможные частые позывы к мочеиспусканию доставляют человеку немалый дискомфорт. Однако снижение качества жизни – это не самое опасное, ведь данный синдром может быть признаком различной степени нарушений функционирования организма.
Давящее чувство бывает:
истинным. После мочеиспускания в пузыре остается некоторое количество жидкости, которая раздражает рецепторы его стенок. Такая ситуация говорит о неправильной работе органов малого таза;
ложным. Периферическая или центральная нервная система имеет функциональные нарушения и посылает импульсы, раздражая нервные окончания пузыря.
На какие заболевания может указывать данное состояние
Ощущение переполненного мочевого пузыря вызывают различные факторы. В любом случае, это не очень хороший признак, требующий вашего внимания и консультации врача. Причиной могут послужить:
воспалительные заболевания мочеполовой системы (уретрит, цистит);
изменение мышечного тонуса и сократительной способности пузыря;
доброкачественные или злокачественные опухолевые образования;
воспалительные процессы в соседних органах (пиелонефрит, аппендицит, энтероколит);
гинекологические заболевания у женщин (воспаление придатков, миома матки, эндометрит);
патологические процессы в пищеварительной системе, запоры, из-за которых происходит сдавливание пузыря.
Особенности проблемы у женщин и мужчин
В период беременности характерным состоянием является постоянное ощущение полного мочевого пузыря у женщин. Оно возникает из-за увеличения матки, а также под воздействием гормонов. Нередко оно сохраняется и после родов, иногда сопровождается недержанием мочи. Это говорит об уменьшении эластичности и тонуса мышц тазового дна.
Если ощущение полного мочевого пузыря у мужчин сопровождается резями, болями при мочеиспускании или оно затруднено, это повод обратиться к медикам, чтоб не пропустить серьезное заболевание и не усугубить его.
Если мочевой пузырь переполнен, а мочеиспускание невозможно – это требует безотлагательного вызова бригады скорой помощи и выведения урины через катетер.
К кому обратиться при проблеме переполненности мочевого пузыря
Любыми нарушениями мочеполовой и мочевыделительной системы, в том числе синдромом полного мочевого пузыря, занимается врач-уролог. Клиника урологии имени Р. М. Фронштейна Первого Московского Государственного Медицинского Университета имени И. М. Сеченова – это узкоспециализированная современная клиника с многолетним практическим опытом, инновационными технологиями диагностики и лечения. Запишитесь на консультацию по телефону или заполните форму на нашем сайте.
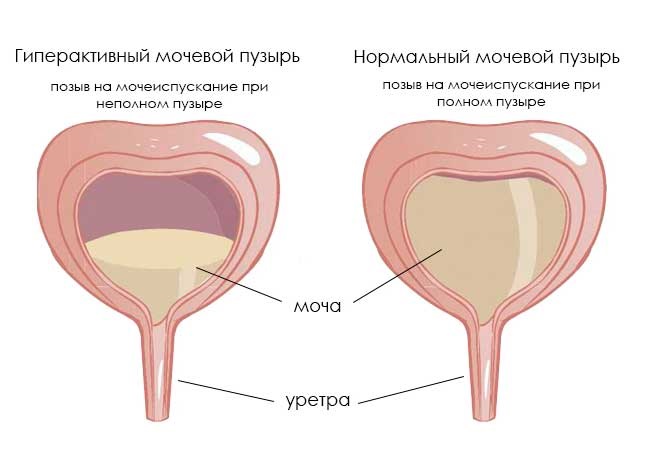
Гиперактивный мочевой пузырь: как справиться с деликатной проблемой
Гиперактивный мочевой пузырь (гиперрефлекторный, ГАМП или ГМП) – форма нейрогенного мочевого пузыря (НМП), при котором у человека появляются проблемы с произвольным сознательным контролем мочеиспускания. Эта форма НМП встречается чаще, чем гипорефлекторная. Основной симптом – частое мочеиспускание, которое может сопровождаться увеличением объема мочи. ГАМП – серьезная проблема, поскольку по распространенности сравним с гипертонией, хроническим бронхитом, астмой и заболеваниями сердца.
Из-за чего может развиться гиперактивный мочевой пузырь
Гиперактивный мочевой пузырь у женщин встречается чаще, чем у мужчин – 60% против 40%. Основной причиной выступают нарушения в работе нервной системы, вызванные:
Еще ГАМП развивается на фоне сахарного диабета, отравления организма алкоголем или химическими веществами. Также расстройство может быть врожденным из-за аномалий в строении мочевыделительного канала.
У мужчин ГАМП может вызывать аденома простаты, из-за которой сужается мочеиспускательный канал. У женщин синдром гиперактивного мочевого пузыря имеет факторы риска, которые увеличивают вероятность столкнуться с таким заболеваниям. В список таких факторов включают:
Еще с ГАМП можно столкнуться в период климакса, когда организму недостает гормонов эстрогенов. Чувствительность детрузора (его сокращение приводит к мочеиспусканию) может повышаться при заместительной гормонотерапии при раке молочной железы. Не меньшее значение в развитии ГАМП имеют стрессовые ситуации и вредные условия труда.
Признаки гиперактивного мочевого пузыря
Нейрогенный гиперактивный мочевой пузырь проявляется в частом мочеиспускании (поллакиурии), причем малыми порциями при незаполненном пузыре. На его фоне может наблюдаться полиурия – увеличенное количество мочи, свыше 1800-2000 мл при норме 1000-1500 мл. В ряде случаев за сутки может выделяться более 3 л мочи. Причем желание помочиться может вызывать звук льющейся воды.
Еще при ГМП возможно недержание мочи, иногда возникающее даже от любого напряжения брюшных мышц. Чаще всего это ургентное недержание, при котором резко появляется желание помочиться, после чего происходит непроизвольное выделение мочи. Другой характерный признак – ноктурия. Это необходимость просыпаться ночью для мочеиспускания более 1-2 раз. Ноктурия, поллакиурия и полиурия могут возникать как одновременно, так и изолировано.
Нередко ГМП сопровождается симптомами, которые указывают на расстройство вегетативной нервной системы. К таким признакам относятся повышение артериального давления и гипергидроз (усиленное потоотделение). Еще ГАМП влияет на социализацию. Человек постоянно боится не успеть в туалет, переживает из-за неприятного запаха. Из-за произвольного выделения мочи может развиваться экзема или мочевой дерматит.
Как лечат ГАМП
Лечение гиперактивного мочевого пузыря у мужчин и женщин производится по одним и тем же принципам. Но терапия не имеет единой схемы. Она носит, в основном, паллиативный характер, т. е. проводится для улучшения качества жизни пациента. Можно сказать одно – лечение гиперактивного мочевого пузыря всегда сложное и комплексное. К основным методам относятся:
В самых сложных случаях, когда не помогают режим и лекарства, прибегают к малоинвазивным операциям. Но решение об их проведении принимает врач. При ГАМП необходимо обратиться к урологу. В Государственном центре урологии вы можете получить квалифицированную медицинскую помощь в рамках ОМС. Для этого вам необходимо записаться на прием к урологу, воспользовавшись формой на сайте или нашим контактным номером.
Лечение функциональных нарушений опорожнения мочевого пузыря
Лечение больных с функциональными нарушениями опорожнения мочевого пузыря является насущной проблемой нейроурологии. Это связано с тем, что до настоящего времени не разработано эффективных и этиопатогенетически обоснованных методов лечения таких больных
Лечение больных с функциональными нарушениями опорожнения мочевого пузыря является насущной проблемой нейроурологии. Это связано с тем, что до настоящего времени не разработано эффективных и этиопатогенетически обоснованных методов лечения таких больных.
Выделяют нейрогенные, миогенные (миопатии) и психогенные (неврозы, шизофрения, истерия и др.) факторы, лежащие в основе функциональных нарушений опорожнения мочевого пузыря. Нейрогенные нарушения и повреждения — основная причина таких нарушений. В отсутствие причины функциональных нарушений опорожнения мочевого пузыря следует думать об идиопатических формах заболевания.
Согласно классификации Международного общества по удержанию мочи, функциональные нарушения опорожнения мочевого пузыря — это результат недостаточной функции мочевого пузыря, гиперактивности уретры или следствие комплексного воздействия обоих нарушений [1]. Недостаточная функция мочевого пузыря возникает вследствие снижения или отсутствия сократительной способности детрузора (арефлексия), которые встречаются при локализации повреждения или неврологического поражения в области фронтальных долей и моста головного мозга, сакрального отдела спинного мозга, при повреждении волокон конского хвоста, тазового сплетения и нервов мочевого пузыря, а также при рассеянном склерозе. Гиперактивность уретры — это следствие наружной детрузорно-сфинктерной диссинергии (ДСД) или нерасслабляющегося (спастического) поперечно-полосатого (п/п) сфинктера уретры, также может проявиться как вариант синдрома Фоулера у женщин. При этом наружная ДСД наблюдается при супрасакральном уровне поражения спинного мозга.
В литературе имеются лишь единичные сообщения о распространенности функциональных нарушений опорожнения мочевого пузыря. Так, P. Klarskov и соавт., оценивая обращаемость в лечебные учреждения Копенгагена, выявили, что ненейрогенные формы нарушения опорожнения мочевого пузыря встречаются в среднем у 7 женщин на 100 000 населения [2]. По данным T. Tammela и соавт., после оперативных вмешательств на органах брюшной полости нарушения опорожнения мочевого пузыря встречаются у 2,9 % пациентов, а после проктологических операций — у 25% больных [3]. Многие авторы считают данную проблему особенно значимой у неврологических больных.
Клиническим проявлением снижения сократительной способности детрузора и нерасслабляющегося п/п сфинктера уретры являются симптомы нарушения опорожнения мочевого пузыря, к которым относятся затрудненное мочеиспускание тонкой, вялой струей, прерывистое мочеиспускание, необходимость прилагать усилия и натуживаться, чтобы начать мочеиспускание, ощущение неполного опорожнения мочевого пузыря.
При отсутствии сократительной способности детрузора в сочетании с паралитическим состоянием п/п сфинктера уретры больные опорожняют мочевой пузырь, искусственно увеличивая внутрибрюшное давление, что клинически проявляется мочеиспусканием слабой струей мочи. При отсутствии сократительной способности детрузора в сочетании со спастическим состоянием наружного сфинктера уретры в большинстве случаев самостоятельное мочеиспускание невозможно и отмечается хроническая задержка мочи.
Нерасслабляющийся п/п сфинктер уретры приводит к инфравезикальной обструкции с симптомами нарушения опорожнения мочевого пузыря.
Клинические проявления наружной ДСД (непроизвольное сокращение п/п сфинктера уретры во время мочеиспускания или непроизвольного сокращения детрузора) включают два вида симптомов, а именно: нарушения опорожнения и накопления мочи в мочевом пузыре. Последние включают учащенное и ургентное мочеиспускание нередко в сочетании с ургентным недержанием мочи и никтурией. Для наружной ДСД характерно неполное опорожнение мочевого пузыря и развитие пузырно-мочеточникового рефлюкса.
Таким образом, различные формы нарушения опорожнения мочевого пузыря могут иметь во многом сходную клиническую картину. В связи с этим правильная и своевременная диагностика функциональных нарушений опорожнения мочевого пузыря является залогом успешного лечения.
Диагностика функциональных нарушений опорожнения мочевого пузыря складывается из сбора жалоб и анамнеза, урологического и неврологического обследования, а также дополнительных методов обследования, среди которых основное место занимает уродинамическое исследование. На начальном этапе обследования обязательна оценка симптомов нижних мочевых путей на основании вопросника I-PSS (Internanional Prostate Symptom Score). Вопросник I-PSS был предложен для оценки нарушений акта мочеиспускания вследствие заболеваний предстательной железы, однако в настоящее время он с успехом применяется и в случаях проявления симптомов заболеваний нижних мочевых путей, вызванных различными факторами, в том числе и неврологического характера.
Для уточнения поведения детрузора и его сфинктеров в фазу опорожнения мочевого пузыря наиболее информативным методом исследования больных является комплексное уродинамическое исследование.
Уродинамическими признаками наружной ДСД, характерной для надкрестцовой локализации патологического процесса, особенно в шейном отделе спинного мозга, являются регистрируемые с помощью электромиографии во время мочеиспускания «всплески» сократительной активности п/п сфинктера уретры и мышц тазового дна. Сокращение мышц тазового дна затрудняет или полностью прерывает поток мочи. Для нерасслабляющегося сфинктера уретры характерно отсутствие снижения электромиографической активности п/п сфинктера уретры во время мочеиспускания. Снижение или отсутствие сократительной способности детрузора уродинамически проявляется отсутствием плавного повышения детрузорного давления в ходе цистометрии или отсутствием позыва к акту мочеиспускания.
Следует подчеркнуть, что только уродинамическое обследование дает возможность достоверно установить форму нарушения функции нижних мочевых путей, приводящих к нарушению опорожнения мочевого пузыря, и во многом определить выбор метода лечения.
Ультразвуковое исследование почек и мочевого пузыря, также как и экскреторная урография, позволяет уточнить анатомическое состояние верхних мочевых путей и количество остаточной мочи в мочевом пузыре. По количеству остаточной мочи в мочевом пузыре после акта мочеиспускания (в норме до 50 мл) можно косвенно судить о функциональном состоянии детрузора и наличии инфравезикальной обструкции.
В таблице перечислены методы лечения больных с функциональными нарушениями опорожнения мочевого пузыря, из которых только медикаментозная терапия и дорзальная ризотомия с электростимуляцией передних корешков могут действительно считаться методами лечения, тогда как другие скорее являются способами опорожнения мочевого пузыря. При этом даже медикаментозная терапия во многом является симптоматическим методом лечения. Несмотря на это, назначение лекарственных средств представляет собой первый этап лечения больных с функциональными нарушениями опорожнения мочевого пузыря. Выбор медикаментов зависит от вида нарушения функции нижних мочевых путей. Так, в случае нарушения сократительной способности детрузора применяют антихолинэстеразные средства и М-холиномиметики, а при гиперактивности уретры — центральные миорелаксанты и α-блокаторы.
У 22 больных со сниженной сократительной способностью детрузора использовали дистигмина бромид (убретид) в дозе 5 мг через день за 30 мин до завтрака в течение 2 мес. При этом через каждые 2 нед делали 7-дневный перерыв в приеме препарата. Механизм действия дистигмина бромида заключается в блокировании ацетилхолинэстеразы, что сопровождается увеличением концентрации ацетилхолина в синаптической щели и соответственно приводит к облегчению передачи нервного импульса.
У всех больных терапевтический эффект развивался в первую неделю приема препарата и выражался в снижении среднего балла I-PSS c 15,9 до 11,3, а количества остаточной мочи — с 82,6 до 54,3 мл. Субъективно пациенты отмечали усиление ощущения позыва и облегчение начала акта мочеиспускания.
Следует отметить, что до настоящего времени остается открытым вопрос о продолжительности лечения антихолинэстеразными средствами. По нашим данным, у 82% больных в разные сроки после окончания 2-месячного курса лечения отмечалось возобновление симптомов, потребовавшее повторного назначения препарата.
К сожалению, мы не накопили собственного опыта применения бетанехола у больных со сниженной сократительной способностью детрузора, так как данный препарат не зарегистрирован для клинического применения в нашей стране и соответственно отсутствует в аптечной сети. Механизм действия бетанехола аналогичен действию ацетилхолина на гладкие миоциты. Данные других авторов показывают, что бетанехол может применяться при лечении больных с легкой степенью нарушения сократительной способности детрузора [4, 5].
α1-адреноблокатор доксазозин (кардура) использовали в ходе лечения 30 больных с гиперактивностью уретры, в том числе 14 пациентов с наружной ДСД и 16 с нарушением произвольного расслабления п/п сфинктера уретры. Доксазозин назначали в дозе 2 мг/сут на ночь.
Через 6 мес средний балл по шкале I-PSS у больных с наружной ДСД снизился с 22,6 до 11,4, количество остаточной мочи уменьшилось с 92,6 до 32,4 мл, а максимальная скорость потока мочи увеличилась с 12,4 до 16,0 мл/сек.
Кроме того, через 6 мес у больных с нарушением произвольного расслабления п/п сфинктера уретры средний балл I-PSS снизился с 14,6 до 11,2, количество остаточной мочи — с 73,5 до 46,2 мл, а максимальная скорость потока мочи увеличилась с 15,7 до 18,4 мл/сек.
Баклофен и тизанидин (сирдалуд) являются центральными миорелаксантами. Они снижают возбуждение моторных нейронов и интернейронов и могут ингибировать передачу нервного импульса в спинном мозге, уменьшая спастичность п/п мышц. По нашим данным, после применения баклофена в дозе 20 мг/сут и тизанидина в дозе 4 мг/сут не было выявлено существенной динамики субъективных и объективных симптомов как у больных с наружной ДСД, так и у пациентов с нарушением расслабления п/п сфинктера уретры. Выраженная слабость мускулатуры конечностей на фоне приема этих препаратов не позволяет увеличивать дозу препаратов, что существенно ограничивает их применение в клинической практике.
Следует отметить, что медикаментозная терапия эффективна у больных с начальными и легкими формами нарушения опорожнения мочевого пузыря. Тем не менее ее целесообразно использовать в качестве первого этапа лечения. В случае недостаточной эффективности медикаментозной терапии необходимо искать новые пути решения проблемы адекватного опорожнения мочевого пузыря.
Предложенная Lapides и соавт. в 80-е гг. прошлого столетия интермиттирующая аутокатетеризация мочевого пузыря до настоящего времени остается одним из основных методов опорожнения мочевого пузыря [6]. Однако этот метод имеет ряд осложнений, к которым относятся инфекции нижних мочевых путей, стриктуры уретры и, самое главное, значительное снижение качества жизни. При невозможности выполнения (неврологические больные с тетраплегией, больные с ожирением) или отказе пациента от аутокатетеризации, у лиц с наружной ДСД и нерасслабляющимся сфинктером уретры, а также со сниженной сократительной способностью детрузора для адекватного опорожнения мочевого пузыря применяют в последние годы имплантацию специальных стентов (производства фирм Balton, Mentor, МедCил) и инъекции ботулинического токсина в зону п/п сфинктера уретры.
 |
| Рисунок 1. Временный уретральный стент |
Временные уретральные стенты имеют форму цилиндра, выполненного из проволочной спирали толщиной 1,1 мм, изготовлены они на основе полимолочной и полигликоликовой кислот с различным периодом разрушения (от 3 до 9 мес) посредством гидролиза (рис. 1). Механические свойства и время разрушения временных стентов зависят от степени поляризации, места и формы зоны имплантации.
Мы имеем опыт применения временных уретральных стентов у семи мужчин с наружной ДСД и у четырех пациентов, у которых отсутствовала сократительная способность детрузора. Временный уретральный стент устанавливали при уретроцистоскопии таким образом, чтобы он «шинировал» как простатический, так и мембранозный отделы уретры. Такое положение стента обеспечивает адекватное опорожнение мочевого пузыря.
У всех больных отмечалось восстановление самостоятельного мочеиспускания сразу после имплантации уретрального стента. Пациенты с наружной ДСД осуществляли мочеиспускание по позыву, а больные с отсутствием сократительной способности детрузора с интервалом 4 ч (6 раз в сутки) с использованием приема Креда. По данным ультразвукового сканирования, через 10 нед после установки стента у больных с наружной ДСД не отмечалось остаточной мочи, а у больных с отсутствием сократительной способности детрузора среднее количество остаточной мочи составило 48 мл и зависело от адекватности выполнения приема Креда. Очень важно, что у больных с наружной ДСД было выявлено снижение максимального детрузорного давления во время мочеиспускания в среднем с 72 до 35 см вод. ст. (профилактика развития пузырно-мочеточникового рефлюкса).
Мы считаем, что временные уретральные стенты обеспечивают адекватное опорожнение мочевого пузыря и показаны тем больным с нарушением опорожнения мочевого пузыря, которым не может быть выполнена интермиттирующая катетеризация мочевого пузыря или которые воздерживаются от нее по различным причинам. Временные стенты могут являться методом отбора больных для установки постоянных (металлических) стентов.
В последние годы в литературе появились сообщения об успешном использовании ботулинического токсина у больных с функциональными нарушениями опорожнения мочевого пузыря. В нашей клинике ботулинический токсин применялся у 16 больных с нарушением опорожнения мочевого пузыря, в том числе у девяти с наружной ДСД, у трех с нерасслабляющимся п/п сфинктером уретры и у четырех с нарушением сократительной способности детрузора. Мы использовали ботулинический токсин типа А фармацевтической фирмы Allergan. Коммерческое название препарата — ботокс (Botox), он представляет собой лиофилизированный порошок белого цвета в вакуумных стеклянных флаконах объемом 10 мл, закрытых резиновой пробкой и герметичным алюминиевым затвором. В одном флаконе содержится 100 ЕД ботулинического токсина типа А.
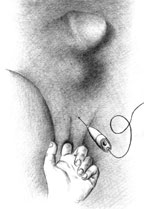 |
| Рисунок 2. Введение ботулинического токсина у мужчин |
Механизм действия ботокса заключается в блокировании выброса ацетилхолина из пресинаптической мембраны в нервно-мышечном синапсе. Фармакологическим эффектом этого процесса является стойкая хемоденервация, а клиническим проявлением — расслабление мышечных структур.
Согласно рекомендациям фирмы-производителя, лиофилизированный порошок разводили 8 мл стерильного 0,9% раствора натрия хлорида без консервантов (1 мл полученного раствора содержит 12,5 ЕД ботокса). Использовали трансперинеальную методику введения препарата. У мужчин под контролем указательного пальца, введенного в прямую кишку, специальную иглу с изоляционным покрытием вводили в точку, находящуюся на 2 см латеральнее и выше анального отверстия (рис. 2). У женщин иглу под контролем указательного пальца, введенного во влагалище, вводили в точку на 1 см латеральнее и выше наружного отверстия уретры на глубину 1,5–2,0 см (рис. 3). Во всех случаях положение иглы контролировали электромиографически по характерному звуку динамика электромиографа. В каждую точку вводили по 50 ЕД ботокса.
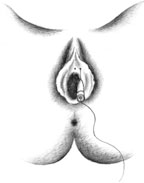 |
| Рисунок 3. Введение ботулинического токсина у женщин |
У всех больных через 10 дней после введения ботулинического токсина исчезла остаточная моча и было отмечено увеличение максимальной скорости потока мочи. Важно, что хемоденервация сфинктера уретры после инъекции ботокса у всех пациентов с нерасслабляющимся п/п сфинктером и наружной ДСД приводила к снижению детрузорного давления, а у больных с нарушением сократительной способности детрузора — к снижению максимального абдоминального давления, вызывающего выделение мочи из наружного отверстия уретры. Это наблюдение представляется крайне важным в отношении профилактики развития пузырно-мочеточникового рефлюкса и сохранения функциональной способности почек. Только у одного больного клинический эффект после инъекции ботокса продолжал сохраняться на протяжении 16 мес, остальным пациентам потребовались повторные инъекции препарата с периодичностью 3–8 мес.
В отдельных случаях, при выраженной инвалидизации больных с нарушением опорожнения мочевого пузыря, используют трансуретральную инцизию или резекцию наружного сфинктера уретры, дренируют мочевой пузырь постоянным уретральным катетером или выполняют цистостомию.
Таким образом, нарушение опорожнения мочевого пузыря может быть следствием различных форм дисфункции нижних мочевых путей. Требуются проведение комплексного уродинамического обследования для уточнения функционального состояния мочевого пузыря и его сфинктеров и выбор адекватного метода опорожнения мочевого пузыря. Отсутствие высокоэффективных и универсальных способов лечения больных с функциональными нарушениями опорожнения мочевого пузыря диктует необходимость поиска новых методов терапии таких больных.
Г. Г. Кривобородов, доктор медицинских наук
М. Е. Школьников, кандидат медицинских наук
РГМУ, Москва
Сморщенный мочевой пузырь ( Микроцистис )
Сморщенный мочевой пузырь — это функциональное или анатомическое уменьшение полости мочевика, возникшее на фоне других заболеваний. Проявляется поллакиурией, никтурией, реже — тяжестью и болью над лобком, интенсивность которых уменьшается после мочеиспускания. Диагностируется с помощью сонографии мочевого пузыря, ретроградной цистографии, уродинамических исследований. Для коррекции расстройства показаны лечение М-холинолитиками, медикаментозная и хирургическая денервация детрузора, гидродилатация, цистопластика после частичной либо радикальной цистэктомии.
МКБ-10
Общие сведения
Сморщенный мочевик (микроцистис) обычно осложняет течение других заболеваний и патологических состояний, приводящих к нарушению иннервации мочевого пузыря, воспалительным процессам в слизистом и мышечном слоях его стенки. У детей и пациентов молодого возраста чаще диагностируют нейрогенный вариант расстройства. В старших возрастных контингентах преобладает органическое рубцово-склеротическое сморщивание органа. Актуальность своевременного выявления патологии обусловлена существенным ухудшением качества жизни больных и высоким риском вторичного нарушения функции почек.
Причины
Уменьшение функциональной и анатомической емкости мочевика может быть обусловлено как нарушением иннервации мышечного слоя, так и органическими повреждениями стенки. Нейрогенный вариант заболевания, вызванный гиперактивностью мочевого пузыря, наблюдается у 15,6%-16% пациентов-мужчин и у 16,9-17,4% заболевших женщин. В его основе лежит временная или постоянная дисфункция спинальных либо краниальных отделов нервной системы, приводящая к гипертонусу мочепузырных мышечных волокон. Основными органическими причинами расстройства являются:
Патогенез
Механизм формирования сморщенного мочевого пузыря зависит от причин, спровоцировавших заболевание. Патогенез функционального микроцистиса обусловлен стойким спазмом гладкомышечных волокон на фоне патологической эфферентной импульсации из пораженного участка спинного или головного мозга. При органической форме расстройства воспалительное поражение уровезикальной стенки завершается ее фиброзом, рубцовой деформацией с атрофией мышечных волокон, их замещением соединительной тканью. Фиброзно-измененный детрузор обладает меньшей эластичностью, что приводит к анатомическому уменьшению объема мочевика.
Симптомы
Заболевание проявляется непреодолимыми позывами к мочеиспусканию, возникающими до 18-23 раз в сутки, в том числе от 6 раз и более ночью. Отмечается уменьшение объема выделившейся мочи в каждой порции. Часть пациентов предъявляет жалобы на ощущение тяжести или сдавливание в надлобоковой области. В редких случаях возникает болезненность внизу живота, интенсивность которой несколько уменьшается после отхождения мочи. Возможно развитие невротической симптоматики с ощущением постоянной усталости, быстрой утомляемостью, раздражительностью, плаксивостью, снижением настроения, тревожностью.
Осложнения
При длительном течении заболевания, развитии склероза в области мочепузырного треугольника со стенозом устьев мочеточников нарушается естественный пассаж мочи. У 75-77% пациентов со сморщенным мочевиком застойные процессы, обусловленные органическими причинами, завершаются развитием гидроуретеронефроза, снижением функциональных возможностей почек, нарастанием признаков хронической почечной недостаточности, осаждением солей в чашечно-лоханочной системе (мочекаменной болезнью). Возникновение пузырно-мочеточникового рефлюкса способствует распространению инфекции на расположенные выше отделы мочевыделительной системы, развитию хронического пиелонефрита.
Диагностика
Диагностический поиск у больных с подозрением на сморщенный мочевой пузырь направлен на оценку емкости органа, функциональной состоятельности детрузора, определение варианта заболевания, выявление причин, приведших к снижению анатомической или функциональной емкости. Больным назначают комплексное инструментальное обследование, включающее такие рекомендованные методы диагностики, как:
Информативным методом выявления возможных причин сморщенного мочевика является цистоскопия, позволяющая оценить состояние слизистой оболочки, обнаружить признаки склеротических процессов, получить образцы тканей для последующего гистологического исследования биоптата. У части пациентов с микроцистисом в общем анализе мочи определяются воспалительные изменения (лейкоцитурия, бактериурия), возбудитель цистита может быть выявлен с помощью посева мочи на микрофлору.
По показаниям для исключения возможной почечной патологии выполняют УЗИ почек, экскреторную урографию, нефросцинтиграфию, биохимический анализ крови, нефрологический комплекс. При подозрении на нейрогенный характер заболевания рекомендованы КТ черепа, МСКТ позвоночника, МРТ головного мозга, пояснично-крестцового отдела позвоночного столба.
Дифференциальная диагностика проводится между функциональной и органической формой расстройства, заболеваниями, которые способны спровоцировать развитие патологии, а также с эндофитным раком мочевого пузыря. По решению врача-уролога больному назначают консультации фтизиатра, инфекциониста, паразитолога, невропатолога, нейрохирурга, онколога.
Лечение сморщенного мочевого пузыря
Основными задачами при ведении больных с микроцистисом является уменьшение частоты мочеиспусканий, увеличение накопительной способности, устранение причин, вызвавших и поддерживающих заболевание. При точном установлении фактора, который спровоцировал расстройство, назначают соответствующее этиопатогенетическое лечение. Для купирования симптоматики в практической урологии применяют следующие терапевтические и хирургические подходы:
Лечение дополняют физиотерапевтическими процедурами, направленными на снижение гиперреактивности сморщенного детрузора: лекарственным электрофорезом холинолитиков и спазмолитиков, ультразвуковой терапией, парафиновыми аппликациями. Немедикаментозные методы, как и коррекция образа жизни с уменьшением психоэмоциональных нагрузок, оказывают больший эффект при нейрогенном уменьшении мочевого пузыря. При органическом поражении они менее значимы, хоть в целом могут облегчить симптоматику за счёт воздействия на вторичную гиперрефлексию.
Прогноз и профилактика
Правильный выбор метода лечения, соответствующего причине и форме заболевания, растяжимости мочепузырной стенки позволяет компенсировать расстройство, а при благоприятном прогнозе полностью восстановить объем сморщенного органа. Эффективность консервативной холинолитической терапии составляет 24-39%, и, поскольку у 47-57% пациентов возникают побочные эффекты, в настоящее время чаще выполняют более результативную хирургическую денервацию или цистопластику.
Профилактика заболевания направлена на предупреждение возникновения туберкулеза, своевременную терапию его легочных и внелегочных форм, лечение циститов различного происхождения, сокращение сроков искусственного отведения мочи с ранним началом тренировок детрузора. Для предупреждения сморщивания после проведения лучевой терапии тазовых органов мочевой пузырь необходимо опорожнять перед каждым сеансом ионизирующего воздействия, а в его полость вводить радиопротективные препараты.