На чем основан способ дистилляции
Дистилляция. Справка
Дистилляция (от лат. distillatio – стекание каплями) – перегонка, разделение жидких смесей на отличающиеся по составу фракции. Процесс основан на различии температур кипения компонентов смеси.
Процесс дистилляции был известен в Древнем Китае и Риме во втором тысячелетии до нашей эры и применялся главным образом для выделения душистых веществ из ароматических растений. Египтяне, постигнув тайны дистилляции вина, изобрели перегонный аппарат (аламбик), получивший впоследствии большое распространение у других народов.
Описание способа дистилляции и его использования в лечебных целях приводится в трудах персидского ученого Авиценны (930–1037).
В Древней Руси упоминание о постройке винокурни для получения «хлебного вина» водки относится к 1174 году.
Определенная роль в совершенствовании процесса дистилляции принадлежит алхимикам средневековья, но наибольшее развитие она получила в конце 19 – начале 20 веков в связи с внедрением в промышленности (спиртовой, нефтеперерабатывающей и др.) высокопроизводительных колонных аппаратов.
В зависимости от физических свойств компонентов разделяемых жидких смесей применяют различные способы дистилляции.
Простая дистилляция проводится частичным испарением кипящей жидкой смеси, непрерывным отводом и последующей конденсацией образовавшихся паров. Так как пары над кипящей жидкой смесью содержат низкокипящих компонентов больше, чем жидкость, то конденсат (называемый дистиллятом) обогащается, а неиспарившаяся жидкость (кубовый остаток) обедняется ими. При простой дистилляции содержание низкокипящих компонентов в паровой и жидкой фазах непрерывно падает. Поэтому состав дистиллята меняется во времени. Простая дистилляция – периодический процесс. Для ускорения процесса применяют полунепрерывную дистилляцию, при которой в дистилляционный куб непрерывно поступает исходная смесь, равная массе уходящих паров.
Фракционная дистилляция, называемая также дробной перегонкой, – одна из разновидностей простой дистилляции. Такую дистилляцию применяют для разделения смеси жидкостей на фракции, кипящие в узких интервалах температур. При этом дистилляты разных составов отводят (последовательно во времени) в несколько сборников. В каждом из этих дистиллятов (фракциях) преобладает один или несколько компонентов исходной смеси с близкими температурами кипения. Простую дистилляцию для улучшения разделения смесей часто комбинируют с противоточной дефлегмацией (частичная конденсация). При этом образующиеся в кубе пары частично конденсируются в дефлегматоре, конденсат (флегма) непрерывно возвращается в куб, а остаток паров после дефлегматора поступает в конденсатор, откуда дистиллят стекает в сборник. Этим способом достигается большее обогащение дистиллята низкокипящими компонентами, т.к. при дефлегмации паров преимущественно конденсируются высококипящие компоненты.
Равновесная дистилляция (однократное испарение) характеризуется испарением части жидкости и продолжительным контактом паров с неиспарившейся жидкостью до достижения фазового равновесия. Разделяемая смесь проходит по трубам, обогреваемым снаружи топочными газами. Образовавшаяся при этом парожидкостная смесь, близкая к равновесному состоянию, поступает в сепаратор для механического отделения жидкости от пара. Пары из сепаратора поступают в конденсатор, откуда дистиллят стекает в приемник, а оставшаяся в сепараторе жидкость отводится в сборник. В этом процессе соотношение между паром и жидкостью определяется материальным балансом и условиями фазового равновесия. Равновесная дистилляция редко применяется для двухкомпонентных смесей; хорошие результаты получают в основном в случае многокомпонентных смесей, из которых можно получить фракции, сильно различающиеся по составу.
Дистилляцию в токе водяного пара или инертных газов применяют, когда необходимо понизить температуру процесса отгонки, в случае разделения нетермостойких компонентов, а также для отгонки веществ с низкой температурой испарения от компонентов с высокой температурой испарения. Пузырьки водяного пара или инертного газа барботируют (продавливают) через слой жидкости. При дистилляции с водяным паром образовавшаяся смесь паров воды и летучего компонента отводится из аппарата и подвергается конденсации и охлаждению. Состав образующихся в кубе паров не зависит от состава жидкости, а температура кипения смеси всегда ниже температуры кипения каждого из компонентов при данном давлении. При дистилляции с инертным газом компоненты раствора испаряются в поток газа, даже если раствор не кипит, а парообразование при испарении может происходить при любых температурах, вне зависимости от внешнего давления, что позволяет вести процесс при низких температурах.
Молекулярная дистилляция основана на разделении жидких смесей свободным их испарением в высоком вакууме 133–13,3 мн/м2 (10–3–10–4 мм ртутного столба) при температуре ниже точки их кипения. Процесс проводят при взаимном расположении поверхностей испарения и конденсации на расстоянии, меньшем длины свободного пробега молекул перегоняемого вещества. Благодаря вакууму молекулы пара движутся от испаряющей поверхности к конденсирующей с минимальным числом столкновений. При молекулярной дистилляции изменение состава пара по сравнению с составом жидкости определяется различием скоростей испарения компонентов. Поэтому этим способом можно разделять смеси, компоненты которых обладают одинаковым давлением паров. При данной температуре жидкости и соответствующем ей давлении паров скорость молекулярной дистилляции растет с понижением давления в аппарате.
Для молекулярной дистилляции применяют аппараты с горизонтальными и вертикальными поверхностями испарения, а также получившие наибольшее промышленное применение центробежные аппараты. В последних процесс характеризуется наименьшими толщиной жидкой пленки (в среднем 0,05 мм) и временем ее пребывания на поверхности нагрева (0,03м–1,2 сек). В центробежных аппаратах на испаритель, представляющий собой быстровращающийся конус (иногда диск), подается разделяемая смесь. Центробежная сила перемещает жидкость от центра к периферии (вверх). Пары перегоняемого вещества собираются на неподвижном конденсаторе, расположенном параллельно поверхности испарителя, откуда дистиллят непрерывно отводится. Остаток после перегонки сбрасывается в кольцевой желоб и выводится из куба. Для увеличения эффекта разделения устанавливают несколько аппаратов последовательно.
Молекулярную дистилляцию применяют для разделения и очистки высокомолекулярных и термически нестойких органических веществ, например для очистки эфиров себациновой, стеариновой, олеиновой и других кислот, для выделения витаминов из рыбьего жира и различных растительных масел, при производстве медицинских препаратов, вакуумных масел и др.
В металлургии понятие дистилляции объединяет пирометаллургические процессы, основанные на переводе восстанавливаемого металла в парообразное состояние с последующей конденсацией. Металлургическая дистилляция – сочетание химического (окислительно-восстановительной реакции) и физического (испарения и конденсации) процессов. Восстановление проводят с использованием углеродистых восстановителей или металлотермическим способом. Возможно выделение свободного металла при окислительном обжиге сульфидных концентратов. Степень разделения при дистилляции определяется различием состава перегоняемой смеси и ее пара. Полнота перехода металла в газовую фазу при дистилляции определяется восстановлением металлов при температурах и давлениях, обеспечивающих получение восстановленного металла в парообразном агрегатном состоянии.
Дистилляция применяется также в химической, лесохимической, фармацевтической и других отраслях промышленности для грубого разделения смесей на фракции, когда не предъявляются высокие требования к чистоте получаемых продуктов, а также для очистки жидких смесей от нелетучих или малолетучих примесей.
Дистилляцию с дефлегмацией применяют в нефтепереработке и лабораторной практике, дистилляция с водяным паром – в химической, нефтехимической, парфюмерной и других отраслях промышленности для отгонки высококипящих компонентов из вязких смесей, содержащих значительные количества твердых или малолетучих жидких веществ. Также путем перегонки (однократной или многократной) на ликеро-водочных заводах получают полуфабрикат для множества алкогольных напитков: коньяка, рома, виски, а в домашних условиях – самогон.
В лабораторной практике условия дистилляции для некоторых видов продуктов стандартизованы. Наиболее известными являются ГОСТ 2177(ASTM D86) – перегонка 100 мл продукта с температурой кипения от комнатной до 400°С при атмосферном давлении. Это сделано для воспроизводимости результатов тестирования бензина, керосина, дизельного топлива, нефти, а также различных растворителей.
Дистилляция является давно известным и проверенным способом глубокой очистки воды.
Хорошо всем известный пример использования дистиллированной воды – заливка в аккумуляторы автомобиля. В быту же дистилляторы не нашли широкого применения.
И дело здесь совсем не в непригодности дистиллированной воды для питья. Вредность такой воды из-за отсутствия в ней «полезных» минеральных веществ – это, скорее, укоренившийся предрассудок. Дистиллированная вода действительно имеет невысокие вкусовые качества, часто ее вкус характеризуют как «затхлый». Однако с точки зрения влияния на здоровья нет никаких свидетельств того, что дистиллированная вода непригодна для питья.
Ограниченность же применения дистилляторов в быту объясняется следующими причинами:
Во-первых, бытовые дистилляторы имеют малую производительность (около одного литра в час).
Во-вторых, в бойлере дистиллятора постоянно образуются осадок, накипь и т.п., которые надо вычищать.
В-третьих, дистилляторы излучают тепло и в довольно значительных количествах.
В-четвертых, дистилляторы потребляют значительное количество электроэнергии, что для многих применений делает их использование менее рентабельным, чем обратный осмос (способ очистки воды, при котором вода, проходит через специальную полупроницаемую мембрану) или деминерализация на ионообменных смолах.
Самогоноварение, дистилляция, ректификация и все что с этим связано… (Часть 1)
Приветствую Вас дорогие Алкобушники и всех «сочувствующих» им…:)
Сразу небольшое вступление от автора:
Я не претендую на звание «гуру» самогоноварения и возможно мои знания в области приготовления алкоголя ошибочны, так же, как знания у людей в древности думающих, что земля плоская.
Поэтому, приветствую конструктивную критику, особенно со ссылками, расчетами, доводами или другими аргументами подкреплёнными наукой, логикой и здравым смыслом.
Цель данного поста раскрыть основы самогоноварения для людей никогда не сталкивающихся с этой темой, а не рассуждать, как лучше отбирать головы и хвосты, сколько нужно делать перегонок или с какого металла лучше аппарат для самогоноварения.
Перед тем как погрузится в пучину теории о домашнем самогоноварении и изучение дистилляции и ректификации и всего, что с этим связано, давайте немного поговорим о тех напитках, что мы видим на прилавках магазинов.
На прилавках магазинов мы видим: виски, коньяк, бурбон, ром, кальвадос, чача, водка, бренди, текила, абсент, джин, самогон.
Для большинства людей это: просто названия крепкого алкоголя, и подавляющее большинство «ценителей» этих напитков думают, что процесс производства каждого из перечисленных напитков кардинально отличается, да и вообще считают, что процесс производства этих напитков тайна за 7-ю замками!
Что еще знает обыватель обо всех этих напитках.
Обычно «среднестатистический ценитель» крепкого алкоголя знает, что эти напитки делятся на следующие группы:
Хотя для некоторых ценителей, ром под «большим» вопросом! Ведь его пили обычные матросы, но раз это заморское пойло, то для большинства оно «премиум класса»!
— ну и третий класс напитков который в последнее время стал стремительно набирать популярность, и является очень интересным продуктом для маркетологов – самогон.
Если про «благородные напитки» и водку всем известно, что их производят на специальных заводах по старинным рецептам, и каждый напиток получают по уникальной технологии, то про самогон знают только то, что его делают в деревне на специальном самогонном аппарате.
А еще всем известно, что самогоноварение запрещено.
Про запрет самогоноварения доходчиво рассказано в короткометражном фильме 1961г. «Самогонщики».
Сразу внесем ясность про запрет на самогоноварение:
На сегодняшний день, гнать самогон для личного потребления не возбраняется!
А вот гнать с целью сбыта (продажи) запрещено!
Это как с помидорами на даче:
Для себя выращивай на здоровье!
А если ты соберешься продать помидорки не оформив все необходимые документы и не заплатив налоги, то ты преступник!
Так, что гнать самогон настолько же законно, как и выращивать помидорки (при условии, что это только для личного употребления, ну или безвозмездного дарения).
А теперь давайте узнаем, как появляется самогон.
Виски, коньяк, бурбон, ром, кальвадос, чача, бренди, текила, абсент, джин, самогон это родственные напитки.
Процесс, а точнее технология производства всех перечисленных напитков одинаковая.
В основе изготовления всех этих напитков лежит дистилляция.
Дистилляция – процесс испарения жидкости с последующей конденсацией и охлаждением пара.
Да, все так просто: нагрели жидкость она испарилась, сконденсировалась, остыла и снова превратилась в жидкость.
А как дистилляция связана со всеми этими напитками, Мы узнаем позже…
А теперь не спеша, начнем с самого начала.
Для начала определим основные моменты:
просто дистиллировав первую попавшуюся жидкость алкоголь не получить!
Алкоголь можно получить только из той жидкости в которой он (алкоголь) присутствует хотя бы в небольшом количестве!
Самая простая брага это: вода + сахар + дрожжи + время
Да, дорогой читатель, ты правильно подумал:
К любому алкоголю человечество обязано дрожжам.
Эти безобидные крошки, которые дают нам вкуснейшую сдобу и благодаря которым появляется второй подбородок у любителей сдобы, причастны еще и ко всему алкоголю!
Семейство дрожжей очень большое:
— хлебопекарные дрожжи (производство хлеба, сдобы, пирожков);
— винные дрожи (дрожжи для производства вина);
— пивные дрожжи (дрожжи для производства пива);
— спиртовые дрожжи (дрожжи для производства браги с максимальным содержанием спирта (18-21%));
— еще есть дикие дрожжи (это предки всех современных дрожжей);
— В магазине за алкоголь просят бумажки (которые мы привыкли называть деньгами);
— Дрожжи за производство алкоголя «просят» сахар.
Не будем вдаваться в подробности, как дрожжи превращают(перерабатывают) сахар в алкоголь и углекислый газ, и какая им от этого выгода.
Так же не буду вдаваться в подробности, как правильно поставить брагу, поскольку основной наш вопрос, как из браги с содержанием алкоголя 12% получают 40-80% алкоголь.
В основе процесса причастного к появлению крепкого алкоголя из браги, который в дальнейшем мы будем называть дистилляцией, лежит процесс испарения жидкости.
Испарение – процесс перехода вещества из жидкого состояния в газообразное, то есть превращение жидкости в пар.
Как мы знаем, а может это станет для кого то из читателей откровением… Разные жидкости (вещества) начинают кипеть (как и собственно активно испаряться) при разной температуре.
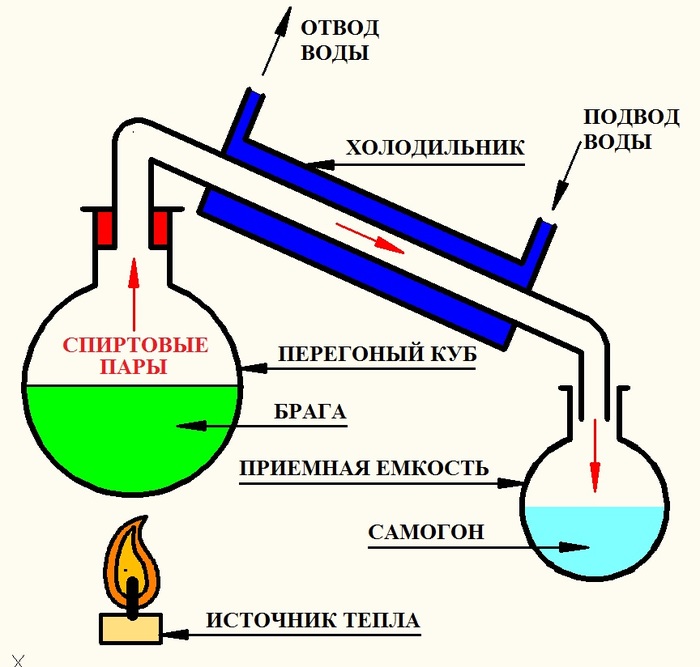
Дистиллятор, он же самогонный аппарат, состоит из:
Есть одно условие для работы дистиллятора – перегонный куб и холодильник должны быть герметично соединены между собой.
С конструкцией дистиллятора разобрались и поэтому начинаем разбираться в том, как и почему работает дистиллятор:
1.В перегонный куб заливается брага или любая спиртосодержащая жидкость.
2.Под перегонный куб помещают источник тепла (печку, свечку и т.д.). Можно и в перегонный куб поместить источник тепла такой источник тепла называется – тэн.
3. При нагревании с браги (состоящей из воды, спирта) начинает активно испаряться жидкость с более низкой температурой кипения. В нашем случае активнее испаряется этиловый спирт с температурой кипения 78°С.
Поскольку в процессе дистилляции в перегонном кубе образуется все больше и больше паров жидкости с более низкой температурой кипения, то рано или поздно они (спиртовые пары) сами себя выталкивают в холодильник.
4. Попав в холодильник «спиртовой пар», охлаждаться и конденсироваться.
5. Конденсат с холодильника под силой тяжести стекает в приемную емкость.
Для тех, кто еще не понял: конденсат спиртовых паров – это и есть более крепкий алкоголь.
Теперь мы знаем устройство и принцип работы самого простого самогонного аппарата!
И в продолжение темы самогоноварения поговорим об апгрейте (усовершенствовании) самогонного аппарата и повышении качества самогона.
И сразу появляется справедливый вопрос:
«Зачем усовершенствовать самогонный аппарат, если он и так работает?
Согласен, аппарат работает, но качество получаемого самогона не самое лучшее.
«Почему не лучшее? Ведь спирт испарятся при +78, а вода при +100!»
А вот на этом моменте и начинается «наука о самогоноварении»!
Почему же при «правильной» перегонке на «правильном» аппарате, вкус и запах будет лучше?
Кроется в составе браги, состав которой влияет на состав самогона.
Появлению спирта в браге мы обязаны дрожжам.
В теории дрожжи производят только этиловый спирт, и брага состоит из воды, спирта, дрожжей.
Но в жизни дрожжи производят не только этиловый спирт, а еще: метанол, изопропиловый, изобутиловый, гептиловый спирт и прочую крайне вредную гадость. И эта вся гадость находится в браге вместе с этиловым спиртом.
Температура кипения у всех названных спиртов и прочей гадости разная (метиловый при +64,5; этиловый кипит при +78С; изобутиловый 84,4С).
При нагревании браги все перечисленные спирты испаряются не одновременно. Сначала испаряются легкокипящие, и по мере выкипания легкокипящих фракций, температура в перегоном кубе повышается и начинают кипеть фракции с более высокой температурой кипения.
Зная, что разные фракции испаряются при разной температуре мы можем разделить их, то есть вначале мы можем отобрать в одну приемную емкость то, что испарилось в первую очередь, а во вторую приемную емкость то, что начало испаряться потом.
Поэтому «по науке» перегонка происходит по следующим образом:
1. сначала отбирают «головы» в отдельную емкость;
2. сменив емкость отбираем тело;
В идеале в «теле» только этиловый спирт.
После отбора «тела» начинают испаряться фракции с более высокой температурой кипения, чем у этилового спирта (назовем их «хвостами»);
3. сменив еще раз емкость отбираем хвосты.
Как уже говорил, в жизни не происходит все идеально: тело, головы, хвосты имеют разную температуру кипения, но на практике они не испаряются строго по очереди. Конечно «Хвосты» не лезут вперед «Голов», но в «тело» попадают и «головы» и «хвосты». То есть испарение не происходит идеально, как в книжке, испаряются все фракции сразу(головы. тело, хвосты), вот только при определенной температуре какая то фракция испаряется активней, но об этом более подробно поговорим позже, а сейчас подведем промежуточный итог:
Перегонка на простершем самогоном аппарате позволяет получить крепкий алкоголь.
И если не перегонять все в одну емкость, а провести дробную перегонку ( перегонка с разделением на фракции), то качество получаемого самогона заметно улучшится, и повторная дробная перегонка позволит еще улучшить качество получаемого самогона.
Разобравшись с устройством простейшего самогонного аппарата и основами самогоноварения, переходим к рассмотрению усовершенствований этого аппарата.
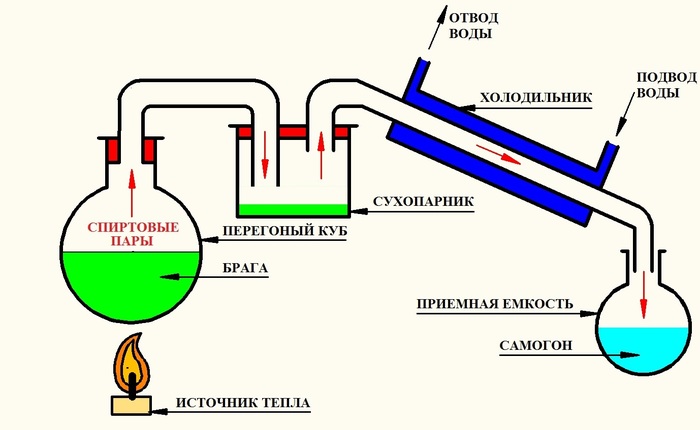
Одним из простейших и возможно первых усовершенствований самогонного аппарата стал сухопарник (пригубник).
Принцип работы сухопарника «до безобразия» прост:
1. Спиртовой пар с перегонного куба перемещается в сухопарник;
2. В сухопарнике спиртовой пар охлаждается частично конденсируется;
3. Из-за постоянно поступающего в сухопарник тепла в виде спиртовых паров из перегонного куба, сконденсированые пары снова закипают и испаряются, но в первую очередь испаряются более легкокипящие фракции, а низкокипящие фракции остаются сконденсированными в сухопарнике.
Вот и весь принцип работы сухопарника.
В завершении поста подведем итог:
-Теперь мы знаем как получают самогон «высшего» качества!
—А еще, как и обещал раскрою «тайну» благородных напитков.
А если говорить простым языком дистиллят – это самогон!
Отличия в производстве всех этих напитков конечно есть:
— Для каждого напитка брага готовиться из разного сырья;
— Некоторые напитки выдерживаю бочках;
— какие то напитки настаивают с травами и повторно перегоняют и т.д.
— виски это самогон, брага которого сделана на солоде. А после перегонки получены напиток выдержан в дубовых бочках.
— бурбон это самогон из браги в основе которой кукуруза и солод.
— у коньяка основой браги стал виноград.
— у бренди брага из фруктов или ягод.
— а у текилы брага сделана из агавы.
И еще, агава это не кактус!
— абсент, это дистиллят который настояли на травах, потом перегнали и снова настояли на травах.
Хотя лучше не говорить. А то он начав спорить стащат Вас на свой уровень, а там задавят опытом.
На этом заканчиваю первую часть.
Надеюсь, что вторую часть буду писать не сильно долго.
Дистилляция
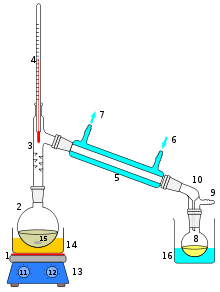
Дистилляция (лат. distillatio — стекание каплями) — перегонка, испарение жидкости с последующим охлаждением и конденсацией паров. Различают дистилляцию с конденсацией пара в жидкость (при которой получаемый конденсат имеет усреднённый состав вследствие перемешивания) и дистилляцию с конденсацией пара в твёрдую фазу (при которой в конденсате возникает распределение концентрации компонентов). Продуктом дистилляции является конденсат или остаток (или и то, и другое) – в зависимости от дистиллируемого вещества и целей процесса. Основными деталями дистилляционного устройства являются обогреваемый контейнер (куб) для дистиллируемой жидкости, охлаждаемый конденсатор (холодильник) и соединяющий их обогреваемый паропровод.
Содержание
История
До X века, у Авиценны дистилляция упоминается как метод получения эфирных масел.
Применение
Дистилляция применяется в промышленности и в лабораторной практике для разделения и рафинирования сложных веществ: для разделения смесей органических веществ (например, разделение нефти на бензин, керосин, соляр и др.; получение ароматических веществ в парфюмерии; получение алкогольного спирта) и для получения высокочистых неорганических веществ (например, металлов: бериллий, цинк, магний, кадмий и др.).
Теория
В теории дистилляции в первую очередь рассматриваются двухкомпонентные вещества. Действие дистилляции основано на том, что концентрация 



При 





Для различных режимов дистилляции выведены уравнения, связывающие содержание второго компонента в конденсате 







При дистилляции вещества с большой концентрацией компонентов с конденсацией пара в жидкость при несильной зависимости коэффициентов активности компонентов от их концентраций взаимосвязь величин 



Для дистилляции с конденсацией пара в жидкость при малом содержании примеси



Дистилляционные уравнения могут использоваться для описания процессов распределения примесей в других фазовых переходах из фазы с интенсивным перемешиванием (таких как переходы жидкий кристалл-кристалл, жидкий кристалл-жидкость, газ-плазма, а также в переходах, связанных с квантово-механическими состояниями – сверхтекучая жидкость, конденсат Бозе-Эйнштейна) – при подстановке в них соответствующих коэффициентов распределения.
Дистилляция с конденсацией пара в жидкость (простая перегонка, фракционная дистилляция, ректификация)
Простая перегонка — частичное испарение жидкой смеси путём непрерывного отвода и конденсации образовавшихся паров в холодильнике. Полученный конденсат называется дистиллятом, а неиспарившаяся жидкость — кубовым остатком.
Фракционная дистилляция (или дробная перегонка) — разделение многокомпонентных жидких смесей на отличающиеся по составу части — фракции путём сбора конденсата частями с различной летучестью, начиная с первой, обогащенной низкокипящим компонентом. Остаток жидкости обогащён высококипящим компонентом. Для улучшения разделения фракций применяют дефлегматор.
Ректификация — способ дистилляции, при котором часть жидкого конденсата (флегма) постоянно возвращается в куб, двигаясь навстречу пару в контакте с ним. В результате этого примеси, содержащиеся в паре, частично переходят во флегму и возвращаются в куб, при этом чистота пара (и конденсата) повышается (См. ректификация, ректификационная колонна).
Дистилляция с конденсацией пара в твёрдую фазу (с конденсацией пара в градиенте температуры; с направленным затвердеванием конденсата; зонная дистилляция)
Дистилляция с конденсацией пара в градиенте температуры – дистилляционный процесс, в котором конденсация в твёрдую фазу осуществляется на поверхности, имеющей градиент температуры, с многократным реиспарением частиц пара. Менее летучие компоненты осаждаются при более высоких температурах. В результате в конденсате возникает распределение примесей вдоль температурного градиента, и наиболее чистая часть конденсата может быть выделена в качестве продукта. Разделение компонентов пара при реиспарении подчиняется собственным закономерностям. Так, при молекулярной дистиляции соотношение между количествами 


Дистилляция с направленным затвердеванием конденсата (дистилляция с вытягиванием дистиллята) – дистилляционный процесс в контейнере удлинённой формы c полным расплавлением дистиллируемого вещества и конденсацией пара в твёрдую фазу по мере вытягивания конденсата в холодную область. Процесс разработан теоретически.
В получаемом конденсате возникает неравномерное распределение примесей, и наиболее чистая часть конденсата может быть выделена в качестве продукта. Процесс является дистилляционным аналогом нормальной направленной кристаллизации. Распределение примеси в конденсате описывается уравнением:

где С – концентрация примеси в дистилляте на расстоянии х от начала, L – высота конденсата при полностью испарившемся дистиллируемом материале.
При движении зонного нагревателя вдоль контейнера сверху вниз в контейнере формируется твёрдый конденсат с неравномерным распределением примесей, и наиболее чистая часть конденсата может быть выделена в качестве продукта. Процесс может быть повторён многократно, для чего конденсат, полученный в предыдущем процессе, должен быть перемещён (без переворота) в нижнюю часть контейнера на место рафинируемого вещества. Неравномерность распределения примесей в конденсате (т. е. эффективность очистки) растёт с увеличением числа повторений процесса.
Зонная дистилляция является дистилляционным аналогом зонной перекристаллизации. Распределение примесей в конденсате описывается известными уравнениями зонной перекристаллизации с заданным числом проходов зоны – при замене коэффициента распределения k для кристаллизации на коэффициент разделения α для дистилляции. Так, после одного прохода зоны

где С – концентрация примеси в конденсате на расстоянии х от начала конденсата, λ – длина жидкой зоны.