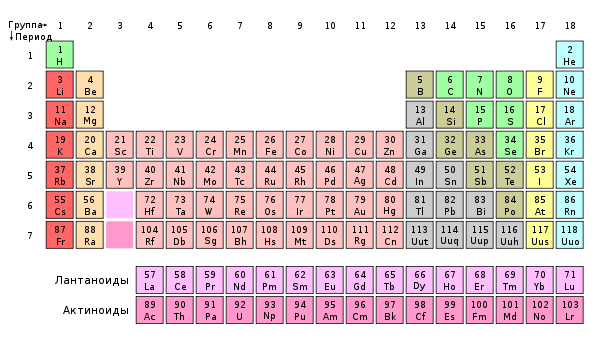
На что делятся группы в химии
Группа периодической системы
Номер группы определяется количеством электронов на внешней оболочке атома (валентных электронов) и, как правило, соответствует высшей валентности атома.
В короткопериодном варианте периодической системы группы подразделяются на подгруппы — главные (или подгруппы A), начинающиеся с элементов первого и второго периодов, и побочные (подгруппы В), содержащие d-элементы. Подгруппы также имеют названия по элементу с наименьшим зарядом ядра (как правило, по элементу второго периода для главных подгрупп и элементу четвёртого периода для побочных подгрупп). Элементы одной подгруппы обладают сходными химическими свойствами.
С возрастанием заряда ядра у элементов одной группы из-за увеличения числа электронных оболочек увеличиваются атомные радиусы, вследствие чего происходит снижение электроотрицательности, усиление металлических и ослабление неметаллических свойств элементов, усиление восстановительных и ослабление окислительных свойств образуемых ими веществ.
Несмотря на то, что в России и в большинстве стран мира признаётся, что Дмитрий Иванович Менделеев изобрел периодическую таблицу, еще до «холодной войны» в США сформировалось мнение, что первооткрываетелем является Уильям Олдинг.
Нумерация групп
Несмотря на это, продолжают применяться ставшие традиционными системы нумерации с использованием римских цифр и латинских букв, отличающиеся для Америки и Европы.
Современная система нумерации содержит следующие группы (старые системы, Европейская и Американская, приведены в скобках):
Полезное
Смотреть что такое «Группа периодической системы» в других словарях:
Группа периодической таблицы — Группа периодической системы химических элементов последовательность атомов по возрастанию заряда ядра, обладающих однотипным электронным строением. Номер группы определяется количеством электронов на внешней оболочке атома (валентных электронов) … Википедия
Четвёртый период периодической системы — К четвёртому периоду периодической системы относятся элементы четвёртой строки (или четвёртого периода) периодической системы химических элементов. Строение периодической таблицы основано на строках для иллюстрации повторяющихся (периодических)… … Википедия
Первый период периодической системы — К первому периоду периодической системы относятся элементы первой строки (или первого периода) периодической системы химических элементов. Строение периодической таблицы основано на строках для иллюстрации повторяющихся (периодических) трендов в… … Википедия
Второй период периодической системы — Ко второму периоду периодической системы относятся элементы второй строки (или второго периода) периодической системы химических элементов. Строение периодической таблицы основано на строках для иллюстрации повторяющихся (периодических) трендов в … Википедия
Пятый период периодической системы — К пятому периоду периодической системы относятся элементы пятой строки (или пятого периода) периодической системы химических элементов. Строение периодической таблицы основано на строках для иллюстрации повторяющихся (периодических) трендов в… … Википедия
Третий период периодической системы — К третьему периоду периодической системы относятся элементы третьей строки (или третьего периода) периодической системы химических элементов. Строение периодической таблицы основано на строках для иллюстрации повторяющихся (периодических) трендов … Википедия
Седьмой период периодической системы — К седьмому периоду периодической системы относятся элементы седьмой строки (или седьмого периода) периодической системы химических элементов. Строение периодической таблицы основано на строках для иллюстрации повторяющихся (периодических) трендов … Википедия
Шестой период периодической системы — К шестому периоду периодической системы относятся элементы шестой строки (или шестого периода) периодической системы химических элементов. Строение периодической таблицы основано на строках для иллюстрации повторяющихся (периодических) трендов в… … Википедия
Короткая форма периодической системы элементов — Короткая форма таблицы Менделеева основана на параллелизме степеней окисления элементов главных и побочных подгрупп: например, максимальная степень окисления ванадия равна +5, как у фосфора и мышьяка, максимальная степень окисления хрома равна +6 … Википедия
Группа — Сюда перенаправляется запрос «Группировка». На эту тему нужна отдельная статья … Википедия
Урок №58. Периодическая таблица химических элементов (короткая форма): А- и Б-группы, периоды
ПЕРИОДИЧЕСКАЯ ТАБЛИЦА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ
Графическим изображением периодического закона является периодическая таблица. Короткая её форма содержит 7 периодов и 8 групп.
Короткая форма таблицы Д.И. Менделеева
Полудлинный вариант таблицы Д.И. Менделеева
Существует ещё и длинный вариант таблицы, он похож на полудлинный, но только лантаноиды и актиноиды не вынесены за пределы таблицы.
Оригинал таблицы Д. И. Менделеева
1. Период – химические элементы, расположенные в строчку (1 – 7)
Малые (1, 2, 3) – состоят из одного ряда элементов
Большие (4, 5, 6, 7) – состоят из двух рядов – чётного и нечётного
Периоды могут состоять из 2 (первый), 8 (второй и третий), 18 (четвертый и пятый) или 32 (шестой) элементов. Последний, седьмой период незавершен.
Все периоды (кроме первого) начинаются щелочным металлом, а заканчиваются благородным газом.
Во всех периодах с увеличением относительных атомных масс элементов наблюдается усиление неметаллических и ослабление металлических свойств. В больших периодах переход свойств от активного металла к благородному газу происходит более медленно (через 18 и 32 элемента), чем в малых периодах (через 8 элементов). Кроме того, в малых периодах слева направо валентность в соединениях с кислородом возрастает от 1 до 7 (например, от Na до Cl). В больших периодах вначале валентность возрастает от 1 до 8 (например, в пятом периоде от рубидия к рутению), затем происходит резкий скачок, и валентность уменьшается до 1 у серебра, потом снова возрастает.
Главные подгруппы состоят из элементов малых и больших периодов.
Побочные подгруппы состоят из элементов только больших периодов.
В главных подгруппах сверху вниз металлические свойства усиливаются, а неметаллические ослабевают. Элементы главных и побочных групп сильно отличаются по свойствам.
Номер группы показывает высшую валентность элемента (кроме N, O, F).
Что такое группа в химии: таблица металлов и неметаллов в периодической системе
Свойства химических элементов позволяют объединять их в соответствующие группы. На этом принципе была создана периодическая система, изменившая представление о существующих веществах и позволившая предположить существование новых, ранее неизвестных элементов….
Периодическая система Менделеева
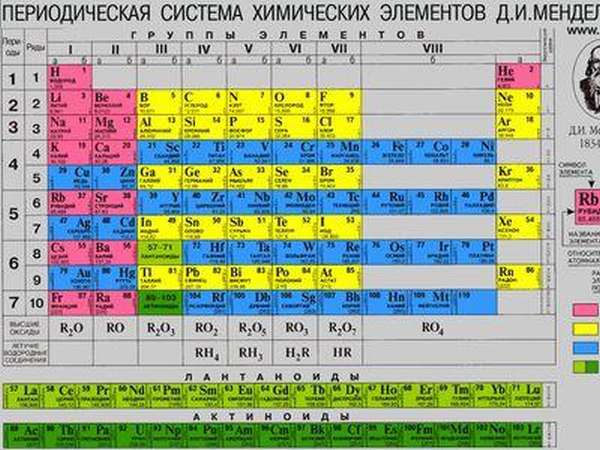
Периодическая система Менделеева в химии свела в единую систему все существующие элементы, прежде считавшиеся просто отдельными веществами.
На основании ее изучения были предсказаны, а впоследствии — синтезированы новые химические вещества. Значение этого открытия для науки невозможно переоценить, оно значительно опередило свое время и дало толчок к развитию химии на многие десятилетия.
Существует три наиболее распространенных варианта таблицы, которые условно именуются «короткая», «длинная» и «сверхдлинная». Основной считается длинная таблица, она утверждена официально. Отличием между ними является компоновка элементов и длина периодов.
Что такое период
Система содержит 7 периодов. Они представлены графически в виде горизонтальных строк. При этом, период может иметь одну или две строки, называемые рядами. Каждый последующий элемент отличается от предыдущего возрастанием заряда ядра (количества электронов) на единицу.
Если не усложнять, период — это горизонтальная строка периодической таблицы. Каждый из них начинается металлом и заканчивается инертным газом. Собственно, это и создает периодичность — свойства элементов изменяются внутри одного периода, вновь повторяясь в следующем. Первый, второй и третий периоды — неполные, они называются малыми и содержат соответственно 2, 8 и 8 элементов. Остальные — полные, они имеют по 18 элементов.
Что такое группа
Группа — это вертикальный столбец, содержащий элементы с одинаковым электронным строением или, говоря проще, с одинаковой высшей валентностью. Официально утвержденная длинная таблица содержит 18 групп, которые начинаются со щелочных металлов и заканчиваются инертными газами.
Каждая группа имеет свое название, облегчающее поиск или классификацию элементов. Усиливаются металлические свойства в независимости от элемента по направлению сверху-вниз. Это связано с увеличением количества атомных орбит чем их больше, тем слабее электронные связи, что делает более ярко выраженной кристаллическую решетку.
Металлы в периодической таблице
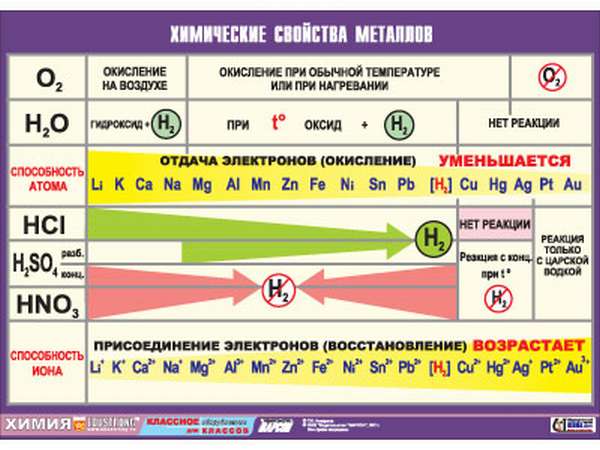
Положение металлов
Какого положение металлов в периодической системе? Элементы расположены по увеличению атомной массы или количества электронов и протонов. Их свойства изменяются периодически, поэтому аккуратного размещения по принципу «один к одному» в таблице нет. Как определить металлы, и возможно ли это сделать по таблице Менделеева? Для того, чтобы упростить вопрос, придуман специальный прием: условно по местам соединения элементов проводится диагональная линия от Бора до Полония (или до Астата). Те, что оказываются слева — металлы, справа — неметаллы. Это было бы очень просто и здорово, но есть исключения — Германий и Сурьма.
Важно! Это работает только в длинной системе, на коротком варианте таблицы Менделеева многие металлы оказываются справа.
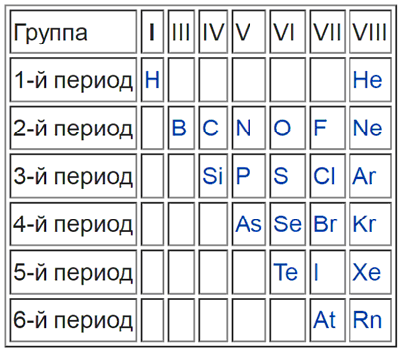
На рисунке можно наглядно увидеть, какие элементы являются неметаллами и как они располагаются в таблице по группам и периодам.
Это интересно! Каково содержание кислорода в воздухе: процентный состав и норма
Общие физические свойства
Существуют общие физические свойства металлов. К ним относятся:
Следует понимать, что свойства металлов очень различаются относительно их химической или физической сути. Некоторые из них мало похожи на металлы в обыденном понимании этого термина. Например, ртуть занимает особенное положение. Она при обычных условиях находится в жидком состоянии, не имеет кристаллической решетки, наличию которой обязаны своими свойствами другие металлы. Свойства последних в этом случае условны, с ними ртуть роднят в большей степени химические характеристики.
Интересно! Элементы первой группы, щелочные металлы, в чистом виде не встречаются, находясь в составе различных соединений.
Самый мягкий металл, существующий в природе — цезий — относится к этой группе. Он, как и другие щелочные подобные вещества, мало общего имеет с более типичными металлами. Некоторые источники утверждают, что на самом деле, самый мягкий металл калий, что сложно оспорить или подтвердить, поскольку ни тот, ни другой элемент не существует сам по себе будучи выделенным в результате химической реакци они быстро окисляются или вступают в реакцию.
Вторая группа металлов — щелочноземельные — намного ближе к основным группам. Название «щелочноземельные» происходит из древних времен, когда окислы назывались «землями», поскольку они имеют рыхлую рассыпчатую структуру. Более-менее привычными (в обиходном смысле) свойствами обладают металлы начиная с 3 группы. С увеличением номера группы количество металлов убывает, замещаясь неметаллическими элементами. Последняя группа состоит из инертных (или благородных) газов.
Определение металлов и неметаллов в таблице Менделеева. Простые и сложные вещества.
Простые вещества (металлы и неметаллы)
Вывод
Соотношение металлов и неметаллов в таблице Менделеева явно перевешивает в пользу первых. Такое положение свидетельствует о том, что группа металлов объединена слишком широко и требует более подробной классификации, что признается научным сообществом.
Это интересно! Основной закон Гесса и следствия из него
Периодическая система состоит из семи периодов, десяти рядов и восьми групп, каждая из которых делится на главную и побочную подгруппы.
Группа периодической системы химических элементов (ПСХЭ) — вертикальный ряд химических элементов, расположенных по возрастанию заряда атомного ядра, которые имеют одинаковую высшую валентность в их соединениях, равную номеру группы. Номер группы указывается римской цифрой.
Например, атом натрия (Z=11) имеет высшую валентность I, т. к расположен в I группе ПСХЭ, а атом хлора (Z=17) – VII, т. к. расположен в VII группе.
Например, все элементы II группы имеют высшую валентность II, поэтому формула высших оксидов элементов II периода в общем виде RO (MgO, CaO, BaO, ZnO и т. п.). Все элементы IV периода проявляют высшую валентность равную IV, поэтому формула высших оксидов элементов IV периода в общем виде RO2 (CO2, SiO2, TiO2, GeO2, и т. п.).
Иключения составляют элементы, указанные в таблице 1.
В короткопериодном варианте периодической системы группы подразделяются на подгруппы — главные (или подгруппы A) и побочные (подгруппы В).
Главные подгруппы начинаются с элементов первого и второго периодов, побочные – с элементов IV периода.
Главная подгруппа содержит элементы малых и больших периодов. Побочная подгруппа содержит элементы только больших периодов.
Рис. 2. Главная и побочная подгруппа 1 группы
Рис. 3. Некоторые главные подгруппы ПСХЭ
Рис. 4. Некоторые побочные подгруппы ПСХЭ
Подгруппы также имеют названия по элементу с наименьшим порядковым номером (как правило, по элементу второго периода для главных подгрупп и элементу четвёртого периода для побочных подгрупп).
Инертные элементы или благородные газы
Элементы одной подгруппы обладают сходными химическими свойствами, т. к. элементы подгрупп сходны между собой по строению внешнего электронного уровня.
Закономерные изменения, наблюдаемые в главных подгруппах.
В каждой главной подгруппе сверху вниз происходит усиление металлических и ослабление неметаллических свойств, также усиливаются восстановительные и ослабевают окислительные свойства элементов и образуемых ими соединений.
Все элементы подочных подгрупп являются металлами.
Вопросы для самопроверки
1. Из каких структурных элементов состоит периодическая система химических элементов.
2. Что такое группа?
3. Сколько групп в периодической системе химических элементов?
4. Элементы каких периодов входят в главную подгруппу?
5. Сколько подгрупп в периодической системе?
6. Элементы каких периодов входят в побочные подгруппы?
7. На сколько подгрупп делится каждая группа?
8. Что общего у элементов одной группы?
9. Что общего у элементов одной подгруппы?
10. Как изменяются свойства элементов главных подгрупп сверху вниз?
11. Какими свойствами обладают элементы побочных подгрупп?
12. Какая группа содержит одну главную и три побочных подгруппы?
1. Из периодов, рядов, групп и подгрупп.
2. Группа — вертикальный ряд химических элементов, расположенных по возрастанию заряда атомного ядра, которые имеют одинаковую высшую валентность в их соединениях, равную номеру группы.
4. Малых и больших. Главная подгруппа начинается элементом малого периода (I или II). См. рис 3.
6. Только больших. Главная подгруппа начинается с элемента IV периода. См. рис 4.
7. I – VII группы делятся на две подгруппы – главную и побочную. VIII группа состоит из одной главной – инертные газы и трех побочных: подгруппа железа, подгруппа кобальта и подргуппа никеля.
8. Как правило, высшая валентность элементов. Она равна номеру группы, в которой находится элемент.
9. Химические свойства, т. к. элементы подгрупп сходны между собой по строению внешнего электронного уровня.
10. В каждой главной подгруппе сверху вниз происходит усиление металлических и ослабление неметаллических свойств, также усиливаются восстановительные и ослабевают окислительные свойства элементов и образуемых ими соединений.
Задачи для самостоятельного решения.
1. В какой группе и подруппе находятся элементы с порядковыми номерами 6, 40, 26, 53, 80? Укажите их символ, русское название, относительную атомную массу.
2. Напишите символ, название, порядковый номер элемента и относительную атомную массу элемента, который находится: а) в III периоде, главной подгруппе VI группы; б) в V периоде, побочной группе II группы; в) в VI периоде, главной подгруппе IV группы;
г) в IV периоде, побочной группе VII группы.
3. Напишите символы, названия и порядковые номера всех элементов малых периодов, которые находятся в главной подгруппе IV группы.
4. Напишите символы, названия и порядковые номера всех элементов, которые находятся в побочной подгруппе II группы.
5. Какие элементы главной подгруппы V группы являются элементами больших периодов? Напишите их символы, русские названия и порядковые номера.
6. Какой элемент: кальций или барий имеет более выраженные металлические свойства и почему?
7. Какой элемент: сера или кислород имеет более выраженные неметаллические свойства и почему?
8. Какой элемент VII группы главной подгруппы является самым активным неметаллом? Почему?
9. Какой элемент I группы главной подгруппы является самым активным металлом? Почему?
10. В каких группах периодической системы все элементы являются металлами?
11. В какой группе всего один неметалл?
12. В каких группах периодической системы все элементы являются неметаллами?
13. Напишите форм, 25, 48, 13, в которых эти элементы имеют высшую валентность.
14. Напишите формулы оксидов всех элементов IV группы главной подгруппы, в которых эти имеют высшую валентность.