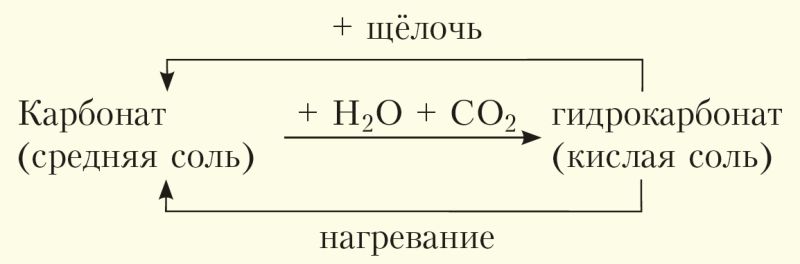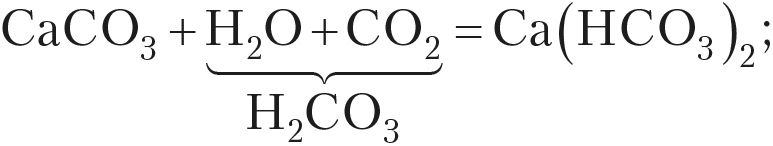На что распадается угольная кислота
Угольная кислота. Свойства, получение, применение и цена угольной кислоты
Вместе получается угольная кислота. Формула вещества записывается как H2CO3. Однако, выделить кислоту в виде порошка, как многие, не получается. Максимум – льдинки. Почему? Давайте разбираться.
Свойства угольной кислоты
Раствор угольной кислоты легко составляется и столь же просто распадается на изначальные компоненты. Особенно активно углекислый газ выделяется при нагреве. При пониженных температурах диссоциация угольной кислоты замедляется.
Это, в частности, заставляет героиню статьи проявлять электролитические свойства. Проводить ток позволяет частичное распадение кислоты на ионы. У твердых электролитов они движутся внутри кристаллических решеток. Угольная кислота выделяет ионы только в растворах.
Так именуют отдельное существование молекул воды и распределенного в ней углекислого газа. Но, встречаются в растворах и карбонатные ионы CO 32- и бикарбонатные частицы HCO3. Все вместе представляет долю кислоты в воде.
В обычных условиях доля угольной кислоты в воде мала, как и в воздухе, почве. В земле вещества, к примеру, от 0,0002 до 0,0005 частей. Ученые считают, что так было не всегда.
Ища причины гигантских размеров древних растений, исследователи пришли к выводу, что в прошлые эпохи и в почве, и в атмосфере, героини статьи было в несколько раз больше.
Растения способны усваивать вещество и пользуются его влиянием на растворимость в земле минеральных веществ, необходимых травам, кустам и деревьям для питания.
Проводились опыты выращивания растений в атмосферах с разным содержанием угольной кислоты. Рекорды показали экземпляры, находящие в воздухе с содержанием H2CO3 от 5-ти до 10-ти процентов.
Получение угольной кислоты
Если извне поступают продукты с явной кислотностью или щелочной средой, буферные агенты удерживают нужный pH, пока «гости» переработаются и выведутся с потом, калом, мочой.
Побочным продуктом углекислота является, так же, при брожении. Так что, соединением запасаются, к примеру, во время изготовления вина. Еще один источник углекислоты – выпуск гашеной извести.
Применение угольной кислоты
В чистом виде угольная кислота нужна не только организму человека растениям, но и на производствах. В процессе сварки, к примеру, героиня статьи служит защитной средой, подобно аргону.
Выходя «на свободу» кислота превращается в пар, поглощая тепло окружающей среды, заполняя площади. В открытых помещениях системы углекислого пожаротушения не используют, лишь в трюмах, кладовых, насосных, отсеках электростанций. Принцип действия сводится к снижению уровня кислорода до 8%. Горение при таком показатели прекращается.
К угнетению дыхательного центра прибегают, в основном, при отравлениях летучими ядами и асфиксии новорожденных. Асфиксия – удушение. У младенцев вызывается, обычно, рвотными массами и первородным калом. Углекислота способствует сокращению легочных тканей, восстановлению их функции.
Удается это, так же, больным волчанкой, бородавками, лепрозными узлами. Соприкасаясь с кислотным льдом, пораженные участки кожи разрушаются. Грубо говоря, угольная кислота вырезает лишнее, подобно лазеру.
В жидком виде углекислота тоже может выступать хладагентом, используется в морозильном оборудовании. Еще одно поле применения – умягчение воды. Ее, правда, улучшает не чистая кислота, а одна из ее солей – атронная известь.
Цена угольной кислоты
Структурная формула угольной кислоты вмещается промышленниками в баллоны и цистерны. Прежде чем поместить героиню статьи в них, ее охлаждают. Это помогает сгустить вещество.
Предложений купить его единицы. Чаще, реализуют углекислые соединения. За димитилкарбонат, к примеру, просят около 1 500 рублей за килограмм. Вещество растворяет эфиры целлюлозы, а посему, применяется в органическом синтезе.
За натриевую соль, а попросту соду, приходится выкладывать 80-200 рублей за килограмм. Ценники разнятся в зависимости от производителей и добавок к продукту. Так, бывает, к примеру, кальцированная сода.
Если смотреть в глобальных масштабах, угольная кислота бесценна. Именно она является источником углерода для живых материй, причем, единственным. Углерод есть и в нефти, вулканических выбросах.
Есть даже мнение, что атланты – не чудо-люди или пришельцы из космоса, а всего лишь достойные «дети» атмосферы, насыщенной соединением воды и углекислого газа. Но, это теория в стиле «РенТВ». Сосредоточимся на научных фактах.
Угольная кислота
реальные: 1) 3,60;
2) 10,33
кажущаяся [1] : 6,37
Содержание
Физические свойства
Молекула угольной кислоты имеет плоское строение. Центральный углеродный атом имеет sp²-гибридизацию. В гидрокарбонат- и карбонат-анионах происходит делокализация π-связи. Длина связи C—O в карбонат-ионе составляет 129 пм.
Химические свойства
Равновесие в водных растворах и кислотность
Угольная кислота существует в водных растворах в состоянии равновесия с гидратом диоксида углерода:

В свою очередь растворённый гидрат диоксида углерода находится в равновесии с газообразным диоксидом углерода:
Данное равновесие при повышении температуры сдвигается вправо, а при повышении давления — влево (подробнее см. Абсорбция газов).
Угольная кислота подвергается обратимому гидролизу, создавая при этом кислую среду:

Однако, для практических расчётов чаще используют кажущуюся константу кислотности, учитывающую равновесие угольной кислоты с гидратом диоксида углерода:
Гидрокарбонат-ион подвергается дальнейшему гидролизу по реакции

Таким образом, в растворах, содержащих угольную кислоту, создается сложная равновесная система, которую можно изобразить в общем виде следующим образом:
Значение pH в такой системе, соответствующей насыщенному раствору диоксида углерода в воде при 25 °C и давлении 760 мм рт. ст., можно рассчитать по формуле:

Разложение
При повышении температуры раствора и/или понижении парциального давления диоксида углерода равновесие в системе 
Взаимодействие с основаниями и солями
Угольная кислота вступает в реакции нейтрализации с растворами оснований, образуя средние и кислые соли — карбонаты и гидрокарбонаты соответственно:




При взаимодействии угольной кислоты с карбонатами образуются гидрокарбонаты:

Получение
Угольная кислота образуется при растворении в воде диоксида углерода:
Содержание угольной кислоты в растворе увеличивается при понижении температуры раствора и увеличении давления углекислого газа.
Также угольная кислота образуется при взаимодействии её солей (карбонатов и гидрокарбонатов) с более сильной кислотой. При этом бо́льшая часть образовавшейся угольной кислоты, как правило, разлагается на воду и диоксид углерода:

Применение
Угольная кислота всегда присутствует в водных растворах углекислого газа (см. Газированная вода).
В биохимии используется свойство равновесной системы 
Органические производные
Некоторые представители подобных соединений перечислены в таблице.
| Класс соединений | Пример соединения |
|---|---|
| Сложные эфиры | поликарбонаты |
| Хлорангидриды | фосген |
| Амиды | мочевина |
| Нитрилы | циановая кислота |
| Ангидриды | пироугольная кислота |
См. также
Примечания
Литература
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Hg2 2+ | Pb 2+ | Sn 2+ | Cu + | Cu 2+ | |
| OH − | P | P | P | — | P | М | Н | М | Н | Н | Н | — | Н | Н | Н | Н | Н | — | — | Н | Н | Н | Н | |
| F − | P | Н | P | P | Р | М | Н | Н | М | Р | Н | Н | Н | Р | Р | М | Р | Р | М | М | Н | Р | Н | Р |
| Cl − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | Н | М | — | Н | Р |
| Br − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | Н | М | Р | H | Р |
| I − | P | P | P | P | Р | Р | Р | Р | Р | Р | ? | Р | — | Р | Р | Р | Р | Н | Н | Н | Н | М | Н | — |
| S 2− | P | P | P | P | — | Р | М | Н | Р | — | — | Н | — | Н | Н | Н | Н | Н | Н | — | Н | Н | Н | Н |
| SO3 2− | P | P | P | P | Р | М | М | М | Н | ? | ? | М | ? | Н | Н | Н | М | Н | Н | Н | Н | ? | Н | ? |
| SO4 2− | P | P | P | P | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Н | Р | Р | Р |
| NO3 − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | — | Р | Р |
| NO2 − | P | P | P | P | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? | ? | ? |
| PO4 3− | P | Н | P | P | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | ? | Н | Н | Н | Н |
| CO3 2− | М | Р | P | P | Р | Н | Н | Н | Н | — | — | Н | — | Н | Н | — | — | Н | — | Н | — | — | ? | — |
| CH3COO − | P | Р | P | P | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | М | Р | — | Р | Р |
| CN − | P | Р | P | P | Р | Р | Р | Р | Р | ? | Н | Н | — | Н | Н | Н | Н | Н | Р | Н | Р | — | — | Н |
| SiO3 2− | H | Н | P | P | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | ? | Н | ? | ? | ? |
 Оксиды углерода Оксиды углерода | ||
|---|---|---|
| Оксиды | CO2 · CO |  |
| Экзотические оксиды | Карбонилы металлов · Угольная кислота · Гидрокарбонаты · Карбонаты · Дикарбонаты · Трикарбонаты | |
Полезное
Смотреть что такое «Угольная кислота» в других словарях:
УГОЛЬНАЯ КИСЛОТА — Н2СО3, очень слабая и непрочная двухосновная кислота. Образуется при растворении диоксида углерода в воде. Дает соли карбонаты и гидрокарбонаты … Большой Энциклопедический словарь
УГОЛЬНАЯ КИСЛОТА — (H2CO3) очень слабая и непрочная двухосновная кислота, образующаяся при растворении в воде диоксида углерода (углекислого газа) CO2. Дает 2 ряда солей: карбонаты и бикарбонаты (гидрокарбонаты). В природе широко распространены нормальные карбонаты … Российская энциклопедия по охране труда
Угольная кислота — УГОЛЬНАЯ КИСЛОТА, H2CO3, образуется при растворении углерода диоксида в воде. Важнейшие производные карбонаты, мочевина (карбамид). … Иллюстрированный энциклопедический словарь
угольная кислота — Н2СО3, очень слабая и непрочная двухосновная кислота. Образуется при растворении диоксида углерода в воде. Даёт соли карбонаты и гидрокарбонаты. * * * УГОЛЬНАЯ КИСЛОТА УГОЛЬНАЯ КИСЛОТА, Н2СО3, очень слабая и непрочная двухосновная кислота.… … Энциклопедический словарь
Угольная кислота — H2CO3, слабая двухосновная кислота, при нормальных условиях существующая только в разбавленных водных растворах. У. к. образуется при растворении в воде двуокиси углерода: 2, при нормальных условиях не превышает 1% от содержания CO2.… … Большая советская энциклопедия
УГОЛЬНАЯ КИСЛОТА — Н2СО3, очень слабая и непрочная двухосновная кислота. Образуется при растворении диоксида углерода в воде. Даёт соли карбонаты и гидрокарбонаты … Естествознание. Энциклопедический словарь
Угольная кислота — (медико санит.) см. Углерод … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
УГОЛЬНАЯ КИСЛОТА — H2CO3, образуется при растворении CO2 в воде. Проявляет св ва слабой к ты. Равновесие CO2+H2O H2CO3 смещено влево, поэтому меньшая часть CO2 находится в р ре в виде H2CO3. Для У. к. константы диссоциации K1=4,27 … Химическая энциклопедия
УГОЛЬНАЯ КИСЛОТА — Н2СО3 очень слабая к та, существующая только в водном р ре. У. к. образуется при растворении углерода диоксида в воде (H2О + CO2 H2CO3). Как двухосновная к та У. к. даёт 2 ряда солей: средние карбонаты и кислые гидрокарбонаты … Большой энциклопедический политехнический словарь
УГОЛЬНАЯ КИСЛОТА, H2CO3 — УГОЛЬНАЯ КИСЛОТА, H2CO3, образуется при растворении углерода диоксида в воде. Важнейшие производные карбонаты, мочевина (карбамид) … Современная энциклопедия
Угольная кислота
Угольная кислота
Она является одной из слабых двухосновных (2 атома водорода) кислот. Кроме того, она неустойчива и при нормальных условиях самопроизвольно распадается на углекислый газ и воду.
Химические свойства угольной кислоты
— реакция с оксидами металлов:
— реакция со щелочами и основаниями:
— реакция с солью, образованной более слабой кислотой:
— при повышенной температуре угольная кислота легко распадается на составляющие углекислый газ и воду :
Фосфорная кислота
Фосфорную кислоту в лаборатории можно получит с помощью химической реакции взаимодействия фосфора и азотной кислоты. реакция протекает так:
Другим способом получают фосфорную кислоту в промышленных масштабах. Для этого природные фосфаты обрабатывают серной кислотой по следующей химической реакции
затем, полученную кислоту фильтруют от сульфата кальция и выпаривают. Таким образом получается более чистая концентрированная кислота.
Фосфорная кислота обладает всеми свойствами кислот. Фосфорная кислота широко применяется при изготовлении химических препаратов, в основном для синтеза органических веществ; в качестве удобрения, лекарств, защитных и лакокрасочных покрытий металлов.
Метафосфаты (соли метафосфорной кислоты, например Na3P3O9, Na4P4O12 ) используются для удаления накипи в котлах, смягчения воды.
Химия. 11 класс
§ 42. Угольная и кремниевая кислоты, их соли
Угольная кислота и её соли
Угольная кислота H2CO3 является двухосновной и относится к слабым кислотам ( рис. 100 ). В свободном состоянии в виде кристаллов она выделена при температуре ниже ‒30 °С лишь во втором десятилетии XXI века.
В водном растворе угольная кислота диссоциирует ступенчато:
В обычных условиях она распадается на углекислый газ и воду:
Угольной кислоте соответствуют два ряда солей: карбонаты (средние) и гидрокарбонаты (кислые). Отметим два важнейших свойства солей угольной кислоты.
1. Взаимодействие с кислотами. Общим свойством карбонатов и гидрокарбонатов является «вскипание» при действии более сильных кислот как на твёрдую соль, так и на её раствор. Происходит выделение газа без цвета и запаха:
Взаимодействие солей с сильными кислотами используют как тест (качественную реакцию) на присутствие солей угольной кислоты — карбонатов и гидрокарбонатов ( Приложение 3 ).
Кроме того, такие реакции могут использоваться для получения углекислого газа в лаборатории, например, из мрамора CaCO3:
2. Термическое разложение. Вторая особенность солей угольной кислоты — их невысокая термическая устойчивость (кроме карбонатов натрия и калия, рубидия и цезия). При нагревании они разлагаются:
Анализируя вышесказанное и уравнения химических реакций предыдущего параграфа, можно сделать заключение, что карбонаты и гидрокарбонаты способны к взаимопревращениям, которые условно можно выразить схемой:
На примере карбоната кальция уравнения реакций, соответствующие данной схеме, выглядят так:
Карбонаты и гидрокарбонаты находят широкое применение в строительстве, быту, оптике, медицине, а также в производстве мыла, стекла, бумаги, являются наполнителями огнетушителей.
Таблица 30.1. Применение солей угольной кислоты