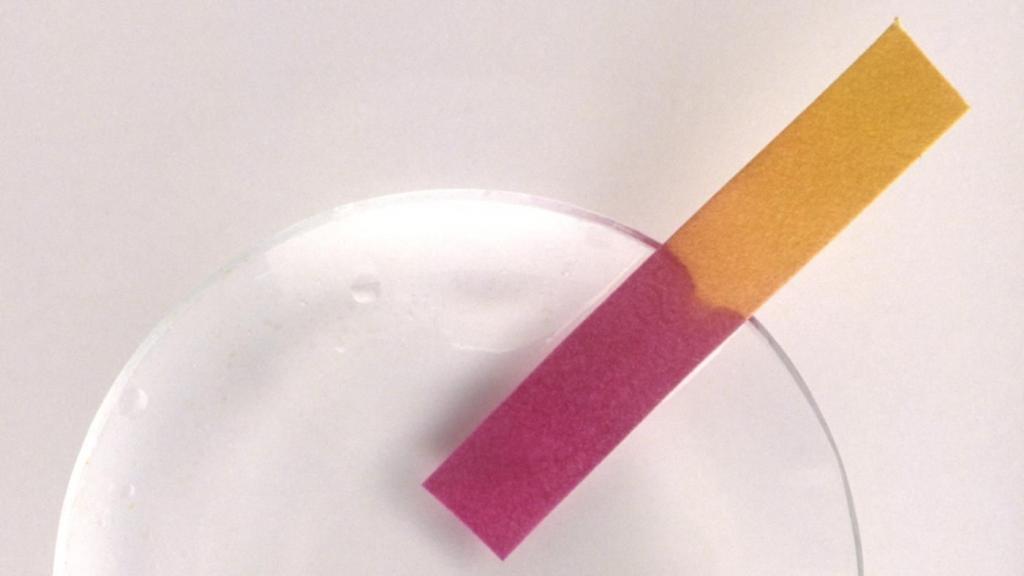На что реагирует лакмус
Что такое лакмус и чем он полезен
Происхождение и получение лакмуса

Вещество добывают промышленным способом из нескольких видов лишайников, произрастающих в Швеции, Норвегии, США, Южной Америке, Анголе, Мадагаскаре, на Канарских и Азорских островах и некоторых других местах. Лакмус и его свойства были открыты примерно в 1300 году. Долгое время добыча материала была монополизирована, способ получения тщательно скрывался. Сначала его добывали следующим методом:
В XVIII веке химики начали применять водный раствор извести и карбоната аммония вместо содово-аммиачного.
Лакмусовая бумага
Индикаторная лакмусовая бумага представляет собой отрезки, пропитанные химическим веществом. Выпускается в виде отдельных полосок или в рулонах. Такой формат является наиболее распространенным.
Использовать лакмусовую бумагу очень легко. Достаточно оторвать одну полоску и погрузить в жидкость, которую необходимо исследовать. Почти сразу же бумага приобретет тот оттенок цвета, который соответствует кислотно-щелочному уровню исследуемого вещества. Вот что такое лакмус в действии.
Сфера применения
Применяется обычно для определения уровня PH в промышленности и в быту. Он используется:
В повседневной жизни также будет нелишним знать, что такое лакмус и как его использовать. Любители растений, цветоводы и садоводы при помощи лакмусовой бумажки смогут определить уровень pH почвы и самодельных удобрений. Оптимальный кислотно-щелочной уровень почвы составляет 6-6,5 единиц для большинства растений. Если показатели отклоняются от нормы, растения замедляют рост, сбрасывают листву или прекращают цветение без видимых причин.
Аквариумные рыбки также чувствительны к уровню pH воды в аквариуме. Оптимальный баланс, который подходит для большинства разновидностей рыб и растений, составляет 6,3-7 единиц. Если показатели превышают отметку 7, растения могут погибнуть, а если опускаются ниже 6, рыбки могут не выжить.
При некоторых заболеваниях важно контролировать кислотно-щелочной баланс крови или мочи. Для этого следует регулярно проводить тесты с лакмусовой бумагой в домашних условиях. В этом случае лечащий врач объяснит, что такое лакмус и как часто его следует применять.
Переносное значение слова «лакмус»
Этот химический термин нередко употребляется в переносном смысле. Вот что значит «лакмус»: нечто, что позволяет выяснить состояние какого-либо объекта, явления, события, системы. Например: «лакмусом наших отношений стал его подарок на 8 Марта».
Лакмус
Добывается из лишаев Rocella tinctoria, Lecanora tartarea и пр., из которых готовится также орсин и орсеин. Под влиянием кислорода воздуха и аммиака красящее вещество этих растений дает орсеин, в присутствии же соды или поташа при этих условиях получаются красящие вещества Л. Для приготовления Л., по Жели, поступают следующим образом. Измельченные растения смешивают с половинным (по весу) количеством поташа и смачивают несколько раз мочой, насыщенной углекислым аммонием, или водным раствором этой соли. Через 3 дня масса принимает рыжий оттенок, через 20-25 дней она становится ярко-красной, а через 30 — синей; лучшего качества Л. получается через 40 дней. Массу после этого смешивают с мелом и гипсом, формуют в небольшие кубики и высушивают, так что в продажном Л., кроме собственно красящих веществ, всегда встречаются аммиачные соли, поташ, мел, гипс, известь и пр. При действии на орсин влажного воздуха, в присутствии аммиака и соды, тоже получается Л. Что касается очистки Л., см. Индикаторы. Наиболее полное исследование лакмуса сделано Кеном (Kane). Он выделил из Л., главным образом, четыре вещества: азолитмин, эритролитмин, эритролеин и спамолитмин. Азолитмин представляет бурый порошок, не растворимый в спирте и мало растворимый в воде; легко растворяется в щелочах и дает синее окрашивание. По Кену, состав его C9H10NO5; другие красящие вещества Л. не содержат азота. Жерар предполагает, что он образуется непосредственно при действии аммиака и воздуха на орсин или при окислении орсеина. По Жерару, этот окислительный процессе идет скорее и легче в присутствии углекислых щелочей, что и объясняет необходимость поташа при фабричном изготовлении Л., именно образующийся в первую фазу орсеин при действии аммиака и кислорода на растительный пигмент лишаев в дальнейшем дает азолитмин. Эритролитмин — вещество красного цвета, плохо растворимое в воде и эфире и хорошо растворимое в спирте, из которого может быть кристаллизовано. С аммиаком дает соединение синего цвета, нерастворимое в воде. Эритролитмин растворим в крепких, щелочах с синим цветом. Состав его, до Кену, С13Н22О6, и он есть продукт окисления эритролеиновой кислоты. Эритролеин не растворим в воде, растворяется в эфире и спирте с красным цветом, со щелочами дает красное окрашивание. Состав его С13Н22О2. Спаниолитмин схож с азолитмином. Состав С9Н7O8. Сернистый водород в момент выделения, хлористое олово и пр. восстанавливают эти вещества и обесцвечивают. Азолитмин, напр., дает бесцветное вещество лейказолитмин; на воздухе оно быстро окисляется и вновь приобретает окраску. Азолитмин и эритролитмин, взболтанные в воде, при пропускании хлора обесцвечиваются и дают хлоропроизводные. По Кену, наиболее существенной составной частью Л. (как индикатора) являются азолитмин и эритролитмин, спаниолитмин встречается редко, а эритролеин со щелочами дает красное окрашивание. О лакмусовой бумаге — см. Индикаторы.
Индикаторная бумага – необычный химический реактив
Индикаторная бумага – необычный химический реактив
В понимании обычного человека химический реактив – это вещество или 
Данный химический реактив используется для определения кислотности (pH – водородного показателя) любой жидкости или смеси. В настоящее время – это наиболее быстрый и дешевый способ определения кислотности как в лабораторных условиях, так и в частной практике – домашних условиях.
Принцип работы индикаторной бумаги
Лакмусовая индикаторная бумага – бумага, пропитанная специальными химреактивами. Она обладает уникальным свойством – в кислотной и щелочной среде меняет свой цвет. В кислотных растворах химический реактив становится красного цвета, в щелочных средах – синеет. Лакмус – это красящий материал природного происхождения, являющийся одним из самых распространенных индикаторов. На самом деле лакмус – это сложная смесь, в состав которой входит до 15 различных субстанций. Этим составом пропитывают фильтровальную бумагу. Таким способом получают индикаторную бумагу. Сырьем для добывания лакмуса являются некоторые растения, например: лишайники.
По сравнению с другими индикаторами лакмус наиболее точно (с минимальной погрешностью) определяет среду нейтрального, щелочного или кислого вещества.
Сферы применения химического реактива: 
— пищевая промышленность (определение кислотности, уровня pH, у напитков и питьевой воды);
— косметология (при производстве кремов, лосьонов и других косметических средств, в состав которых входит определенное сочетание стабилизаторов и эмульгаторов);
— цветоводство и садоводство (при изготовлении садовых растворов);
— медицина (при лабораторном исследовании мочи, грудного молока, слюны);
— микробиология (в процессе исследования живых микроорганизмов);
— аналитическая химия;
— мыловарение;
— научно-практические цели.
Данный вид химического реактива часто используют и для определения уровня pH в бассейнах, аквариумах, котлах и т.д..
Работа с лакмусовой бумагой
Все лабораторные работы для определения уровня кислотности нужно проводить в специальной лабораторной посуде из лабораторного стекла или пластика. Данное условие обязательно, так как щелочная или кислая среда – это агрессивная среда, которая может взаимодействовать с другими химическими соединениями. Лабораторная посуда из стекла – самая надежная защита от погрешностей в лабораторных исследованиях, так как она не взаимодействует с химической средой, помещенной в нее. Нужно учесть, что к этому списку не относятся высококонцентрированные щелочи, кислоты и другие агрессивные химические соединения.
Порядок работы с индикаторной бумагой достаточно прост:
— оторвать небольшую полоску;
— опустить ее в лабораторную посуду с измеряемой жидкостью на несколько секунд;
— извлечь полоску;
— провести сравнение цвета полоски с прилагаемой цветовой шкалой для определения показателя pH в необходимом растворе.
Индикаторная бумага в большинстве случаев выпускается в виде полосок, отрывной бумаги, их еще называют – тест-полосками, а также в коробках, рулонах, пеналах, тубусах. Сами по себе индикаторные полоски бывают с:
— напечатанной цветной шкалой на упаковке;
— нанесенными значениями pH на полоске;
— указанной индикаторной шкалой непосредственно на самой тесте-полоске.
Диапазон измерений:
— от 4 до 6 – кислая;
— 7 – нейтральная;
— от 8 до 11 – щелочная;
— от 12 до 14 – высокая щелочность.
В чем преимущества лакмусовой бумаги?
— быстрый результат;
— простота в использовании;
— высокая степень точности с минимальным показателем погрешности;
— экономичность;
— удобство;
— надежность;
— доступная цена;
— защита рук от прямого контакта с исследуемым раствором.
Гидрохинон купить, хлористый кальций купить, пропиленгликоль купить, а также большой перечень других химреактивов, в том числе лабораторного оборудования, посуды и приборов предлагает специализированный интернет магазин химических реактивов Москва розница, и опт «Прайм Кемикалс Групп». У нас Вы найдете широкий ассортимент товаров, необходимых для лабораторного оснащения: от перчаток нитриловых до аналитических весов. Возможна доставка любого товара как по Москве, так и по Московской области.
“Prime Chemicals Group” – высококачественная продукция по доступной цене!
Что такое лакмусовая бумажка? Особенности ее применения
Лакмусовая бумажка – простое, доступное приспособление, которое дает возможность быстро измерять показатели кислотно-щелочной среды жидкостей и их смесей. Наиболее часто такой индикатор применяют для определения химической активности телесных жидкостей, в частности слюны, мочи, грудного молока, прочего. Лакмусовая бумажка также подходит для работы с водой, всевозможными растворами.
Индикатор может пригодиться не только специалистам, что проводят лабораторные исследования. Влажная лакмусовая бумажка нередко используется в быту. Она поможет больше узнать о собственном организме.
Что представляет собой лакмус?
Цвета лакмусовой бумажки
При контакте с азотной кислотой лакмусовая бумага приобретает темно-красный оттенок. Схожий цвет индикатор имеет и в случае взаимодействия с соляной и серной кислотой. Указанные химические вещества называют сильными кислотами. В свою очередь, винная, уксусная и лимонная кислоты имеют определение слабых. При контакте с ними бумажка окрашивается в розовый цвет.
Как определяется щелочная среда? В случае взаимодействия с веществами данной категории лакмусовый индикатор приобретает синий оттенок. Большинство таких субстанций имеют едкий характер. Поэтому работать с ними, применяя лакмусовую бумагу, следует осторожно. Безопасными являются лишь нашатырный спирт и известковая вода. Несмотря на низкую химическую активность, эти вещества также относятся к категории щелочей.
Как пользоваться лакмусовой бумагой?
Результатом выполнения процедуры станет окрашивание лакмусовой бумаги в определенный оттенок. Последний необходимо сравнить с цветовой шкалой, которая находится в инструкции к применению индикатора. Если полученный оттенок равен цифровому значению 7 на шкале, это означает, что исследуемое вещество имеет нейтральный характер. Получение pH менее 7 подскажет о том, что произошла кислотная реакция, а более – щелочная.
Лакмусовый индикатор в быту
Подходит лакмусовая бумага для организации здорового питания. В частности, ее применение дает возможность исследовать показатели pH напитков, а также блюд, на основе которых строится рацион.
В бытовых условиях применение индикатора позволяет определить качество воды в аквариуме, исследовать почву, что используется для выращивания комнатных растений.
В итоге
Как видно, лакмусовая бумажка является универсальным средством для определения химической активности отдельных сред. Успешно используют такой индикатор не только в лабораторных условиях. Его умелое применение дает возможность получать ценные сведения о характере различных веществ в быту.
ЛАКМУС
Лакмус — добывается из лишаев Rocella tinctoria, Lecanora tartarea и проч., из которых готовится также орсин и орсеин. Под влиянием кислорода воздуха и аммиака красящее вещество этих растений дает орсеин, в присутствии же соды или поташа при этих условиях получаются красящие вещества Л. Для приготовления Л., по Жели, поступают следующим образом. Измельченные растения смешивают с половинным (по весу) количеством поташа и смачивают несколько раз мочой, насыщенной углекислым аммонием, или водным раствором этой соли. Через 3 дня масса принимает рыжий оттенок, через 20—25 дней она становится ярко-красной, а через 30 — синей; лучшего качества Л. получается через 40 дней. Массу после этого смешивают с мелом и гипсом, формуют в небольшие кубики и высушивают, так что в продажном Л., кроме собственно красящих веществ, всегда встречаются аммиачные соли, поташ, мел, гипс, известь и пр. При действии на орсин влажного воздуха, в присутствии аммиака и соды, тоже получается Л. Что касается очистки Л., см. Индикаторы. Наиболее полное исследование лакмуса сделано Кеном (Каnе). Он выделил из Л., главным образом, четыре вещества: азолитмин, эритролитмин, эритролеин и спамолитмин. Азолитмин представляет бурый порошок, не растворимый в спирте и мало растворимый в воде; легко растворяется в щелочах и дает синее окрашивание. По Кену, состав его C 9H10NO5; другие красящие вещества Л. не содержат азота. Жерар предполагает, что он образуется непосредственно при действии аммиака и воздуха на орсин или при окислении орсеина. По Жерару, этот окислительный процессе идет скорее и легче в присутствии углекислых щелочей, что и объясняет необходимость поташа при фабричном изготовлении Л., именно образующийся в первую фазу орсеин при действии аммиака и кислорода на растительный пигмент лишаев в дальнейшем дает азолитмин. Эритролитмин — вещество красного цвета, плохо растворимое в воде и эфире и хорошо растворимое в спирте, из которого может быть кристаллизовано. С аммиаком дает соединение синего цвета, нерастворимое в воде. Эритролитмин растворим в крепких, щелочах с синим цветом. Состав его, до Кену, С 13 Н 22 О 6, и он есть продукт окисления эритролеиновой кислоты. Эритролеин не растворим в воде, растворяется в эфире и спирте с красным цветом, со щелочами дает красное окрашивание. Состав его С 13 Н 22 О 2. Спаниолитмин схож с азолитмином. Состав С 9 Н 7O8. Сернистый водород в момент выделения, хлористое олово и пр. восстанавливают эти вещества и обесцвечивают. Азолитмин, напр., дает бесцветное вещество лейказолитмин; на воздухе оно быстро окисляется и вновь приобретает окраску. Азолитмин и эритролитмин, взболтанные в воде, при пропускании хлора обесцвечиваются и дают хлоропроизводные. По Кену, наиболее существенной составной частью Л. (как индикатора) являются азолитмин и эритролитмин, спаниолитмин встречается редко, а эритролеин со щелочами дает красное окрашивание. О лакмусовой бумаге — см. Индикаторы. С. Я. Вуколов. Δ.
ЛА́КМУС, у, ч.
Кислоти кислі на смак, вони однаково діють на лакмус (з навч. літ.);
// перен. Те, за допомогою чого можна перевірити чи виявити певні показники, характерні ознаки тощо.
Нема такого лакмусу, щоб їх [слова] перевірити. Це потрібно для самої людини (Ю. Мушкетик);
Саме преса найчастіше буває не тільки лакмусом стану суспільства, але й деякою мірою його “лікарем” (з газ.).
2. Те саме, що Ла́кмусовий папі́р (див. папі́р ).
⊲ ЛАКМУС 1749, а, м.Гол. lakmoes, через нем. Lackmus. Вещество, краснеющее от кислот и синеющее от щелочей; краска синего цвета, в состав которой входит это вещество. Лакмус синий в качеств ѣ против иностраннаго, токмо оной к высоким работам из масла не употребляется. ПСЗ XIII 167. Лакмус красен становится. Минер. В. 270. Лакмус или Турниса: краска голубаго темнаго цв ѣ та. Ршт. Худ. 43. — Ср. турниса.
Лакмусовый, ая, ое. В лакмусовом раствор ѣ (Lakmus) становится синь. Минер. В. 173.