Наджелудочковая экстрасистолия на экг что это
Что такое наджелудочковая экстрасистолия? Причины возникновения, диагностику и методы лечения разберем в статье доктора Колесниченко Ирины Вячеславовны, кардиолога со стажем в 24 года.
Определение болезни. Причины заболевания
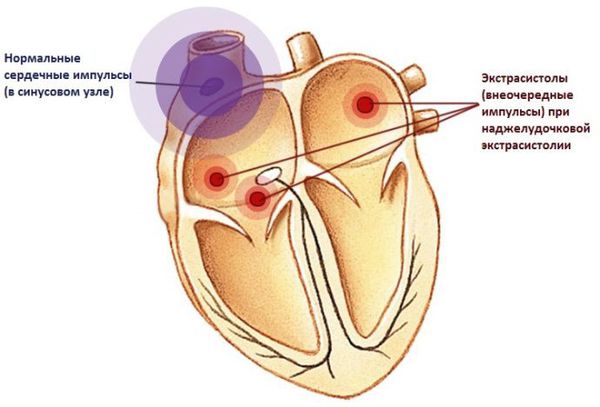
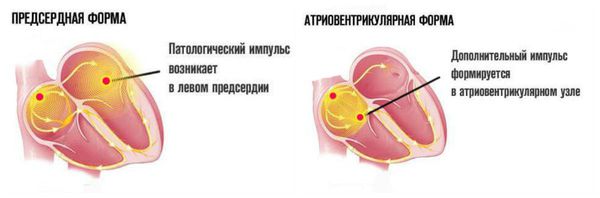
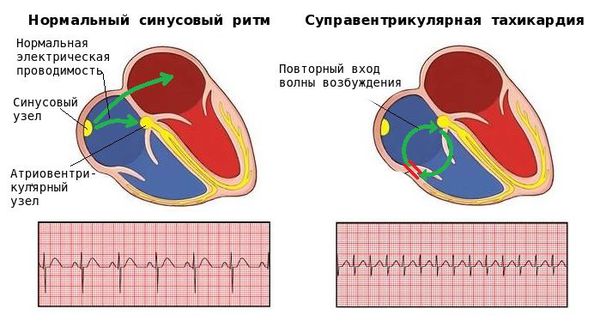
В норме сердце работает упорядоченно. Ритм сердцу задает синусовый узел, который генерирует электрические импульсы. Под их воздействием сначала сокращаются предсердия, затем желудочки. Иногда ритм сердца нарушается и возникает преждевременное возбуждение и сокращение сердца или его отделов, которое называется экстрасистолией.
Причины возникновения экстрасистолии могут быть кардиальными и внекардиальными. Кардиальные связаны с заболеваниями сердечно-сосудистой системы (органическая экстрасистолия). Внекардиальные причины связывают с болезнями других органов и систем, а также с действием определённых факторов (функциональная экстрасистолия). В ряде случаев наджелудочковая экстрасистолия не связана с проблемами сердца или других органов и действием провоцирующих факторов. В этом случае диагностируется идиопатическая экстрасистолия.
Причины функциональной экстрасистолии:
Выявить этиологический фактор, вызвавший наджелудочковую экстрасистолию, очень важно: от этого будет зависеть рекомендуемое лечение.
Симптомы наджелудочковой экстрасистолии
Заподозрить у больного наджелудочковую экстрасистолию несложно, если она ощущается. Чаще всего пациенты жалуются на чувство перебоев в работе сердца: преждевременные сокращения, паузы, замирания. Если аритмия возникает ночью, пациент может проснуться и ощутить тревогу. Реже больных беспокоят приступы частых неритмичных сердцебиений, в этом случае требуется исключение пароксизмальной (приступообразной) мерцательной аритмии.
Иногда может отмечаться любопытная закономерность: наиболее неприятными являются «безобидные» функциональные экстрасистолы, не связанные с повреждением сердца. А более серьёзные нарушения ритма человек может вообще не ощущать. Вероятно, это связано с порогом чувствительности к аритмии у пациентов и степенью повреждения сердечной мышцы.
Периоды наджелудочковой экстрасистолии обычно не сопровождаются серьёзными нарушениями гемодинамики (кровоснабжения). Однако у пациентов с органическим повреждением сердца могут возникать боли в грудной клетке различного характера, возможно появление или усиление одышки, слабости, головокружений, также снижается переносимость физических нагрузок.
Наджелудочковая экстрасистолия при вегето-сосудистой дистонии сопровождается сильной утомляемостью, слабостью, повышенным потоотделением, периодической головной болью, головокружениями, раздражительностью.
Патогенез наджелудочковой экстрасистолии
Существует несколько механизмов происхождения экстрасистол:
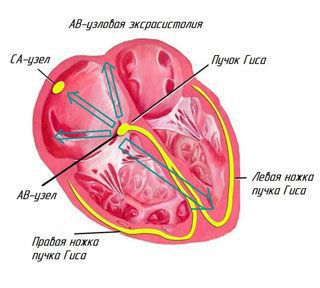
Нужно отметить, что эктопический (неправильный) импульс из предсердий распространяется сверху вниз по проводящей системе сердца. Внеочередной импульс, возникающий в АВ-соединении, распространяется в двух направлениях: сверху вниз по проводящей системе желудочков и снизу вверх (в обратную сторону) по предсердиям.
Выявление этиопатогенетического механизма (т. е. причины и механизма развития) возникновения наджелудочковых экстрасистол имеет очень важное значение, так как это определяет терапевтическую тактику.
При тщательном расспросе больного можно не только выявить признаки различных заболеваний сердца, но и установить частоту и регулярность курения, употребления чая, кофе, алкоголя, психостимуляторов и наркотических средств, а также ряда лекарственных препаратов, провоцирующих наджелудочковую экстрасистолию. Механизм возникновения экстрасистол в этом случае связан со стимуляцией симпатической нервной системы.
У всех пациентов с НЖЭ необходимо проверять функцию щитовидной железы, т. к. изменение её функционального состояния иногда становится причиной аритмии. Например, повышение уровня гормонов щитовидной железы может вызвать сердцебиения, наджелудочковые и желудочковые экстрасистолы, фибрилляцию предсердий. Если в последующем потребуется назначить антиаритмический препарат «Амиодарон», обязательно нужно проверить уровень гормонов ТТГ, Т3 и Т4.
В случае острого развития наджелудочковой экстрасистолии необходимо исключить гипокалиемию, т. е. снижение уровня калия в крови.
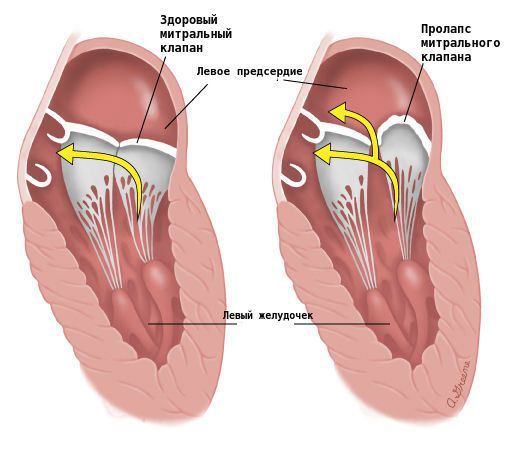
Связь первого эпизода и повторных усилений экстрасистолии, которая течёт волнообразно, с инфекциями указывает на перенесённый миокардит. Появление или усиление экстрасистолии может быть единственным или одним из проявлений ИБС. В этом случае характерно усиление перебоев в работе сердца при физических нагрузках, когда проявляется несоответствие кровоснабжения сердца и возросшей потребности в кровотоке. При других выявленных органических заболеваниях сердца (пороки сердца, кардиомиопатии, гипертоническое сердце, пролапс митрального клапана) тяжесть наджелудочковой экстрасистолии нередко связана с величиной расширения предсердий.
Классификация и стадии развития наджелудочковой экстрасистолии
Классификация наджелудочковых экстрасистол по месту возникновения:
По частоте возникновения:
По плотности:
Одиночные экстрасистолы могут возникать хаотично или быть по типу бигеминии (каждое второе сокращение является экстрасистолой), тригеминии и квадригеминии (каждый третий и четвертый комплекс является внеочередным). Такая экстрасистолия, когда внеочередные комплексы появляются после одного, двух, трёх синусовых, называется ритмированной.
Осложнения наджелудочковой экстрасистолии
Диагностика наджелудочковой экстрасистолии
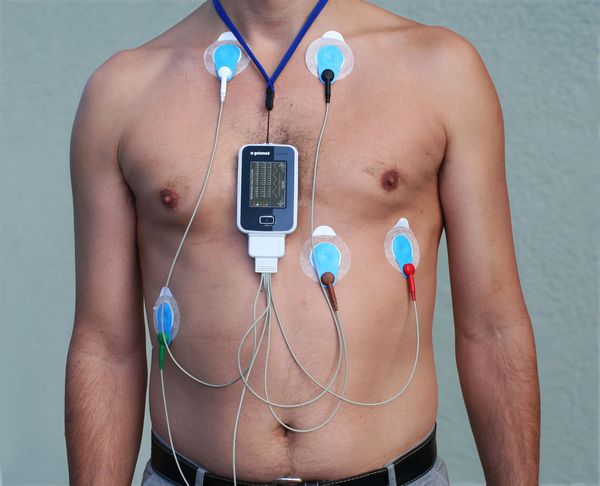
Диагноз наджелудочковой экстрасистолии можно поставить на основании жалоб пациента, согласно объективному обследованию, данным аускультации (выслушивания) сердца, по результатам проведения электрографического исследования (ЭКГ), суточного ЭКГ-мониторирования по Холтеру.
После оценки жалоб при объективном обследовании во время аускультации или пальпации пульса экстрасистолы определяются как преждевременные сокращения на фоне нормального синусового ритма. Пауза после наджелудочковой экстрасистолы не очень длительная (по этому признаку можно заподозрить её наджелудочковое происхождение). При бигеминии и тригеминии, а также частой экстрасистолии может определяться дефицит пульса. Однако подтвердить диагноз НЖЭ можно только с помощью инструментальных исследований.
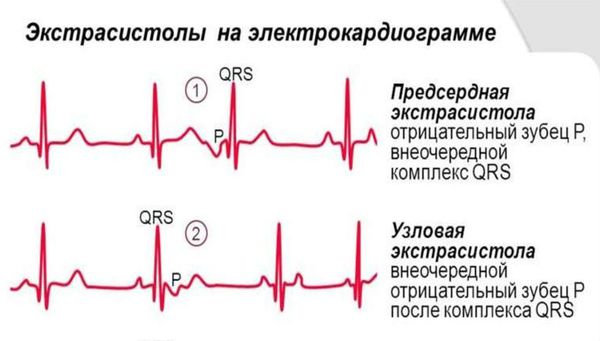
В первую очередь пациенту проводится ЭКГ, которое может зафиксировать внеочередной комплекс. Нередко на ЭКГ наджелудочковые экстрасистолы выявляются случайно (при отсутствии жалоб).
Характерные признаки наджелудочковой экстрасистолы:
Так как ЭКГ проводится в короткий промежуток времени, а внеочередное возбуждение не всегда возникает в момент его снятия, такой вид исследования не позволяет выявить проблему в 100 % случаев. Для точной диагностики обязательно должно применяться суточное или более длительное (в течение двух суток, например) мониторирование ЭКГ, которое называется холтеровским (по фамилии автора, предложившего эту методику). Для оценки частоты наджелудочковых экстрасистол исследование должно проводиться в отсутствие антиаритмической терапии. Допустимым считается количество экстрасистол не более 30 в час.
После записи данные ЭКГ-мониторирования расшифровываются специалистом и становится возможным:
Нужно отметить, что принципиально важно оценить частоту НЖЭ, т. к. от этого будет зависеть тактика лечения.
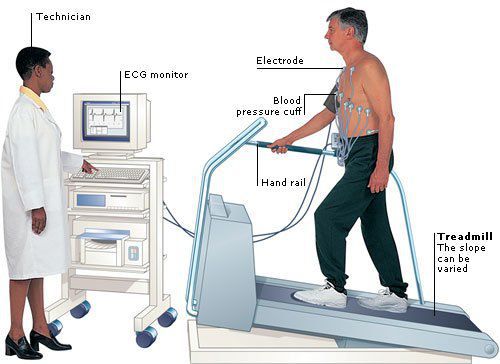
Наджелудочковая экстрасистолия может быть впервые выявлена во время проведения пробы с физической нагрузкой (велоэргометрия или тредмил-тест).
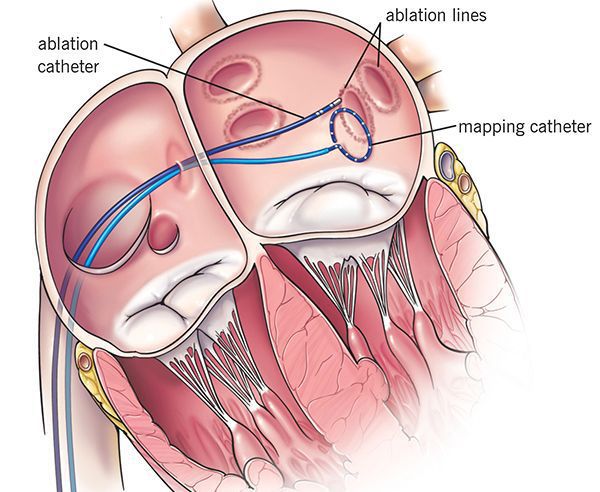
Показанием к проведению электрофизиологического исследования (ЭФИ) может стать необходимость более точного установления места возникновения экстрасистол (при частой монотопной наджелудочковой экстрасистолии) в случае последующего хирургического лечения. При ЭФИ посредством электрической стимуляции миокарда возрастает нагрузка на сердце. Такая стимуляция проводится с помощью электродов, подающих к сердечной мышце электротоки физиологической мощности с высокой частотой. В итоге миокард начинает сокращаться быстрее, возникает спровоцированное учащение сердцебиения (тахикардия). При высокой частоте сердечных сокращений могут появляться различные виды аритмии в том числе наджелудочковая экстрасистолия.
Лечение наджелудочковой экстрасистолии
НЖЭ может носить доброкачественный характер. В этом случае риск внезапной смерти очень низкий, иногда пациент даже не ощущает нарушения ритма. Такая экстрасистолия не всегда требует лечения.
Если есть возможность, нужно устранить этиологический фактор:
Пациенту рекомендуется наладить режим дня. Рацион питания следует дополнить продуктами, богатыми калием и магнием, они благоприятно влияют на сердечно-сосудистую систему.
Показаниями к проведению антиаритмической терапии являются:
1. Плохая переносимость наджелудочковой экстрасистолии. В этом случае необходимо определить, в каких ситуациях и в какое время суток чаще всего возникает нарушение сердечного ритма, после чего приурочить приём препарата к этому времени.
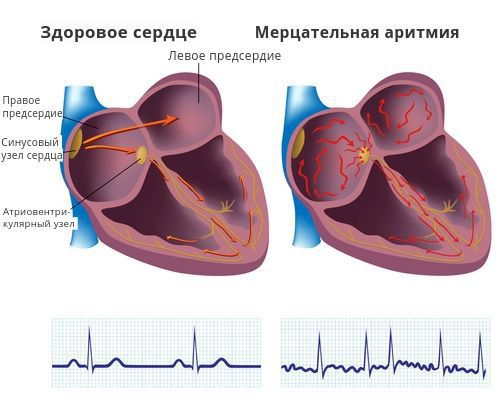
2. Возникновение НЖЭ (не обязательно частой) у пациентов с пороками сердца (в первую очередь с митральным стенозом) и другими органическими заболеваниями сердца. У таких больных прогрессируют перегрузка и расширение предсердий. Наджелудочковая экстрасистолия в данном случае служит предвестником возникновения мерцательной аритмии.
4. Частая (700-1000 экстрасистол в сутки и более) НЖЭ тоже требует назначения антиаритмической терапии даже в том случае, если она расценивается как идиопатическая, поскольку есть риск развития осложнений. Подход в этих случаях должен быть дифференцированным. Возможен и отказ от антиаритмической терапии, если на то есть основания:
Антиаритмические препараты, применяемые при НЖЭ:
Прогноз. Профилактика
Наджелудочковая экстрасистолия относится к часто встречаемым нарушениям сердечного ритма. Редкие, одиночные преждевременные сокращения сердца у здоровых людей не приводят к угрожающим последствиям для здоровья и жизни. Более опасна частая экстрасистолия с наличием эпизодов пароксизмальной наджелудочковой тахикардии, которые могут приводить к расстройствами гемодинамики и развитию мерцательной аритмии.
Для профилактики НЖЭ рекомендуются следующие мероприятия:
Наджелудочковая экстрасистолия
Наджелудочковая экстрасистолия – это один из видов аритмии. При этом происходит внеочередное возбуждение какого-либо отдела сердца, вызванное возникновением преждевременного импульса в верхних отделах сердца или в антривентрикулярном узле.
Причины наджелудочковой экстрасистолии разнообразны. Экстрасистолы бывают функциональными и органическими. Функциональные могут возникать у людей со здоровым сердцем, в частности у детей и высокорослых юношей. Это редкая одиночная наджелудочковая экстрасистолия с количеством сокращений менее 30 в течение часа.
К функциональным принято относить экстрасистолы следующего происхождения: нейрогенного; дисэлектролитного; дисгормонального; токсического; лекарственного.
Нейрогенные, в свою очередь, делятся на гипоадренергические, гиперадренергические и вагусные.
Гипераденергические экстрасистолы связаны с усиленной физической и умственной работой, эмоциональным возбуждением, принятием алкоголя, курением, употреблением острой пищи.
Гипоаденергические распознаются с трудом. Их существование подтверждается экспериментальными данными и клиническими наблюдениями.
При вагусной экстрасистолии перебои с сокращением сердца случаются после еды и во время сна, то есть в горизонтальном положении.
Органические наджелудочковые экстарсистолии обусловлены заболеваниями сердца, среди которых:
Синусовая экстрасистолия чаще всего обусловлена хронической ИБС. Об органической природе наджелудочковой экстрасистолии можно говорить, если она развивается:
при синусовой тахикардии;
исходит из нескольких очагов (политопная);
связана со стенокардией;
экстрасистол больше чем 30 в час во время мониторной регистрации ЭКГ и больше 5 в минуту при осмотре врача.
Наджелудочковая экстрасистолия – это один из видов аритмии. При этом происходит внеочередное возбуждение какого-либо отдела сердца, вызванное возникновением преждевременного импульса в верхних отделах сердца или в антривентрикулярном узле.
Этиология и виды наджелудочковых экстрасистолий
Причины наджелудочковой экстрасистолии разнообразны. Экстрасистолы бывают функциональными и органическими.
Функциональные могут возникать у людей со здоровым сердцем, в частности у детей и высокорослых юношей. Это редкая одиночная наджелудочковая экстрасистолия с количеством сокращений менее 30 в течение часа.
К функциональным принято относить экстрасистолы следующего происхождения:
Увеличение щитовидной железы и ее повышенная функция часто могут быть причиной наджелудочковой экстрасистолии
Нейрогенные, в свою очередь, делятся на гипоадренергические, гиперадренергические и вагусные.
Гипераденергические экстрасистолы связаны с усиленной физической и умственной работой, эмоциональным возбуждением, принятием алкоголя, курением, употреблением острой пищи.
Гипоаденергические распознаются с трудом. Их существование подтверждается экспериментальными данными и клиническими наблюдениями.
При вагусной экстрасистолии перебои с сокращением сердца случаются после еды и во время сна, то есть в горизонтальном положении.
Органические наджелудочковые экстарсистолии обусловлены заболеваниями сердца, среди которых:
Синусовая экстрасистолия чаще всего обусловлена хронической ИБС. Об органической природе наджелудочковой экстрасистолии можно говорить, если она развивается:
Кроме этого наджелудочковая экстрасистолия классифицируется следующим образом:
Зачастую у людей с наджелудочковой экстрасистолией отсутствуют симптомы. Наиболее характерные признаки:
ЭКСТРАСИСТОЛИЯ: клиническое значение, диагностика и лечение
Экстрасистолами называют преждевременные комплексы (преждевременные сокращения), выявляемые на ЭКГ. По механизму возникновения преждевременные комплексы подразделяются на экстрасистолы и парасистолы. Различия между экстрасистолией и парасистолией являютс
Экстрасистолами называют преждевременные комплексы (преждевременные сокращения), выявляемые на ЭКГ. По механизму возникновения преждевременные комплексы подразделяются на экстрасистолы и парасистолы. Различия между экстрасистолией и парасистолией являются чисто электрокардиографическими или электрофизиологическими. Клиническое значение и лечебные мероприятия при экстрасистолии и парасистолии абсолютно одинаковы. По локализации источника аритмии электросистолы разделяют на наджелудочковые и желудочковые.
Экстрасистолы, несомненно, являются самым распространенным нарушением ритма сердца. Они часто регистрируются и у здоровых лиц. При проведении суточного мониторирования ЭКГ статистической «нормой» экстрасистол считается примерно до 200 наджелудочковых экстрасистол и до 200 желудочковых экстрасистол в сутки. Экстрасистолы могут быть одиночными или парными. Три и более экстрасистолы подряд принято называть тахикардией («пробежки» тахикардии, «короткие эпизоды неустойчивой тахикардии»). Неустойчивой тахикардией называют эпизоды тахикардии продолжительностью менее 30 с. Иногда для обозначения 3–5 экстрасистол подряд используют определение «групповые», или «залповые», экстрасистолы. Очень частые экстрасистолы, особенно парные и рецидивирующие «пробежки» неустойчивой тахикардии, могут достигать степени непрерывно-рецидивирующей тахикардии, при которой от 50 до 90% сокращений в течение суток составляют эктопические комплексы, а синусовые сокращения регистрируются в виде единичных комплексов или коротких кратковременных эпизодов синусового ритма.
В практической работе и научных исследованиях основное внимание уделяют желудочковой экстрасистолии. Одной из наиболее известных классификаций желудочковых аритмий является классификация B. Lown и M. Wolf (1971).
Предполагалось, что высокие градации экстрасистол (классы 3–5) являются наиболее опасными. Однако в дальнейших исследованиях было установлено, что клиническое и прогностическое значение экстрасистолии (и парасистолии) практически целиком определяется характером основного заболевания, степенью органического поражения сердца и функциональным состоянием миокарда. У лиц без признаков поражения миокарда с нормальной сократительной функцией левого желудочка (фракция выброса больше 50%) экстрасистолия, включая эпизоды неустойчивой желудочковой тахикардии и даже непрерывно-рецидивирующей тахикардии, не влияет на прогноз и не представляет опасности для жизни. Аритмии у лиц без признаков органического поражения сердца называют идиопатическими. У больных с органическим поражением миокарда (постинфарктный кардиосклероз, дилатация и/или гипертрофия левого желудочка) наличие экстрасистолии считается дополнительным прогностически неблагоприятным признаком. Но даже в этих случаях экстрасистолы не имеют самостоятельного прогностического значения, а являются отражением поражения миокарда и дисфункции левого желудочка.
В 1983 г J. T. Bigger предложил прогностическую классификацию желудочковых аритмий.
Однако, как было отмечено, независимого прогностического значения желудочковая экстрасистолия не имеет. Сами по себе экстрасистолы в большинстве случаев безопасны. Экстрасистолию даже называют «косметической» аритмией, подчеркивая этим ее безопасность. Даже «пробежки» неустойчивой желудочковой тахикардии тоже относят к «косметическим» аритмиям и называют «энтузиастическими выскальзывающими ритмами» (R. W. Campbell, K. Nimkhedar, 1990). В любом случае лечение экстрасистолии с помощью антиаритмических препаратов (ААП) не улучшает прогноз. В нескольких крупных контролируемых клинических исследованиях было выявлено заметное повышение общей смертности и частоты внезапной смерти (в 2–3 раза и более) у больных с органическим поражением сердца на фоне приема ААП класса I, несмотря на эффективное устранение экстрасистол и эпизодов желудочковой тахикардии. Наиболее известным исследованием, в котором впервые было выявлено несоответствие клинической эффективности препаратов и их влияния на прогноз, является исследование CAST. В исследовании CAST («исследование подавления аритмий сердца») у больных, перенесших инфаркт миокарда, на фоне эффективного устранения желудочковой экстрасистолии препаратами класса I С (флекаинид, энкаинид и морицизин) выявлено достоверное увеличение общей смертности в 2,5 раза и частоты внезапной смерти в 3,6 раза по сравнению с больными, принимавшими плацебо. Результаты исследования заставили пересмотреть тактику лечения не только пациентов с нарушениями ритма, но и кардиологических больных вообще. Исследование CAST является одним из основных в становлении «медицины, основанной на доказательствах». Только на фоне приема β- адреноблокаторов и амиодарона отмечено снижение смертности больных с постинфарктным кардиосклерозом, сердечной недостаточностью или реанимированных пациентов. Однако положительное влияние амиодарона и особенно β-адреноблокаторов не зависело от антиаритмического действия этих препаратов.
Выявление экстрасистолии (как и любого другого варианта нарушений ритма) является поводом для обследования, направленного прежде всего на выявление возможной причины аритмии, заболевания сердца или экстракардиальной патологии и определения функционального состояния миокарда.
ААП не излечивают от аритмии, а только устраняют ее на период приема препаратов. При этом побочные реакции и осложнения, связанные с приемом практически всех препаратов, могут быть гораздо более неприятными и опасными, чем экстрасистолия. Таким образом, само по себе наличие экстрасистолии (независимо от частоты и «градации») не является показанием для назначения ААП. Бессимптомные или малосимптомные экстрасистолы не требуют проведения специального лечения. Таким больным показано диспансерное наблюдение с проведением эхокардиографии примерно 2 раза в год для выявления возможных структурных изменений и ухудшения функционального состояния левого желудочка. Л. М. Макаров и О. В. Горлицкая (2003) при длительном наблюдении за 540 больными с идиопатической частой экстрасистолией (более 350 экстрасистол в час и более 5000 в сутки) выявили у 20% больных увеличение полостей сердца («аритмогенная кардиомиопатия»). Причем более часто увеличение полостей сердца отмечалось при наличии предсердной экстрасистолии.
Показания для лечения экстрасистолии:
Лечение экстрасистолии
Необходимо объяснить больному, что малосимптомная экстрасистолия безопасна, а прием антиаритмических препаратов может сопровождаться неприятными побочными эффектами или даже вызвать опасные осложнения. Прежде всего необходимо устранить все потенциально аритмогенные факторы: алкоголь, курение, крепкий чай, кофе, прием симпатомиметических препаратов, психоэмоциональное напряжение. Следует немедленно приступить к соблюдению всех правил здорового образа жизни.
При наличии показаний для назначения ААП у больных с органическим поражением сердца используют β-адреноблокаторы, амиодарон и соталол. У больных без признаков органического поражения сердца, кроме этих препаратов, применяют ААП класса I: Этацизин, Аллапинин, Пропафенон, Кинидин Дурулес. Этацизин назначают по 50 мг 3 раза в день, Аллапинин — по 25 мг 3 раза в день, Пропафенон — по 150 мг 3 раза в день, Кинидин Дурулес — по 200 мг 2–3 раза в день.
Лечение экстрасистолии проводят методом проб и ошибок, последовательно (по 3–4 дня) оценивая эффект приема антиаритмических препаратов в средних суточных дозах (с учетом противопоказаний), выбирая наиболее подходящий для данного больного. Для оценки антиаритмического эффекта амиодарона может потребоваться несколько недель или даже месяцев (применение более высоких доз амиодарона, например по 1200 мг/сут, может сократить этот период до нескольких дней).
Эффективность амиодарона в подавлении желудочковых экстрасистол составляет 90–95%, соталола — 75%, препаратов класса I C — от 75 до 80% (B. N. Singh, 1993).
Критерий эффективности ААП — исчезновение ощущения перебоев, улучшение самочувствия. Многие кардиологи предпочитают начинать подбор препаратов с назначения β-адреноблокаторов. У больных с органическим поражением сердца при отсутствии эффекта от β-адреноблокаторов применяют Амиодарон, в том числе в комбинации с первыми. У больных с экстрасистолией на фоне брадикардии подбор лечения начинают с назначения препаратов, ускоряющих ЧСС: можно попробовать прием пиндолола (Вискен), эуфиллина (Теопек) или препаратов класса I (Этацизин, Аллапинин, Кинидин Дурулес). Назначение холинолитических препаратов типа белладонны или симпатомиметиков менее эффективно и сопровождается многочисленными побочными явлениями.
В случае неэффективности монотерапии оценивают эффект комбинаций различных ААП в уменьшенных дозах. Особенно популярны комбинации ААП с β-адреноблокаторами или амиодароном.
Есть данные, что одновременное назначение β-адреноблокаторов (и амиодарона) нейтрализует повышенный риск от приема любых антиаритмических средств. В исследовании CAST у больных, перенесших инфаркт миокарда, которые наряду с препаратами класса I C принимали β-адреноблокаторы не было отмечено увеличения смертности. Более того, было выявлено снижение частоты аритмической смерти на 33%!
Особенно эффективна комбинация β-адреноблокаторов и амиодарона. На фоне приема такой комбинации наблюдалось еще большее снижение смертности, чем от каждого препарата в отдельности. Если ЧСС превышает 70–80 уд./мин в покое и интервал P–Q в пределах 0,2 с, то проблемы с одновременным назначением амиодарона и β-адреноблокаторов нет. В случае брадикардии или АВ-блокады I–II степени для назначения амиодарона, β-адреноблокаторов и их комбинации необходима имплантация кардиостимулятора, функционирующего в режиме DDD (DDDR). Есть сообщения о повышении эффективности антиаритмической терапии при сочетании ААП с ингибиторами АПФ, блокаторами рецепторов ангиотензина, статинами и препаратами омега-3-ненасыщенных жирных кислот.
Некоторые противоречия существуют в отношении применения амиодарона. С одной стороны, некоторые кардиологи назначают амиодарон в последнюю очередь — только при отсутствии эффекта от других препаратов (считая, что амиодарон довольно часто вызывает побочные явления и требует длительного «периода насыщения»). С другой стороны, возможно, более рационально начинать подбор терапии именно с амиодарона как наиболее эффективного и удобного для приема препарата. Амиодарон в малых поддерживающих дозах (100–200 мг в день) редко вызывает серьезные побочные явления или осложнения и является скорее даже более безопасным и лучше переносимым, чем большинство других антиаритмических препаратов. В любом случае при наличии органического поражения сердца выбор небольшой: β-адреноблокаторы, амиодарон или соталол. При отсутствии эффекта от приема амиодарона (после «периода насыщения» — как минимум по 600–1000 мг/сут в течение 10 дней) можно продолжить его прием в поддерживающей дозе — 0,2 г/сут и, при необходимости, оценить эффект последовательного добавления препаратов класса I С (Этацизин, Пропафенон, Аллапинин) в половинных дозах.
У больных с сердечной недостаточностью заметное уменьшение количества экстрасистол может отмечаться на фоне приема ингибиторов АПФ и Верошпирона.
Следует отметить, что проведение суточного мониторирования ЭКГ для оценки эффективности антиаритмической терапии утратило свое значение, так как степень подавления экстрасистол не влияет на прогноз. В исследовании CAST выраженное увеличение смертности отмечено на фоне достижения всех критериев полного антиаритмического эффекта: уменьшения общего количества экстрасистол более чем на 50%, парных экстрасистол — не менее чем на 90% и полное устранение эпизодов желудочковой тахикардии. Основным критерием эффективности лечения является улучшение самочувствия. Это обычно совпадает с уменьшением количества экстрасистол, а определение степени подавления экстрасистолии не имеет значения.
В целом последовательность подбора ААП у больных с органическим заболеванием сердца, при лечении рецидивирующих аритмий, включая экстрасистолию, можно представить в следующем виде.
У больных без признаков органического поражения сердца можно использовать любые препараты, в любой последовательности или использовать схему, предложенную для больных с органическим заболеванием сердца.
Краткая характеристика ААП
β-адреноблокаторы. После исследования CAST и опубликования результатов метаанализа исследований по применению ААП класса I, в котором было показано, что практически все ААП класса I способны увеличивать смертность у больных с органическим поражением сердца, β-адреноблокаторы стали самыми популярными антиаритмическими препаратами.
Антиаритмический эффект β-адреноблокаторов обусловлен именно блокадой β-адренергических рецепторов, т. е. уменьшением симпатико-адреналовых влияний на сердце. Поэтому β-адреноблокаторы наиболее эффективны при аритмиях, связанных с симпатико-адреналовыми влияниями — так называемые «катехоламинзависимые» или «адренергические аритмии». Возникновение таких аритмий, как правило, связано с физической нагрузкой или психоэмоциональным напряжением.
Катехоламинзависимые аритмии в большинстве случаев одновременно являются «тахизависимыми», т. е. возникают при достижении определенной критической частоты сердечных сокращений, например во время физической нагрузки частая желудочковая экстрасистолия или желудочковая тахикардия возникают только при достижении частоты синусового ритма 130 сокращений в минуту. На фоне приема достаточной дозы β-адреноблокаторов больной не сможет достичь частоты 130 уд./мин при любом уровне физической нагрузки, таким образом предотвращается возникновение желудочковых аритмий.
β-адреноблокаторы являются препаратами выбора для лечения аритмий при врожденных синдромах удлинения интервала Q–T.
При аритмиях, не связанных с активацией симпатической нервной системы β-адреноблокаторы гораздо менее эффективны, но добавление β-адреноблокаторов нередко значительно увеличивает эффективность других антиаритмических препаратов и снижает риск аритмогенного эффекта ААП класса I. Препараты класса I в сочетании с β-адреноблокаторами не увеличивают смертность у больных с им поражением сердца (исследование CAST).
При так называемых «вагусных» аритмиях β-адреноблокаторы оказывают аритмогенное действие. «Вагусные» аритмии возникают в состоянии покоя, после еды, во время сна, на фоне урежения ЧСС («брадизависимые» аритмии). Вместе с тем в некоторых случаях при брадизависимых аритмиях эффективно применение пиндолола (Вискен) — β-адреноблокатора с внутренней симпатомиметической активностью (ВСА). Кроме пиндолола к β-адреноблокаторам с ВСА относятся окспренолол (Тразикор) и ацебутолол (Сектраль), однако в максимальной степени внутренняя симпатомиметическая активность выражена именно у пиндолола.
Дозы β-адреноблокаторов регулируют в соответствии с антиаритмическим эффектом. Дополнительным критерием достаточной β-блокады является снижение ЧСС до 50 уд./мин в состоянии покоя. В прежние годы, когда основным β-адреноблокатором был пропранолол (Анаприлин, Обзидан), известны случаи эффективного применения пропранолола при желудочковых аритмиях в дозах до 960 мг/сут и более, например до 4 г в день! (R. L. Woosley et al., 1979).
Амиодарон. Амиодарон таблетки 0,2 г. (оригинальным препаратом является Кордарон) обладает свойствами всех четырех классов ААП и, кроме того, оказывает умеренное a-блокирующее действие. Амиодарон, несомненно, является самым эффективным из существующих антиаритмических препаратов. Его даже называют «аритмолитическим препаратом».
Основным недостатком амиодарона является высокая частота экстракардиальных побочных эффектов, которые при длительном приеме наблюдаются у 10–75% больных. Однако необходимость в отмене амиодарона возникает у 5–25% (J. A. Johus et al., 1984; J. F. Best et al., 1986; W. M. Smith et al., 1986). К основным побочным эффектам амиодарона относятся: фотосенсибилизация, изменение цвета кожи, нарушение функции щитовидной железы (как гипотиреоз, так и гипертиреоз), повышение активности печеночных трансаминаз, периферические нейропатии, мышечная слабость, тремор, атаксия, нарушения зрения. Большинство этих побочных эффектов обратимы и исчезают после отмены или при уменьшении дозы амиодарона. Гипотиреоз можно контролировать с помощью приема левотироксина. Наиболее опасным побочным эффектом амиодарона является поражение легких («амиодароновое поражение легких») — возникновение интерстициального пневмонита или, реже, легочного фиброза. У большинства больных поражение легких развивается только при длительном приеме сравнительно больших поддерживающих доз амиодарона — более 400 мг/сут. Такие дозы крайне редко применяют в России. Поддерживающая доза амиодарона в России обычно составляет 200 мг/сут или даже меньше (по 200 мг в день 5 дней в неделю). B. Clarke и соавторы (1985) сообщают лишь о трех случаях из 48 наблюдений возникновения этого осложнения на фоне приема амиодарона в дозе 200 мг в сутки.
В настоящее время изучается эффективность дронедарона, деривата амиодарона без йода. Предварительные данные свидетельствуют об отсутствии экстракардиальных побочных эффектов у дронедарона.
Соталол. Соталол (Соталекс, Сотагексал) таблетки 160 мг применяется в средней суточной дозе 240–320 мг. Начинают с назначения 80 мг 2 раза в день. При рефрактерных аритмиях иногда используют прием соталола до 640 мг/сут. β-адреноблокирующее действие соталола проявляется начиная с дозы 25 мг.
На фоне приема соталола имеется повышенный риск развития желудочковой тахикардии типа «пируэт». Поэтому прием соталола желательно начинать в стационаре. При назначении соталола необходимо тщательно контролировать величину интервала Q–T, особенно в первые 3 дня. Корригированный интервал Q–T не должен превышать 0,5 с. В этих случаях риск развития тахикардии типа «пируэт» менее 2%. С увеличением дозы соталола и степени удлинения интервала Q–T значительно увеличивается риск развития тахикардии типа «пируэт». Если корригированный интервал Q–T превышает 0,55 с — риск тахикардии типа «пируэт» достигает 11%. Поэтому при удлинении интервала Q–T до 0,5 с необходимо уменьшить дозу соталола или отменить препарат.
Побочные эффекты соталола соответствуют типичным побочным эффектам β-адреноблокаторов.
Этацизин. Этацизин таблетки 50 мг. Наиболее изученный отечественный препарат (создан в СССР). Для лечения аритмий применяется с 1982 г. Быстрое достижение клинического эффекта позволяет с успехом использовать Этацизин у лиц без органического поражения сердца для лечения желудочковых и наджелудочковых нарушений ритма: экстрасистолии, всех вариантов пароксизмальных и хронических тахиаритмий, в том числе мерцательной аритмии, при синдроме Вольфа–Паркинсона–Уайта. Наиболее эффективен Этацизин у пациентов с ночными аритмиями, а также при желудочковой экстрасистолии.Средняя суточная доза Этацизина составляет 150 мг (по 50 мг 3 раза в день). Максимальная суточная доза — 250 мг. При назначении этацизина для предупреждения рецидивирования мерцательной аритмии, наджелудочковых и желудочковых тахикардий его эффективность, как правило, превосходит эффективность других АПП класса I. Препарат хорошо переносится, необходимость в отмене возникает примерно у 4% больных. Основные побочные эффекты: головокружение, головная боль, «онемение» языка, нарушение фиксации взора. Обычно побочные реакции наблюдаются сравнительно редко, и их выраженность уменьшается после первой недели приема Этацизина.
Аллапинин. Отечественный препарат Аллапинин, таблетки 25 мг (создан также в СССР) применяется в клинической практике с 1986 г. Назначают по 25–50 мг 3 раза в день. Максимальная суточная доза составляет 300 мг. Аллапинин довольно эффективен при наджелудочковых и желудочковых аритмиях. Основные побочные явления — головокружение, головная боль, нарушение фиксации взора. Необходимость в отмене возникает примерно у 6% больных. Одной из особенностей аллапинина и теоретически его недостатком является наличие β-адреностимулирующего действия.
Пропафенон (Ритмонорм, Пропанорм), таблетки 150 мг, ампулы 10 мл (35 мг). Назначают по 150–300 мг 3 раза в день. При необходимости дозу увеличивают до 1200 мг/сут. Пропафенон, кроме замедления проведения, слегка удлиняет рефрактерные периоды во всех отделах сердца. Кроме того, пропафенон обладает небольшим β-адреноблокирующим действием и свойствами антагонистов кальция.
К основным побочным эффектам пропафенона относятся головокружение, нарушение фиксации взора, атаксия, тошнота, металлический вкус во рту.
Хинидин. В настоящее время в России используют в основном Кинидин Дурулес, табл. по 0,2 г. Разовая доза составляет 0,2–0,4 г, средняя суточная доза — от 0,6 до 1,0 г. Максимальная суточная доза хинидина в прежние годы (когда хинидин был основным антиаритмическим препаратом) достигала 4,0 г! В настоящее время такие дозы не используются и примерной максимальной суточной дозой хинидина можно считать 1,6 г.
В небольших дозах (600–800 мг/сут) хинидин хорошо переносится. Побочные явления возникают обычно при более высоких дозах. К наиболее частым побочным эффектам при приеме хинидина относятся нарушения функции желудочно-кишечного тракта: тошнота, рвота, понос. Реже отмечаются головная боль, головокружения, ортостатическая гипотония. Самое опасное осложнение от приема хинидина — возникновение желудочковой тахикардии типа «пируэт». По данным литературы, это осложнение наблюдается у 1–3% больных, принимающих хинидин.
П. Х. Джанашия, доктор медицинских наук, профессор
С. В. Шлык, доктор медицинских наук, профессор
Н. М. Шевченко, доктор медицинских наук, профессор
РГМУ, Москва