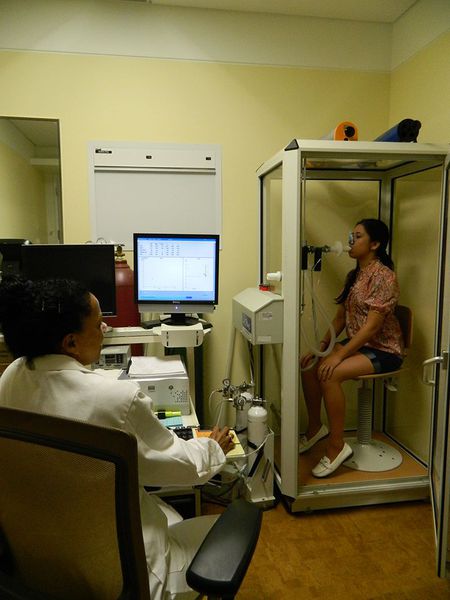
Нарушение легочной вентиляции по обструктивному типу что это
Хроническая обструктивная болезнь легких – взгляд педиатра
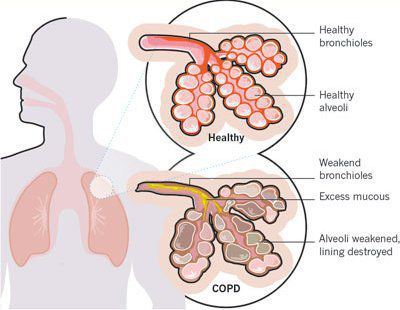
Хроническая обструктивная болезнь легких (ХОБЛ) считается заболеванием лиц старше 40 лет. Основной причиной заболевания является длительное курение или вдыхание других частиц и газов [2]. В определении ХОБЛ отмечено характерное для него необратимое ограничение воздушного потока, которое имеет прогрессирующий характер и связано с аномальной воспалительной реакцией легких на вредные частицы и газы [1]. Подчеркивается, что хроническое ограничение воздушного потока является следствием повреждения мелких дыхательных путей (обструктивный бронхиолит) и деструкции паренхимы легкого (эмфизема). Именно хроническое воспаление мелких дыхательных путей приводит к этим изменениям [1, 2]. Недавние научные исследования указывают на то, что ХОБЛ поддается терапии и может быть предотвратима [2].
Среди причин ХОБЛ основное внимание уделяют факторам внешней среды, таким как курение, длительное воздействие профессиональных факторов (пыль, химические раздражители, пары) и атмосферное/домашнее загрязнение воздуха [1].
Известно, что не во всех случаях факторы риска вызывают ХОБЛ. Механизмы возникновения этого заболевания еще в значительной степени не изучены, и возможно, что одной из причин, способствующих возникновению ХОБЛ, являются хронические воспалительные заболевания легких, возникающие в детском возрасте, продолжающиеся у подростков и переходящие к взрослым. В первую очередь это те заболевания, которые охватывают оба легких и протекают с преимущественным поражением мелких дыхательных путей и паренхимы легкого. Имеются данные о том, что антенатальное повреждение легких может являться фактором риска для формирования ХОБЛ у взрослых [3].
Частота хронических заболеваний легких (ХЗЛ) у детей в России не известна. Существуют данные об общей респираторной заболеваемости и распространенности отдельных нозологических форм (бронхиальная астма, муковисцидоз), а также данные отдельных пульмонологических центров, которые значительно отличаются в связи с неоднозначным подходом к диагностике некоторых заболеваний. Официальные статистические данные не учитывают всех нозологических форм ХЗЛ. Частота хронических заболеваний легких без бронхиальной астмы оценивается в 0,6–1,2 на 1000 детского населения [38, 45].
Однако эпидемиологические исследования распространенности только бронхиальной астмы, проведенные у детей в соответствии с международными критериями, указывают на частоту 4–10% [3, 4, 5, 6].
В последние годы отмечается рост респираторной заболеваемости, а также увеличение числа больных с хроническими заболеваниями легких и врожденными пороками развития, являющимися основой некоторых хронических заболеваний легких [7, 8].
В таблице представлены основные нозологические формы хронических заболеваний легких у детей, которые отвечают критериям, упомянутым выше.
Бронхиальная астма
Бронхиальная астма и ХОБЛ, несмотря на сходство симптомов, — это разные заболевания. Хотя не исключается их сочетание [1]. Для астмы характерно хроническое эозинофильное воспаление дыхательных путей, регулируемое CD4+ Т-лимфоцитами, в то время как при ХОБЛ воспаление имеет нейтрофильный характер и характеризуется повышенным содержанием макрофагов и CD8+ Т-лимфоцитов. К тому же ограничение потока воздуха при астме может быть полностью обратимым. Астма считается фактором риска развития ХОБЛ [9]. У курящих, больных астмой, снижение функции легких развивается быстрее, чем у курящих, но не болеющих астмой [10]. Несмотря на более благоприятное течение бронхиальной астмы у детей, у большинства больных симптомы болезни сохраняются в подростковом периоде [4, 5]. В настоящее время удельный вес подростков среди детей с астмой составляет 36–40% [11]. Причем у 20% подростков формируется более тяжелое течение заболевания, а у 33% отмечается стабильное течение болезни. 10% подростков имеют стойкие нарушения функции внешнего дыхания (ФВД) при отсутствии клинических симптомов астмы [11].
Поскольку астма является наиболее частым хроническим заболеванием легких в детском возрасте и ее частота нарастает [4, 5, 6], эти больные должны учитываться как группа риска в связи с возможным развитием ХОБЛ.
Пороки развития трахеи, бронхов, легких и легочных сосудов
Эта группа заболеваний включает в себя пороки развития, связанные с недоразвитием бронхолегочных структур: агенезия, аплазия, гипоплазия легких; пороки развития стенки трахеи и бронхов, как распространенные, так и ограниченные, кисты легких, секвестрации легких, пороки развития легочных вен, артерий и лимфатических сосудов. Многие пороки развития являются причиной рецидивирования бронхолегочного воспаления и составляют основу для вторичного формирования хронического воспалительного процесса.
Как возможная основа формирования ХОБЛ наибольший интерес представляют распространенные пороки развития бронхов (бронхомаляция, трахеобронхомаляция, синдром Вильямса–Кемпбелла). В зависимости от распространенности и степени поражения бронхов клиническая симптоматика может варьировать от рецидивирующего обструктивного бронхита до выраженного хронического бронхолегочного процесса с гипоксемией, дыхательной недостаточностью, гнойным эндобронхитом, формированием легочного сердца. Последние симптомы более характерны для синдрома Вильямса–Кемпбелла [12, 13, 14]. Для клинической симптоматики характерны: влажный кашель, одышка, деформация грудной клетки, наличие распространенных влажных разнокалиберных и сухих хрипов. Обструктивный синдром является следствием недоразвития хрящевого каркаса и повышенной подвижности стенки бронхов, а также бактериального воспалительного процесса, быстро формирующегося в бронхиальном дереве [12, 13]. При исследовании ФВД выявляются комбинированные нарушения вентиляции с преобладание обструкции [14]. Эндобронхит визуально имеет катаральный или гнойный характер, с выраженным нейтрофильным цитозом [15].
Возрастная динамика зависит от распространенности процесса и эффективности лечебных и профилактических мероприятий. У большинства больных состояние улучшается и стабилизируется, старше 18 лет они наблюдаются с диагнозом «бронхоэктатическая болезнь» или «хронический бронхит» [13]. У части больных формируется легочное сердце и имеет место ранняя инвалидизация [14].
Облитерирующий бронхиолит
Облитерирующий бронхиолит — заболевание мелких бронхов, морфологической основой которого является концентрическое сужение или полная облитерация просвета бронхиол и артериол при отсутствии изменений в альвеолярных ходах и альвеолах, приводящая к развитию эмфиземы.
Заболевание является следствием бронхиолита, острого инфекционного заболевания, поражающего преимущественно детей в возрасте 6–24 мес. У детей первых двух лет причиной болезни чаще всего бывает респираторно-синцитиальная и аденовирусная (3, 7, 21 тип) инфекция. У детей более старшего возраста — легионеллезная и микоплазменная [16, 17]. Возможно развитие заболевания после трансплантации легких [18]. Синдром одностороннего сверхпрозрачного легкого (синдром Маклеода) является вариантом этого заболевания. Клинически облитерирующий бронхиолит проявляется рецидивирующим, малопродуктивным кашлем, одышкой, бронхоообструктивным синдромом, локальными физикальными данными в виде ослабленного дыхания и мелкопузырчатых хрипов.
Диагноз ставится на основании характерных клинических данных и наличия рентгенологических признаков повышенной прозрачности части легкого. При сцинтиграфии выявляется резкое снижение кровотока в зоне поражения, а при бронхографии — локальная облитерация бронхов ниже 5–6 генерации при отсутствии признаков пневмосклероза. При бронхоскопии чаще выявляется катаральный эндобронхит. Для большинства больных (75%) характерны стойкие вентиляционные нарушения обструктивного типа и умеренная гипоксемия [19, 20, 21].
Возрастная динамика болезни зависит от объема поражения. Характерно отсутствие прогрессирования облитерации бронхиол и вентиляционных нарушений, но при двустороннем процессе возможно развитие легочного сердца и ранняя инвалидизация больных [19, 20, 21]. Заболевание, при объеме поражения не более одной доли легкого, имеет благоприятный прогноз, но признаки хронического обструктивного бронхита сохраняются.
Хронический бронхит
Для заболевания характерно диффузное поражение бронхиального дерева, хроническое течение с периодами обострения и ремиссии [не менее двух-трех обострений в течение подряд двух лет], продуктивный кашель и постоянные влажные разнокалиберные хрипы в легких. У детей заболевание, аналогичное хроническому бронхиту взрослых, встречается редко. Чаще всего хронический бронхит является симптомом других хронических болезней легких и диагностируется при исключении бронхиальной астмы, локальных пневмосклерозов, муковисцидоза, синдрома цилиарной дискинезии, иммунодефицитных состояний и других хронических заболеваний легких. У подростков хронический бронхит может иметь место вследствие причин, вызывающих хронические бронхиты у взрослых (курение, профессиональные вредности, загрязнение окружающей среды) [23].
Критерии диагностики: влажный кашель, диффузные влажные хрипы в легких при наличии 2–3 обострений заболеваний в год на протяжении двух лет.
Возрастная динамика: зависит от основного заболевания.
Бронхолегочная дисплазия
Бронхолегочная дисплазия (БЛД) — хроническое заболевание легких детей первых двух лет жизни, возникающее в перинатальном периоде преимущественно у глубоко недоношенных детей, получающих респираторную терапию в неонатальном периоде, протекающее с преимущественным поражением бронхиол и паренхимы легких, развитием эмфиземы, фиброза и/или нарушением репликации альвеол, проявляющееся кислородозависимостью в возрасте 28 суток жизни и старше, дыхательной недостаточностью, бронхообструктивным синдромом, рентгенографическими изменениями и характеризующееся регрессом клинических проявлений по мере роста ребенка.
Причиной БЛД чаще являются жесткие режимы искусственной вентиляции легких (ИВЛ) с высокими концентрациями кислорода и/или высокого давления на вдохе. Развивается обычно при лечении тяжелого синдрома дыхательных расстройств [7, 24, 25]. Есть данные о наследственной предрасположенности к БЛД [26].
В основе заболевания лежит нарушение архитектоники легочной ткани и, часто, бронхиальная гиперреактивность [27, 28, 29]. Патоморфологические процессы развиваются в первые дни жизни в виде интерстициального отека с гиалиновыми мембранами, ателектазов, чередующихся с участками эмфиземы. В последующие 15–20 дней развивается метаплазия и гиперплазия эпителия и мышечного слоя мелких бронхов, что приводит к прогрессирующей атрофии альвеолярной паренхимы. На втором месяце процесс завершается массивным фиброзом с деструкцией альвеол, формированием буллезных участков в легком, редукцией кровотока, часто и правожелудочковой недостаточностью. Нарушение газообмена в легком может приводить к необходимости длительной ИВЛ [26].
Клинически проявляется гипоксемией, дыхательной недостаточностью, симптомами бронхиальной обструкции; рентгенологически выявляются обычно грубые изменения в виде фиброза, кист, изменений прозрачности легочной ткани, деформаций бронхов [27, 29].
Возрастная динамика. У большинства детей, даже с тяжелыми формами бронхолегочной дисплазии, имеется тенденция к улучшению со временем. К пятилетнему возрасту функциональное состояние дыхательной системы становится сопоставимым с развитием дыхательной системы у их сверстников. [28]. В раннем возрасте отмечаются признаки обструкции мелких бронхов [29]. У многих детей течение заболевания осложняется гиперреактивностью дыхательных путей, что приводит к необходимости их госпитализации при острых вирусных заболеваниях и относит детей к группе риска по развитию астмы [29]. Долгосрочный прогноз затруднен, поскольку больные, у которых данная патология впервые была выделена в самостоятельную нозологическую форму, к настоящему времени достигли только периода полового созревания.
Интерстициальные заболевания легких
Из этой группы заболеваний интерес представляет хронический вариант течения гиперчувствительного пневмонита (экзогенный аллергический альвеолит).
Экзогенный аллергический альвеолит представляет собой заболевание иммунопатологического характера, вызванное вдыханием органической пыли, содержащей различные антигены, и проявляющееся диффузным поражением альвеолярной и интерстициальной ткани легкого с последующим развитием пневмофиброза [23, 30–33]. Течение заболевания характеризуется кашлем, диффузными крепитирующими и мелкопузырчатыми хрипами, одышкой, рестриктивными и обструктивными нарушениями вентиляции. Обязательно указание на контакт с источником причинно-значимого аллергена. Рентгенологически характеризуется диффузными инфильтративными и интерстициальными изменениями [35, 36].
Возрастная динамика. Заболевание чаще выявляется у детей школьного возраста и характеризуется медленно прогрессирующим течением. Применение современных методов терапии позволяет добиться длительной ремиссии [31].
Прочие варианты альвеолитов могут либо излечиваться в детском возрасте (острый экзогенный аллергический альвеолит), либо имеют быстро прогрессирующее течение с неблагоприятным прогнозом (идиопатический фиброзирующий альвеолит) [31, 32].
Дефицит альфа-1-антитрипсина
Альфа-1-антитрипсин (А-1-АТ) является белком, продуцируемым клетками печени. Его основная функция — блокирующее действие по отношению к ферменту эластазе, продуцируемой лейкоцитами для уничтожения микроорганизмов и мельчайших ингалированных частиц. А-1-АТ инактивирует избыток эластазы, и при его отсутствии эластаза оказывает повреждающее действие на альвеолярные структуры легких, вызывая развитие эмфиземы [72]. Идентифицировано 24 варианта молекулы А-1-АТ, которые кодируются серией ко-доминантных аллелей, обозначаемой как система Pi. Большинство (90%) людей гомозиготны по гену М (фенотип PiM.), 2–3% — PiMZ, 3–5% — PiMS (т. е. гетерозиготны по гену М) и обеспечивают нормальное содержание А-1-АТ в сыворотке крови (20–53 mmol/L или 150–350 mg/dL). Наиболее часто дефицит А-1-АТ связан с аллелью Z или гомозиготами PiZ (ZZ). Содержание А-1-АТ у этих больных составляет 10–15% от нормы. Концентрация А-1-АТ выше 11 mmol/L считается защитной. Эмфизема развивается, если уровень А-1-АТ ниже 9 mmol/L Другие генотипы связаны с аллелями PiSZ, PiZ/Null и PiNull [37]. Сообщается о роли дефицита А-1-АТ в патогенезе ХОБЛ [1, 2]. Для заболевания характерно формирование панлобулярной эмфиземы. Дефицит A-1-AT обычно начинает проявляться в возрасте 35–40 лет умеренной одышкой, повышением прозрачности легочных полей (особенно нижних участков) и необратимыми обструктивными изменениями. Со временем эмфизема усиливается, развиваются признаки хронического бронхита; курение и повторные легочные инфекции ускоряют процесс [37]. У подростков описаны случаи прогрессирующей эмфиземы, но у маленьких детей болезнь не выявляет специфических черт: острые респираторные заболевания у них могут протекать с обструктивным синдромом или по типу рецидивирующего бронхита. Вопрос о дефиците A-1-AT возникает у детей с выраженной диффузной эмфиземой на рентгенограмме, стойкой обструкцией и нарушением легочного кровотока. Обеднение кровотока в участках легких может быть первым проявлением заболевания, описаны и повторные пневмонии с быстрым формированием буллезной эмфиземы.
Синдром цилиарной дискинезии
В основе заболевания лежит наследственный дефект цилиарного эпителия — отсутствие динеиновых ручек и дислокация внутренних структур в ресничках цилиарного эпителия [38, 39, 40]. Следствием этого является застой секрета в дыхательных путях, инфицирование и формирование хронического воспалительного процесса. Дисфункция цилиарного эпителия может сочетаться с неподвижностью сперматозоидов у мужчин и нарушением функций эпителия фаллопиевых труб у женщин. Синдром Картагенера (обратное расположение внутренних органов, хронический синусит и бронхоэктазы) является частным случаем синдрома цилиарной дискинезии. Клинические проявления возникают обычно в раннем возрасте. После повторных заболеваний верхних дыхательных путей, бронхитов и пневмоний выявляются признаки хронического бронхолегочного процесса. Типично также упорное, трудно поддающееся лечению поражение носоглотки (хронический синусит, ринит, аденоидит). У части больных формируется деформация грудной клетки и изменения концевых фаланг пальцев по типу «барабанных палочек». Основным типом легочных изменений является ограниченный пневмосклероз с деформацией бронхов, чаще двусторонний. Характерен распространенный гнойный эндобронхит, имеющий упорное течение. У больных с синдромом Картагенера описаны и другие пороки (сердца, почек), а также гипофункция эндокринных желез [40].
Цилиарная дискинезия в отсутствие обратного расположения органов также проявляется повторными бронхитами и пневмониями, развитием хронического бронхита, но у многих больных грубой патологии легких не развивается, что, очевидно, связано с меньшей степенью дисфункции ресничек. Диагноз подтверждается электронной микроскопией биоптата слизистой оболочки носа или бронхов, а также исследованием подвижности ресничек в фазово-контрастном микроскопе.
У больных с синдромом дисфункции цилиарного эпителия с возрастом отмечается положительная динамика течения болезни, хотя признаки хронического бронхита и хронического синусита сохраняются. У больных с синдромом Картагенера, при недостаточно эффективной терапии, возможно развитие распространенных пневмосклеротических изменений в легких и формирование легочного сердца.
Следует отметить, что ряд наследственных заболеваний, таких как муковисцидоз, иммунодефицитные состояния, протекают с хроническим поражением легких. Однако эти заболевания, как правило, манифестируют в раннем детском возрасте, протекают с гнойным эндобронхитом и дыхательной недостаточностью. Прогноз этих заболеваний серьезен.
Среди основных причин ХОБЛ упоминаются факторы внешней среды. Эти же причины способствуют формированию хронических болезней легких у детей и подростков. Во-первых, это курение табака. По данным МЗиСР РФ в 7–8 классах систематически курят 8–12 процентов школьников. К 11 классу школы уже курит около половины мальчиков и четверть девочек [41]. В Москве (данные 2000 г.) 36,9% подростков начинают курить в возрасте до 13 лет. Пробовали курить 79,9% юношей и 73,7% девушек и систематически курят 52% учащихся 11 классов. Более 60% некурящих как минимум час в неделю вынуждены вдыхать окружающий табачный дым [42]. Пассивное курение в 2–3 раза повышает респираторную заболеваемость детей раннего возраста и, в частности, рецидивирующими бронхитами. При этом имеется прямая зависимость заболеваемости от числа выкуриваемых родителями сигарет [41, 43].
Загрязнение воздуха промышленными выбросами неблагоприятно сказывается на функции органов дыхания. Основными загрязняющими факторами являются пылевые частицы и газы (SO2, окислы азота, фенолы и другие органические вещества), раздражающие слизистые оболочки [43].
Кратковременные пики выбросов при неблагоприятных метеоусловиях ведут к увеличению числа бронхитов и ларингитов, обструктивных эпизодов у детей с астмой, наблюдаемому в течение нескольких последующих дней.
При длительном воздействии происходит снижение функциональных показателей дыхания, повышение реактивности бронхов. В зонах промышленного загрязнения атмосферного воздуха высок процент часто болеющих детей и частота рецидивирующих бронхитов, в т. ч. обструктивных, что особенно выражено у дошкольников. Распространенность этих видов патологии в школьном возрасте снижается, но у большого процента школьников скоростные показатели ФВД остаются сниженными на 10–20%. Это снижение тем более выражено, чем больше срок проживания ребенка в загазованной зоне. У детей практически не бывает специфических пылевых заболеваний (силикоз, асбестоз и т. д.) [43, 44, 45].
В микрорайонах, примыкающих к предприятиям, выбросы которых содержат органическую пыль (споры плесневых грибов, пух и перья, муку, древесную и соломенную пыль), растет число аллергических заболеваний (астма, альвеолит). Усиление аллергизации отмечается и в зонах вблизи бензоколонок. Сильно загрязняет воздух открытый огонь, прежде всего кухонные газовые плиты, особенно при недостаточной вентиляции; концентрация окислов азота в кухне с газовой плитой может достигать высокого уровня; респираторная заболеваемость детей, живущих в квартирах с газовыми плитами, выше, чем в квартирах с электрическими [44]. Jedrychowski W. et al. [46] пытались определить, как влияет качество воздуха в помещении в постнатальном периоде на функцию легких у школьников. Исследовав 1096 детей, авторы выяснили, что снижение показателей функции внешнего дыхания может быть связано с загрязнением воздуха в жилых помещениях при использовании печного отопления и длительным пребыванием детей в экологически неблагоприятных условиях.
Известно, что низкий социоэкономический статус приводит к повышенной респираторной заболеваемости [44]. Но в нашей стране такие систематические исследования пока не проводятся.
Заключение
Таким образом, ни одно из хронических заболеваний легких, возникающих в детском возрасте, не является аналогом ХОБЛ у взрослых в том понимании, которое соответствует этой нозологической форме в настоящее время. Но целый ряд болезней и факторов внешней среды может способствовать возникновению этого заболевания. Роль этих состояний в патогенезе ХОБЛ заслуживает дальнейшего изучения.
Какие возможности профилактики ХОБЛ уже в детском возрасте?
В первую очередь, это профилактика курения у детей и подростков. Необходим ряд мероприятий, которые помогли бы снизить количество курящих подростков, обеспечили профилактику пассивного курения детей и курения беременных женщин.
Профилактика респираторных инфекций, таких как респираторный синцитиальный вирус, аденовирусная, приведет к снижению частоты хронических бронхиолитов, которые могут являться одной из причин формирования ХОБЛ. Использование методов иммунизации детского населения поможет снизить заболеваемость этими инфекциями.
Совершенствование системы выхаживания недоношенных детей, использование щадящих методов ИВЛ снизит частоту бронхолегочной дисплазии.
Лучший способ предотвращения ХОБЛ лежит в оптимизации антенатального состояния плода путем предотвращения курение матери и его влияния как на плацентарную функцию, так и на эмбриональный рост дыхательных путей; а также ограничение послеродовых воздействий, которые могут вызывать бронхообструкцию, таких как вирусные инфекции, неблагоприятная экология внешней среды и жилища.
Перспективным является исследование генетической предрасположенности к формированию бронхообструктивного синдрома.
Литература
И. К. Волков, доктор медицинских наук, профессор
Первый МГМУ им. И. М. Сеченова, Москва
Что такое хроническая обструктивная болезнь легких (ХОБЛ)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Никитина И. Л., врача УЗИ со стажем в 26 лет.
Определение болезни. Причины заболевания
Данная болезнь коварна тем, что основные симптомы болезни, в частности, при табакокурении проявляются лишь через 20 лет после начала курения. Оно долгое время не даёт клинических проявлений и может протекать бессимптомно, однако, в отсутствии лечения незаметно прогрессирует обструкция дыхательных путей, которая становится необратимой и ведёт к ранней нетрудоспособности и сокращению продолжительности жизни в целом. Поэтому тема ХОБЛ представляется в наши дни особенно актуальной.
Важно знать, что ХОБЛ — это первично хроническое заболевание, при котором важна ранняя диагностика на начальных стадиях, так как болезнь имеет тенденцию к прогрессированию.
Если врач поставил диагноз «Хроническая обструктивная болезнь лёгких (ХОБЛ)», у пациента возникает ряд вопросов: что это значит, насколько это опасно, что изменить в образе жизни, какой прогноз течения болезни?
Итак, хроническая обструктивная болезнь лёгких или ХОБЛ – это хроническое воспалительное заболевание с поражением мелких бронхов (воздухоносных путей), которое приводит к нарушению дыхания за счёт сужения просвета бронхов. [1] С течением времени в лёгких развивается эмфизема. Так называется состояние, при котором снижается эластичность лёгких, то есть их способность сжиматься и расширяться в процессе дыхания. Лёгкие при этом находятся постоянно как будто в состоянии вдоха, в них всегда, даже во время выдоха, остается много воздуха, что нарушает нормальный газообмен и приводит к развитию дыхательной недостаточности.
Основными причинами заболевания ХОБЛ являются:
К другим причинам относятся:
Симптомы хронической обструктивной болезни легких
ХОБЛ — болезнь второй половины жизни, чаще развивается после 40 лет. Развитие болезни — постепенный длительный процесс, чаще незаметный для пациента.
Обратиться к врачу заставляют появившиеся одышка и кашель — самые распространённые симптомы заболевания (одышка почти постоянная; кашель частый и ежедневный, с выделениями мокроты по утрам). [2]
Типичный пациент с ХОБЛ — курящий человек 45-50 лет, жалующийся на частую одышку при физической нагрузке.
Кашель — один из самых ранних симптомов болезни. Он часто недооценивается пациентами. На начальных стадиях болезни кашель носит эпизодический характер, но позже становится ежедневным.
Мокрота также относительно ранний симптом заболевания. На первых стадиях она выделяется в небольших количествах, в основном по утрам. Характер слизистый. Гнойная обильная мокрота появляется во время обострения заболевания.
Одышка возникает на более поздних стадиях заболевания и отмечается вначале только при значительной и интенсивной физической нагрузке, усиливается при респираторных заболеваниях. В дальнейшем одышка модифицируется: ощущение недостатка кислорода во время обычных физических нагрузкок сменяется тяжёлой дыхательной недостаточностью и через время усиливается. Именно одышка становится частой причиной для того, чтобы обратиться к врачу.
Когда можно заподозрить наличие ХОБЛ?
Вот несколько вопросов алгоритма ранней диагностики ХОБЛ: [1]
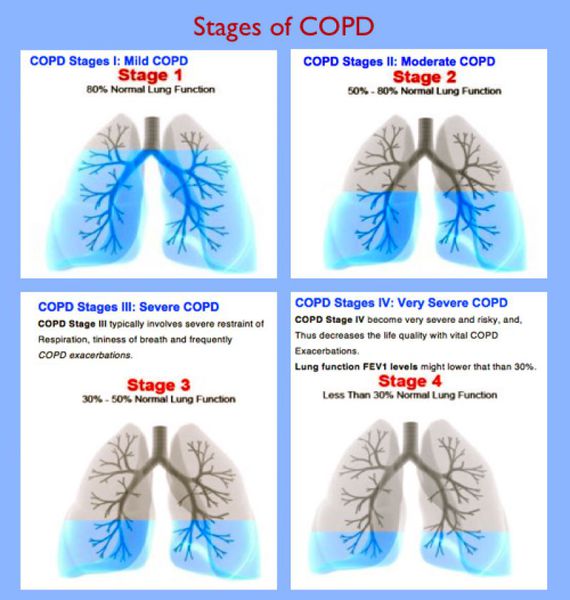
При положительно ответе более чем на 2 вопроса необходимо проведение спирометрии с бронходилятационным тестом. При показателе теста ОФВ1/ФЖЕЛ ≤ 70 определяется подозрение на ХОБЛ.
Патогенез хронической обструктивной болезни легких
При ХОБЛ страдают как дыхательные пути, так и ткань самого лёгкого — лёгочная паренхима.
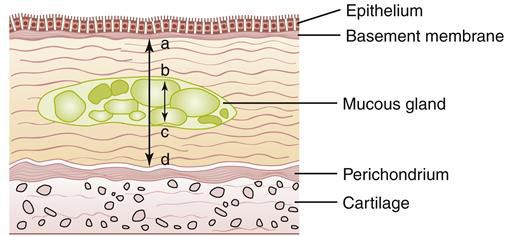
Начинается заболевание в мелких дыхательных путях с закупорки их слизью, сопровождающейся воспалением с формированием перибронхиального фиброза (уплотнение соединительной ткани) и облитерации (зарастание полости).
При сформировавшейся патологии бронхитический компонент включает:
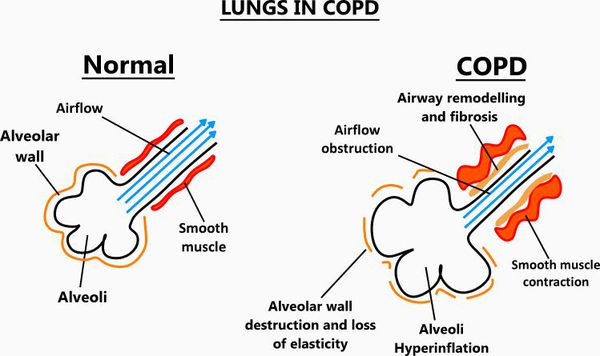
Эмфизематозный компонент приводит к разрушению конечных отделов дыхательных путей — альвеолярных стенок и поддерживающих структур с образованием значительно расширенных воздушных пространств. Отсутствие тканевого каркаса дыхательных путей приводит к их сужению вследствие тенденции к динамическому спадению во время выдоха, что становится причиной экспираторного коллапса бронхов. [4]
Ко всему прочему, разрушение альвеолярно-капиллярной мембраны влияет на газообменные процессы в лёгких, снижая их диффузную способность. В результате этого возникают уменьшение оксигенации (кислородное насыщения крови) и альвеолярной вентиляции. Происходит избыточная вентиляция недостаточно перфузируемых зон, приводящая к росту вентиляции мёртвого пространства и нарушению выведения углекислого газа СО2. Площадь альвеолярно-капиллярной поверхности уменьшена, но может быть достаточной для газообмена в состоянии покоя, когда эти аномалии могут не проявляться. Однако при физической нагрузке, когда потребность в кислороде возрастает, если дополнительных резервов газообменивающихся единиц нет, то возникает гипоксемия — недостаток содержания кислорода в крови.
Появившаяся гипоксемия при длительном существовании у пациентов с ХОБЛ включает ряд адаптивных реакций. Повреждение альвеолярно-капиллярных единиц вызывает подъём давления в лёгочной артерии. Поскольку правый желудочек сердца в таких условиях должен развивать большее давление для преодоления возросшего давления в лёгочной артерии, он гипертрофируется и расширяется (с развитием сердечной недостаточности правого желудочка). Кроме того, хроническая гипоксемия способна вызывать увеличение эритропоэза, который впоследствии увеличивает вязкость крови и усиливает правожелудочковую недостаточность.