Нарушение синтеза порфиринов что это
Нарушение синтеза порфиринов что это
Наследственные анемии встречаются сравнительно редко, преимущественно у мужчин. Приобретенные формы чаще всего связаны с интоксикациями. Как правило, причинами приобретенного нарушения синтеза порфиринов являются свинцовое отравление, а также дефицит витамина В6.
Патогенез (что происходит?) во время Анемий, обусловленных нарушениями синтеза утилизацией порфиринов:
Нарушение синтеза протопорфирина характеризует невозможность связывания железа и в результате этого его накопления в организме. Если железо поступает преимущественно в печень, то возникает ее цирроз; при отложении железа в поджелудочной железе развивается сахарный диабет.
Степень клинических проявлений заболевания зависит от выраженности анемии. Жалобы носят общий характер и обычно сводятся к слабости, повышенной утомляемости. С детства у больных обнаруживается умеренная гипохромная анемия. С годами малокровие углубляется. Появляются клинические признаки избыточного отложения железа в организме. Может развиться выраженная мышечная слабость, иногда обнаруживаются признаки сахарного диабета, у части больных периодически появляются боли в животе, неприятные ощущения в области правого подреберья, возможны одышка, отеки на ногах, сердцебиение.
При объективном обследовании у части больных выявляется темная окраска кожи, обнаруживается увеличение печени, иногда селезенки.
После внутримышечного введения 500 мг десферала у больных с нарушением синтеза порфиринов выводится железа 5-10 мг/сут. при норме 0,6-1,2 мг/сут.
Иногда диагностике помогает исследование биосинтеза порфиринов in vitro из 6-аминолевулиновой кислоты: к эритроцитам больного прибавляют 6-аминолевулиновую кислоту, из которой за 4 ч инкубации при покачивании образуется большое количество порфиринов.
Дифференциальная диагностика
Нарушение синтеза порфиринов необходимо заподозрить в ситуации, когда у больных (преимущественно мужчин) при гипохромной анемии отмечается высокое содержание железа сыворотки крови. Также в случаях гипохромной анемии отмечается высокое содержание железа в сыворотке крови при талассемиях, к тому же талассемии встречаются гораздо чаще, чем наследственные анемии, связанные с нарушением синтеза порфиринов. Так же как и при талассемиях, при анемии, связанной с нарушением синтеза порфиринов, обнаруживаются признаки неэффективного разрушения эритроцитов, мишеневидные эритроциты.
Для талассемии более характерно увеличение селезенки. Содержание железа сыворотки, как правило, ниже, чем при анемии, обусловленной нарушением синтеза порфиринов.
Диагностике помогают определение содержания порфиринов эритроцитов и исследование биосинтеза порфиринов in vitro (в пробирке) из 6-аминолевулиновой кислоты. Талассемия наследуется по доминантному типу, а именно гетерозиготная талассемия выявляется в различных поколениях семьи.
Для апластической анемии типично резкое снижение уровня тромбоцитов и нейтрофилов, в костном мозге отмечается уменьшение числа мегакариоцитов. При исследовании костного мозга определяется большое количество жира.
Заболевание приходится дифференцировать с приобретенной дизэритропоэтической анемией или, как ее часто называют, рефрактерной сидеробластной анемией.
Лечение Анемий, обусловленных нарушениями синтеза утилизацией порфиринов:
Лечение наследственной анемии, возникшей в результате нарушения активности ферментов, участвующих в образовании белков порфиринов, необходимо начинать с витамина В6. Целью данной терапии является достижение стойкой ремиссии заболевания. У животных с дефицитом витамина В6, кроме дерматита, глоссита и поражения нервной системы, развивается гипохромная анемия с увеличением содержания железа сыворотки и отложением железа в органах.
Не у всех больных с наследственным нарушением синтеза порфиринов эффективен витамин В6, почти у половины он бесполезен. Дозы витамина В6 для лечения данной болезни должны быть большими (6%-ный раствор в дозе 5-8 мл/сут.). Пиридоксальфосфат намного превосходит по эффективности витамин В6. Данный препарат выпускается в таблетированной форме в дозировке по 20 мг, а также в ампулах по 10 мг препарата в растворе. Доза пиридоксальфосфата при лечении анемии составляет 30-40 мг/сут. при внутримышечном введении или 80–120 мг/сут. при приеме внутрь. Действие препарата отмечается быстрее, чем при использовании витамина В6.
Для выведения избыточного количества железа из организма необходимо длительно применять десферал по 500 мг/сут. Целесообразно 3-6 раз в год проводить месячные курсы лечения указанным препаратом. Иногда само лечение десфералом приводит к ремиссии.
Прогноз
Прогноз удовлетворительный, если оказывает эффект витамин В6 или пиридоксальфосфат и применяется десферал, и значительно хуже при поздно начатом лечении и необратимых изменениях, связанных с сидерозом органов.
Диагностика и лечение острых порфирий
Общая информация
Краткое описание
Национальное гематологическое общество
НАЦИОНАЛЬНЫЕ КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ
ДИАГНОСТИКА И ЛЕЧЕНИЕ ОСТРЫХ ПОРФИРИЙ
Москва 2018 г.
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Порфирии подразделяются на эритропоэтические и печѐночные в зависимости от ткани, где происходит преимущественное нарушение метаболизма порфиринов (см. классификация I) [10]. Вместе с тем, порфирии могут подразделяться на формы с поражением кожных покровов и острые, провоцируемые формы (см. классификация II).
— Поздняя кожная порфирия
Этиология и патогенез
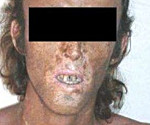
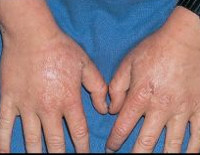
Повышенная светочувствительность кожных покровов связана с фотохимическими реакциями, спровоцированными порфиринами. Избыток порфиринов в коже подвергается активному воздействию спектра солнечного излучения с длинами волн 400 – 410 нм, что приводит к образованию реактивных частиц, например, супероксид аниона, активирующего ксантин-оксидазу, и других метаболитов, повреждающих клетки базальной мембраны. Повторные атаки приводят к развитию нескольких слоѐв базальных мембран и образованию пласта кровеносных сосудов в поверхностных слоях дермы. Реактивные кислородсодержащие частицы также могут приводить к высвобождению гистамина из тучных клеток, усиливая явления фототоксичности.
Изменения кожи. Уропорфириноген – основной метаболит при поздней кожной порфирии стимулирует синтез фибробластами коллагена. При эритропоэтической протопорфирии жирорастворимый протопорфириноген откладывается в стенке сосудов дермы, приводя к их утолщению.
Пигментирование кожи и гипертрихоз наблюдаются в периорбитальных областях при поздней кожной порфирии и эритропоэтических порфириях, однако, механизм этих изменений до конца не изучен.
Эпидемиология
50-100 случаев на 100000 человек.
Клиническая картина
Cимптомы, течение
-эритема, волдыри на открытых участках кожи.
Диагностика
— качественного скрининг-теста свежего образца мочи больного с использованием реактива Эрлиха по методу Watson-Schwartz. При наличии в моче избытка ПБГ образуется окрашенный продукт розово-красного цвета;
— количественного определения содержания ПБГ в моче (норма не превышает 2 мг/л).
Следующим этапом диагностики является определение активности ферментов в клетках крови. Это позволяет подтвердить диагноз у больных с клиническими проявлениями заболеваний и выявить бессимптомных носителей. Несмотря на распространѐнность и удобство диагностики бессимптомного носительства порфирий путѐм оценки активности специфического фермента в клетках, этот метод не является абсолютно достоверным [8,6].
Дифференциальный диагноз
— соматизация и синдром хронической усталости
Первичный этап диагностики, на практике, является самым сложным и ответственным для врача. Вариативность течения и симптоматики ОП (особенно при атипичном и моносимптомном вариантах развития) создают значительные трудности в своевременной постановке этого диагноза, нередко уводя врача в сторону ошибочных предположений. Выполнение же скрининг теста на наличие избытка ПБГ в моче всем обращающимся без анализа первичных жалоб нерационально с точки зрения временных и материальных затрат. Опытным путѐм, подтверждѐнным статистическими данными, выделены характерные для ранних сроков течения и специфичные для ОП симптомы. Разработана шкала, содержащая данные анамнеза и симптомы как характерные для клинического течения острых порфирий, так и наиболее часто ложно приписываемых ОП. Скрининг имеющихся у пациентов симптомов и сопоставление этих симптомов с симптоматикой, представленной в таблице (приложение 1)*, позволяет по сумме баллов судить о степени вероятности наличия порфирии у больного. Такой подход позволяет минимизировать число ятрогений, связанных с назначением пациентам с неустановленным диагнозом порфириногенных препаратов.
Лечение
4. Рибоксин 2%-10мл в разведении на 100-200 мл 0.9% раствора NaCl, в/в капельно 1-2 раза в сутки, ежедневно 2-4 недели.
Нарушение синтеза порфиринов что это
Анемии, связанные с нарушением синтеза порфиринов относится к группе анемий, обусловленных недостаточностью эритропоэза.
Анемии этой группы обусловлены недостаточной или аномальной утилизацией внутриклеточного железа при синтезе гемоглобина, несмотря на нормальное или даже повышенное содержание железа в митохондриях эритрокариоцитов. Такие дефекты могут быть связаны с наследственными нарушениями, главным образом при синтезе порфиринов или с приобретенным характером поражения, например, в результате отравления свинцом или недостаточности витамина В6. Отличительным признаком этого типа анемий является насыщение организма железом, в связи с чем ранее использовался термин «сидероахрестические», т. е. железонасыщенные анемии.
В результате дефицита одного из ферментов синтеза тема развивается порфирия. При порфирии из-за нарушения синтеза тема снимается механизм обратной связи, прекращается ингибирование скорость-лимитирующего фермента АЛК-синтетазы, поэтому при легких формах порфии удается поддерживать адекватный синтез тема (анемия не развивается), а происходит накопление промежуточных продуктов.
Синтез порфиринов происходит в виде двух изомеров III и I. III изомер порфиринов используется для синтеза тема. При нарушении этого пути изомер I синтезируется в большем количестве, чем в норме. Эритроциты, содержащие гемоглобин с изомером I, имеют меньшую продолжительность жизни и быстро разрушаются в селезенке (болезнь Гюнтера или врожденная эритропоэтическая порфирия).
Анемии при нарушениях обмена порфиринов
Развитие анемии обусловлено недостаточной или аномальной утилизацией внутриклеточного железа при синтезе гемоглобина, несмотря на нормальное или даже повышенное содержание железа в митохондриях эритроидных предшественников.
Наследственные и приобретенные анемии, связанные с нарушением синтеза порфиринов, характеризуются гипохромией, высоким содержанием железа сыворотки и гемосидерозом органов.
Содержание железа в сыворотке значительно повышено (до 100 мкмоль/л), трансферрин насыщен железом почти на 100%. При исследовании содержания порфиринов в эритроцитах у некоторых больных обнаруживается снижение протопорфирина до 3-9 мкмоль/л (норма 18-90 мкмоль/л) и повышение копропорфирина до 60-75 мкмоль/л (норма до 12 мкмоль/л). В отдельных случаях снижается как протопорфирин, так и копропорфирин. Содержание δ-аминолевулиновой кислоты и копропорфирина в моче нормальное.
Приобретенные анемии обусловлены нарушением синтеза порфиринов, возникающие чаще при отравлении свинцом или дефиците витамина В6.
В костном мозге отмечается резкое увеличение кольцевидных сидеробластов (рис. 28). В периферической крови постепенно снижается содержание гемоглобина до 50-60 г/л, эритроциты с выраженной гипохромией (низкие цветовой показатель, МСН, МСНС), выявляется анизо-пойкилоцитоз, появляется базофильная пунктация эритроцитов (рис. 29).
Содержание железа в сыворотке крови повышается до 350-550 мкг/дл, насыщение трансферрина железом достигает 100%. В сыворотке крови отмечается высокая концентрация ферритина. Самым характерным биохимическим признаком свинцового отравления является увеличение концентрация в моче δ-аминолевулиновой кислоты и копропорфирина, в эритроцитах повышено содержание протопорфирина.
Нарушение синтеза порфиринов что это
Идентифицированы различные типы порфирии, каждый из которых связан с дефектом одного из восьми ферментов, участвующих в синтезе гема (кроме 5-аминолевулинатсинтетазы). Определены гены, кодирующие эти ферменты, и их хромосомная локализация. Во многом известны молекулярные повреждения, лежащие в основе различных типов заболевания.
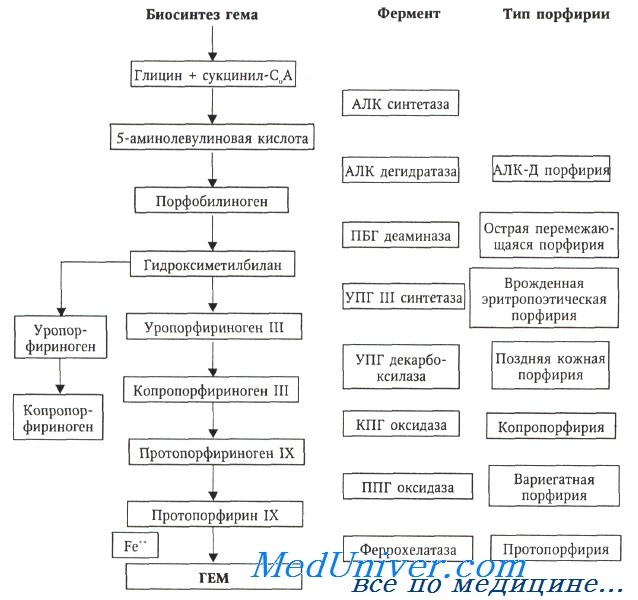
АЛК — 5-аминолевулиновая кислота, ПБГ — порфобилиноген, УПГ — уропорфириноген, КПГ — копропорфириноген, ППГ — протопорфириноген
Биосинтетический блок, возникающий вследствие ферментативных дефектов, наиболее сильно проявляется в печени и костном мозге — органах, в которых синтезируется основное количество гема. Для каждого типа порфирии характерны клинические и патоморфологические особенности, отражающие дефект определенного фермента и тип наследования.
В целом для порфирии характерны два основных клинических синдрома: кожная фотосенсибилизация и синдром неврологических расстройств. Фотосенсибилизация кожи — результат реакции откладывающихся в коже порфиринов на солнечное облучение. Неврологические расстройства обусловлены повышенной продукцией и экскрецией порфириновых предшественников АЛК и порфобилиногена. При дефектах двух и более ферментов, участвующих в синтезе гема, диагностируется двойная порфирия.
Генетические и метаболические нарушения при порфириях 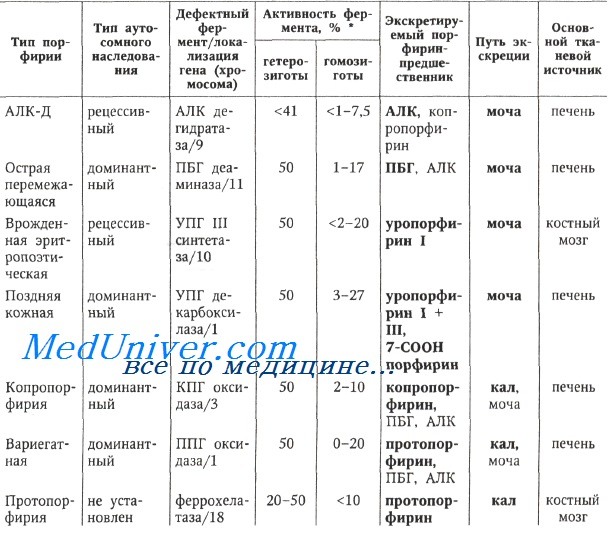
Классификация порфирий
I. Порфирии с кожной фотосенсибилизацией:
— Врожденная эритропоэтическая порфирия
— Поздняя кожная порфирия
— Протопорфирия
II. Острые или индуцированные порфирии:
— Порфирии с неврологическими проявлениями
— Острая перемежающаяся порфирия
— АЛК-Д порфирия
— Порфирии с неврологическими и кожными проявлениями
— Вариегатная порфирия
— Копропорфирия
III. Двойные порфирии
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Порфирия ( Порфириновая болезнь )
Порфирии ‒ большая группа наследственных заболеваний, характеризующихся нарушением биосинтеза гема и накоплением его токсичных метаболитов. Клинические проявления крайне разнообразны – от светочувствительности и кожных высыпаний до болей в животе, полного паралича и острых психозов. Диагностика осуществляется с помощью молекулярно-генетических тестов, специальных лабораторных методов определения порфиринов и их предшественников в моче и кале, оценки активности ферментов в крови. Лечение заключается в мероприятиях, направленных на снижение образования токсических метаболитов, их выведение из крови, проведении симптоматической терапии и хирургических вмешательств.
МКБ-10
Общие сведения
Причины порфирий
В подавляющем большинстве случаев причиной порфирий выступают генетические мутации, обусловливающие неполноценность активности того или иного фермента, участвующего в биосинтезе гема. Исключением является поздняя кожная порфирия (спорадическая форма), которая развивается вследствие заболеваний печени (алкогольный гепатит, вирусный гепатит С) или длительной интоксикации тяжелыми металлами. Наследование порфирий происходит по аутосомно-доминантному или аутосомно-рецессивному типу. Синтезирование гема протекает в 8 последовательных этапов, за каждый отвечает свой фермент, кодируемый определенным геном. Для каждой формы порфирии существует специфичный ферментативный дефект.
Гем представляет собой комплексное соединение порфиринов с двухвалентным железом. Наибольшее количество гема образуется в печени и костном мозге. В печени гем входит в состав белков, участвующих в клеточном дыхании, расщеплении токсичных свободных радикалов и обезвреживании различных ксенобиотиков. В костном мозге гем используется для образования гемоглобина. Результатом сниженной активности ферментов является торможение синтеза гема на определенном уровне, что ведет к накоплению его токсичных промежуточных метаболитов.
Помимо генетической мутации, для развития острых порфирий необходимо воздействие провоцирующих факторов, стимулирующих выработку порфиринов. Такими факторами являются голодание, длительная инсоляция, стрессы, алкоголь, инфекции, интоксикация тяжелыми металлами (ртуть, свинец), лекарственные средства, подвергающиеся метаболизму системой цитохрома P-450 (нестероидные противовоспалительные препараты, антибиотики, антиконвульсанты, оральные контрацептивы, седативные средства). Особую роль играют колебания женских половых гормонов во время менструаций или беременности. У женщин месячные являются наиболее частым провоцирующим фактором, а беременность ассоциируется с тяжелым течением заболевания.
Патогенез
В результате неполноценности ферментов, участвующих в образовании гема, и действия провоцирующих факторов происходит увеличение концентрации его токсичных продуктов обмена. Для хронических порфирий характерно накопление протопорфирина, копропорфирина и упопорфирина. При острых формах возрастает количество порфобилиногена и дельта-аминолевулиновой кислоты (ДАЛК).
Порфирины накапливаются в коже и под действием ультрафиолетового излучения (солнечного света) запускают процесс перекисного окисления липидов, вызывая деструкцию и гибель клеток кожи. Копропорфирин и протопорфирин усиливают пигментацию кожи и ускоряют рост волос (гипертрихоз). Плохо растворимый в воде протопорфирин откладывается в клетках печени, закупоривает портальные тракты и желчные протоки. Отложение уропорфирина в эритроцитах приводит к их ускоренному разрушению в селезенке (гемолиз). Предшественники порфиринов (ДАЛК и порфобилиноген), накапливаясь в нервной ткани, вызывают демиелинизацию и аксональную дегенерацию нервных волокон.
Классификация
В основу разных классификаций порфирий положены различные критерии: клиническая симптоматика, локализация нарушения метаболизма порфиринов или тканевая тропность. Наиболее целесообразно выделять следующие виды порфирий:
Симптомы порфирий
При острых порфириях развиваются сильные боли в животе, задержка стула, учащение сердцебиения, повышение артериального давления, изменение цвета мочи (от розового до красно-бурого). Тяжесть состояния пациента в основном обусловлена неврологическими симптомами – болью по всему телу, снижением чувствительности, прогрессирующей мышечной слабостью, иногда достигающей полного паралича, судорожными припадками, различными психическими расстройствами (тревожность, психомоторное возбуждение, бред, галлюцинации).
При поздней кожной форме возникает гиперпигментация участков кожи, подвергающихся постоянному воздействию солнечного света (лицо, шея, ушные раковины, верхняя часть груди, кисти рук). Кожа приобретает землистый или бронзовый оттенок. Также характерны гипертрихоз лобно-височной области лица, фотосенсибилизация, проявляющаяся повышенной ранимостью кожи и образованием пузырей с жидкостным содержимым. После вскрытия пузырей формируются эрозии. На местах разрешения эрозий образуются атрофические рубцы.
При эритропоэтических порфириях наблюдаются более выраженные признаки светочувствительности, чем при ПКП (ранимость, пузыри, эрозии). При длительном нахождении на свету появляется покраснение и сильное жжение кожи. Обширные эрозии оставляют после себя грубые рубцы на лице, что приводит к обезображиванию внешнего вида больного. В результате множественных рубцов на коже кистей рук развиваются контрактуры суставов, что значительно затрудняет их движения. Моча становится красной или розовой, а зубы окрашиваются в красно-коричневый цвет (эритродонтия). Из-за увеличенной селезенки могут появиться тяжесть или ноющие боли в левом подреберье. Специфический признак ЭПП – утолщение, огрубение и уплотнение кожи вокруг рта и глаз, на крыльях и спинке носа, на тыльных поверхностях кистей.
Осложнения
Нарушения порфиринового обмена ухудшают течение сердечно-сосудистых заболеваний, неблагоприятно влияют на углеводный метаболизм и повышают риск развития сахарного диабета 2 типа. Острые формы порфирий вследствие выраженной полинейропатии осложняются параличом дыхательной мускулатуры, аспирационной пневмонией, отеком головного мозга, тромбоэмболиями, рабдомиолизом. Постоянные эрозии кожных покровов могут привести к бактериальным инфекциям. При ЭПП из-за отложения нерастворимого в воде протопорфирина может развиться цирроз печени и печеночная недостаточность.
Диагностика
При подозрении на порфирию пациента направляют к врачу-гематологу. При постановке диагноза учитывается наличие заболевания у близких родственников, возраст больного, обстоятельства возникновения симптомов (инсоляция, прием лекарств или алкоголя, голодание, инфекции, менструации, беременность). Лабораторная диагностика порфирий следующая:
Эритропоэтические порфирии дифференцируют с дерматологическими заболеваниями (буллезным пемфигоидом, вульгарной пузырчаткой), с гематологическими патологиями, протекающими со спленомегалией (лейкозами, лимфомами, аутоиммунными гемолитическими анемиями) с болезнями почек. ПКП дифференцируют с заболеваниями печени, гемохроматозом, надпочечниковой недостаточностью. Острые порфирии следует дифференцировать с хирургическими заболеваниями, сопровождающимися сильной болью в животе, неврологическими и психиатрическими патологиями.
Лечение порфирий
Пациентов с острыми и эритропоэтическими порфириями необходимо госпитализировать отделение гематологии. Лечение ПКП возможно как в стационаре, так и в амбулаторных условиях. На сегодняшний день не существует эффективных методов, полностью ликвидирующих нарушения обмена порфиринов. Основной упор делается на патогенетическую и симптоматическую терапию, а также на устранение провоцирующих факторов. Способы лечения зависят от вида порфирий: