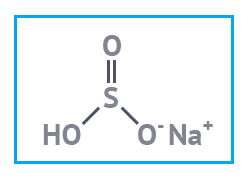
Натрия гидросульфат что это такое
Гидросульфат натрия: способы получения и химические свойства
Гидросульфат натрия NaHSO4 — кислая соль щелочного металла натрия и серной кислоты. Белое кристаллическое вещество. Плавится без разложения, при дальнейшем нагревании разлагается.
Относительная молекулярная масса Mr = 120,06; относительная плотность для ж. и тв. состояния d = 2,742; tпл = 186º C;
Способ получения
1. В результате взаимодействия холодной и концентрированной серной кислоты и гидроксида натрия, образуется гидросульфат натрия и вода:
2. Твердый сульфат натрия реагирует с концентрированной серной кислотой. В результате реакции образуется гидросульфат натрия:
3. При температуре до 50º C в результате реакции между твердым хлоридом натрия и концентрированной серной кислотой происходит образование гидросульфата натрия и газа хлороводорода:
Химические свойства
1. Гидросульфат натрия разлагается при температуре 250–320º C в вакууме с образованием пиросульфата натрия и воды :
2. Гидросульфат натрия может взаимодействовать со сложными веществами :
2.2. С хлоридом натрия гидросульфат натрия реагирует при температуре 450–800º C с образованием сульфата натрия и хлороводородной кислоты:
3. Гидросульфат натрия может взаимодействовать с простыми веществами-металлами :
Гидросульфат натрия
Гидросульфат натрия (пищевая добавка Е514(ii), кислый сернокислый натрий, бисульфат натрия) — кислая соль натрия и серной кислоты с формулой NaHSO4, бесцветные кристаллы. Образует кристаллогидрат NaHSO4·H2O. Пищевая добавка Е514(ii) относится к регуляторам кислотности искусственного происхождения, является производной серной кислоты, используется в технологических целях в процессе производства пищевых продуктов.
Получение
Гидросульфат натрия получают действием серной кислоты на гидроксид или сульфат натрия:
Физические свойства
Применение
Различают два типа применяемых в пищевой промышленности сульфатов натрия:
Польза и вред
Научные данные о пользе применения пищевой добавки Е514(ii) для здоровья человека в настоящий момент отсутствуют. Биологической ценности не представляет.
Относится к 4 классу опасности. При чрезмерном употреблении может провоцировать расстройства желудка и кишечника, тошноту.
Беременность и грудное вскармливание
Применение при беременности
Адекватных и хорошо контролируемых исследований о возможности применения гидросульфата натрия у беременных женщин не проведено.
Применение в период грудного вскармливания
Специальных исследований о возможности применения гидросульфата натрия в период грудного вскармливания не проведено.
Особые указания
В Российской Федерации, Евросоюзе, на Украине и в большинстве стран мира пищевая добавка Е514(ii) разрешена для применения в пищевой промышленности.
Классификация
Категория при беременности по FDA
N ( не классифицировано FDA )
Поделиться этой страницей
Подробнее по теме
Ознакомьтесь с дополнительной информацией о действующем веществе Гидросульфат натрия:
Гидросульфит натрия (Е222)

Свойства гидросульфита натрия
Кроме свойств консерванта и антиоксиданта, гидросульфит натрия обладает свойствами стабилизатора и отбеливателя. Внешне он представляет собой кристаллическую массу жёлтого или белого цвета или же порошок, обладающий мощным запахом диоксида серы. Данное вещество достаточно неустойчиво: в сочетании с водой образуется пиросульфит. В воде гидросульфит натрия растворяется, а вот в спиртах, жирах и маслах этого не наблюдается.
Синтез гидросульфита натрия производится за счёт соединения карбоната натрия и диоксида серы. Произведённое таким образом вещество пожароопасно, если наблюдается контакт с водой в воздушном пространстве с высоким содержанием кислорода. В то же время в чистом виде он не несёт никакой опасности. При контакте с водой происходит выделение серы и возгорание. Человеческое тело может потреблять добавку E222 в день до 0,7 миллиграммов на один килограмм веса.
Упаковка добавки E222
Согласно международным нормам, упаковывать и перевозить гидросульфит натрия можно в двух видах тары. К первому виду относятся стальные бочки, помещённые в бочки из фанеры. Другой вид упаковки – полиэтиленовые мешки, помещённые в стальные бочки с толщиной стенок выше полумиллиметра. Таким образом, обеспечивается максимальная герметичность тары и пресекаются любые попытки контакта вещества с окружающим воздухом. Как уже было упомянуто выше, достаточно совсем немного воды, чтобы вызвать опасную реакцию. Фасуют гидросульфит натрия по 50 килограммов в одну тару. Данные меры предписаны во всех нормативно-правовых актах стран, которые занимаются производством, поставкой или применением добавки E222.
Основные производители гидросульфита натрия
Вообще такое вещество, как гидросульфит натрия, можно произвести в любой частной лаборатории благодаря простоте реакции соединения веществ, необходимых для его изготовления. Но ввиду опасности этого вещества его производство ведётся только крупными химическими компаниями, которые уже имеют налаженный круг потребителей. К таким фирмам можно отнести:
Применение гидросульфита натрия

Процесс борьбы с микробами таков: гидросульфит натрия контактирует с водой и продуктами брожения. Так, образуется сернистый газ, в котором погибают бактерии, грибки и дрожжи.
Гидросульфит натрия – это добавка, известная, пожалуй, всем кондитерам в Украине и России. E222 добавляется в желе и мороженое, повидло и джемы. Но не сладостями едиными. На этикетках упаковок сушёных фруктов, мяса, колбас, рыбных продуктов питания, консервированных и свежемороженых овощей и фруктов также можно увидеть присутствие гидросульфита натрия. E222 – это практически незаменимое вещество для изготовления полуфабрикатов на грибной и картофельной основе, а также жидких пектинов.
Также добавка E222 используется и в других сферах промышленности. В частности при производстве тканей и покраске хлопка гидросульфит натрия снимает активные красители. Гидросульфит натрия является хорошим восстановительным средством для различных красителей, а также консервирующим – для беления тканей. Применяется это вещество и в более тяжёлой промышленности. К примеру, в биохимической инженерии с его помощью поддерживают отсутствие воздуха в реакторе. Имеет гидросульфит натрия своё применение в лёгкой и химической промышленности.
Польза и вред гидросульфита натрия для человеческого организма
Многочисленными научными исследованиями доказано, что пищевая добавка E222 абсолютно бесполезна для человеческого здоровья. Более того, она может наносить ощутимый вред организму. В США и странах Европейского союза гидросульфит находится под запретом использования в пищевой промышленности и в виноделии в особенности. В то же время в России, Украине и других странах СНГ до сих пор добавляется в продукты питания.
Дело в том, что в Украине и России пока не зарегистрированы летальные случаи употребления данного консерванта. Однако отмечается, что эта добавка может стать причиной возникновения аллергических реакций, а также вызвать некоторые проблемы в работе желудка. В США же в 70-ых годах XX века было зарегистрировано несколько летальных исходов. Люди умирали после употребления в пищу сырых фруктов, в которые для сохранения вкуса добавлялся гидросульфит натрия. Также было отмечено несколько десятков случаев поступления в медучреждения больных с острыми формами заболеваний желудочно-кишечного тракта и серьёзной аллергией, вызванной как раз данным веществом. Позже, в 1980 году, это стало причиной запрета применения данной добавки в пищевой промышленности.
Отмечается, что именно гидросульфит натрия является основной причиной разрушения в организме человека витамина B1. Этот витамин имеет большое значение для обмена в организме углеводов, белков и жиров. При этом разрушения витамина B1 происходит как раз в тех органах, где он откладывается больше всего, то есть в почках, печени, сердце и мозге.
Специалисты рекомендуют заменять добавку E222 какими-нибудь другими консервантами. Например, прекрасно подойдёт сорбиновая кислота, маркирующаяся отметкой E200. Видя в магазинах продукты питания, в состав которых входит добавка E222, покупатель сам должен решить, брать ему этот продукт или нет. На данный момент в винодельческой промышленности проводятся исследования и разработки замены данному веществу, которое смогло бы настолько хорошо убивать бактерии и дрожжи в вине. В любом случае добавку E222 однозначно нельзя назвать полезной для здоровья, поэтому врачами рекомендуется сократить потребление продуктов, которые могли бы содержать гидросульфит натрия.
Гидросульфат натрия
| Гидросульфат натрия | |
| Общие | |
|---|---|
| Систематическое наименование | Гидросульфат натрия |
| Традиционные названия | Сернокислый натрия, кислый |
| Химическая формула | NaHSO4 |
| Физические свойства | |
| Состояние (ст. усл.) | бесцветные кристаллы |
| Молярная масса | 120,06 г/моль |
| Плотность | 2,472 г/см³ |
| Термические свойства | |
| Температура плавления | 186 °C |
| Химические свойства | |
| Растворимость в воде | 28,6 0 ; 50 100 г/100 мл |
Гидросульфат натрия — кислая соль натрия и серной кислоты с формулой NaHSO4, бесцветные кристаллы. Образует кристаллогидрат NaHSO4•H2O.
Содержание
Получение
Физические свойства
Химические свойства
Применение
Литература
Полезное
Смотреть что такое «Гидросульфат натрия» в других словарях:
Гидросульфат аммония — Общие Систематическое наименование Гидросульфат аммония Традиционные названия Сернокислый кислый аммоний Химическая формула NH4HSO4 Физические свойства Состояни … Википедия
Натрия фосфаты — Известны следующие фосфаты натрия: Дигидрофосфат натрия NaH2PO4 Гидрофосфат натрия Na2HPO4 Ортофосфат натрия Na3PO4 Применение Употребляются для буферных растворов различного назначения, как эмульгаторы в пищевой промышленности … Википедия
натрия гидросульфат — natrio hidrosulfatas statusas T sritis chemija formulė NaHSO₄ atitikmenys: angl. sodium hydrogen sulfate; sodium hydrosulfate rus. натрий кислый сернокислый; натрия бисульфат; натрия гидросульфат ryšiai: sinonimas – natrio vandenilio… … Chemijos terminų aiškinamasis žodynas
Натрия сульфат — сернокислый натрий, Na2SO4, соль; бесцветные кристаллы. Встречается в природе в виде минерала Тенардита; плотность 2,698 г/см3, tпл 884 °С. Растворимость в воде (%): 16,3 (20 °С), 29,8 (100 °C). Безводный Na2SO4 устойчив выше температуры… … Большая советская энциклопедия
НАТРИЯ СУЛЬФАТ — Na2SO4, бесцв. кристаллы; известен в четырех полиморфных модификациях (см. табл.); показатели преломления: меньший 1,469, средний = 1,476, больший 1,481; кристаллизуется из водных р ров выше 32,384 °С. В интервале от 1,2 до 32,4 °С… … Химическая энциклопедия
натрия бисульфат — natrio hidrosulfatas statusas T sritis chemija formulė NaHSO₄ atitikmenys: angl. sodium hydrogen sulfate; sodium hydrosulfate rus. натрий кислый сернокислый; натрия бисульфат; натрия гидросульфат ryšiai: sinonimas – natrio vandenilio… … Chemijos terminų aiškinamasis žodynas
Сульфат натрия — Сульфат натрия … Википедия
Хлорид натрия — Хлорид натрия … Википедия
Гидроксид натрия — Гидроксид натрия … Википедия
Гипохлорит натрия — Общие … Википедия
Натрий гидросульфит — широко востребованный в промышленности реактив
Гидросульфит натрия — неорганическое соединение, 
В природе не встречается. Получают его в результате воздействия газообразной двуокиси серы на водный раствор карбоната или гидрокарбоната (сода) натрия. Полученный раствор потом подвергается кристаллизации.
Свойства
Кристаллическое вещество белого цвета, иногда с легким желтоватым или сероватым оттенком. С резким запахом двуокиси серы. Водорастворимо. Не растворяется в спиртах, маслах, жирах. Водный раствор имеет светло-желтый цвет, иногда с коричневым оттенком. Горит, не взрывается. При нагревании выше +65 °С разлагается с выделением ядовитого сернистого ангидрида.