Нвр что это такое расшифровка в медицине
Нвр что это такое расшифровка в медицине
Национальные водные ресурсы
налогооблагаемые временные разницы
Смотреть что такое «НВР» в других словарях:
Заработная плата — Содержание 1 Функции заработной платы 1.1 Мотивационная … Википедия
Бут, Владимир — Владимир Бут Общая информация Полное имя Владимир Владимирович Бут Прозвище <<<прозвище>>> … Википедия
Бут В. — Владимир Бут Общая информация Полное имя Владимир Владимирович Бут Прозвище <<<прозвище>>> … Википедия
Бут В. В. — Владимир Бут Общая информация Полное имя Владимир Владимирович Бут Прозвище <<<прозвище>>> … Википедия
Бут Владимир — Владимир Бут Общая информация Полное имя Владимир Владимирович Бут Прозвище <<<прозвище>>> … Википедия
Бут Владимир Владимирович — Владимир Бут Общая информация Полное имя Владимир Владимирович Бут Прозвище <<<прозвище>>> … Википедия
Владимир Бут — Общая информация Полное имя Владимир Владимирович Бут Прозвище <<<прозвище>>> … Википедия
Владимир Владимирович Бут — Владимир Бут Общая информация Полное имя Владимир Владимирович Бут Прозвище <<<прозвище>>> … Википедия
Жерри-Кристиан Тчуйсе — Общая информация Полное имя <<<полное имя>>> … Википедия
Жерри-Кристиан Тчуйссе — Жерри Кристиан Тчуйсе Общая информация Полное имя <<<полное имя>>> … Википедия
Врач объяснил, как расшифровать свои анализы на антитела к COVID-19
С результатами подобных анализов корреспондент «Российской газеты» обратилась к сертифицированному специалисту по физической реабилитации, члену Европейской ассоциации амбулаторной реабилитации Леониду Дьякову.
Антитела: иммунный ответ
Леонид Леонидович, в лаборатории люди получают результаты исследования, естественно, безо всяких комментариев. Их отправляют к врачам. Но к ним сейчас пробиться нелегко, да и не каждый рискует сидеть в очередях. В итоге человек мучительно вглядывается в непонятные обозначения, думает, плохо это или хорошо. Расскажите, что значит: «Антитела обнаружены».
Тест на антитела может показать, сталкивался ли человек с коронавирусом, даже если симптомов COVID-19 у него не было. Если антитела обнаружены, значит, организм среагировал на встреченный вирус. Они могут сохраняться, даже если самого вируса в организме уже нет. Этот тест говорит только о том, что произошел некий иммунный ответ.
Таким образом, выявление антител в крови является информативным свидетельством текущего или прошлого инфекционного процесса и помогает выявить стадию развития инфекции.
Обнаружение IgM указывает на недавнее инфицирование SARS-CoV-2. Они появляются непосредственно после контакта с носителем вируса, на третий-четвертый день. Через семь-десять дней они уже точно присутствуют в крови.
Потом они «стареют»?
Леонид Дьяков: Общий период вероятного выявления антител класса M не превышает двух месяцев. В течение этого времени IgM антитела постепенно полностью сменяются на IgG. Последние начинают формироваться в среднем на 21-й день.
Если еще есть IgM, и уже появились иммуноглобулины класса G, то это означает позднюю инфекцию. Просто IgM еще не сошли на нет.
Получается, наличие IgM не обязательно говорит об активной инфекции?
Леонид Дьяков: Да. Эти антитела могут выявляться и на стадии выздоровления.
Когда в крови выявляются только IgG, это говорит о том, что пациент выздоровел, и у него сформировался иммунитет к SARS-CoV-2. Если уровень IgG достаточно высок, то можно стать донором иммунокомпетентной плазмы. Например, IgG больше 40, а IgM больше 1,5, либо IgG больше 80, а IgM равно нулю.
То есть, если в крови выявлены обе группы антител, это означает, что человек уже выздоравливает?
Леонид Дьяков: Совершенно верно. Еще раз повторю: иммуноглобулины М говорят о том, что человек в данный момент болеет коронавирусом. Это не обязательно тяжелые формы, состояние может быть и бессимптомным. А иммуноглобулины G говорят о том, перенес ли он коронавирусную инфекцию в прошлом.
Далее, в графе «Дополнительная информация», вообще непонятная шифровка. А чем непонятнее, тем ведь страшнее. К примеру, вот передо мной результаты, переданные одним пациентом: «ОПсыв 0,0338; КП 1,45». Что кроется за этим?
От чего зависит количество антител в организме?
Лучше не болеть
Заразен ли человек, чей анализ мы расшифровываем?
Леонид Дьяков: По данному тесту нельзя определить, заразен ли еще человек. В принципе, с такими показателями, которые вы предоставили, пациент не заразен.
Но чтобы достоверно знать это, следует все же сдать еще мазок. Именно он покажет, выделяется ли вирус во внешнюю среду. Если он будет отрицательный, то человек стопроцентно не заразен. Без этой уверенности я бы рекомендовал соблюдение мер социальной дистанции и индивидуальной защиты даже в случае обнаружения только антител класса IgG.
А вы верите в то, что все должны переболеть, и тогда с эпидемией будет покончено?
Леонид Дьяков: В этом, конечно, есть логика. Но проблема в том, что вирус дает достаточно серьезные осложнения. И не все болеют в легкой или бессимптомной форме.
Люди, узнавшие что у них обнаружены антитела, начинают думать, когда же, где подхватили заразу. Вспоминают, когда болели. Может ли данный тест показывать антитела не только на COVID-19, но и на перенесенные другие ОРЗ или ОРВИ?
Леонид Дьяков: Исключено. Это специфичный тест именно на антитела к коронавирусной инфекции.
Человек припомнил, что сильно болел в феврале, ему было очень плохо. Мог тогда быть коронавирус?
Леонид Дьяков: Иммуноглобулин G с тех пор не сохранился бы.
То есть, носители антител могут, в принципе, радоваться, что переболели коронавирусом, практически не заметив этого?
Леонид Дьяков: Те, кто переболел легко или бессимптомно, вырабатывают низкий уровень иммуноглобулина G и могут заболеть повторно.
Чем тяжелее протекает заболевание, тем больше антител произведет иммунная система, и тем дольше они проживут в крови после болезни.
Однако есть информация, что сохраняются так называемые клетки памяти. Организм запоминает, как вырабатывать эти антитела, при каких условиях и в каком количестве. И в случае повторного контакта с вирусом организм начинает синтезировать IgG-антитела значительно быстрее, не за 21 день, а за три. И они способны «смягчать» течение заболевания, препятствовать развитию тяжелых осложнений.
Дышите глубже
Получается, что в принципе сдавать тест на антитела и не совсем нужно. Какая разница, болел человек или нет, если этого особо и не заметил, а никаких таких преимуществ наличие антител не дает. Все так же нужно предохраняться от заражения…
Леонид Дьяков: Мое личное мнение, если человек чувствует себя хорошо, особой надобности в тестировании нет. Ведь с тем же успехом можно поискать у себя вирус герпеса и другие.
Однако тестирование поможет решить проблему в более глобальном масштабе, выработать стратегию борьбы с коронавирусом, поскольку по количеству иммунных людей можно спрогнозировать, когда случится спад эпидемии.
Что делать тем, у кого обнаружены антитела класса IgM?
Леонид Дьяков: Если нет явных признаков заболевания, нужно побольше двигаться, гулять на свежем воздухе, дышать полной грудью, чтобы работали легкие, а кислород циркулировал в крови.
Все материалы сюжета «COVID-19. Мы справимся!» читайте здесь.
Нарушение ритма сердца и проводимости (аритмии сердца)
Тел.: 8-800-25-03-03-2
(бесплатно для звонков из регионов России)
Санкт-Петербург, наб. реки Фонтанки, д. 154
Тел.: +7 (812) 676-25-25
Санкт-Петербург, В.О., Кадетская линия, д. 13-15
Тел.: +7 (812) 676-25-25
Санкт-Петербург, ул. Циолковского, д.3
Тел.: +7 (812) 676-25-10
Практически у 80% пациентов с ишемической болезнью сердца регистрируются аритмии различного характера и до 65% из них угрожают жизни. НРС могут быть самостоятельными или являться осложнением заболеваний сердечно-сосудистой системы и других органов и систем
С учетом частоты сердечных сокращений их можно подразделить на две большие группы:
1. Брадиаритмии:
2. Тахиаритмии:
Важно отличать нарушения ритма сердца, вызванные органическим (необратимым) поражением миокарда, и функциональные нарушения. Как правило, функциональные нарушения встречаются при здоровом сердце и могут быть вызваны психогенными, рефлекторными и гуморальными расстройствами. Функциональные нарушения ритма сердца встречаются достаточно часто, важно выявить и исключить вызывающие их причины, что позволит избавить человека от аритмии.
Органические нарушения возникают при: коронарной ишемии, гемодинамических пороках сердца и крупных сосудов, сердечной недостаточности, гипертонии. Они могут появляться при токсическом воздействии (медикаментозных препаратов, алкоголя и др.) или инфекционно токсическом (ревматизм, вирусные инфекции, миокардиты различной этиологии и др.), гормональных сдвигах. Аритмии бывают врожденные (синдром WPW, врожденная АВ блокада и др.) и приобретенными, вызванные внешними воздействиями (миокардит,операции и травмы сердца и др.).
Основные симптомы (проявления аритмий)
Брадиаритмии:
Тахиаритмии:
Обычно диагностика аритмий осуществляется врачом поликлиники, кардиологом или врачом скорой помощи. Имеет значение сбор анамнеза, физикальное обследование, и различные инструментально-диагностические методы. Наиболее важным является регистрация НРС на ЭКГ (для предъявления аритмологу).
На сегодняшний день в специализированных или многопрофильных клиниках пациентов консультирует врач кардиохирург-аритмолог и определяет необходимость и возможность эндоваскулярного интервенционного (малотравматичного) лечения нарушения ритма сердца. В нашей Клинике есть все необходимые ресурсы для диагностики и лечения аритмий
К методам диагностики нарушения ритма сердца относят:
Тилт-тест – проба с пассивным ортостазом. Проводится на специальном поворотном столе. Позволят выявить или исключить связь между развитием обморочных состояний и нарушениями сердечного ритма.
Лечение аритмий: хирургическая коррекция нарушений ритма сердца
В нашей Клинике выбор способа лечения нарушения ритма сердца осуществляется специа-листом с учетом клинической картины заболевания, данных инструментально-диагностических исследований и рекомендаций Российского кардиологического обще-ства, Всероссийского научного общества аритмологов.
Самостоятельный прием препаратов, самолечение различными методами является крайне не желательным и не безопасным, если неизвестен и не учитывается характер, механизм и причина аритмии.
Существует несколько способов лечения нарушения ритма сердца:
Операция выполняется под местной анестезией в условиях рентгеноперационной длительностью до 40-55 минут.
Эффективным и радикальным методом лечения тахиаритмий является катетерная аблация (деструкция) очага аритмии. Операция, в среднем, длится не более 1 часа, и через сутки пациент может быть выписан из стационара.
Нвр что это такое расшифровка в медицине
Хронический гастрит является наиболее распространенным заболеванием и занимает одно из первых мест в структуре заболеваний тракта. По оценке различных авторов, он встречается у 50–80% населения нашей страны [1, 2]. Открытие Н.pylori австралийскими учеными и в 1983 году явилось поистине революционным и вызвало невероятный прогресс в гастроэнтерологии. Современным интернистам это принесло «понимание того, что микроорганизм H.pylori является важным участником формирования таких патологических состояний, как острый и хронический гастрит, язвенная болезнь желудка и двенадцатиперстной кишки, рак и желудка» [3] и позволило выйти на разработку новых, более эффективных этиопатогенетических принципов лечения и профилактики этих заболеваний.
Helicobacter pylori (Н.pylori) — грамотрицательная микроаэрофильная бактерия, колонизирующая слизистую оболочку желудка и ассоциированная с атрофическим гастритом, язвенной болезнью желудка и двенадцатиперстной кишки, аденокарциномой и экстранодальной желудка. H.pylori является одним из самых распространенных возбудителей инфекционных заболеваний. Согласно некоторым оценкам, более половины населения мира инфицированы этим микроорганизмом. Инфекция H.pylori часто не имеет клинических проявлений. Только у определенной части инфицированных с течением времени развивается хронический атрофический гастрит и рак желудка. В 2005 году первооткрыватели бактерии — Робин Уоррен (Robin Warren) и Барри Маршал (Barry Marshall) — были удостоены Нобелевской премии по физиологии и медицине «за открытие бактерии Helicobacter pylori и ее роли в развитии гастрита и язвы желудка». Интенсивное изучение H.pylori показало, что у 80% больных, страдающих раком желудка, в анамнезе была зафиксирована инфекция H. pylori. Это явилось одной из причин, по которым в 1995 году Международная ассоциация по изучению рака (IARC, ВОЗ) признала H.pylori канцерогеном I класса.
Новые европейские рекомендации по инфекции H.pylori, представленные на очередном XXIV заседании Международной рабочей группы по изучению Helicobacter pylori и родственным бактериям при хронических воспалительных процессах пищеварительного тракта и раке желудка (XXIVth International Workshop on Helicobacter and related bacteria in chronic digestive inflammation and gastric cancer) 11–13 cентября 2011 года, были посвящены не только новым подходам к терапии, но и современным методам диагностики инфекции Н.pylori. Эти методы делятся на инвазивные и неинвазивные. Все инвазивные методы диагностики предусматривают проведение эндоскопического исследования с забором биопсийного материала — биоптатов слизистой оболочки желудка. Эндоскопическое исследование является одним из самых важных методов оценки слизистой оболочки желудка у пациентов с H.pylori ассоциированной патологией. Применение узкоспектральной эндоскопии в комбинации с оптическим увеличением изображения позволяет дифференцировать патологические изменения, которые при обычной эндоскопии не могут быть выявлены. Неинвазивные методы — это различного рода иммунологические исследования, позволяющие определять наличие антител в сыворотке крови или бактериального антигена Н.pylori в фекалиях, ПЦР исследование с определением ДНК Н.pylori в фекалиях и уреазный дыхательный тест с С13 или С14 меченным атомом углерода.
История открытия Helicobacter pylori
Таблица 1. Распространенность инфекции H.pylori и смертность от рака желудка в странах с различным уровнем
| Страна | Инфицированность H. pylori, % | Смертность (рак желудка) |
| Китай Россия и Япония | 80-100 60-80 | Более 30 человек на 100 000 населения |
| Алжир Коста-Рика Кот-Дивуар Нигерия Чили Эквадор | 75-95 | Более 30 человек на 100 000 населения |
| Австралия Бельгия Великобритания Израиль Канада Новая Зеландия США Франция | 4 5 9 15 13,6 5 23 20 | Менее 10 человек на 100 000 населения |
Приведенные данные свидетельствуют о более высокой заболеваемости раком желудка в тех регионах, где выше показатели заболеваемости H.pylori ассоциированным гастритом.
Современные методы лабораторной диагностики инфекции Helicobacter pylori
С момента открытия Н.pylori прошло чуть более тридцати лет. За этот период времени было разработано большое количество методов лабораторной диагностики, позволяющих выявлять и идентифицировать этот микроорганизм. Однако в настоящее время ни один из существующих методов лабораторной диагностики инфекции Н.pylori не универсален. Пределы возможностей этих методов могут быть ограничены не только их чувствительностью, но, зачастую, зависят от возраста пациента, его индивидуальных особенностей, стадии заболевания, а также индивидуальных особенностей течения инфекции. Все существующие на сегодняшний день методы лабораторной диагностики инфекции Н.pylori делятся на две большие группы: инвазивные и неинвазивные методы (табл. 2).
Таблица 2. Методы лабораторной диагностики инфекции Н.pylori
| Инвазивные методы | Неинвазивные методы |
| Бактериологический метод Гистологический метод Молекулярно-биологический метод (ПЦР) Фазово-контрастная микроскопия Быстрый Уреазный тест | Серологический метод Молекулярно-биологический метод (ПЦР) Уреазный дыхательный тест |
Принципиальное значение для практики имеет проведение диагностики Н.pylori инфекции до лечения (первичная диагностика), и после проведения противохеликобактерной терапии (контроль эффективности выбранной схемы лечения). Первичная диагностика Н.pylori инфекции должна осуществляться методами, непосредственно выявляющими бактерию или продукты ее жизнедеятельности в организме больного. Таким требованиям удовлетворяют следующие методы диагностики:
1. Бактериологический метод — посев биоптата слизистой оболочки желудка или двенадцатиперстной кишки на среду с целью выделения чистой культуры Н.pylori.
2. Дыхательный тест — определение в выдыхаемом больным воздухе изотопов С13 или С14, которые выделяются в результате расщепления в желудке больного меченой мочевины под действием фермента уреазы Н.pylori.
3. Быстрый Уреазный тест — определение уреазной активности в биоптате слизистой оболочки желудка или двенадцатиперстной кишки путем помещения его в жидкую или гелеобразную среду, содержащую субстрат, буфер и индикатор.
4. Гистологический метод — золотой стандарт диагностики Н.pylori инфекции и хронического гастрита.
Бактериологический метод является единственным методом исследования, обладающим 100% специфичностью. Он позволяет выделить чистую культуру Н.pylori, провести ее идентификацию, изучить морфологические, биохимические и биологические свойства бактерий. В эпидемиологической практике выделение чистой культуры Н.pylori необходимо для внутривидового типирования штаммов, что может быть использовано при мониторинге для дифференциации между реинфекцией новым штаммом и рецидивированием инфекции, которое может быть обусловлено тем же штаммом. В научной практике бактериологический метод важен, так как позволяет изучать факторы патогенности Н.pylori и изготовлять препараты для серологической диагностики. Как и любой метод диагностики, бактериологический метод исследования обладает не только достоинствами, но и недостатками, которые зачастую ограничивают его широкое использование в клинической практике. К недостаткам этого метода относятся, прежде всего, необходимость специального лабораторного оборудования, реактивов, специальных питательных сред, а также обученных специалистов. Все это сопряжено с большими материальными затратами. Результаты бактериологического исследования отсрочены от момента взятия биопсийного материала минимум на 3–5 дней, а при необходимости получения данных о чувствительности Н.pylori к антибактериальным препаратам длительность исследования увеличивается и составляет в среднем 6–7 дней. Кроме того, для проведения бактериологического исследования необходимо проведение эзофагогастродуоденоскопии с забором биопсийного материала.
Быстрый урезаный тест основан на определении в биоптате слизистой оболочки желудка местной уреазной активности H.pylori. Быстрота изменения окраски индикатора (с желтого цвета на красный или малиновый) зависит от уреазной активности, которая в свою очередь зависит от количества бактерий. К недостаткам теста относится его инвазивность, невозможность морфологической оценки состояния слизистой оболочки желудка, а также получение ложноотрицательных (при малом количестве микробных тел) или ложноположительных результатов (контаминирование материала другими уреазопродуцентами, например H.heilmannii — спиралевидной бактерии рода Helicobacter, которую возможно обнаружить у 0,25% пациентов при проведении гастроскопии [12]).
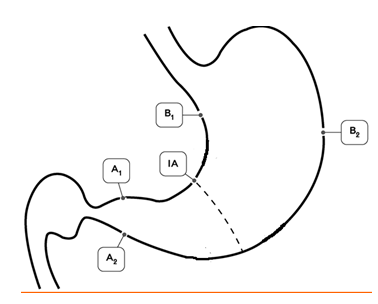
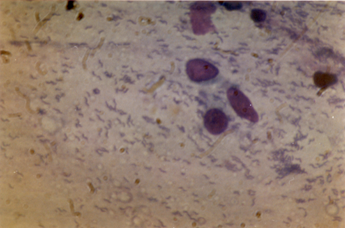
Гистологический метод — золотой стандарт диагностики инфекции H.pylori, который является наиболее объективным методом, так как позволяет обнаружить возбудитель инфекции, определить положение бактериальных тел в слизи, покрывающей слизистую оболочку желудка, наблюдать взаимоотношение Н.pylori с апикальной мембраной эпителиоцитов, а также определить пути взаимодействия бактерии с тканями макроорганизма (рис. 2). Забор биопсийного материала производится из зон слизистой оболочки желудка с признаками наиболее активного воспалительного процесса (максимально выраженная гиперемия и отeк). Биопсия и забор материала для диагностики инфекции из области дна язв и эрозий, а также из их краев, является ошибкой, так как в них нет эпителиальных клеток, обладающих свойствами, необходимыми для адгезии и колонизации Н.pylori. Поскольку бактерии Н.pylori могут быть распределены неравномерно в различных отделах желудка, для повышения чувствительности метода, а также для оценки состояния слизистой оболочки и определения типа и локализации гастрита, степени его выраженности биоптаты целесообразно брать из антрального, фундального отделов, а также области угла желудка (рис. 1).
Рисунок 1. Схема выполнения биопсии слизистой оболочки желудка с целью достоверной диагностики инфекции H.Pylori и гастрита в пяти зонах желудка: две биопсии — в антральном отделе (А1 и А2), две биопсии — в теле желудка (В1 и В2) и одна биопсия в зоне угла желудка (IА).
Рисунок 2. Диагностика инфекции Н.pylori при окраске гистологического препарата красителем акридиновым оранжевым, бактерии определяются в виде мелких, слегка извитых палочек, находящихся в слое слизи над поверхностью эпителия желудка в непосредственной близости от слизистой оболочки желудка и на поверхности эпителиальных клеток.
Классификация количественной и качественной оценки инфекции H. pylori, степени воспаления при гастрите, атрофии и кишечной метаплазии была предложена в Сиднейской системе и ее Хьюстонской модификации, однако эта система не позволяла оценивать прогноз повреждения. Современная классификация и оценка степени и стадии гастрита OLGA (Operative Link for Gastritis Assessment) основана на оценке стадийности и степени выраженности атрофического гастрита в фундальном и антральном отделах желудка [13, 14]. Под степенью гастрита понимается выраженность суммарной воспалительной инфильтрации (нейтрофильными лейкоцитами и мононуклеарными клетками), под стадией — выраженность атрофии. Чем выше выраженность атрофии и больше объем поражения слизистой оболочки желудка, тем выше риск развития неоплазии. Таким образом, новая система определения стадии гастрита OLGA обеспечивает определение прогноза развития предраковых изменений, позволяет клиницисту получить представление о распространенности повреждения слизистой оболочки желудка и степени риска развития рака желудка [15, 16].
В последние годы в клинической практике начал использоваться серологический скрининг заболеваний желудка, включающий определение в сыворотке крови антител класса G к H.pylori (.pylori IgG), пепсиногена I (РG1) и гастрина 17 (G17). Анти- H.pylori IgG являются наилучшим маркером наличия гастрита и обладают высокой чувствительностью и низкой специфичностью в диагностике атрофического гастрита. РG1 и G17 указывают на наличие атрофического гастрита с высокой специфичностью и низкой чувствительностью. Комбинация этих трех тестов (Гастропанель, Биохит, Финляндия) обладает высокой чувствительностью (83%) и специфичностью (95%) в диагностике атрофического гастрита [17]. В проведенном на базе Ярославской областной клинической онкологической больницы и Медицинском центре диагностики и профилактики (г. Ярославль) исследовании, заключавшемся в определении у больных ранним раком желудка и мультифокальным атрофическим гастритом, была обнаружена функциональная недостаточность слизистой оболочки тела желудка (низкий уровень PG1), полученные значения PG1 в этих группах пациентов были достоверно ниже по сравнению с группами больных антральным атрофическим и неатрофическим гастритами. Это свидетельствует о том, что сывороточный PG1 может рассматриваться в качестве маркера риска развития рака желудка. При атрофии антрального отдела желудка происходит снижение выработки постпрандиального G17. Серологический метод с определением G17, РG1 и анти H. pylori IgG может служить методом скрининга атрофического гастрита и рака желудка в крупнопопуляционных исследованиях ввиду его очевидных преимуществ — удобства и безопасности для пациента наряду с высокой эффективностью. Использование серологического теста для выявления предопухолевой патологии и рака желудка на ранних стадиях может способствовать улучшению своевременной диагностики данной патологии, что в итоге должно положительным образом сказаться на уровне заболеваемости и смертности [18].
Генотипирование Helicobacter pylori
Новые эндоскопические технологии диагностики хронического гастрита, ассоциированного с H.pylori
Эндоскопическое исследование — один из самых важных методов оценки слизистой оболочки желудка. Применение дополнительных методик и техник, таких как эндоскопия в узком спектре света, эндоскопия с оптическим увеличением изображения, хромоэндоскопия, позволяют детально изучить структурные особенности слизистой оболочки желудка.
Увеличительная эндоскопия
Первое эндоскопическое исследование с применением оптического увеличения эндоскопического изображения желудка было выполнено еще в 1967 году в Японии (Okuyama) [24]. Это послужило отправной точкой для развития новых эндоскопических технологий, направленных на изучение мельчайших структур поверхности слизистой оболочки. В настоящее время существует два способа увеличения — электронное и оптическое. Изображение, полученное при помощи электронного увеличения, имеет такое же разрешение, как и обычное эндоскопическое изображение. В то время как при применении оптического увеличения становятся видимыми мельчайшие детали, которые невозможно обнаружить при обычном исследовании. Эндоскопы с увеличением оснащены с подвижными линзами в дистальной части аппарата и по своей функциональности сопоставимы с обычными световыми микроскопами. Довольно часто эндоскопическое исследование с увеличением применяется совместно с хромоскопией. Однако применение красителей не позволяет визуализировать микрососудистую архитектонику, что очень важно в дифференциальной диагностике неопластических изменений, к тому же эта дополнительная манипуляция увеличивает время исследования.
Узкоспектральная эндоскопия (narrow band imaging — NBI) — это новая оптическая диагностическая методика, которая основана на использовании специальных оптических фильтров, суживающих спектр световой волны. Обычные эндоскопические системы используют практически весь видимый световой спектр от 400 до 800 нм. Новая система использует преимущества в основном двух световых волн длиной 415 и 445 нм в диагностике сосудистых структур слизистой оболочки пищеварительного тракта, так как эти световые волны хорошо поглощаются гемоглобином. Таким образом, световые фильтры позволяют получить детальное изображение сосудистого рисунка тканей, его изменений, характерных для патологических участков воспалительного генеза, а также для предраковых заболеваний и ранних форм рака. Кроме этого, новая эндоскопическая система повышает контрастность изображения, что создает эффект виртуальной хромоскопии. С технической точки зрения применение функции узкого спектра света в желудке без оптического увеличения нецелесообразно в связи с тем, что получаемое изображение оказывается слишком темным и «шумным». Это происходит того, что при растяжении стенок желудка воздухом во время исследования его просвет становится слишком большим. Поэтому гораздо важнее и актуальнее проводить исследование в узком спектре света совместно с увеличением [25]. Первоначально хромоскопия и эндоскопия в узком спектре света в комбинации с увеличением применялись для оценки раннего рака желудка перед эндоскопической резекцией слизистой оболочки. С дальнейшим внедрением этих технологий в клиническую практику методики оценки микрососудистой архитектоники и микроструктуры поверхности слизистой оболочки стали успешно применятся для диагностики многих других патологических состояний желудка, таких как H.pylori ассоциированный гастрит, кишечная метаплазия, атрофия [26].
Нормальная слизистая оболочка желудка
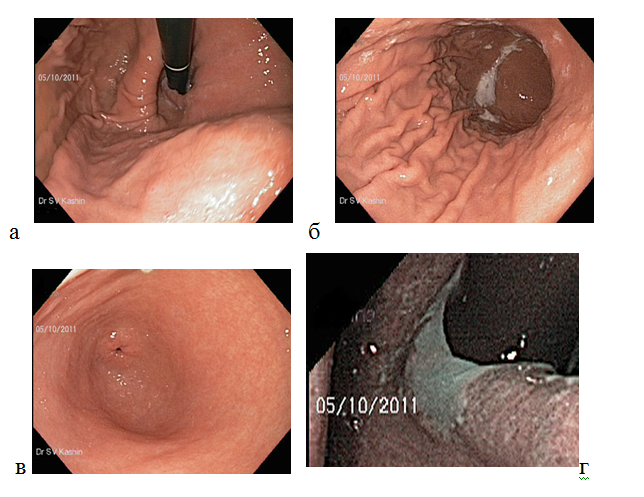
В желудке выделяют четыре анатомических зоны: кардия, фундальный отдел (дно желудка), тело желудка, пилорический (антральный) отдел. Поверхность слизистой оболочки всех отделов желудка выстлана однослойным призматическим железистым эпителием. Для рельефа внутренней поверхности желудка характерно наличие трех видов образований — продольных желудочных складок, желудочных полей и желудочных ямочек. Желудочные складки (plicae gastricae) образованы слизистой оболочкой и подслизистой основой. Желудочные поля (areae gastricae) представляют собой отграниченные друг от друга бороздками участки слизистой оболочки. Они имеют многоугольную форму и размер поперечника от 1 до 16 мм. Наличие полей объясняется тем, что железы желудка располагаются группами, отделенными друг от друга прослойками соединительной ткани. Поверхностно лежащие вены в этих прослойках просвечивают в виде красноватых линий, выделяя границы между полями. Желудочные ямочки (foveolae gastricae) — это углубления эпителия в собственной пластинке слизистой оболочки. Они встречаются по всей поверхности желудка. Число ямочек в желудке достигает почти трех миллионов. Желудочные ямочки имеют микроскопические размеры, но величина их неодинакова в различных отделах желудка. В кардиальном отделе и теле желудка их глубина составляет всего ¼ толщины слизистой оболочки. В пилорической части желудка ямочки более глубокие. Они занимают около половины толщины всей слизистой оболочки [27]. При обычном эндоскопическом исследовании нормальная слизистая оболочка желудка цвета, ее цвет зависит от степени васкуляризации и растяжения — чем больше растяжение, тем бледнее слизистая оболочка. Слизистая оболочка имеет мелкозернистую поверхность благодаря наличию желудочных полей (рис. 4) [28].
Рисунок 4. Нормальная слизистая оболочка тела желудка при стандартном осмотре в белом световом режиме. Вид тела желудка (а) при инверсии (изгибе дистального конца эндоскопа на 180о) и (б) — при прямом осмотре эндоскопом; (в) — слизистая оболочки антрального отдела желудка; (г) — осмотр в узкоспектральном режиме: более контрастное изображение поверхности слизистой оболочки кардиального и субкардиального отделов желудка, мелкозернистая структура эпителия, четкая граница с плоским эпителием пищевода (указана стрелками).
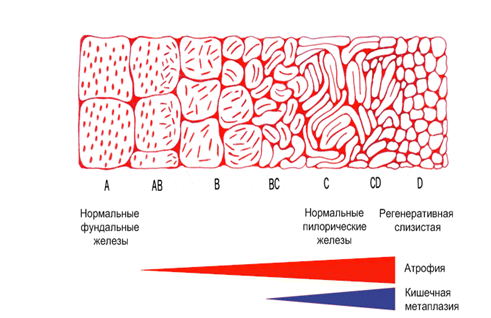
Применение узкоспектральной эндоскопии в комбинации с оптическим увеличением изображения позволяет дифференцировать патологические изменения, которые при обычной эндоскопии не могут быть выявлены. Однако следует отметить, что применение этих технологий не может полностью обеспечить различение абсолютно нормальной слизистой оболочки от гастрита с минимальными изменениями. При осмотре слизистой оболочки с увеличением оцениваются две основные характеристики — микроструктура поверхности слизистой оболочки (ямочный рисунок — pit pattern) и микрососудистая структура (рисунок субэпителиальной капиллярной сети (subepithelial capillary network — SECN). Более тридцати лет назад Sakaki предложил классификацию типов рисунка слизистой оболочки желудка при использовании фиброскопа с увеличением в 30 раз. Согласно этой классификации (рис. 5), выделяют чистые типы (А, В, С, D) и смешанные типы (АВ, ВС, CD). Типы, А и В соответствуют нормальной слизистой оболочке. Дальнейшие изменения рисунка ямок свидетельствуют о более выраженных предопухолевых изменениях, таких как атрофия и кишечная метаплазия (показаны красной и синей полосами в нижней части рисунка). Для диспластических изменений и опухолевого процесса типы рисунка могут соответствовать С (полосатый тип) и D (нерегулярный, зернистый, ячеистый рисунок) типам рисунка.
А — точечные ямки (dotted pits)
В — короткие линейные ямки (short linear pits)
С — полосатые борозды (striped grooves)
D — ячеистые борозды ( grooves)
Рисунок 5. Схема классификации типов рисунка поверхности слизистой оболочки желудка при увеличительной эндоскопии (по Sakaki).
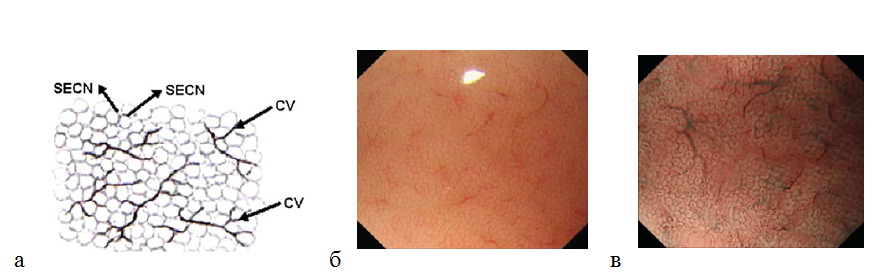
Оценивая микрососудистую архитектонику в теле желудка, можно определить рисунок субэпителиальной капиллярной сети (SECN) в виде пчелиных сот ( network) с коллекторными венулами. Полигональные петли субэпителиальных капилляров окружают каждую желудочную ямку, формируя под эпителием сеть в виде пчелиных сот. Далее ветви сосудистой сети сходятся в коллекторные венулы. При осмотре в узкоспектральном режиме с оптическим увеличением изображения микроструктура поверхности слизистой оболочки становиться более отчетливой: определяются ямки округлой или овальной формы. Ямки гистологически соответствуют желудочным железам. Коллекторные венулы (CV) располагаются глубже, чем субэпителиальная капиллярная сеть, поэтому при осмотре в узком спектре света имеют более насыщенный зеленый цвет. Так как в режиме NBI участки с большей васкуляризацией становятся темными, наблюдается специфическая картина слизистой оболочки тела желудка: светлые участки окружены темным ободком [29] (рис. 6). Правильная форма и взаиморасположение сосудов и структур слизистой оболочки являются наиболее важными ее характеристиками для дифференцировки нормальной и патологически измененной слизистой оболочкой желудка.
Рисунок 6. (а) — рисунок (схема) субэпителиальной капиллярной сети (SECN) в виде пчелиных сот с коллекторными венулами (CV); (б) — нормальная слизистая оболочка тела желудка: эндоскопическое изображение поверхности слизистой оболочки с увеличением изображения: субэпителиальный капиллярный рисунок в виде пчелиных сот с коллекторными венулами; (в) — эндоскопия с увеличением изображения в узкоспектральном световом режиме: более отчетливо видны желудочные ямки округлой или овальной формы, сосудистый рисунок.
Нормальная слизистая оболочка в антральном отделе
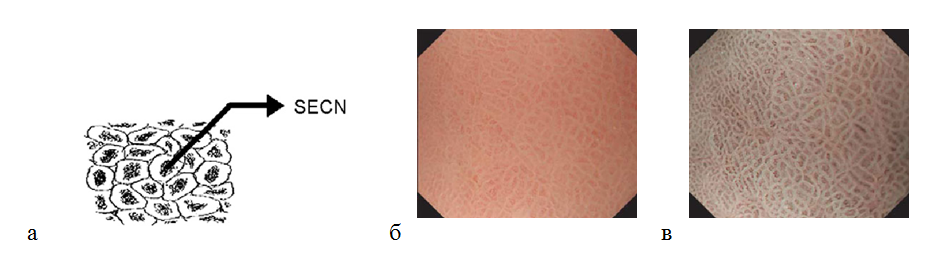
Слизистая оболочка антрального отдела желудка имеет другую картину. При исследовании микрососудистой архитектоники определяется кольцеобразная () субэпителиальная капиллярная сеть. Коллекторные венулы визуализируются реже, так как они находятся в более глубоких частях собственной пластинки, в отличие от тела желудка. Ямки имеют линейный или сетчатый рисунок. Каждый субэпителиальный капилляр расположен в апикальной части желудочной ямки в виде кольца, которое разделяется линейными или сетчатыми бороздками. В отличие от слизистой оболочки тела желудка, в антральном отделе более темные участки окружены светлым ободком (рис. 7). По размерам эти структуры в антральном отделе больше, чем в теле желудка.
Рисунок 7. (а) — кольцеобразная субэпителиальная капиллярная сеть (SECN) в антральном отделе желудка; (б) — нормальная слизистая оболочка антрального отдела желудка: эндоскопическое изображение поверхности слизистой оболочки с увеличением изображения: кольцеобразный субэпителиальный капиллярный рисунок; (в) — эндоскопия с увеличением изображения в узкоспектральном световом режиме: более отчетливо определяется кольцеобразный субэпителиальный капиллярный рисунок и сетчатая микроструктура поверхности слизистой оболочки.