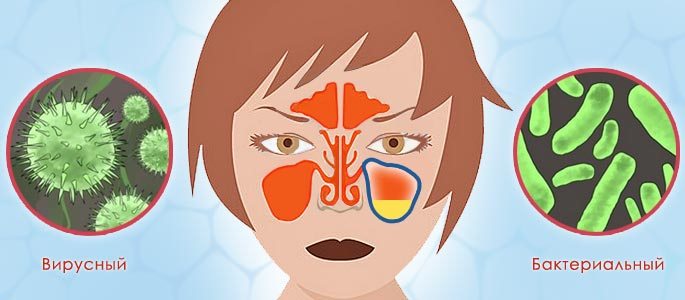
Как понять что присоединилась бактериальная инфекция у ребенка
ОРВИ и бактериальная инфекция у детей – в чем отличия
Они бывают 2-х видов – вирусные и бактериальные. И если, с первыми организм борется сам, то вторые должен лечить специалист. Каждый родитель должен знать и понимать их основные различия.
Острые респираторные вирусные инфекции –самые распространенные, ими болеют все –дети и взрослые во всех странах мира. Практически каждый взрослый несколько раз в год переносит ОРВИ, а у детей они составляют до 75% от всех детских болезней. Часто у ребенка с ослабленным иммунитетом к вирусной, как новая волна, присоединяется бактериальная инфекция дыхательных путей.
Это самая примитивная форма жизни. Микроорганизм-паразит, который не может размножаться вне живой клетки. Внедряясь внутрь, он вынуждает её производить тысячи своих копий. При этом, она погибает, или прекращает выполнять свои функции, а у человека возникают болезненные симптомы.
Что такое бактерии?
Это одноклеточные организмы, размножающиеся делением клетки, способны жить самостоятельно вокруг и внутри нас.
Вирусы способны поражать бактерии, используя их для размножения.
Вирусы и бактерии – микроскопические организмы, вызывающие заболевания у людей, животных и растений, живут в любой, вплоть до агрессивной, среде.
Попадая в организм человека они начинают размножаться. Инкубационный период может быть от нескольких часов до года и больше. Действие их проявляется характерными симптомами, опираясь на которые опытный врач отличает вид инфекции.
Интенсивность симптомов – самый первый критерий. У бактериальных инфекций они проявляются сильнее и в более тяжелой форме.
Особенности вирусной инфекции
ОРВИ – это целая группа болезней, возникающих при заражении разнообразными вирусами. Отличить один от другого можно по анализам, необходимость проведения которых определяет врач.
Заражение проявляется во всем теле, так как вирус редко поражает только одну область.
Особенности бактериальной инфекции
Она чаще всего присоединяется к вирусной, когда иммунитет уже ослаблен, при этом всегда имеет четкую локализацию – нос, уши или легкие.
Различить инфекции можно по анализу крови. Для лечения бактериальной требуются антибиотики и помощь врача.
Квалифицированную консультацию педиатра можно получить в медицинском центре «Таврия».
Здесь же можно сдать все необходимые анализы:
Анализы необходимы для определения типа возбудителя инфекции и постановки точного диагноза. Назначенные физиопроцедуры можно сделать здесь же.
Как отличить вирусный насморк от бактериального
Причины вирусного и бактериального насморка
Причиной ринита чаще всего становятся вирусные и бактериальные инфекции, вызывающие респираторные заболевания.
Абсолютное большинство ринитов, около 90% от общего количества, имеют вирусную природу. Возбудителями простудного заболевания являются разные типы вирусов гриппа и парагриппа, адено- и риновирусы.
Вирусы довольно активны в период холодного сезона – осенью и зимой. Однако «подхватить» инфекцию можно в ситуации, если рядом находится носитель, так как она передается воздушно-капельным путем. Развитию вирусного насморка способствует сниженный иммунитет.
При этом импульсом к развитию бактериального ринита тоже в большинстве случаев является вирусная инфекция. Вирус проникает в клетки и вызывает патологический процесс, на фоне которого снижается иммунитет, и организм становятся более уязвимым перед патогенными микробами. В отдельных случаях бактериальная инфекция является первичной, и ринит возникает без участия вирусов.
Развитию бактериального ринита способствуют:
Чем отличаются симптомы
Помогут определить, вирусный это или бактериальный насморк, симптомы. Признаками бактериальной природы заболевания являются:
При правильном подборе лечения бактериальный ринит проходит через 7-10 дней.
Вирусный ринит также имеет свою характерную симптоматику:
Как правило, заболевание проходит в течение 5 дней.
Отличия вирусного и бактериального насморка у детей и взрослых одинаковы. При этом ребенок переносит насморк, независимо от его природы, тяжелее, чем взрослые. Особенно это характерно для малышей младенческого возраста, которые находятся на грудном вскармливании. Из-за нарушения носового дыхания им тяжелее брать грудь, из-за чего могут возникать расстройства пищеварения.
Как самостоятельно понять, какой насморк

Если же у человека ухудшается самочувствие, температура поднимается до высоких показателей, болезнь продолжает прогрессировать, не проходит через 10 дней и более, необходимо обратиться к врачу. Специалист назначит общий анализ крови, риноскопию, лабораторное исследование мазка из носовых каналов.
Особенности лечения вирусного и бактериального ринита
Для правильного выбора терапии нужно знать, чем отличается вирусный насморк от бактериального.
В период лечения пациенту рекомендуется обильное питье, которое поможет вывести продукты распада и избежать обезвоживания при высокой температуре.
Вирусный насморк нельзя лечить антибиотиками. Вирусы не погибают от веществ, предназначенных бактериям, а бесконтрольный прием таких лекарств может серьезно навредить организму. Кроме того, он становится более уязвимым перед патогенными микробами, так как снижается их восприимчивость к антибиотикотерапии.
Для лечения вирусного ринита назначают противовирусные препараты, промывания носовой полости средствами на основе морской воды, физиотерапевтические процедуры.
Проблемы лечения вирусно-бактериальных респираторных инфекций у «часто и длительно болеющих» иммунокомпрометированных детей
Высокая частота заболеваемости детей повторными острыми респираторными инфекциями вирусного и/или бактериального происхождения всегда являлась весьма серьезной проблемой. Таких пациентов принято называть «часто и длительно болеющими» (ЧДБ). ЧД
Высокая частота заболеваемости детей повторными острыми респираторными инфекциями вирусного и/или бактериального происхождения всегда являлась весьма серьезной проблемой. Таких пациентов принято называть «часто и длительно болеющими» (ЧДБ). ЧДБ — это не нозологическая форма. Использование в педиатрии этой терминологии призвано акцентировать внимание клиницистов различных специальностей, в первую очередь, педиатров, оториноларингологов, пульмонологов, на проблемах детей, имеющих излишне частые (повторные) острые респираторные вирусно-бактериальные инфекции (ОРЗ, ОРВИ) различной этиологии. Многочисленными авторами показано сохранение неуклонного роста числа детей, принадлежащих к группе ЧДБ, составляющих 20–65% детской популяции, при этом отмечается резистентность (неотвечаемость) данной категории больных к традиционным методам терапии. На ЧДБ детей приходится 50–60% всех регистрируемых заболеваний. Около 20% ЧДБ детей болеют ОРЗ практически ежемесячно. В 40% случаев к 7–8 годам у ЧДБ детей формируется хроническая патология, при этом риск хронизации прямо пропорционален увеличению кратности эпизодов ОРЗ в течение года.
ОРВИ у ЧДБ детей нередко характеризуются затяжным течением и присоединением осложнений в виде обострений хронических очагов бактериальной инфекции ЛОР-органов, респираторного и урогенитального тракта. В ряде случаев пациенты из группы ЧДБ нуждаются в помощи клинического иммунолога, поскольку имеют серьезные нарушения функционирования иммунной системы и интерферонового статуса. Таким пациентам, как правило, показана адекватная иммунодиагностика, исследование интерферонового статуса, микробиоценоза слизистых (ПЦР, бакпосевы) с последующим проведением интерфероно- и/или иммунотерапии, санации хронических очагов инфекции на фоне диагностического мониторинга.
Наиболее часто педиатрами для формирования групп детей ЧДБ используются возрастные критерии, предложенные Барановым А. А. и Альбицким В. Ю. (1986): на первом году жизни — 4 и более острых и обострений хронических заболеваний в год, на втором-третьем годах жизни — 6 и более ОРЗ в год, на четвертом году — 5 и более, на пятом-шестом годах — 4 и более, на седьмом году жизни и старше — 3 и более ОРЗ в течение года.
В то же время необходимо отметить, что по нашим данным к ЧДБ взрослым пациентам относятся лица, страдающие ОРЗ более 2–3 раз в году, и в ряде случаев длительность заболеваний может колебаться от 7 до 14 и более дней (Нестерова И. В., Малиновская В. В. и соавт., 2005). При этом нами отмечено, что более чем в 50% случаев взрослые субъекты из числа ЧДБ в детстве также относились к группе ЧДБ. Примерно половина из них имела ремиссию в течение 4–6 лет, в которую они выходили, как правило, в период полового созревания. В последующем возврат к частым ОРЗ происходил на фоне различных провоцирующих факторов: тяжелый психоэмоциональный и/или физический стресс, оперативные вмешательства, наркоз, травмы, тяжелый грипп, ветряная оспа, перенесенная в возрасте старше 18 лет, использование больших доз глюкокортикоидов, неспецифических противовоспалительных препаратов и т. д. Эти наблюдения, по всей видимости, свидетельствуют об имеющихся в ряде случаев генетически обусловленных дисфункциях иммунной системы и системы интерферонов у лиц ЧДБ. В то же время манифестацию повторных ОРЗ необходимо рассматривать как проявление «индикаторных инфекций» ассоциированных с недостаточностью функционирования системы интерферонов (ИФН) и иммунной системы — иммунодефицитов, первичного или вторичного характера. Как правило, у детей или взрослых субъектов, имеющих сочетание ряда факторов риска, возможность реализации генетической предрасположенности к частым заболеваниям возрастает. Формирование контингента ЧДБ, детей и взрослых, во многом определяется неадекватностью реагирования иммунной системы и системы интерферонов на различные неблагоприятные воздействия, приводящие к развитию вторичной иммунной недостаточности (Нестерова И. В., 2008).
Именно с персистенцией вирусных и бактериальных антигенов, возникающей на фоне нарушений иммунитета и в то же время их усугубляющей, в последние годы связывают рецидивирующее течение респираторных заболеваний. Причем у 40–60% детей ОРЗ имеют вирусную природу. Среди вирусов ведущее место занимают риносинцитиальные (РС) вирусы, аденовирусы, риновирусы, вирусы гриппа и парагриппа. При неосложненном течении ОРЗ главенствующая роль отводится, как правило, моновирусной инфекции. Элиминация вирусных антигенов значительно затрудняется при частых рецидивах ОРЗ, особенно при наличии вторичной иммунной недостаточности. Так, вирусы гриппа, парагриппа, РС-вирусы, риновирусы, аденовирусы удается идентифицировать в течение продолжительного времени после острого периода болезни — от 2 недель до нескольких месяцев. От 10% до 30% ОРЗ у детей имеют бактериальное происхождение. Из бактериальных возбудителей, вызывающих острые заболевания органов дыхания, доминирующая роль принадлежит пневмококкам, гемофильной палочке. Однако развитие бактериального процесса может быть обусловлено и такими условно-патогенными микроорганизмами, как золотистый стафилококк, клебсиелла, представителями семейства кишечных палочек.
Особую настороженность вызывает возросшая частота заболеваний дыхательных путей, вызванных хламидиями, микоплазмами, уреаплазмами. Эти внутриклеточные паразиты способны к длительной персистенции в клетках эпителия респираторного тракта, особенно у иммунокомпрометированных детей, что и служит причиной инициации бронхообструктивного синдрома, а в дальнейшем формирования хронических воспалительных заболеваний легких, в том числе бронхиальной астмы.
Этиологическая значимость вирусно-бактериальных ассоциаций установлена в 25–30% острых заболеваний респираторного тракта. Клинически смешанная инфекция обусловливает неосложненное и осложненное течение ОРЗ. В случаях развития у детей острого воспалительного процесса нижних дыхательных путей смешанной этиологии вирусный компонент обычно предшествует бактериальному. Наслоение микробной инфекции нередко связывают с агрессией аутофлоры. При повторных ОРЗ, наряду с инфицированием новыми микроорганизмами, происходит активация латентной, персистирующей инфекции вирусного и бактериального генеза, что утяжеляет течение болезни, способствует хронизации процесса.
Ведущими отличительными признаками в клинической картине у ЧДБ детей являются: 1) резистентность (неотвечаемость) к традиционной терапии ОРЗ вирусной или бактериальной этиологии в соответствии с российскими формулярами; 2) проводимое традиционное лечение не предотвращает упорного рецидивирования (повтора) респираторных инфекций; 3) частота повторных инфекций превышает допустимый возрастной уровень и колеблется от 4–6–10 до 12–24 и более в год; 4) длительность ОРЗ превышает 7 дней и может колебаться от 8 до 14 и более дней; 5) ОРЗ вирусной этиологии провоцируют обострение хронических очагов бактериальной инфекции: хронического тонзиллита, хронических риносинуситов, хронического фаринготрахеита, хронического обструктивного бронхита и т. д.; 6) ОРЗ вирусной этиологии осложняется повторными пневмониями, резистентными к традиционной терапии.
Иммунная система (ИС) обеспечивает контроль за поддержанием антигенного гомеостаза в течение всей жизни человека, т. е. контроль как за проникновением чужеродных микроорганизмов и вирусов, так и генетической однородностью клеточных популяций самого организма. Главная функция иммунной системы: иммунологический надзор — распознавание «своего» и «не своего» (чужого), сохранение «своего» и мгновенное уничтожение «чужого». Таким образом, реализуется важнейший феномен иммунитета — феномен защиты организма от проникновения и негативного влияния любых чужеродных субстанций. В реализации реакций иммунной системы принимают участие два важнейших механизма: врожденный иммунитет и адаптивный (приобретенный) иммунитет.
Респираторные вирусы — облигатные внутриклеточные паразиты. Они различаются по своему строению и способам размножения. Одни из них вызывают острые инфекции и достаточно быстро элиминируются из организма хозяина, другие способны к персистенции.
К основным механизмам противовирусной защиты респираторного тракта относят: локальный иммунитет слизистых респираторного тракта (секреторный IgA, ИФН альфа, ИФН бета, провоспалительные цитокины, секретируемые эпителиальными клетками респираторного тракта), систему ИФН (ИФН альфа, ИФН бета, ИФН гамма), естественные киллерные клетки (CD3 + CD16 + CD56 + ), Т-клеточное звено иммунитета (CD3 + CD8 + ; CD3 + CD56 + ; CD8 + CD25 + ; CD3 + CD4 + ; CD8 + HLA-DR; CD4 + CD25 + ), гуморальные механизмы (нейтрализующие противовирусные антитела класса IgG). В настоящее время известно три основных типа ИФН: ИФН альфа, ИФН бета, ИФН гамма. В инфицированных вирусами клетках респираторного эпителия возрастает продукция ИФН альфа и ИФН бета. Эффекты ИФН альфа и ИФН бета: 1) активация противовирусных механизмов в неинфицированных клетках респираторного эпителия — протективный эффект, клетки приобретают невосприимчивость к вирусной инфекции; 2) активация генов с прямой противовирусной активностью. Антивирусные эффекты ИФН альфа и ИФН бета развиваются через несколько часов и длятся 1–2 дня.
Формирование иммунной системы и становление противовирусного иммунитета является результатом реализации генетической программы онтогенеза, для полноценного завершения которой необходима внешняя и внутренняя антигенная стимуляция. В этом аспекте неизбежные инфекции респираторного тракта у детей раннего возраста должны вести к иммунному тренингу организма. Склонность детей, особенно первых лет жизни, к ОРЗ отчасти обусловлена возрастными особенностями развития их ИС, в том числе и местного иммунитета. В свою очередь, слишком частые ОРЗ не могут негативно не влиять на становление ИС растущего организма, так, постоянная вирусно-бактериальная стимуляция ИС у детей ЧДБ ведет к возникновению нарушений ее функционирования, что сопровождается формированием стойкой иммунной недостаточности — вторичного иммунодефицита (ВИД). ВИД может быть представлен нарушениями как общего, так и местного иммунитета и носить комбинированный или изолированный характер.
В таблице приведена частота встречаемости нарушений различных механизмов противовирусного иммунитета у ЧДБ детей.
С целью повышения функциональной активности ИС, системы ИФН и ускорения восстановления их нарушенных функций, направленных на элиминацию вирусных и бактериальных антигенов, необходимо проведение заместительной и/или модулирующей иммунотерапии, восстанавливающей и модулирующей силу иммунного ответа, что должно обеспечить адекватный иммунный ответ на присутствие инфекционного патогена с последующей его элиминацией.
Тактика иммунотропной терапии при ВИД с синдромом вирусных и вирусно-бактериальных инфекций отличается тем, что в основе восстановления системы интерферонов и иммунной системы лежит базисная терапия отечественным рекомбинантным ИФН альфа-2 — Вифероном. Далее проводится необходимая иммунотерапия заместительного или модулирующего характера. При этом тактика иммунотерапии и, в первую очередь, ее длительность зависят от вида ВИД — острого или хронического. У детей ЧДБ, как правило, имеет место хронический или персистирующий ВИД, т. е. нарушения функционирования системы ИФН и иммунной системы существуют достаточно длительное время — от 6 месяцев до нескольких лет. Безусловно, при такой ситуации, в отличие от острых ВИД, когда иммунотерапия может занимать от 10 до 14 дней, проведение иммунотерапии в рамках программы иммунореабилитации детей ЧДБ занимает от 2,5–4,5 месяцев, в редких случаях до 2–3 лет.
Разработанная нами программа иммунореабилитации (Нестерова И. В., 1992) включает следующие положения:
Иммунотерапия, заместительного и модулирующего характера, органично включается в программы иммунореабилитации. К лекарственным препаратам, используемым для заместительной иммунотерапии, относятся внутривенные иммуноглобулины IgG и IgM обогащенные (Интраглобин и Пентаглобин), специфические иммуноглобулины против цитомегаловирусной инфекции (Цитотект), интерфероны (комплексный препарат рекомбинантного ИФН альфа-2 с антиоксидантами — Виферон в различных дозировках), тимические факторы (Тимоген, Тактивин).
Иммуномодулирующая терапия — «золотой стандарт» иммунотерапии. Результатом ее влияний при ВИД с инфекционным синдромом является восстановление работы дефектных звеньев иммунной системы, нивелирование гиперэргических реакций, восстановление адекватности реагирования иммунной системы на имеющиеся воспалительные процессы различной этиологии.
Одним из обязательных условий проведения иммуномодулирующей терапии при ВИД с вирусно-бактериальным инфекционным синдромом является выполнение ее в рамках традиционного лечения. При этом на начальных этапах в зависимости от вида инфекционного синдрома иммуномодулирующая терапия должна обязательно сочетаться с антибактериальной, противовирусной и/или противогрибковой терапией (Нестерова И. В., 2008).
С нашей точки зрения иммуномодулирующая терапия, используемая в лечении ЧДБ детей, должна иметь направленный характер: точкой приложения используемого иммуномодулирующего препарата должно являться то или иное поврежденное звено иммунной системы. При этом используется преимущественная направленность влияния(ний) иммуномодулятора. Так, для восстановления Т-клеточного звена предпочтительным является применение Тактивина, Тимогена, Имунофана, для восстановления гуморального звена, ЕКК, НГ Ликопида и Полиоксидония. Для восстановления системы ИФН — Виферона, который при определенных условиях обладает и иммуномодулирующими свойствами, направленными на восстановление Т-клеточного звена, системы нейтрофильных гранулоцитов. Для иммунопрофилактики и иммунотерапии бактериальных инфекций у детей ЧДБ может проводиться пролонгированная (в течение 5–6 месяцев) терапия топическими иммуномодуляторами — низкоиммуногенными вакцинами (ИРС 19, Имудон, Рибомунил, Бронхо-мунал и т. д.).
Интерферонотерапия с использованием Виферона обладает не только интерферонкорригирующей, иммуномодулирующей, но и противовирусной активностью и в большинстве случаев при возникновении ОРВИ может использоваться локально и системно, без синтетических противовирусных препаратов. Синтетические противовирусные препараты (Арбидол, Ремантадин) лучше использовать в остром периоде ОРВИ при среднетяжелом или тяжелом течении. При необходимости синтетические противовирусные препараты хорошо сочетаются с Вифероном. Хорошо известным фактом является повреждение клеточных мембран, наблюдаемое в ходе развития инфекционного процесса, что по данным В. В. Малиновской (1998) служит основной причиной снижения противовирусной активности интерферона. С целью восстановления взаимоотношений между антиокислительной активностью плазмы крови и перекисным окислением липидов в состав препарата Виферон введены токоферола ацетат и аскорбиновая кислота — антиоксиданты, являющиеся мембраностабилизирующими компонентами. В сочетании с ними противовирусная активность рекомбинантного ИФН альфа-2 возрастает в 10–14 раз, при этом отсутствуют побочные эффекты (повышение температуры тела, лихорадка, гриппоподобные явления, психогенная депрессия), возникающие при парентеральном введении препаратов других природных и рекомбинантных ИФН. Ректальное введение Виферона и комбинация с антиоксидантами, по-видимому, обеспечивают эти позитивные эффекты, также как и быструю высокую концентрацию и длительную циркуляцию в крови ИФН альфа-2. Следующим позитивным моментом является установленный факт: при применении Виферона в течение двух лет не выявлены антитела, нейтрализующие противовирусную активность рекомбинантного ИФН альфа-2. Особенности лекарственной формы Виферона — мазь, гель, ректальные суппозитории в различных дозах создают возможность проведения локальной и системной интерферонотерапии.
Нами разработаны основные принципы дифференцированной терапии Вифероном при вторичных ВИД с синдромом повторных ОРВИ, т. е. для детей ЧДБ (Нестерова И. В., 2003; 2005; 2007):
Ниже приведена разработанная нами ранее программа терапии Вифероном для детей ЧДБ с повторными ОРВИ:
Общая продолжительность курса 2,5–3,5 месяца.
NB! При необходимости (значительное снижение уровней индуцированного ИФН альфа!) начальная доза Виферона может увеличиваться в 1,5–2 раза, а курс лечения продлеваться до достижения позитивного клинического эффекта.
Использование описанных выше подходов в лечении детей ЧДБ позволяет получать позитивные результаты, которые можно видеть при оценке клинической эффективности лечения: значительно снижается количество ОРВИ с 10–18 в году до 2–3 в году, сокращается число бактериальных осложнений в 4–6 раз, ускоряется выход в клиническую ремиссию в 6–8 раз, длительность ремиссии увеличивается в 8–10 раз, с 7–10 дней до 100–150 дней, повышается качество жизни детей. Положительные клинические эффекты сопровождаются позитивной динамикой со стороны системы ИФН и иммунной системы.
Таким образом, дети из группы ЧДБ, страдающие повторными («упорно-рецидивирующими») ОРВИ, упорно-рецидивирующими вирусно-бактериальными инфекциями респираторного тракта и ЛОР-органов, в ряде случаев иммунокомпрометированы — имеют серьезные нарушения в иммунной системе по типу ВИД и в системе ИФН. Они нуждаются в проведении адекватной пролонгированной интерфероно- и позитивной направленной иммунотерапии, которые должны органично включаться в программы иммунореабилитации и сопровождаться обязательным мониторированием иммунного статуса и системы ИФН. Описанная выше тактика интерфероно- и иммунотерапии позволяет достигать положительных клинико-иммунологических эффектов: более легкого течения заболеваний в остром периоде, сокращения периода острых проявлений, значительного удлинения периода ремиссии, уменьшения количества бактериальных осложнений на фоне восстановления функционирования иммунной системы и системы ИФН.
И. В. Нестерова, доктор медицинских наук, профессор
Учебно-научный медицинский центр Управления делами Президента РФ, Москва
Таблица
Дефекты противовирусного иммунитета у ЧДБ детей (частота встречаемости в %)
Как не допустить осложнений при ОРВИ
Как нам уже известно, лечение ОРВИ заключается только в снятии симптомов, причиняющих дискомфорт ребенку (устранение высокой температуры тела, заложенности носа и др.). Однако, используя этот необходимый минимум, многие родители становятся обеспокоены вопросом: «А все ли они сделали правильно? Вдруг этого недостаточно, и у малыша возникнут осложнения?».
И если по какой-то причине у ребенка все-таки развиваются осложнения, крайним остается врач, не назначивший десятки лекарственных препаратов. На самом деле, риск появления осложнений одинаковый как у детей, которых «не лечили», так и у детей, которых «залечили». Постараемся со всем этим разобраться.
Основные причины бактериальных осложнений
Существует 2 основные причины развития осложнений:
Первая – это сама бактерия, проникшая в детский организм и вызвавшая в нем различные заболевания (отиты, синуситы, пневмонии и т.д.).
Вторая – если изначально ребенок заразился не бактериальной инфекцией, а вирусной, но после этого у него возникло бактериальное осложнение. Причина явления до конца не изучена.
При частых рецидивах бактериальных инфекций необходимо показать ребенка врачу-иммунологу. Рассмотрим основные показания для консультации специалиста:
1. Наличие в семейном анамнезе первичных иммунодефицитов.
2. Более 3 случаев катаральных отитов или более одного гнойного отита у ребенка за год.
3. Наличие более одного тяжелого синусита за год.
4. Более одного случая заболевания пневмонией за год.
5. Незначительный эффект от приема антибиотиков (при курсе в 2 и более месяцев терапии).
6. Наличие осложнений после проведения вакцинации ослабленными живыми вакцинами.
7. Недостаточная прибавка ребенка в росте и весе.
8. Наличие рецидивирующих глубоких абсцессов кожи и мягких тканей.
9. Более одной перенесенной тяжелой инфекции за год (менингита, сепсиса, остеомиелита и др.).
10. Наличие молочницы в ротовой полости, грибковой инфекции на коже.
11. Необходимость во внутривенном введении антибиотиков для борьбы с инфекцией.
12. Рецидивы системных инфекций, вызванных типичными микобактериями (например, туберкулеза).
Распространенные заблуждения
Существует популярное заблуждение о том, что сопли могут «опуститься» и вызвать бронхит. Миф возникает в том случае, когда у ребенка с насморком через какое-то время дополнительно появляется кашель. На самом деле все просто: вирус мог поразить не только слизистую носа, но и эпителий бронхов, а проявления воспалительного процесса в бронхах возникли позже насморка. То, что происходит в легких, не имеет никакого отношения к соплям.
Не менее известный миф – от промывания носа может возникнуть отит. На сегодняшний момент известно, что «намыть» отит при промывании невозможно. У детей чаще возникают отиты, чем у взрослых по причине анатомических особенностей строения носоглотки: частого наличия гипертрофии (увеличения) аденоидов, а также короткой, широкой и горизонтально расположенной евстахиевой трубы.
Некоторые люди при промывании носа ощущают недолговременные неприятные ощущения в ушах. Связано это не с развитием отита, а с неправильной техникой промывания. Процедура должна проводиться с наклоном головы вперед и вбок. Доказано, что дети, страдающие частыми рецидивами отитов, при регулярном промывании носа значительно снижали частоту возникновения патологии.
Как избежать осложнений?
Вначале рассмотрим мероприятия, НЕ спасающие ребенка от осложнений при ОРВИ:
Минимизировать риски развития осложнений помогут своевременная вакцинация, ведение активного образа жизни (ежедневные прогулки, закаливание организма, занятие спортом), правильное сбалансированное питание, отказ родителей ребенка и его близкого окружения от курения.