Митохондриальная дисфункция что это у взрослых
Митохондриальная миопатия
Митохондриальные миопатии — это группа заболеваний мышц, которые возникают в результате нарушения функции тканевого дыхания при патологиях митохондрий. Болезни проявляются нарастающей мышечной слабостью, атрофией мускулатуры, прогрессирующими двигательными расстройствами, которые могут сопровождаться судорогами, поражениями сердца, ухудшением слуха и зрения. Диагностика предполагает лабораторные (исследование мышечных биоптатов, генетическое тестирование, биохимические анализы), инструментальные методы (ЭМГ, церебральное МР-сканирование). Лечение включает симптоматические препараты, физиотерапию, ЛФК.
МКБ-10
Общие сведения
Термин «митохондриальная миопатия» объединяет в себе несколько патологий со сходным патогенезом. Наиболее часто дети страдают синдромами MELAS, MERRF, синдромом Кернса-Сайра с хронической прогрессирующей наружной офтальмоплегией. Изучение молекулярно-генетических особенностей этих болезней началось в 1980-х гг. Распространенность патологий у детей составляет около 11,5 случая на 100 тыс. населения. Из-за мультисистемности поражения, клинического полиморфизма, вариабельности течения этот вид миопатии представляет серьезные трудности в диагностике.
Причины
Миопатии обусловлены наследственными либо спорадическими мутациями в митохондриальной ДНК или в ядерных генах, контролирующих работу митохондрий. Известно более 300 вариантов генных дефектов — однонуклеотидных замен, делеций, вызывающих нарушения функционирования митохондрий. Митохондриальные миопатии имеют ряд генетических аспектов, выделяющих их среди всех наследственных заболеваний. Принципиальные различия:
Патогенез
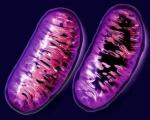
Митохондрия — универсальная органелла, присутствующая во всех клетках, кроме эритроцитов. Она имеет дыхательную цепь, которая включает 5 ферментных комплексов из нескольких десятков субъединиц каждый. Ферменты обеспечивают окислительное фосфорилирование для синтеза АТФ — аденозинтрифосфата, выступающего основным источником энергии в организме.
При митохондриальных заболеваниях может быть 4 варианта патогенетических механизмов развития. Как правило, при поражениях мышц наблюдаются дефекты электронного транспорта и окислительного фосфорилирования, что сопровождается нарушениями образования энергетических молекул. Другие варианты расстройств включают нарушения обмена пирувата, дефекты метаболизма жирных кислот, дисфункцию цикла Кребса.
При миопатиях отмечаются полисистемные расстройства. Мышечная и нервная ткань, больше других зависимые от энергопроизводства, страдают в первую очередь. Поражение проявляется нарушениями обмена веществ в мышцах, дегенеративными процессами, атрофией миофибрилл и их замещением соединительной тканью. Со временем патологический процесс распространяется на сердечную мышцу, эндокринную систему, почки и печень, что определяет различные «маски» миопатии.
Симптомы митохондриальной миопатии
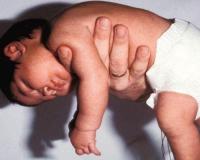
Патологии манифестируют у детей раннего возраста, иногда они присутствуют с рождения. Общим признаком является миопатический синдром, который включает прогрессирующую мышечную слабость, снижение тонуса скелетной мускулатуры, непереносимость физических нагрузок. Типично отставание в моторном развитии: дети поздно начинают сидеть, ползать, ходить, у них сохраняется неуклюжесть движений, проблемы с поддержанием равновесия.
Клинические особенности определяются типом заболевания. При синдроме MERRF мышечная слабость сопровождается разнообразными судорожными приступами (атоническими, тонико-клоническими, миоклоническими), расстройствами координации вследствие мозжечковой атаксии. Для синдрома MELAS характерны повторные инсульты, умственная отсталость, нейросенсорная тугоухость.
У детей распространен синдром Кернса-Сайра, при котором клинические признаки дополняются расстройствами глотания, нарушениями работы проводящей системы сердца, снижением слуха. Хроническая прогрессирующая наружная офтальмопатия может возникать как компонент болезни Кернса-Сайра, так и развиваться изолированно, что чаще бывает в старшем возрасте.
Осложнения
Отличительными особенностями миопатического синдрома являются необратимость, неуклонное прогрессирование. Сначала мышечная слабость появляется в проксимальных отделах конечностей, затем поражает все тело ребенка: в процесс вовлекается гладкая мускулатура органов дыхания и пищеварения, что чревато дыхательной недостаточностью, аспирационными пневмониями, тотальным параличом. Такие пациенты теряют способность к самообслуживанию, требуют круглосуточного ухода.
Миопатии осложняются деформациями позвоночника, искривлениями нижних конечностей на фоне слабости мышечного корсета. Вследствие атрофии зрительных нервов у больных с синдромом MERRF возникает слепота. Опасным последствием многих вариантов митохондриальной патологии являются инсульты, эпилептический статус, мозговой отек, которые становятся основными причинами летального исхода.
Диагностика
Первичное обследование детей с подозрением на митохондриальную миопатию проводится у невролога, для уточнения диагноза показана консультация генетика. При осмотре учитывается неврологический статус ребенка, показатели мышечной силы и тонуса, уровень развития когнитивных навыков. Постановка диагноза требует комплексного обследования, включающего следующие методы:
Лечение митохондриальных миопатий
В клинической неврологии отсутствуют эффективные методы терапии патологии у детей. Суть медицинской помощи сводится к уменьшению моторного дефицита, своевременной коррекции осложнений, стимуляции обменных процессов в митохондриях. Наибольшую результативность демонстрируют следующие группы медикаментов:
Важным компонентом лечения у детей является нейродиетология, которая предполагает исключение веществ, оказывающих негативное влияние на обменные процессы (терапия «обхождения блока»). Рекомендована кетогенная диета, другие виды высокожировых диет. По показаниям проводится лечебное энтеральное или парентеральное питание, в тяжелых случаях устанавливается гастростома.
Прогноз и профилактика
Митохондриальная дисфункция что это у взрослых
Митохондриальные миопатии — это группа заболеваний мышц, которые возникают в результате нарушения функции тканевого дыхания при патологиях митохондрий. Болезни проявляются нарастающей мышечной слабостью, атрофией мускулатуры, прогрессирующими двигательными расстройствами, которые могут сопровождаться судорогами, поражениями сердца, ухудшением слуха и зрения. Диагностика предполагает лабораторные (исследование мышечных биоптатов, генетическое тестирование, биохимические анализы), инструментальные методы (ЭМГ, церебральное МР-сканирование). Лечение включает симптоматические препараты, физиотерапию, ЛФК.
МКБ-10
Общие сведения
Термин «митохондриальная миопатия» объединяет в себе несколько патологий со сходным патогенезом. Наиболее часто дети страдают синдромами MELAS, MERRF, синдромом Кернса-Сайра с хронической прогрессирующей наружной офтальмоплегией. Изучение молекулярно-генетических особенностей этих болезней началось в 1980-х гг. Распространенность патологий у детей составляет около 11,5 случая на 100 тыс. населения. Из-за мультисистемности поражения, клинического полиморфизма, вариабельности течения этот вид миопатии представляет серьезные трудности в диагностике.

Причины
Миопатии обусловлены наследственными либо спорадическими мутациями в митохондриальной ДНК или в ядерных генах, контролирующих работу митохондрий. Известно более 300 вариантов генных дефектов — однонуклеотидных замен, делеций, вызывающих нарушения функционирования митохондрий. Митохондриальные миопатии имеют ряд генетических аспектов, выделяющих их среди всех наследственных заболеваний. Принципиальные различия:
Патогенез
Митохондрия — универсальная органелла, присутствующая во всех клетках, кроме эритроцитов. Она имеет дыхательную цепь, которая включает 5 ферментных комплексов из нескольких десятков субъединиц каждый. Ферменты обеспечивают окислительное фосфорилирование для синтеза АТФ — аденозинтрифосфата, выступающего основным источником энергии в организме.
При митохондриальных заболеваниях может быть 4 варианта патогенетических механизмов развития. Как правило, при поражениях мышц наблюдаются дефекты электронного транспорта и окислительного фосфорилирования, что сопровождается нарушениями образования энергетических молекул. Другие варианты расстройств включают нарушения обмена пирувата, дефекты метаболизма жирных кислот, дисфункцию цикла Кребса.
При миопатиях отмечаются полисистемные расстройства. Мышечная и нервная ткань, больше других зависимые от энергопроизводства, страдают в первую очередь. Поражение проявляется нарушениями обмена веществ в мышцах, дегенеративными процессами, атрофией миофибрилл и их замещением соединительной тканью. Со временем патологический процесс распространяется на сердечную мышцу, эндокринную систему, почки и печень, что определяет различные «маски» миопатии.
Симптомы митохондриальной миопатии
Патологии манифестируют у детей раннего возраста, иногда они присутствуют с рождения. Общим признаком является миопатический синдром, который включает прогрессирующую мышечную слабость, снижение тонуса скелетной мускулатуры, непереносимость физических нагрузок. Типично отставание в моторном развитии: дети поздно начинают сидеть, ползать, ходить, у них сохраняется неуклюжесть движений, проблемы с поддержанием равновесия.
Клинические особенности определяются типом заболевания. При синдроме MERRF мышечная слабость сопровождается разнообразными судорожными приступами (атоническими, тонико-клоническими, миоклоническими), расстройствами координации вследствие мозжечковой атаксии. Для синдрома MELAS характерны повторные инсульты, умственная отсталость, нейросенсорная тугоухость.
У детей распространен синдром Кернса-Сайра, при котором клинические признаки дополняются расстройствами глотания, нарушениями работы проводящей системы сердца, снижением слуха. Хроническая прогрессирующая наружная офтальмопатия может возникать как компонент болезни Кернса-Сайра, так и развиваться изолированно, что чаще бывает в старшем возрасте.
Осложнения
Отличительными особенностями миопатического синдрома являются необратимость, неуклонное прогрессирование. Сначала мышечная слабость появляется в проксимальных отделах конечностей, затем поражает все тело ребенка: в процесс вовлекается гладкая мускулатура органов дыхания и пищеварения, что чревато дыхательной недостаточностью, аспирационными пневмониями, тотальным параличом. Такие пациенты теряют способность к самообслуживанию, требуют круглосуточного ухода.
Миопатии осложняются деформациями позвоночника, искривлениями нижних конечностей на фоне слабости мышечного корсета. Вследствие атрофии зрительных нервов у больных с синдромом MERRF возникает слепота. Опасным последствием многих вариантов митохондриальной патологии являются инсульты, эпилептический статус, мозговой отек, которые становятся основными причинами летального исхода.
Диагностика
Первичное обследование детей с подозрением на митохондриальную миопатию проводится у невролога, для уточнения диагноза показана консультация генетика. При осмотре учитывается неврологический статус ребенка, показатели мышечной силы и тонуса, уровень развития когнитивных навыков. Постановка диагноза требует комплексного обследования, включающего следующие методы:
Лечение митохондриальных миопатий
В клинической неврологии отсутствуют эффективные методы терапии патологии у детей. Суть медицинской помощи сводится к уменьшению моторного дефицита, своевременной коррекции осложнений, стимуляции обменных процессов в митохондриях. Наибольшую результативность демонстрируют следующие группы медикаментов:
Важным компонентом лечения у детей является нейродиетология, которая предполагает исключение веществ, оказывающих негативное влияние на обменные процессы (терапия «обхождения блока»). Рекомендована кетогенная диета, другие виды высокожировых диет. По показаниям проводится лечебное энтеральное или парентеральное питание, в тяжелых случаях устанавливается гастростома.
Прогноз и профилактика
Вы можете поделиться своей историей болезни, что Вам помогло при лечении митохондриальной миопатии.
1. Митохондриальные болезни: миопатии, энцефаломиопатии и энцефаломиелополиневропатии/ В.М. Казаков, А.А. Скоромец, Д.И. Руденко, Т.Р. Стучевская// Неврологический журнал. — 201 — №
2. Митохондриальная патология у детей/ В.М. Студеникин, О.В. Глоба// Лечащий врач. — 201 — №
3. Влияние дисфункции митохондрий на клинические проявления наследственных миопатий/ Д.А. Харламов, В.С. Сухоруков// Российский вестник перинатологии и педиатрии. — 201 — №
4. Митохондриальные миопатии в сочетании с кардиомиопатией. Новые подходы к лечению/ О.С. Страхова, Ю.М. Белозеров, С.В. Перминов, В.В. Давыдкин// Альманах клинической медицины. — 200 — №
Митохондриальная дисфункция при метаболическом синдроме
В основе морфологических, биохимических и функциональных изменений при жировой болезни (ЖБП) печени лежат гиперпродукция свободных жирных кислот (СЖК), увеличение их поступления в печень, а также гиперактивация свободнорадикального окисления (СРО). На фоне усиления СРО возрастает интенсивность перекисного окисления липидов (ПОЛ). Избыточное отложение жира в гепатоцитах приводит к развитию жировой дистрофии. Гиперпродукция и окисление СЖК в митохондриях способствуют образованию свободных радикалов, которые подавляют выработку клеточных антиоксидантов. Следствием этого становятся окислительный стресс и клеточный энергодефицит.
Таким образом, при ЖБП избыточный пул свободных радикалов способствует повреждению сначала митохондриальных структур, затем клеточных мембран в целом, гибели клетки путем некроза или быстрой инициации апоптоза. Все это приводит к достаточно выраженному фибротическому повреждению органа, усугубляя гипоксию.
Тем временем активация свободнорадикальных процессов продолжается. В результате избытка СЖК, поступающих в печень в большом количестве, в частности, из жировой ткани, развиваются гипоксические изменения, усиливается тканевая гипоксия и митохондриальная дисфункция, гиперактивация СРО.
Данные процессы инициируются прежде всего за счет гипоксии, а не нарушения кровоснабжения и микроциркуляции в печени, поскольку в момент, когда включаются компенсаторные механизмы активации энергопродукции, запускается и продукция избыточного количества радикалов. Учитывая, что при ЖБП клетка существует в условиях энергодефицита, продукции естественных антиоксидантных систем не хватает для нейтрализации процесса. Начинается прогрессивное поражение печени с повреждением ее митохондрий.
Многие специалисты рассматривают гипоксию как один из ведущих факторов, влияющих на развитие ЖБП, поскольку при ЖБП промежуточным звеном между избыточным поступлением СЖК и развитием окислительного стресса является тканевая гипоксия. Именно гипоксические явления, сопряженные с дефицитом аденозинтрифосфата и нарушением митохондриального окисления, приводят к активации СРО, роль которого в патогенезе заболеваний печени сегодня хорошо известна. При этом во всех тканях происходят изменения вследствие индукции факторов, защищающих клетку от гипоксии.
Важнейшую роль при тканевой гипоксии играет кислородчувствительный протеиновый комплекс – гипоксия-индуцибельный фактор, который активируется в местах регуляции кислородных путей и обеспечивает быстрый ответ на гипоксию. Но этот же фактор будет отвечать и за неоплазию гепатоцита.
Факторы развития ЖБП усиливаются под действием митохондриальной дисфункции с нарушением митохондриального окислительного фосфорилирования, повреждением эндоплазматического ретикулума, изменением генной активности, в том числе генов, отвечающих за глюконеогенез, транспорт глюкозы, с одновременным увеличением синтеза провоспалительных цитокинов и нарушением в итоге углеводного и липидного обмена.
Гипоксия, независимо от типа (тканевая или интермиттирующая), приводит к появлению состояний, характерных для метаболического синдрома: инсулинорезистентности, нарушению функции жировой ткани, сердца, эндотелиальной дисфункции.
Развитие жировой дистрофии у пациентов с вирусными гепатитами, в том числе не употребляющих алкоголь, также тесно связано с митохондриальной дисфункцией. Место первичной репликации вируса гепатита C – митохондрии гепатоцитов. Он может вызвать митохондриальную дисфункцию, что повышает риск развития печеночной недостаточности, фиброзирования. На фоне митохондриальной дисфункции усугубляются стеатоз, инсулинорезистентность, апоптоз, фиброз печени.
Перицеллюлярный фиброз у пациентов, имеющих гипоксические эпизоды, – необратимый фактор. Формируется перицеллюлярный фиброз с нарушением обменных процессов между клетками, образованием цирротических изменений и нарушением кровоснабжения с ухудшением микроциркуляции. Это приводит к развитию тяжелых осложнений и развитию перманентной гипоксии, которая будет сопровождаться неконтролируемым ростом СРО и в итоге спровоцирует гибель органа.
При гипоксии, развивающейся в случае ЖБП и фиброза, в клетке в первую очередь наступают изменения в митохондриях, за исключением жировых вакуолей, формирующихся еще ранее. Количество митохондрий не сопровождается увеличением плотности их внутренних мембран. При ЖБП и фиброзе возрастает объем митохондрий. Образуются гигантские митохондрии, заполняющие большую площадь клетки, но продуцирующие энергии меньше, чем совокупность неизмененных митохондрий в нормальной клетке. Развивается тяжелый энергодефицит.
Этиологические факторы возникновения митохондриальной дисфункции разнообразны: нарушение бета-окисления, прием лекарственных средств и алкоголя, действие вирусных агентов и др.
Активация сукцинат-оксидазного окисления в условиях гипоксии способствует коррекции физиологических процессов в клетке на уровне митохондрий – нормализует электрон-транспортную функцию дыхательной цепи, активирует ферменты. Это ненадолго облегчает поступление кислорода в клетку и восстанавливает аэробный энергетический обмен. Между тем активация сукцинат-оксидазного окисления не может длиться бесконечно, поскольку является временным компенсаторным механизмом.
В условиях дефицита антиоксидантного субстрата, активной работы цитохромов, которые начинают окислять избыток жирных кислот, усиливается процесс пероксидации. Возрастание активности провоспалительных ферментов и других факторов приводит к поддержанию и развитию воспалительного процесса.
В настоящее время ученые рассматривают подходы к компенсации митохондриальных нарушений с помощью методов биомедицины.
При традиционном способе коррекции митохондриальных нарушений при гипоксии современная медицина использует вещества, способные защитить клетку от гипоксии.
Сукцинатсодержащие препараты обладают антигипоксантным, антиоксидантным, мембраностабилизирующим и детоксицирующим действием. Экзогенно вводимый сукцинат (янтарная кислота) при гипоксии поддерживает активность сукцинатдегидрогеназного звена – ФАД-зависимого звена цикла Кребса, менее чувствительного к гипоксии по сравнению с НАД-зависимыми оксидазами. Окисление сукцината наиболее устойчиво к оксидативному повреждению. Это позволяет определенное время поддерживать энергопродукцию в клетке при наличии в митохондриях субстрата окисления, в данном звене – сукцината. Таким образом, превращение янтарной кислоты в организме связано с производством энергии, необходимой для обеспечения жизнедеятельности. Благодаря уникальным свойствам янтарная кислота считается универсальным гепатотропным препаратом для применения при различных поражениях печени как в лечебных, так и в лечебно-профилактических целях.
Сегодня на фармацевтическом рынке представлен отечественный препарат Ремаксол (компания-производитель «ПОЛИСАН»). Это не только сбалансированный полиионный инфузионный раствор. В его состав входят также физиологически активные компоненты – янтарная кислота, метионин, инозин и никотинамид. Препарат Ремаксол не только оказывает гепатопротекторный эффект, но и улучшает энергетическое обеспечение гепатоцитов, повышает устойчивость мембран гепатоцитов к ПОЛ, восстанавливает активность ферментов антиоксидантной защиты.
Эффективность применения препарата Ремаксол в терапии ЖБП обусловлена воздействием на основные механизмы развития повреждения печени, что позволяет корригировать митохондриальную дисфункцию, повреждение мембран гепатоцитов и окислительный стресс. Препарат Ремаксол может быть использован как средство инициальной терапии в рамках патогенетеческого лечения, а также при невозможности элиминации этиологического фактора. Указанные гепатопротекторные свойства Ремаксола делают его перспективным в лечении нарушений функции печени.
Митохондриальная дисфункция что это у взрослых
— органеллы, которые находятся в каждой клетке нашего организма (кроме зрелых эритроцитов) и отвечают за производство энергии. Эти органеллы стали частью клетки около 2 млрд лет назад, когда археи установили симбиотические взаимоотношения с альфа-протеобактериями. Поэтому митохондрии — полуавтономные органеллы, так как они имеют собственный наследственный материал в виде кольцевой молекулы ДНК и окружены двумя мембранами.
Роль митохондрий в клетке не сводится к созданию АТФ («энергетической валюты» клетки) в процессе окислительного фосфорилирования, протекающего на внутренней мембране. Они — ключевые игроки в жизни и смерти клетки.
— это комплекс мероприятий, направленных на улучшение митохондриальной функции не только при МХ заболеваниях, но и при возраст-зависимых заболеваниях.
Термин «митохондриальная медицина» возник изначально в связи с наследственными митохондриальными заболеваниями. Сейчас понятие этого термина расширилось и на возрастную дисфункцию митохондрий.
В клетке находится большое количество митохондрий, только часть из которых могут быть дисфункциональными. Для того чтобы в клетке нарушилась митохондриальная функция, количество «больных» митохондрий должно преодолеть некоторую пороговую черту.
Считается, что для нарушения работы клетки (ткани) «нерабочими» должно быть около 60-80% митохондрий. До этого накопление дисфункциональных митохондрий остается бессимптомным, а значит, окно возможностей терапии сужается.
Между тем, маркеры для диагностики митохондриальной дисфункции существуют — есть ряд маркеров-кандидатов. Разрабатываются новые методики для диагностики работы митохондрий.
Все существующие и потенциальные маркеры диагностики митохондриальной дисфункции можно подразделить на группы.
Косвенно свидетельствует о нарушении работы дыхательной цепи. К этой группе методов относятся методики, входящие в гайдлайны диагностики митохондриальных заболеваний (ref), — определение уровня лактата, пирувата, их соотношения; количественное определение аминокислот, органических кислот и ацилкарнитинов), измерение ферментов — креатинкиназы, цитрат-синтазы, сукцинат-дегидрогеназы, цитрохром-с-оксидазы.
Данные методы достаточно удобны, однако, обладают невысокой специфичностью.
Также к этой группе методов относятся более новые подходы: метаболомика, определение сывороточных цитокинов и микроРНК.
Важная группа маркеров, так как нарушение генетического аппарата митохондрий является не только следствием нарушения работы митохондрий, но и причиной их дисфункции. Показано возраст-зависимое накопление генетических нарушений митохондрий. Для некоторых субстратов показана хорошая корреляция с возрастом.
К этой группе методов относят определение количества мтДНК, точечных мутаций, частой делеции (del4977bp)и других делеций, количества внеклеточной мтДНК и метилирования мтДНК.
Количество мтДНК является важным маркером. В статье Nature (2018) использовали линию мышей со встроенной генной конструкцией. У них можно было «включать» истощение мтДНК и «выключать», после чего количество мтДНК восстанавливалось. У мышек при истощении мтДНК наблюдались все внешние признаки старения, — морщинистость кожи и облысение. При этом восстановление мтДНК полностью обращало данные изменения. Помимо этого, возрастные изменения иммунитета сопровождаются снижением активации увеличения копий мтДНК при активации Т-клеток, что показано в работе, сравнивающей иммунный ответ у молодых, пожилых и здоровых долгожителей (O’Hara, 2019). Восстановление копий мтДНК замедляло старение сосудов у мышей по показателям снижения эластичности сонной артерии, скорости пульсовой волны в аорте, содержанию эластина и коллагена (Foote K., 2018).
Частая делеция (4977 bp) является является еще одним интересным генетическим биомаркером, так как ее уровень с возрастом растет, а в митохондрии с делецией не могут функционировать. Накопление этой делеции происходит в тканях с низкой пролиферативной активностью (скелетные мышцы, мозг, сердце), криминалисты используют этот маркер в своей работе для определения возраста (Meissner, 1997), она обнаруживается в коже при фотостарении и даже в волосах. У мышей есть свой аналог частой делеции митохондрий. Этому генетическому повреждению митохондрий посвящена целая теория старения (Dun-XianTan, 2019). Согласно ей, нарастающий уровень врожденного иммунитета направляет свою активность на митохондрии, являющиеся, в некоторой мере, чужеродными агентами. А митохондрии с делецией в этом случае получают селективное преимущество, хотя и являются дисфункциональными.
Часто используется спортсментами, включают оценку аэробной способности митохондрий при помощи физиологии упражнений по показателям: максимальное потребление кислорода (МПК), артерио-венозная разница содержания кислорода. Может также сопровождаться инвазивным измерением различных биомаркеров в крови на различных этапах физической нагрузки.
Метод может использоваться и как подтверждение дисфункции, и как метод терапии, и как метод оценки эффективности терапии. Он является неинвазивным, доступным и чувствительным, хотя и требует специального оборудования и не всегда подходит для всех возрастных групп.