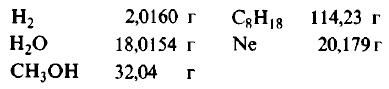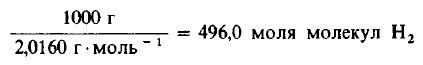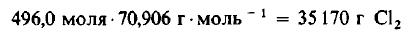Моль это единица чего
Урок 5. Моль и молярная масса
В уроке 5 «Моль и молярная масса» из курса «Химия для чайников» рассмотрим моль как единицу измерения количества вещества; дадим определение числу Авогадро, а также научимся определять молярную массу и решать задачи на количество вещества. Базой для данного урока послужат основы химии, изложенные в прошлых уроках, так что если вы изучаете химию с нуля, то рекомендую их просмотреть хотя бы мельком.
Единица измерения количества вещества
До этого урока мы обсуждали лишь индивидуальные молекулы и атомы, а их массы мы выражали в атомных единицах массы. В реальной жизни с индивидуальными молекулами работать невозможно, потому что они ничтожно малы. Для этого химики взвешивают вещества ни в а.е.м., а в граммах.
Чтобы перейти от молекулярной шкалы измерения масс в лабораторную шкалу, используют единицу измерения количества вещества под названием моль. 1 моль содержит 6,022·10 23 частиц (атомов или молекул) и является безразмерной величиной. Число 6,022·10 23 носит название Число Авогадро, которое определяется как число частиц, содержащихся в 12 г атомов углерода 12 C. Важно понимать, что 1 моль любого вещества содержит всегда одно и то же число частиц (6,022·10 23 ).
Молярная масса вещества
Молярная масса – это масса 1 моля вещества, выраженная в граммах. Молярную массу одного моля любого химического элемента без труда находят из таблицы Менделеева, так как молярная масса численно равна атомной массе, но размерности у них разные (молярная масса имеет размерность г/моль). Запишите и запомните формулы для вычисления молярной массы, количества вещества и числа молекул:
где m — масса вещества, n — количество вещества (число молей), М — молярная масса, N — число молекул, NA — число Авогадро. Благодаря молярной массе вещества химики могут вести подсчет атомов и молекул в лаборатории просто путем их взвешивания. Этим и удобно использование понятия моль.
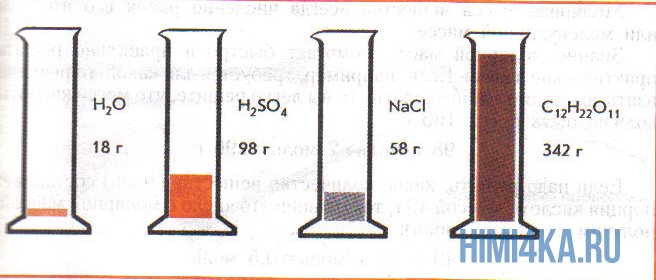
На рисунке изображены четыре колбы с различными веществами, но в каждой из них всего 1 моль вещества. Можете перепроверить, используя формулы выше.
Задачи на количество вещества
Пример 1. Сколько граммов Н2, Н2O, СН3ОН, октана (С8Н18) и газа неона (Ne) содержится в 1 моле?
Решение: Молекулярные массы (в атомных единицах массы) перечисленных веществ приведены в таблице Менделеева. 1 моль каждого из названных веществ имеет следующую массу:
Поскольку массы, указанные в решении примера 1, дают правильные относительные массы взвешиваемых молекул, указанная масса каждого из перечисленных веществ содержит одинаковое число молекул. Этим и удобно использование понятия моля. Нет даже необходимости знать, чему равно численное значение моля, хотя мы уже знаем, что оно составляет 6,022·10 23 ; эта величина называется числом Авогадро и обозначается символом NA. Переход от индивидуальных молекул к молям означает увеличение шкалы измерения в 6,022·10 23 раз. Число Авогадро представляет собой также множитель перевода атомных единиц массы в граммы: 1 г = 6,022·10 23 а.е.м. Если мы понимаем под молекулярной массой массу моля вещества, то ее следует измерять в граммах на моль; если же мы действительно имеем в виду массу одной молекулы, то она численно совпадает
с молекулярной массой вещества, но выражается в атомных единицах массы на одну молекулу. Оба способа выражения молекулярной массы правильны.
Пример 2. Сколько молей составляют и сколько молекул содержат 8 г газообразного кислорода O2?
Решение: Выписываем из таблицы Менделеева атомную массу атома кислорода (O), которая равна 15,99 а.е.м, округляем до 16. Так как у нас молекула кислорода, состоящая из двух атомов O, то ее атомная масса равна 16×2=32 а.е.м. Хорошо, а теперь переводим ее в молярную массу: 32 а.е.м = 32 г/моль. Это означает, что 1 моль (6,022·10 23 молекул) O2 имеет массу 32 грамма. Ну и в заключении по формулам выше находим количество вещества (моль) и число молекул, содержащихся в 8 граммах O2:
Пример 3. 1 молекула Н2 реагирует с 1 молекулой Сl2, в результате чего образуются 2 молекулы газообразного хлористого водорода НСl. Какую массу газообразного хлора необходимо использовать, чтобы он полностью прореагировал с 1 килограммом (кг) газообразного водорода?
Решение: Молекулярные массы H2 и Cl2 равны 2,0160 и 70,906 г/моль соответственно. Следовательно, в 1000 г H2 содержится
Даже не выясняя, сколько молекул содержится в одном моле вещества, мы можем быть уверены, что 496 моля Cl2 содержат такое же число молекул, как и 496,0 моля, или 1000 г, H2. Сколько же граммов Cl2 содержится в 496 молях этого вещества? Поскольку молекулярная масса Cl2 равна 70,906 г/моль, то
Пример 4. Сколько молекул H2 и Cl2 принимает участие в реакции, описанной в примере 3?
Решение: В 496 молях любого вещества должно содержаться 496 моля × 6,022·10 23 молекул/моль, что равно 2,99·10 26 молекул.
Чтобы наглядно показать, сколь велико число Авогадро, приведем такой пример: 1 моль кокосовых орехов каждый диаметром 14 сантиметров (см) мог бы заполнить такой объем, какой занимает наша планета Земля. Использование молей в химических расчетах рассматривается в следующей главе, но представление об этом пришлось ввести уже здесь, поскольку нам необходимо знать, как осуществляется переход от молекулярной шкалы измерения масс к лабораторной шкале.
Надеюсь урок 5 «Моль и молярная масса» был познавательным и понятным. Если у вас возникли вопросы, пишите их в комментарии.
Моль (единица)
Моль (обозначение — моль, mol) — единица измерения количества вещества. Соответствует количеству вещества, содержащему столько специфицированных структурных единиц (атомов, молекул, ионов, электронов или любых других частиц), сколько содержится атомов в 12 граммах нуклида углерода 12 C.
Количество частиц в одном моле любого вещества постоянно и носит название числа Авогадро (NA).
Кратные и дольные единицы
Десятичные кратные и дольные единицы образуют с помощью стандартных приставок СИ.
| Кратные | Дольные | ||||||
|---|---|---|---|---|---|---|---|
| величина | название | обозначение | величина | название | обозначение | ||
| 10 1 моль | декамоль | дамоль | damol | 10 −1 моль | децимоль | дмоль | dmol |
| 10 2 моль | гектомоль | гмоль | hmol | 10 −2 моль | сантимоль | смоль | cmol |
| 10 3 моль | киломоль | кмоль | kmol | 10 −3 моль | миллимоль | ммоль | mmol |
| 10 6 моль | мегамоль | Ммоль | Mmol | 10 −6 моль | микромоль | мкмоль | µmol |
| 10 9 моль | гигамоль | Гмоль | Gmol | 10 −9 моль | наномоль | нмоль | nmol |
| 10 12 моль | терамоль | Тмоль | Tmol | 10 −12 моль | пикомоль | пмоль | pmol |
| 10 15 моль | петамоль | Пмоль | Pmol | 10 −15 моль | фемтомоль | фмоль | fmol |
| 10 18 моль | эксамоль | Эмоль | Emol | 10 −18 моль | аттомоль | амоль | amol |
| 10 21 моль | зеттамоль | Змоль | Zmol | 10 −21 моль | зептомоль | змоль | zmol |
| 10 24 моль | йоттамоль | Имоль | Ymol | 10 −24 моль | йоктомоль | имоль | ymol |
| применять не рекомендуется | |||||||
Примечание: единица измерения йоктомоль может использоваться лишь формально, так как столь малые количества вещества должны измеряться отдельными частицами (1 имоль формально равен 0,602 частицы).
| Единицы СИ |
|---|
| Основные: метр | килограмм | секунда | ампер | кельвин | кандела | моль |
| Производные: радиан | стерадиан | герц | градус Цельсия | катал | ньютон | джоуль | ватт | паскаль | кулон | вольт | ом | сименс | фарад | вебер | тесла | генри | люмен | люкс | беккерель | грэй | зиверт |
Полезное
Смотреть что такое «Моль (единица)» в других словарях:
Моль (единица кол-ва вещ-ва) — Моль, единица количества вещества, т. е. величины, оцениваемой количеством содержащихся в физической системе тождественных структурных элементов (атомов, молекул, ионов и других частиц или их специфических групп). М. равен количеству вещества… … Большая советская энциклопедия
Моль (единица кол-ва вещ-ва) — Эта статья посвящена единице измерения. См. также: насекомые моли. Моль (обозначение моль, mol) единица измерения количества вещества. Соответствует количеству вещества, содержащему столько специфицированных структурных единиц (атомов, молекул,… … Википедия
моль — 1. МОЛЬ, и; ж. Небольшая бабочка, гусеница которой является вредителем шерстяных вещей, хлебных зёрен и растений. 2. МОЛЬ, и; ж.; МОЛЬ, я; м. Спец. Лес, сплавляемый по реке брёвнами, не связанными в плот. По реке плыла м. Пробираться на лодке… … Энциклопедический словарь
Моль (значения) — Моль многозначное слово: Моль единица измерения количества вещества, Моль представитель молей (под названием «моли» объединяют в нетаксономическую группу мелких насекомых из отряда чешуекрылых). Населённые пункты Моль … … Википедия
МОЛЬ — единица количества вещества в СИ, определяемая как количество вещества, содержащее столько же формульных (структурных) единиц этого вещества (атомов, молекул, ионов, электронов и др.), сколько содержится атомов в 12 г изотопа углерода 12 (12С);… … Большая политехническая энциклопедия
МОЛЬ — • МОЛЬ (Mohl) Хуго фон (1805 1872), немецкий ботаник, пионер в исследовании анатомии и физиологии КЛЕТОК растений. Сформулировал гипотезу о том, что ядро клетки окружено гранулированным коллоидным веществом, которое в 1846 г. он назвал… … Научно-технический энциклопедический словарь
МОЛЬ — МОЛЬ, единица количества вещества в СИ. Обозначение моль. В 1 моле содержится столько молекул (атомов, ионов или каких либо других структурных элементов вещества), сколько атомов содержится в 0,012 кг 12С (углерода с атомной массой 12). число… … Современная энциклопедия
МОЛЬ — единица количества вещества СИ, обозначается моль. В 1 моле содержится столько молекул (атомов, ионов или каких либо др. структурных элементов вещества), сколько атомов содержится в 0,012 кг 12С (углерода с атомной массой 12), т. е. 6,022.1023… … Большой Энциклопедический словарь
Моль — МОЛЬ, единица количества вещества в СИ. Обозначение моль. В 1 моле содержится столько молекул (атомов, ионов или каких либо других структурных элементов вещества), сколько атомов содержится в 0,012 кг 12С (углерода с атомной массой 12). Число… … Иллюстрированный энциклопедический словарь
Моль — Эта статья посвящена единице измерения. У слова «Моль» есть и другие значения: см. Моль (значения). Моль (русское обозначение: моль; международное: mol) единица измерения количества вещества в Международной системе единиц (СИ), одна из семи … Википедия
Моль это единица чего
Моль, молярная масса
В химических процессах участвуют мельчайшие частицы – молекулы, атомы, ионы, электроны. Число таких частиц даже в малой порции вещества очень велико. Поэтому, чтобы избежать математических операций с большими числами, для характеристики количества вещества, участвующего в химической реакции, используется специальная единица – моль.
Моль — это такое количество вещества, в котором содержится определенное число частиц (молекул, атомов, ионов), равное постоянной Авогадро
Постоянная Авогадро NA определяется как число атомов, содержащееся в 12 г изотопа 12 С:
Таким образом, 1 моль вещества содержит 6,02 • 10 23 частиц этого вещества.
Исходя из этого, любое количество вещества можно выразить определенным числом молей ν (ню). Например, в образце вещества содержится 12,04 • 10 23 молекул. Следовательно, количество вещества в этом образце составляет:
где N – число частиц данного вещества;
NA – число частиц, которое содержит 1 моль вещества (постоянная Авогадро).
Молярная масса вещества (M) – масса, которую имеет 1 моль данного вещества.
Эта величина, равная отношению массы m вещества к количеству вещества ν, имеет размерность кг/моль или г/моль. Молярная масса, выраженная в г/моль, численно равна относительной относительной молекулярной массе Mr (для веществ атомного строения – относительной атомной массе Ar).
Например, молярная масса метана CH4 определяется следующим образом:
M(CH4)=16 г/моль, т.е. 16 г CH4 содержат 6,02 • 10 23 молекул.
Молярную массу вещества можно вычислить, если известны его масса m и количество (число молей) ν, по формуле:
Соответственно, зная массу и молярную массу вещества, можно рассчитать число его молей:
или найти массу вещества по числу молей и молярной массе:
Необходимо отметить, что значение молярной массы вещества определяется его качественным и количественным составом, т.е. зависит от Mr и Ar. Поэтому разные вещества при одинаковом количестве молей имеют различные массы m.
Пример 
Решение
Молярная масса метана M(CH4) равна 16 г/моль;
молярная масса этана M(С2Н6) = 2 • 12+6=30 г/моль.
Отсюда:
Таким образом, моль – это порция вещества, содержащая одно и то же число частиц, но имеющая разную массу для разных веществ, т.к. частицы вещества (атомы и молекулы) не одинаковы по массе.
Вычисление ν используется практически в каждой расчетной задаче.
Образцы решения задач
Задача №1. Вычислите массу (г) магния, взятого количеством вещества 0, 5 моль?
M (Mg ) = Ar ( Mg ) = 24 г/моль (из периодической системы)
m ( Mg ) = 24 г/моль · 0,5 моль = 12 г
Задача №2. Вычислите массу (г) 12,04 · 10 23 молекул оксида цинка Zn О ?
n (Zn O )= 12,04 * 10 23 молекул
следовательно, формула для расчёта
M(ZnO) = Ar(Zn) + Ar(O) = 65 + 16 = 81 г / моль
m = 81 г/моль · (12,04 * 10 23 /6.02 · 10 23 1/моль) = 162 г
Задания для закрепления
Заполните таблицу (округляя числа до целых )
Моль (единица)
Природа частиц
Молярная масса
Молярная концентрация
Молярная фракция
В смеси газов парциальное давление каждого компонента пропорционально его молярному соотношению.
Первая таблица стандартного атомного веса (атомной массы) была опубликована Джоном Дальтоном (1766–1844) в 1805 году на основе системы, в которой относительная атомная масса водорода была определена как 1. Эти относительные атомные массы были основаны на стехиометрическом соотношении. пропорции химических реакций и соединений, факт, который в значительной степени способствовал их принятию: химику не нужно было подписываться под атомной теорией (недоказанная гипотеза в то время), чтобы использовать таблицы на практике. Это привело бы к некоторой путанице между атомными массами (продвигаемой сторонниками атомной теории) и эквивалентными весами (продвигаемыми ее противниками и которые иногда отличались от относительных атомных масс на целочисленный коэффициент), которая сохранялась на протяжении большей части девятнадцатого века.
Стандартизация
Развитие масс-спектрометрии привело к принятию кислорода-16 в качестве стандартного вещества вместо природного кислорода. [ необходима цитата ]
| Основа шкалы | Основание шкалы относительно 12 C = 12 | Относительное отклонение от шкалы 12 C = 12 |
|---|---|---|
| Атомная масса водорода = 1 | 1,00794 (7) | -0,788% |
| Атомная масса кислорода = 16 | 15,9994 (3) | + 0,00375% |
| Относительная атомная масса 16 O = 16 | 15.9949146221 (15) | + 0,0318% |
Крот был сделан седьмой базовой единицей СИ в 1971 году 14-м CGPM. [13]
2019 новое определение базовых единиц СИ
В 2011 году на 24-м заседании Генеральной конференции по мерам и весам (CGPM) был согласован план возможного пересмотра определений базовой единицы СИ в неопределенный срок.
16 ноября 2018 года после встречи ученых из более чем 60 стран на CGPM в Версале, Франция, все базовые единицы СИ были определены в виде физических констант. Это означало, что каждая единица СИ, включая моль, не будет определяться в терминах каких-либо физических объектов, а скорее они будут определяться константами, которые по своей природе являются точными. [1]
Такие изменения официально вступили в силу 20 мая 2019 года. После таких изменений термин «один моль» вещества был переопределен как содержащий «ровно 6.022 140 76 × 10 23 элементарных сущностей «этой субстанции. [14] [15]
С момента его принятия в Международную систему единиц в 1971 году возникла многочисленная критика концепции крота как единицы, такой как метр или секунда :
Как и химики, инженеры-химики широко используют моль единицы, но для промышленного использования могут быть более подходящими другие кратные единицы. Например, единицей измерения объема в системе СИ является кубический метр, что намного больше, чем обычно используемый литр в химической лаборатории. Когда количество вещества также выражается в кмоль (1000 моль) в промышленных процессах, численное значение молярности остается прежним.
В метрической системе инженеры-химики когда-то использовали килограмм-моль (обозначение кг-моль ), которое определяется как количество единиц в 12 кг при температуре 12 ° C, и часто называют моль грамм-моль (обозначение g- моль ) при работе с лабораторными данными. [21]
Освещение теплицы и камеры выращивания для растений иногда выражается в микромолях на квадратный метр в секунду, где 1 моль фотонов = 6,02 × 10 23 фотонов. [22]
Моль это единица чего
Моль принят в качестве единицы СИ XIV Генеральной конференцией по мерам и весам в 1971 году. Точное определение моля формулируется так [2] :
Моль есть количество вещества системы, содержащей столько же структурных элементов, сколько содержится атомов в углероде-12 массой 0,012 кг. При применении моля структурные элементы должны быть специфицированы и могут быть атомами, молекулами, ионами, электронами и другими частицами или специфицированными группами частиц.
Из определения моля непосредственно следует, что молярная масса углерода-12 равна 12 г/моль точно.
1/12 массы атома углерода-12 называют атомной единицей массы (обозначение а. е. м.). Отсюда следует, что 1 а. е. м. = 0,001/ NA кг.
Из определения а. е. м. вытекает, что молярная масса вещества, выраженная в граммах на моль, численно равна массе молекулы этого вещества, выраженной в атомных единицах массы.
Кратные и дольные единицы
Десятичные кратные и дольные единицы образуют с помощью стандартных приставок СИ. Причём, единица измерения йоктомоль может использоваться лишь формально, так как столь малые количества вещества должны измеряться отдельными частицами (1 имоль формально равен 0,602 частицы).
| Кратные | Дольные | ||||||
|---|---|---|---|---|---|---|---|
| величина | название | обозначение | величина | название | обозначение | ||
| 10 1 моль | декамоль | дамоль | damol | 10 −1 моль | децимоль | дмоль | dmol |
| 10 2 моль | гектомоль | гмоль | hmol | 10 −2 моль | сантимоль | смоль | cmol |
| 10 3 моль | киломоль | кмоль | kmol | 10 −3 моль | миллимоль | ммоль | mmol |
| 10 6 моль | мегамоль | Ммоль | Mmol | 10 −6 моль | микромоль | мкмоль | µmol |
| 10 9 моль | гигамоль | Гмоль | Gmol | 10 −9 моль | наномоль | нмоль | nmol |
| 10 12 моль | терамоль | Тмоль | Tmol | 10 −12 моль | пикомоль | пмоль | pmol |
| 10 15 моль | петамоль | Пмоль | Pmol | 10 −15 моль | фемтомоль | фмоль | fmol |
| 10 18 моль | эксамоль | Эмоль | Emol | 10 −18 моль | аттомоль | амоль | amol |
| 10 21 моль | зеттамоль | Змоль | Zmol | 10 −21 моль | зептомоль | змоль | zmol |
| 10 24 моль | йоттамоль | Имоль | Ymol | 10 −24 моль | йоктомоль | имоль | ymol |
| применять не рекомендуется | |||||||
См. также
Примечания
Полезное
Смотреть что такое «Моль» в других словарях:
МОЛЬ — жен. тля (от малый) крошечный сумеречник (бабочка), метличка; гусеничка его, которая точит меха и шерстяную одежу, Tinca. Есть моль шубная, платяная, сырная, хлебная, овощная. Моль пропадает от хмелю, камфары. | Моль овощная, тля, мотылица,… … Толковый словарь Даля
МОЛЬ — жен. тля (от малый) крошечный сумеречник (бабочка), метличка; гусеничка его, которая точит меха и шерстяную одежу, Tinca. Есть моль шубная, платяная, сырная, хлебная, овощная. Моль пропадает от хмелю, камфары. | Моль овощная, тля, мотылица,… … Толковый словарь Даля
моль — 1. МОЛЬ, и; ж. Небольшая бабочка, гусеница которой является вредителем шерстяных вещей, хлебных зёрен и растений. 2. МОЛЬ, и; ж.; МОЛЬ, я; м. Спец. Лес, сплавляемый по реке брёвнами, не связанными в плот. По реке плыла м. Пробираться на лодке… … Энциклопедический словарь
МОЛЬ — единица количества вещества в СИ, определяемая как количество вещества, содержащее столько же формульных (структурных) единиц этого вещества (атомов, молекул, ионов, электронов и др.), сколько содержится атомов в 12 г изотопа углерода 12 (12С);… … Большая политехническая энциклопедия
моль — источено молью.. Словарь русских синонимов и сходных по смыслу выражений. под. ред. Н. Абрамова, М.: Русские словари, 1999. моль тля, мотылица Словарь русских синонимов … Словарь синонимов
МОЛЬ — 1) название пива в Нимвегене. 2) шерстяная материя. 3) у пчеловодов: сплетение вверху улья. Словарь иностранных слов, вошедших в состав русского языка. Чудинов А.Н., 1910. моль 1 ит. molle мягкий) муз. то же, что минор 1 (противоп. дур). 2… … Словарь иностранных слов русского языка
моль — Ед. кол ва вещ ва, т.е. величины, оценив. кол вом содерж. в физич. системе тождест. структур, элементов (атомов, молекул, ионов и др. частиц или их специфич. групп), м. равен кол ву вещ ва системы, содерж. столько же структурных элементов… … Справочник технического переводчика
МОЛЬ — • МОЛЬ (Mohl) Хуго фон (1805 1872), немецкий ботаник, пионер в исследовании анатомии и физиологии КЛЕТОК растений. Сформулировал гипотезу о том, что ядро клетки окружено гранулированным коллоидным веществом, которое в 1846 г. он назвал… … Научно-технический энциклопедический словарь
моль — МОЛЬ, и, жен. Маленькая бабочка, гусеница к рой является вредителем меха, шерсти, хлебных зёрен, растений. Молью изъедено (также перен.: о чём н. явно устарелом, отжившем; неод.). | прил. молевый, ая, ое. II. МОЛЬ, я, муж. (спец.). Сплав леса… … Толковый словарь Ожегова
МОЛЬ — (моль, mol), ед. СИ кол ва в ва. В 1 М. содержится столько молекул (атомов, ионов или к. л. др. структурных элементов в ва), сколько атомов содержится в 0,012 кг 12С (нуклида углерода атомной массой 12), (см. АВОГАДРО ПОСТОЯННАЯ). Физический… … Физическая энциклопедия
-моль — МОЛЬ, в знач. неизм. прил. (муз.). То же, что мольный. Соната а моль. Толковый словарь Ушакова. Д.Н. Ушаков. 1935 1940 … Толковый словарь Ушакова