Молочница у ребенка после антибиотиков чем лечить
Вагинальный кандидоз (молочница)
Статья проверена врачом-акушером-гинекологом, к.м.н. Сазоновой Ю.М., носит общий информационный характер, не заменяет консультацию специалиста.
Для рекомендаций по диагностике и лечению необходима консультация врача.
Для лечения молочницы наши специалисты подберут современные препараты, которые подходят именно вам (таблетки для приема внутрь, крем, свечи, вагинальные таблетки), а также дадут рекомендации, позволяющие избежать рецидивов заболевания. В Клиническом госпитале на Яузе принимают гинекологи, имеющие многолетний опыт в диагностике и лечении вагинального кандидоза.
Вагинальный кандидоз (молочница) стал в наше время настолько привычным и распространенным заболеванием, что часто женщины сами ставят себе диагноз, а затем занимаются самолечением. А зря, ведь для успешной борьбы с болезнью важно не только устранить ее симптомы, но, прежде всего, определитьпричины возникновения вагинального кандидоза.
Вагинальный кандидоз — разновидность инфекции, при которой происходит поражение слизистой оболочки половых органов дрожжеподобными грибками рода Candida. Заболевание вызывает значительный дискомфорт, влияет на самочувствие и отрицательно сказывается на половой жизни.
Причины молочницы
Вагинальный кандидоз может быть спровоцирован многими факторами. Заболеванию могут способствовать стрессовые ситуации (в том числе операции), снижение иммунитета, сопутствующие инфекционные заболевания, кандидоз кишечника, беременность, нарушение вагинальной и кишечной микрофлоры, например, из-за приема антибиотиков, неправильное питание, постоянное использование тампонов, ношение синтетического, облегающего белья.
Многих женщин интересует, может ли молочница передаваться при половом контакте? Хотя это не половая инфекция, но в ряде случаев кандидоз передается половым путем, если мужчина страдает грибковым заболеванием мочеполовой сферы (например, кандидозным баланопоститом). Да, молочница у мужчин редко, но тоже бывает.
Симптомы кандидоза влагалища
При появлении одного из перечисленных признаков, нужно обратиться к врачу. Как выглядит молочница на фото и рисунке можно увидеть слева.
Диагностика и лечение молочницы в Клиническом госпитале на Яузе
Диагностика
Диагностика вагинального кандидоза начинается с опроса пациентки. Важное значение имеют некоторые гинекологические (бактериальный вагиноз, воспалительные процессы в женской половой системе) и сопутствующие заболевания (сахарный диабет, кандидоз и дисбактериоз кишечника и др.). Нередко развитие молочницы после длительного приёма антибиотиков, гормонов, иммуносупрессоров.
При осмотре выявляется характерная клиническая картина – белый налёт на воспаленной слизистой половых органов, обильные, творожистые выделения.
Исследование мазка из влагалища обнаруживает грибковую флору. При необходимости проводится посев с определением вида грибка и его чувствительности к антимикотическим препаратам (культуральный анализ). Среди дополнительных исследований могут быть рекомендованы обследование на половые инфекции, сахарный диабет и диагностика микрофлоры кишечника.
Лечение
Как вылечить молочницу?
Общая и местная антимикотическая терапия
Гинекологи Клинического госпиталя на Яузе проводят эффективное лечение молочницы у женщин. Сегодня существует множество лекарств для борьбы с кандидозом: средства для приема внутрь, крем, вагинальные таблетки, свечи от молочницы. Среди наиболее популярных препаратов при вагинальном кандидозе флукостат, флуконазол (пероральные таблетки), клотримазол (вагинальные таблетки или крем), пимафуцин (свечи) и множество других лекарств. Подобрать оптимальную для Вас схему лечения должен врач.
Снижение роли предрасполагающих факторов
Чтобы избежать рецидивов, необходимо определить и устранить факторы, способствующие заболеванию. Если возможно, отказаться от приёма глюкокортикостероидов и цитостатиков. При сахарном диабете скорректировать медикаментозно уровень глюкозы в крови. Восстановить нормальную микрофлору в кишечнике. Кроме того, нужно с осторожностью принимать антибиотики. Обострение/возникновение молочницы после или во время курса антибиотикотерапии – обычное дело. Поэтому приём антибиотиков нужно сочетать с приёмом противогрибковых средств и пробиотиков. Необходимо соблюдать личную гигиену, поддерживать иммунитет, избегать стрессовых ситуаций.
Половая жизнь при молочнице
Многих интересует, можно ли при молочнице и её лечении вести половую жизнь? Можно, защищаясь презервативом. Нередко для достижения хороших результатов лечение вагинального кандидоза рекомендуется проходить вместе со своим половым партнером.
Молочница при беременности
Развитие вагинального кандидоза при беременности несёт опасность для будущей матери и для плода. Возрастает угроза развития воспалительных процессов во время беременности, послеродовых осложнений, инфицирования плода, способного привести к грибковому поражению его органов и даже гибели. Возможно заражение ребёнка в процессе родов.
Лечение молочницы у беременных затрудняется запретом на приём антимикотических препаратов внутрь. Допустимо местное лечение с помощью вагинальных таблеток и свечей (наиболее безопасными среди них при беременности считается Пимафуцин).
Тем большее значение приобретает соблюдение правил личной гигиены, а также защита от стресса, правильное питание с достаточным количеством витаминов, прогулки, здоровый сон, способствующие укреплению естественной иммунной защиты.
При появлении признаков молочницы у беременной женщины необходимо сразу обратиться к акушеру-гинекологу, чтобы провести своевременное адекватное лечение и избежать осложнений.
Для диагностики и успешного лечения вагинального кандидоза приходите в Клинический госпиталь на Яузе.
Цены на услуги Вы можете посмотреть в прайсе или уточнить по телефону, указанному на сайте.
КИШЕЧНЫЙ ДИСБАКТЕРИОЗ
Что понимают под дисбактериозом? Какие методы диагностики являются современными и достоверными? Какие лекарственные препараты применяются при дисбактериозе? Вкишечнике человека находится свыше 500 различных видов микробов, общее количество которых
Что понимают под дисбактериозом?
Какие методы диагностики являются современными и достоверными?
Какие лекарственные препараты применяются при дисбактериозе?
Нормальная микробная флора кишечника
Количество анаэробов (пептострептококки, бактероиды, клостридии, пропионобактерии) составляет около 10% в тонкой и до 20% в толстой кишке. На долю энтеробактерий приходится 1% от суммарной микрофлоры слизистой оболочки.
Кишечные палочки, энтерококки, бифидобактерии и ацидофильные палочки обладают выраженными антагонистическими свойствами. В условиях нормально функционирующего кишечника они способны подавлять рост несвойственных нормальной микрофлоре микроорганизмов.
Расщепление непереваренных пищевых веществ в толстой кишке осуществляется ферментами бактерий, при этом образуются разнообразные амины, фенолы, органические кислоты и другие соединения. Токсические продукты микробного метаболизма (кадаверин, гистамин и другие амины) выводятся с мочой и в норме не оказывают влияния на организм. При утилизации микробами неперевариваемых углеводов (клетчатки) образуются короткоцепочечные жирные кислоты. Они обеспечивают клетки кишки энергоносителями и, следовательно, улучшают трофику слизистой оболочки. При дефиците клетчатки может нарушаться проницаемость кишечного барьера вследствие дефицита короткоцепочечных жирных кислот. В результате кишечные микробы могут проникать в кровь.
Под влиянием микробных ферментов в дистальных отделах подвздошной кишки происходит деконъюгация желчных кислот и преобразование первичных желчных кислот во вторичные. В физиологических условиях от 80 до 95% желчных кислот реабсорбируется, остальные выделяются с фекалиями в виде бактериальных метаболитов. Последние способствуют нормальному формированию каловых масс: тормозят всасывание воды и тем самым препятствуют излишней дегидратации кала.
Дисбактериоз
В понятие дисбактериоза кишечника входит избыточное микробное обсеменение тонкой кишки и изменение микробного состава толстой кишки. Нарушение микробиоценоза происходит в той или иной степени у большинства больных с патологией кишечника и других органов пищеварения. Следовательно, дисбактериоз является бактериологическим понятием. Он может рассматриваться как одно из проявлений или осложнение заболевания, но не самостоятельная нозологическая форма.
Крайней степенью дисбактериоза кишечника является появление бактерий желудочно-кишечного тракта в крови (бактериемия) или даже развитие сепсиса.
Состав микрофлоры кишечника нарушается при болезнях кишечника и других органов пищеварения, лечении антибиотиками и иммунодепрессантами, воздействиях вредных факторов внешней среды.
Клинические проявления дисбактериоза зависят от локализации дисбиотических изменений.
Дисбактериоз тонкой кишки
При дисбактериозе тонкой кишки численность одних микробов в слизистой оболочке тонкой кишки увеличена, а других уменьшена. Отмечается увеличение Eubacterium (в 30 раз), α-стрептококков (в 25 раз), энтерококков (в 10 раз), кандид (в 15 раз), появление бактерий рода Acinetobacter и вирусов герпеса. Уменьшается от 2 до 30 раз количество большинства анаэробов, актиномицетов, клебсиелл и других микроорганизмов, являющихся естественными обитателями кишечника.
Причиной дисбактериоза могут быть: а) избыточное поступление микроорганизмов в тонкую кишку при ахилии и нарушении функции илеоцекального клапана; б) благоприятные условия для развития патологических микроорганизмов в случаях нарушения кишечного пищеварения и всасывания, развития иммунодефицита и нарушений проходимости кишечника.
Повышенная пролиферация микробов в тонкой кишке приводит к преждевременной деконъюгации желчных кислот и потере их с калом. Избыток желчных кислот усиливает моторику толстой кишки и вызывает диарею и стеаторею, а дефицит желчных кислот приводит к нарушению всасывания жирорастворимых витаминов и развитию желчнокаменной болезни.
Бактериальные токсины и метаболиты, например фенолы и биогенные амины, могут связывать витамин В12.
Некоторые микроорганизмы обладают цитотоксическим действием и повреждают эпителий тонкой кишки. Это ведет к уменьшению высоты ворсинок и углублению крипт. При электронной микроскопии выявляется дегенерация микроворсинок, митохондрий и эндоплазматической сети.
Дисбактериоз толстой кишки
Состав микрофлоры толстой кишки может меняться под влиянием различных факторов и неблагоприятных воздействий, ослабляющих защитные механизмы организма (экстремальные климатогеографические условия, загрязнение биосферы промышленными отходами и различными химическими веществами, инфекционные заболевания, болезни органов пищеварения, неполноценное питание, ионизирующая радиация).
Клинические особенности дисбактериоза
Особенностей клинического течения заболевания у больных с различными вариантами дисбактериоза толстой кишки, по данным бактериологических анализов кала, в большинстве случаев установить не удается. Можно отметить, что больные хроническими заболеваниями кишечника чаще инфицируются острыми кишечными инфекциями по сравнению со здоровыми. Вероятно, это связано со снижением у них антагонистических свойств нормальной микрофлоры кишечника и, прежде всего, частым отсутствием бифидобактерий.
Особенно большую опасность представляет псевдомембранозный колит, развивающийся у некоторых больных, длительно лечившихся антибиотиками широкого спектра действия. Этот тяжелый вариант дисбактериоза вызывается токсинами, выделяемыми синегнойной палочкой Clostridium difficile, которая размножается в кишечнике при угнетении нормальной микробной флоры.
Основным симптомом псевдомембранозного колита является обильная водянистая диарея, началу которой предшествовало назначение антибиотиков. Затем появляются схваткообразные боли в животе, повышается температура тела, в крови нарастает лейкоцитоз. Эндоскопическая картина псевдомембранозного колита характеризуется наличием бляшковидных, лентовидных и сплошных «мембран», мягких, но плотно спаянных со слизистой оболочкой. Изменения наиболее выражены в дистальных отделах ободочной и прямой кишок. Слизистая оболочка отечная, но не изъязвлена. При гистологическом исследовании обнаруживают субэпителиальный отек с круглоклеточной инфильтрацией собственной пластинки, капиллярные стазы с выходом эритроцитов за пределы сосудов. На стадии образования псевдомембран под поверхностным эпителием слизистой оболочки возникают экссудативные инфильтраты. Эпителиальный слой приподнимается и местами отсутствует; оголенные места слизистой оболочки прикрыты лишь слущенным эпителием. На поздних стадиях болезни эти участки могут занимать большие сегменты кишки.
Очень редко наблюдается молниеносное течение псевдомембранозного колита, напоминающее холеру. Обезвоживание развивается в течение нескольких часов и заканчивается летальным исходом.
Таким образом, оценка клинической значимости дисбиотических изменений должна основываться прежде всего на клинических проявлениях, а не только на результатах исследования микрофлоры кала.
Методы диагностики
Диагностика дисбактериоза представляет собой сложную и трудоемкую задачу. Для диагностики дисбактериоза тонкой кишки применяют посев сока тонкой кишки, полученного с помощью стерильного зонда. Дисбактериоз толстой кишки выявляют с помощью бактериологических исследований кала.
Микробная флора образует большое количество газов, в том числе водорода. Это явление используют для диагностики дисбактериоза. Концентрация водорода в выдыхаемом воздухе натощак находится в прямой зависимости от выраженности бактериального обсеменения тонкой кишки. У больных с заболеваниями кишечника, протекающими с хронической рецидивирующей диареей и бактериальным обсеменением тонкой кишки, концентрация водорода в выдыхаемом воздухе значительно превышает 15 ppm.
Для диагностики дисбактериоза применяют также нагрузку лактулозой. В норме лактулоза не расщепляется в тонкой кишке и метаболизируется микробной флорой толстой кишки. В результате количество водорода в выдыхаемом воздухе повышается (рис. 1).
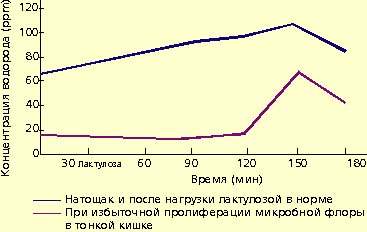 |
| Рисунок 1. Концентрация водорода в выдыхаемом воздухе |
Наиболее частыми бактериологическими признаками дисбактериоза толстой кишки являются отсутствие основных бактериальных симбионтов — бифидобактерий и уменьшение количества молочнокислых палочек. Увеличивается количество кишечных палочек, энтерококков, клостридий, стафилококков, дрожжеподобных грибов и протея. У отдельных бактериальных симбионтов появляются патологические формы. К ним относятся гемолизирующая флора, кишечные палочки со слабо выраженными ферментативными свойствами, энтеропатогенные кишечные палочки и т. д.
Углубленное изучение микробиоценоза показало, что традиционные методы не позволяют получить истинную информацию о состоянии микрофлоры кишечника. Из 500 известных видов микробов в целях диагностики обычно изучаются лишь 10-20 микроорганизмов. Важно, в каком отделе — в тощей, подвздошной или толстой кишках — исследуется микробный состав. Поэтому перспективы разработки клинических проблем дисбактериоза в настоящее время связывают с применением химических методов дифференциации микроорганизмов, позволяющих получить универсальную информацию о состоянии микробиоценоза. Наиболее широко для этих целей используются газовая хроматография (ГХ) и газовая хроматография в сочетании с масс-спектрометрией (ГХ-МС). Этот метод позволяет получить уникальную информацию о составе мономерных химических компонентов микробной клетки и метаболитов. Маркеры такого рода могут быть определены и использованы для детектирования микроорганизмов. Главным преимуществом и принципиальным отличием этого метода от бактериологических является возможность количественного определения более 170 таксонов клинически значимых микроорганизмов в различных средах организма. При этом результаты исследования могут быть получены в течение нескольких часов.
Проведенные нами исследования микробиоценоза в крови и биоптатов слизистой оболочки тонкой и толстой кишок у больных с синдромом раздраженного кишечника позволили обнаружить отклонения от нормы до 30-кратного увеличения или уменьшения многих компонентов. Существует возможность оценки изменений микрофлоры кишечника на основании данных анализа крови методом ГХ-МС-микробных маркеров.
 |
Лечение
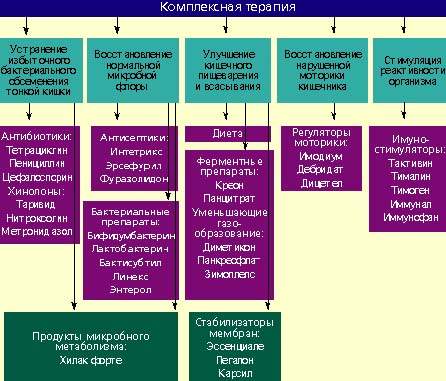
Лечение дисбактериоза должно быть комплексным (схема) и включать в себя следующие мероприятия:
Антибактериальные препараты
Антибактериальные препараты необходимы в первую очередь для подавления избыточного роста микробной флоры в тонкой кишке. Наиболее широко применяются антибиотики из группы тетрациклинов, пенициллинов, цефалоспорины, хинолоны (таривид, нитроксолин) и метронидазол.
Однако антибиотики широкого спектра действия в значительной степени нарушают эубиоз в толстой кишке. Поэтому они должны применяться только при заболеваниях, сопровождающихся нарушениями всасывания и моторики кишечника, при которых, как правило, отмечается выраженный рост микробной флоры в просвете тонкой кишки.
Антибиотики назначают внутрь в обычных дозах в течение 7–10 дней.
При заболеваниях, сопровождающихся дисбактериозом толстой кишки, лечение лучше проводить препаратами, которые оказывают минимальное влияние на симбионтную микробную флору и подавляют рост протея, стафилококков, дрожжевых грибов и других агрессивных штаммов микробов. К ним относятся антисептики: интетрикс, эрсефурил, нитроксолин, фуразолидон и др.
При тяжелых формах стафилококкового дисбактериоза применяют антибиотики: таривид, палин, метронидазол (трихопол), а также бисептол-480, невиграмон.
Антибактериальные препараты назначают в течение 10–14 дней. В случае появления в кале или кишечном соке грибов показано применение нистатина или леворина.
У всех больных с диареей, ассоциированной с антибиотиками, протекающей с интоксикацией и лейкоцитозом, возникновение острой диареи следует связывать с Cl. difficile.
В этом случае срочно делают посев кала на Cl. difficile и назначают ванкомицин по 125 мг внутрь 4 раза в сутки; при необходимости доза может быть увеличена до 500 мг 4 раза в день. Лечение продолжают в течение 7-10 суток. Эффективен также метронидазол в дозе 500 мг внутрь 2 раза в сутки, бацитрацин по 25 000 МЕ внутрь 4 раза в сутки. Бацитрацин почти не всасывается, в связи с чем в толстой кишке можно создать более высокую концентрацию препарата. При обезвоживании применяют адекватную инфузионную терапию для коррекции водно-электролитного баланса. Для связывания токсина Cl. difficile используют холестирамин (квестран).
Бактериальные препараты
Живые культуры нормальной микробной флоры выживают в кишечнике человека от 1 до 10% от общей дозы и способны в какой-то мере выполнять физиологическую функцию нормальной микробной флоры. Бактериальные препараты можно назначать без предварительной антибактериальной терапии или после нее. Применяют бифидумбактерин, бификол, лактобактерин, бактисубтил, линекс, энтерол и др. Курс лечения длится 1-2 месяца.
Возможен еще один способ устранения дисбактериоза — воздействие на патогенную микробную флору продуктами метаболизма нормальных микроорганизмов. К таким препаратам относится хилак форте. Он создан 50 лет назад и до настоящего времени применяется для лечения больных с патологией кишечника. Хилак форте представляет собой стерильный концентрат продуктов обмена веществ нормальной микрофлоры кишечника: молочной кислоты, лактозы, аминокислот и жирных кислот. Эти вещества способствуют восстановлению в кишечнике биологической среды, необходимой для существования нормальной микрофлоры, и подавляют рост патогенных бактерий. Возможно, продукты метаболизма улучшают трофику и функцию эпителиоцитов и колоноцитов. 1 мл препарата соответствует биосинтетическим активным веществам 100 млрд. нормальных микроорганизмов. Хилак форте назначают по 40–60 капель 3 раза в день на срок до 4 недель в сочетании с препаратами антибактериального действия или после их применения.
Совсем недавно появились сообщения о возможности лечения острой диареи, ассоциированной с антибактериальной терапией и Cl. difficile, большими дозами пре- и пробиотиков.
Регуляторы пищеварения и моторики кишечника
У больных с нарушением полостного пищеварения применяют креон, панцитрат и другие панкреатические ферменты. С целью улучшения функции всасывания назначают эссенциале, легалон или карсил, т. к. они стабилизируют мембраны кишечного эпителия. Пропульсивную функцию кишечника улучшают имодиум (лоперамид) и тримебутин (дебридат).
Стимуляторы реактивности организма
Для повышения реактивности организма ослабленным больным целесообразно применять тактивин, тималин, тимоген, иммунал, иммунофан и другие иммуностимулирующие средства. Курс лечения должен составлять в среднем 4 недели. Одновременно назначаются витамины.
Профилактика дисбактериоза
Первичная профилактика дисбактериоза представляет очень сложную задачу. Ее решение связано с общими профилактическими проблемами: улучшением экологии, рациональным питанием, улучшением благосостояния и прочими многочисленными факторами внешней и внутренней среды.
Вторичная профилактика предполагает рациональное применение антибиотиков и других медикаментов, нарушающих эубиоз, своевременное и оптимальное лечение болезней органов пищеварения, сопровождающихся нарушением микробиоценоза.
Уретрит у ребенка
Содержание статьи:
Детский уретрит — это воспаление мочеиспускательного канала, имеющее инфекционно-воспалительное происхождение. Возникает в результате попадания в уретру патогенных микроорганизмов (вирусы, бактерии, простейшие). Вероятность развития данной патологии увеличивается при несоблюдении правил интимной гигиены, нарушениях мочеиспускания, врожденных аномалий развития органов мочевыделительной системы.
Клинически уретрит проявляется частым болезненным мочеиспусканием. Моча мутная, имеет зловонный запах. Наблюдается общая интоксикация организма. Для диагностики заболевания пациенту назначают анализы мочи (бактериологический, клинический), УЗИ мочевого пузыря, уретры. Основные клинические рекомендации при лечении уретрита у детей включают прием лекарственных препаратов (НПВС, противоаллергические средства, антибиотики, антиоксиданты), общеукрепляющее лечение и физиотерапию.
Причины заболевания
Основными причинами развития уретрита у детей являются:
1. Снижение иммунной защиты организма.
2. Медицинские процедуры:
4. Неправильное питание (раздражение и воспаление уретры происходит в результате злоупотребления кислой, острой, соленой, маринованной пищей).
5. Несоблюдение правил интимной гигиены.
6. Инфекционно-воспалительные патологии органов мочеполовой системы:
7. Врожденные аномалии развития органов мочевыделительной системы.
Симптомы
Заболевание обычно проявляется повышением температуры тела (у детей младше 5 лет), зудом и жжением в области репродуктивных органов, болями при мочеиспускании, покраснением и отеком слизистой половых органов.
Уретрит у детей-мальчиков проявляется следующими клиническими признаками:
Уретрит у детей-девочек проявляется болями внизу живота, резями при мочеиспускании, зудом в половых органах, частыми походами в туалет.
При появлении первых симптомов заболевания необходимо немедленно показать ребенка урологу и пройти обследование. Если уретрит не лечить, то он быстро переходит в хроническую форму, а также вызывает развитие воспалительных процессов в мочевом пузыре, почках, яичках. Со временем хроническое воспаление может привести к развитию бесплодия.
Виды заболевания
По причине возникновения выделяют следующие виды уретрита:
1. Инфекционный. Возникает в результате воздействия патогенной и условно-патогенной микрофлоры:
2. Неинфекционный. Возникает в результате аллергических реакций, травм уретры.
По виду возбудителя выделяют следующие виды уретрита:
По локализации воспаления уретрит бывает:
По механизму развития выделяют следующие виды заболевания:
По клиническому течениюуретрит может быть острым (до 14 дней) и хроническим (от 14 дней и более). Хроническая форма заболевания обычно развивается при отсутствии своевременной терапии.
Диагностика
На первом приеме уролог проводит сбор анамнеза, узнает, на что жалуется пациент, определяет возможные провоцирующие факторы. Далее врач проводит физикальный осмотр, который включает в себя пальпацию поясницы, живота, осмотр наружного отверстия уретры.
Для более точной диагностики заболевания используют следующие лабораторные и инструментальные методы исследования:
На основании клинических симптомов уретрита у ребенка, данных лабораторных и инструментальных исследований врач назначает курс лечения.
Методы лечения уретрита у детей
Основными задачами терапии при воспалении мочеиспускательного канала являются купирование воспалительного процесса и устранение патогенной микрофлоры. После этого неприятные симптомы исчезают, и ребенок выздоравливает. Неосложненный уретрит можно лечить в амбулаторных условиях. Дети в тяжелом состоянии, с сильной интоксикацией организма, а также с сопутствующими патологиями органов мочевыделительной системы подлежат госпитализации.
Чем лечить уретрит у ребенка?В зависимости от причин возникновения и степени тяжести заболевания врач может назначить прием следующих лекарственных средств:
После купирования воспаления активно используют физиотерапию. При воспалении уретры наибольший эффект дают электрофорез, СВЧ, озокеритовые и парафиновые аппликации. Также показан прием хвойных ванн, которые оказывают общеукрепляющее и антисептическое действие.
Профилактика
Чтобы избежать развития заболевания необходимо соблюдать следующие рекомендации:
Последствия уретрита
Если вовремя не начать терапию или не долечить болезнь, то уретрит может перейти в хроническую форму. Кроме этого, воспалительный процесс может перекинуться на соседние органы, что приводит к возникновению следующих патологических состояний организма:
Хронический уретрит во взрослом возрасте может стать причиной бесплодия.
Источники: