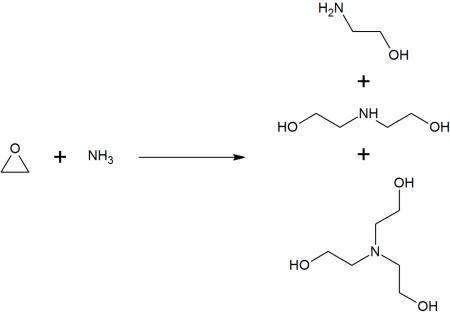Моноэтаноламин для чего используется
Моноэтаноламин
| Моноэтаноламин | |
|---|---|
 | |
 | |
| Систематическое наименование | 2-Аминоэтан-1-ол 2-Аминоэтанол |
| Сокращения | МЭА |
| Традиционные названия | 2-Амино-l-Этанол, Этаноламин, Моноэтаноламин, β-Аминоэтанол, коламин, глицинол |
| Хим. формула | C2H7NO |
| Молярная масса | 61,08 г/моль |
| Плотность | 1,012 г/см³ |
| Динамическая вязкость | 0,019 Па·с |
| Энергия ионизации | 8,96 ± 0,01 эВ |
| Т. плав. | 10,3 °C |
| Т. кип. | 170 °C |
| Т. всп. | 85 °C |
| Т. свспл. | 450 °C |
| Пр. взрв. | 3 ± 1 об.% |
| Давление пара | 0,4 ± 0,1 мм рт.ст. |
| pKa | 9,50 |
| Растворимость в воде | смешивается |
| Растворимость в гептане | 0,41 г/100 мл |
| Показатель преломления | 1,4539 (20°C) |
| ГОСТ | ТУ 2423-159-00203335-2004 ГОСТ 19234-87 |
| Рег. номер CAS | 141-43-5 |
| PubChem | 700 |
| Рег. номер EINECS | 205-483-3 |
| SMILES | |
| RTECS | KJ5775000 |
| ChEBI | 16000 |
| ChemSpider | 13835336 |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Содержание
Физические свойства
Вязкая маслянистая жидкость с температурой кипения 170 °C. Имеет слабый аминный запах. Смешивается с водой во всех отношениях. Хорошо растворим в этаноле, бензоле, хлороформе.
Получение
В промышленности синтез этаноламина проводится присоединением аммиака к этиленоксиду в присутствии небольшого количества воды. Процесс осуществляют в одну стадию при температуре 90—130 °С и давлении 7—10 МПа.
Наряду с моноэтаноламином при этом получаются диэтаноламин и триэтаноламин. При соотношении этиленоксид/аммиак (1:15) в продуктах реакции содержится 78,3 % моно-, 16 % ди- и 4,4 % триэтаноламинов. Этиленоксид в реакции реагирует нацело.
Соотношение этаноламинов в смеси регулируют концентрацией NH3, температурой процесса и повторным направлением в реакцию одного или двух этаноламинов.
Образующуюся смесь этаноламинов, H2O и NH3 разделяют ректификацией, при этом аммиак в сжиженном виде повторно направляют в реактор.
В лаборатории этаноламин получают действием аммиака на этиленхлоргидрин (2-хлорэтанол):
Химические свойства
Этаноламин — слабое основание (pKa=9.50). С минеральными и сильными органическими кислотами образует соли.
При взаимодействии со сложными эфирами и карбоновыми кислотами или их ангидридами и хлорангидридами моноэтаноламин превращается в соответствующие N-(2-гидрооксиэтил)амиды кислот:
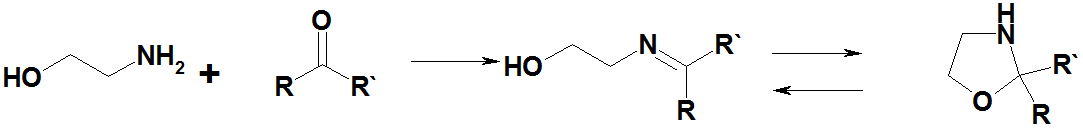
Моноэтаноламин с альдегидами (за исключением формальдегида) и кетонами даёт основания Шиффа, последние обычно находятся в равновесии с изомерными оксазолидинами:
При взаимодействии солей моноэтаноламина с KCN или NaCN и альдегидами и кетонами образуются N-(гидроксиэтил)аминонитрилы:
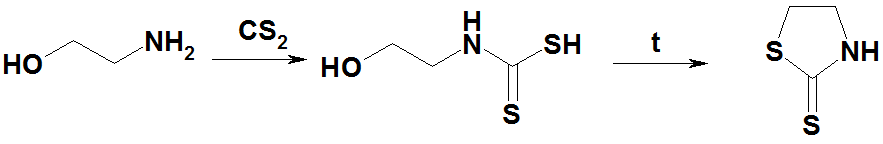
Моноэтаноламин при реакции с CS2 образует N-(2-гидроксиэтил)дитиокарбаминовую кислоту, которая при нагревании даёт меркаптотиазолин:
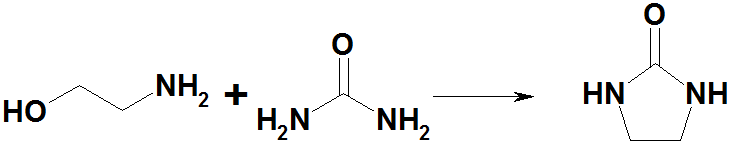
При нагревании с мочевиной образуется этиленмочевина:
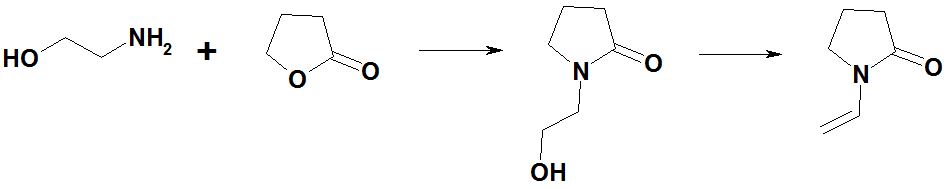
С γ-бутиролактоном — N-(2-гидроксиэтил)пирролидон, который далее превращается в N-винилпирролидон:
Аммонолиз моноэтаноламина в присутствии H2 и катализаторов гидрирования (Ni или Cu) приводит к образованию этилендиамину:
Биологическая роль
Этаноламин всегда присутствует в незначительном количестве в организме человека и животных при полноценном белковом питании. В организме он образуется при декарбоксилировании аминокислоты серина. Дальнейшие пути превращений связаны либо с синтезом одного из фосфатидов — кефалина, являющегося фосфатидилэтаноламином, либо с превращением этаноламина в холин.
Применение
Водные растворы этаноламина обладают щелочной реакцией и хорошо поглощают кислые газы (диоксид углерода, диоксид серы, сероводород, а также газообразные и летучие тиолы). При нагреве раствора поглощённые газы выделяются, регенерированный раствор повторно направляют для поглощения. Благодаря обратимости растворы этаноламина широко используются в качестве абсорбента в различных процессах газоочистки (например, удаление примесей сероводорода, углекислого газа и тиолов в нефтегазовой и нефтехимической промышленности) и для разделения газов (в частности, абсорбция углекислого газа из смеси газов при производстве водорода конверсией метана).
Применяется в средствах для окраски волос в качестве заменителя раствора аммиака.
Этаноламин также является исходным веществом в промышленном синтезе таурина.
Безопасность
Летальная доза (ЛД50 700 мг/кг (для белых мышей, перорально).
При остром отравлении возникает раздражение слизистых оболочек, урежение дыхания, двигательное возбуждение, судороги. У белых крыс, вдыхавших воздух с концентрацией этаноламина 0,2—0,4 мг/л по 5 часов ежедневно в течение 6 месяцев наблюдались изменения функционального состояния центральной нервной системы и функций печени, незначительная анемия и ретикулоцитоз, повышенный диурез и белок в моче.
Крысы, подвергавшиеся практически непрерывному отравлению в течение 30 суток при концентрации 0,164 мг/л, погибали через 14—24 суток, но выживали в тех же условиях в течение 90 дней при концентрации 0,029 мг/л. Морские свинки при непрерывном вдыхании 0,184 мг/л погибали между 10 и 28 днём. Концентрация 0,037 мг/л переносилась в течение 90 суток, а 0,12 мг/л вызывала лишь слабые признаки отравления. Собаки пережили в течение 30 дней вдыхание 0,25 мг/л и 0,015 мг/л в течение 60 дней.
Моноэтаноламин. Свойства и области применения.
Различные химические вещества используются в промышленности, в разных отраслях производства. О многих из них нам практически ничего не известно, так как в этом нет особой надобности. Но если ваша работа так или иначе связана с химикатами, вам было бы интересно узнать подробнее о химических веществах, с которыми вы часто сталкиваетесь.
Моноэтаноламин. Свойства и области применения.
Моноэтаноламин — химическое вещество, которое сильно опасно для здоровья человека. C2H7NO — химическая формула этого химиката. Основными областями применения являются нефтяные и газовые отрасли. Служит абсорбентом и поглощает органические соединения и кислые газы, вещества с серой. Применяется в производстве пластмасс, красок (в том числе содержится в краске для волос), моющих препаратов, фармацевтике.
Так же моноэтаноламин бесцветен и находится в жидком состоянии. Имеет едкий аммиачный запах. Взрывоопасен. Температура хранения не должна превышать установленных норм : от — 40 до + 50 градусов по Цельсию. Пары моноэтаноламина особо опасны в воздушно-газовой смеси. Среди требований хранения — проветриваемые или открытые площадки. Запрещено хранение бочек рядом с хлором или азотной кислотой. Едкие вещества так же лучше держать подальше от моноэтаноламина.
Моноэтаноламин. Угроза для здоровья.
Моноэтаноламин представляет особую опасность для здоровья человека и животных. Вдыхание паров даже в малых дозах несет серьезную угрозу для организма. Смертельно опасен. Вызывает раздражительные слизистой, кожных кокровов. При отравлении наблюдается замедление сердцебиение, замедленное дыхание, мышечные судороги, а так же двигательное возбуждение.
Для животных более мелкие дозы вещества уже являются смертельными. Согласно проводимым опытам на крысах и морских свинках, отравление моноэтаноламином в любом случае приводит к смерти в зависимости от количества содержащегося в воздухе химиката.
Транспортировка
Выполнение транспортировки и доставки моноэтаноламина осуществляется согласно правил перевозки опасных грузов. Перед выполнением транспортировки лучше всего проконсультироваться со специалистами.
Моноэтаноламин
| Синонимы | 2-аминоэтанол, этаноламин, 2-гидроксиэтиламин, коламин, МЭА, аминоэтиловый спирт |
| Международное название | ethanolamine, 2-aminoethanol, monoethanolamine, MEA |
| CAS № | 141-43-5 |
| ТУ | 2423-159-00203335-2004, 2423-065-05807977-2004 |
| Производство | Россия |
| Марка/Сорт | Высший, первый, второй, третий |
| Упаковка | Металлическая бочка 210-230 кг |
| Химическая формула | H2NC2H4OH |
Склады отгрузки продукции
МЭА вступает в реакции, характерные для аминов и спиртов. Моноэтаноламин окисляется, дегидрируется, взаимодействует с гидробромидом, сложными эфирами, минеральными и карбоновыми кислотами, их ангидридами, хлорангидридами, альдегидами, кетонами, сероуглеродом, мочевиной, диоксидом углерода, металлическим натрием. МЭА вызывает коррозию у соединений и сплавов меди.
Этаноламины впервые были синтезированы Вюрцем в 1860 году нагреванием этиленхлоргидрина и водного раствора аммиака в герметичной трубе. А в 1897 году Кнорр сообщил о реакции этилена с аммиаком и разделении моно-, ди-, триэтаноламинов фракционной дистилляцией. Несмотря на то, что производство моноэтаноламинов стало доступно с 1931 года, значимость промышленного получения этаноламинов стала расти только в 1945 году с началом широкомасштабного производства оксида этилена. На сегодняшний день индустрия этаноламинов занимает значительный сегмент мирового химического комплекса.
Производство этаноламинов относится к среднетоннажным. Большинство технологических линий построено по принципу гибких технологических схем, и в состоянии обеспечить выпуск нескольких десятков наименований продуктов как по действующим стандартам, так и по специальным требованиям потребителей.
Моноэтаноламин получают взаимодействием аммиака или водного раствора аммиака с окисью этилена, процесс осуществляется в одну стадию. В результате этого взаимодействия получается смесь трех аминов, различающихся между собой степенью замещения атомов водорода у аммиака группой CH2CH2OH. Состав смеси этаноламинов регулируют количеством аммиака, температурой процесса и направлением в рецикл одного или двух этаноламинов. Образующуюся смесь этаноламинов, воды и аммиака разделяют ректификацией, при этом аммиак в сжиженном виде направляют в рецикл, а воду, моно-, ди- и триэтаноламины выделяют ректификацией. Реакция образования этаноламинов протекает с выделением тепла, которое отводят охлаждающим рассолом, циркулирующим в межтрубном пространстве колонны. Температуру в реакционной массе поддерживают не выше 65 °С. Продукты реакции, вытекающие из нижней части колонны, подогревают до 80 °С в подогревателе и направляют в отгонную колонну. При подогреве до 115 °С из раствора отгоняют аммиак, двуокись углерода, часть воды. Из нижней части отгонной колонны отводят водный раствор этаноламинов – этаноламин-сырец. Его подвергают ректификации в двухколонном ректификационном агрегате. Моноэтаноламин выпускают различных сортов: высшего, первого, второго и третьего.
Моноэтаноламин обладает высокой поглотительной способностью по отношению к токсичным газам, используется там, где требуется высокая степень очистки от них. МЭА отвечает основному требованию извлечения кислых газов при высоких температурах (110-120 °С) и обеспечивает рециркуляцию с большим поглощением кислых компонентов из потока газа. Так моноэтаноламин применяется для очистки газов от сероводорода и углекислоты. Растворимость углекислоты в водных растворах МЭА зависит от концентрации раствора, температуры абсорбции и в значительно меньшей степени от парциального давления диоксида углерода.
В промышленности обычно используются растворы, содержащие по массе 15-20% моноэтаноламина. Применение более концентрированных растворов нецелесообразно из-за резкого возрастания коррозии, потерь амина и увеличения вязкости раствора, что снижает коэффициент абсорбции. Чтобы достичь глубокой регенерации раствора МЭА, требуемой для достижения тонкой очистки газа от углекислоты, регенерацию ведут под давлением 0,25-0,30 МПа и при температуре 120-130 °С. При более низком давлении и температуре степень регенерации раствора моноэтаноламина снижается. При более высоком давлении и температуре резко возрастает коррозия нижней части регенератора и кипятильников.
Моноэтаноламин стабилен при нормальных условиях хранения и обращения. Нагревание, перегрев приводят к деструкции МЭА.
По внешнему виду моноэтаноламин (МЭА) представляет собой прозрачную жидкость с резким аммиачным запахом, не содержащую механических примесей.
Моноэтаноламин (МЭА) поставляется в промышленной упаковке:
| Наименование | Масса, кг |
| Металлическая бочка | 210-230 |
Моноэтаноламин (МЭА) рекомендуется транспортировать и хранить при следующих условиях:
При соблюдении условий транспортировки и хранения в невскрытой заводской упаковке гарантийный срок хранения моноэтаноламина высшего и первого сортов составляет 1 год с даты изготовления, МЭА второго и третьего сортов – 3 года с даты изготовления.
Моноэтаноламин (МЭА) широко используется в промышленности:
Безналичный расчёт (выставление счёта на оплату).
Наличными при получении на складе ХИМПЭК в Московской области.
Доставка автотранспортом или железнодорожным транспортом по России и в близлежащие страны.
Самовывоз со склада ХИМПЭК в Московской области.
Минимальный объём заказа:
Металлическая бочка 210-230 кг
Минимальная сумма заказа:
2000 рублей.
Моноэтаноламин
Стандарт качества
ТУ 2423-159-00203335-2004
Формула
Описание
Органическое соединение, имеет вид густой маслянистой жидкости. Смешивается с водой, обладает сильными щелочными свойствами.
Жидкость с характерным запахом, хорошо растворим в воде во всех соотношениях, плохо растворяется в эфирах, бензоле, толуоле. Моноэтаноламин – горючая жидкость, его водные растворы – трудно горючи. По степени воздействия на организм относится к веществам II класса опасности. Обладает щелочными свойствами, поэтому при попадании на открытые участки кожи, есть риск ожога. Средствами тушения являются распыленная вода, воздушно-механическая пена, порошок.
Моноэтаноламин (МЭА) получают взаимодействием окиси этилена и аммиака.
Применение
Применяют в качестве абсорбентов «кислых» газов (СО2, H2S, SO2 и др.), в процессах очистки технологических газов на предприятиях нефтеперерабатывающей, газодобывающей и хим. отраслей промышленности; как сырье для получения эмульгаторов, диспергаторов, стабилизаторов пен, моющих и чистящих средств, шампуней, ПАВ и др. Моноэтаноламин используют в органическом синтезе для получения этилендиамина, N-винилпирролидона и др.
Транспортировка
Любым видом транспорта, как легковым, так и железнодорожным в специальных цистернах, с соблюдением правил безопасности как при перевозке горю-чих веществ.
Хранение
Должно производиться в стальных бочках вдали от отопительных приборов в крытых помещениях. Также, не допускается его хранение вместе с агрессивными или едкими веществами, например в присутствии азотной кислоты или хлора.
Гарантийный срок хранения МЭА высшего и первого сортов – один год, второго и третьего сортов – три года со дня изготовления.
Физико-химические свойства :
| Наименование показателя | Норма | |
| Высший сорт | Первый сорт | |
| Массовая доля моноэтаноламина, %, не менее | 98,8 | 98,0 |
| Массовая доля диэтаноламина, %, не менее | 0,6 | 1,0 |
| Массовая доля воды, %, не менее | 0,6 | 1,0 |
| Цветность, единицы ханзена, не более | 50 | — |
| Плотность при 20°С, г/см 3 | 1,015-1,018 | 1,015-1,018 |
Безопасность
Моноэтаноламин – легко воспламеняющаяся жидкость. Паро-воздушные смеси взрывоопасны. Температура вспышки: 85/93 °С. По воздействию на человека представляет вещество второго класса опасности. Острая токсичность. Опасный продукт разложения: кислота аминоуксусная. Ко всему этому моноэтаноламин соединение обладающее щелочными признаками и свойствами, поэтому при попадании на кожу может образоваться ожог. Средства индивидуальной защиты: респираторы, защитные очки, перчатки, лицевой щиток. Тушат вещество с помощью обыкновенной воды, порошковых соединений или же пены.
Отгрузка от 1 кг! Доставка по РФ! Работаем только с Юридическими лицами (в т.ч. ИП) и только по безналичному расчёту!
Моноэтаноламин
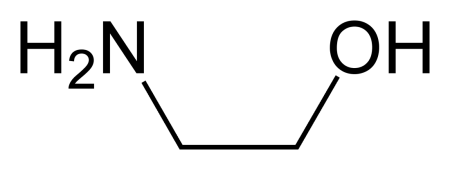
Моноэтаноламин, он же этаноламин — это простейший стабильный аминоспирт. Вместе с этим он является как первичным амином, так и первичным спиртом. Известен также под тривиальным названием «коламин».
При нормальных условиях существует в виде вязкой маслянистой жидкости. Обладает слабым запахом аминов, легко растворяется в этаноле, бензоле и хлороформе, а вот с водой смешивается в любых пропорциях.
Формула моноэтаноламина — C2H7NO.
Чтобы получить этаноламин в промышленности, аммиак присоединяют к этиленоксиду в присутствии небольшого количества воды. Этот процесс осуществляется в одну стадию, причём образуются и другие вещества — диэтаноламин и триэтаноламин.
Что касается свойств моноэтаноламина, то они зависят от того, к какому классу веществ он относится. Это слабое основание, способное вступать в реакцию с кислотами — как с минеральными, так и с органическими. Продуктом такой реакции будет соль.
Также моноэтаноламин способен превращаться в амиды кислот. Для этого необходимо смешать его со сложными эфирами и карбоновыми кислотам. Также в этом случае подойдут их ангидриды или хлорангидриды.
Это вещество активно взаимодействует с сероуглеродом. Продуктом такой реакции является дитиокарбаминовая кислота, которую в дальнейшем можно нагреть и получить меркаптотиазолин.
К тому же моноэтаноламин реагирует с мочевиной, образуя в ходе такого взаимодействия этиленмочевину.
Применение
Раствор этаноламина — эффективный абсорбент. Он вступает в щелочную реакцию и активно поглощает кислые газы. При повышении температуры он регенерирует их. Именно поэтому данное вещество часто применяют в нефтегазовой и нефтехимической промышленности: оно незаменимо в процессе газоочистки.
Что касается промышленного синтеза веществ, моноэтаноламин служит для синтеза таурина.
Широко известен в такой отрасли, как косметология, поскольку служит одной из составляющих в процессе производства краски для волос. Моноэтаноламин — отличный заменитель аммиака.
Техника безопасности
В соответствии с уровнем воздействия вещества на организм человека и окружающую среду, класс опасности моноэтаноламина — второй. Из-за щёлочных свойств при попадании на кожу может возникнуть серьёзный ожог.
Необходимо при работе с этим веществом защитить кожу, слизистые оболочки и органы дыхания. Поможет стандартный набор: защитный костюм, респиратор, щиток для лица, специальные очки и перчатки.
Кроме того, моноэтаноламин легко воспламеняется, поэтому при работе с ним важно, чтобы рядом не было горючих веществ. Пары очень токсичны и взрывоопасны. В случае возгорания необходимо потушить очаг либо распылённой водой, либо воздушно-механической пеной или порошком.
Транспортировка
Перед отправкой моноэтаноламин распределяют по стальным, плотно закатанным бочкам. Перевозить его нужно строго в крытых транспортных средствах, учитывая все правила перевозки опасного груза.
Наиболее предпочтительные виды транспорта — железнодорожный и автомобильный.
Хранение
Хранить моноэтаноламин нужно в герметично закрытых бочках. Для этого выбирают крытые складские помещения, и бочки размещают как можно дальше от приборов отопления. Если в них вещество первого и высшего сортов, хранить его можно год, второго и третьего сортов — три года со дня изготовления.