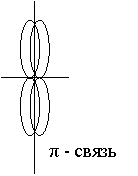
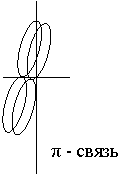
Можно ли утверждать что водородная связь обладает направленностью насыщаемостью
Лекции по химии
вторник, 20 марта 2012 г.
Насыщаемость и направленность
Насыщаемость
Максимальная ковалентность у элементов 2 го периода равна 4, т.к. на внешнем энергетическом уровне у них находятся 4 орбитали (s и p) и может разместиться максимум 8 электронов 2s 2 2p 6 (2+6=8) 8:2=4.
Атомы элементов 3 го периода и т.д. имеют и d-орбитали и ковалентность может = 9; 3s 2 3p 6 3d 10 (2+6+10=18); 18:2=9.
Способность атомов участвовать в образовании ограниченного числа ковалентных связей называется насыщаемостью.
Направленность
Свойства молекулы, её способность вступать в химическое взаимодействие с другими молекулами (реакционная способность) зависят не только от прочности химических связей в молекуле, но в значительной мере и от её пространственного строения. Этот раздел химии называется стереохимией.
Образование ковалентной связи осуществляется за счет перекрывания электронных облаков взаимодействующих атомов. При этом область перекрывания располагается в определенном направлении к атомам. Иначе говоря обладает направленностью.
Например, молекула водорода.
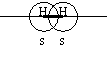
В образовании σ связи могут принимать участие и р-электроны. Например: HF

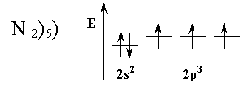

Пи связь и сигма неравноценны, т.к. энергия из разрыва различна.
Водородная связь
Межмолекулярные взаимодействия
Ориентационные силы притяжения возникают между полярными молекулами (диполь-диполь взаимодействие). Эти силы возникают между полярными молекулами. Индукционные взаимодействия — это взаимодействие между полярной молекулой и неполярной. Неполярная молекула поляризуется из-за действия полярной, что и порождает дополнительное электростатическое притяжение.
Особый вид межмолекулярного взаимодействия — водородные связи.
Водородные связи — это межмолекулярные (или внутримолекулярные) химические связи, возникающие между молекулами, в которых есть сильно полярные ковалентные связи — H-F, H-O или H-N. Если в молекуле есть такие связи, то между молекулами будут возникать дополнительные силы притяжения.
Механизм образования водородной связи частично электростатический, а частично — донорно–акцепторный. При этом донором электронной пары выступают атом сильно электроотрицательного элемента (F, O, N), а акцептором — атомы водорода, соединенные с этими атомами. Для водородной связи характерны направленность в пространстве и насыщаемость.
Водородные связи возникают между следующими веществами:
Водородная связь оказывает влияние на физические и химические свойства веществ. Так, дополнительное притяжение между молекулами затрудняет кипение веществ. У веществ с водородными связями наблюдается аномальное повышение тепературы кипения.
Водородная связь
Водородная связь весьма распространена и играет важную роль в биологических объектах. Рассмотрим ее образование подробнее.
Образование водородной связи
При возникновении подходящих условий водородная связь возникает самопроизвольно.
Какие же условия приводят к возникновению водородной связи?
Можно предположить, что в любом ряду веществ с молекулами одинаковой формы и полярности температуры плавления и кипения должны повышаться прямо пропорционально возрастанию молекулярной массы, однако существуют некоторые несоответствия.
На следующем рисунке приведены кривые зависимости температуры кипения гидридов элементов 6 группы от молекулярной массы.
Так, для гидридов элементов 6 группы наблюдается последовательное увеличение температур кипения и плавления с увеличением молекулярной массы (номера периода), но из этой закономерности выпадает вода.
В 5 группе аномально высокие температуры кипения и плавления наблюдаются у аммиака NH3, а в 7 группе – у HF, по сравнению с гидридами элементов соответствующих групп.
Почему вода, аммиак и фтороводород имеют аномально высокие температуры кипения и плавления?
Это связано с присутствием в воде, аммиаке и фтороводороде водородных связей.
Водородная связь — это внутри- или межмолекулярная связь, которая образуется с соединениях между атомами водорода и атомами, имеющими большую электроотрицательность (N, O, F).
Механизм образования водородной связи, вследствие электростатического притяжения атомов — электростатический. Но частично он также носит донорно–акцепторный характер.
Образуемые соединения имеют большую полярность, возникает диполь. Атом водорода находится на положительном конце диполя. Этот диполь может взаимодействовать с неподеленной электронной парой кислорода (и азота, и фтора), который принадлежит другой или этой же молекуле. Таким образом, донором электронной пары являются атомы F, O или N, а акцептором — атомы водорода.
Графически, на рисунках, водородная связь обозначается тремя точками:
Виды водородной связи
Характеристика водородной связи
Водородная связь характеризуется
N-H···Y ˂ O-H···Y ˂ F-H···Y
Т.е., связь тем прочнее, чем меньше размер атома с неподеленными парами — N, O, F и больше его электроотрицательность. Среди них более прочную водородную связь образует тот, неподеленная электронная пара которого менее сильно притягивается к своему ядру.
Водородная связь в химии — как и где образуется, свойства, примеры
Водородная связь встречается во всех областях химии и проявляется в виде межмолекулярного или внутримолекулярного взаимодействия особых групп, одна из которых обязательно содержит реакционно-способный атом водорода с положительным зарядом. Это глобальное явление, называемое также H-связью, отличается от других объединений химических частиц тем, что образуется самопроизвольно в подходящих условиях, а не в результате направленного воздействия.
Характерные особенности
Этот тип связи возникает в молекулах, когда их атом водорода, поляризованный положительно, взаимодействует с атомом другой молекулы, имеющим заряд отрицательный. Расстояние между атомами-участниками процесса должно оказаться меньше, чем сумма их радиусов. Выделяют два вида H-связей:
Энергия H-связи обладает низкими прочностными характеристиками: она в несколько раз ниже, чем у остальных подобных взаимодействий. Это позволяет ей существовать промежуточным звеном между основными химическими связями (ковалентной, ионной и металлической) и силами притяжения и отталкивания Ван-дер-Ваальса, стремящимися удержать частицы в твёрдом или жидком состоянии. Кристаллические решётки с молекулами в узлах — характерная особенность веществ с водородной связью. Примеры можно привести различные:
Механизм образования водородной связи считается смешанным — одновременно электростатическим и донорно-акцепторным. Решающая роль в этом принадлежит повышению электроотрицательности одного атома (A), позволяющей оттягивать в свою сторону электронную пару другого атома (H), принимающего участие в этом взаимодействии. В результате:
Образовавшиеся атомы водорода, заряд которых частично положителен, обладают способностями притягивать другие молекулы, содержащие электроотрицательные группы. Эти электростатические взаимодействия и обуславливают появление Н-связей, для формирования которых необходимы три обязательных элемента:
Такое донорство в обычных условиях никогда не осуществляется на все 100%. Атом-донор остается химически связанным с водородом. Графически это обозначается в виде линии из точек, указывающей, что сила взаимодействия слабее ковалентной связи. Схема записи структуры выглядит следующим образом: Б ··· Нd+ — Аd-.
Только три химических элемента полностью проявляют донорские способности, и их атомы поставляют протоны для образования Н-связей: азот (N), кислород (O) и фтор (F). В атомах-акцепторах недостатка не наблюдается. Низкомолекулярным соединениям H-связь придаёт способность в обычных условиях иметь жидкое агрегатное состояние, как это происходит у этанола (C2H5OH), метанола (CH3OH) и воды (H2O), или становиться сжижающимися при охлаждении газами — аммиаком (NH3) и гидрофторидом (HF).
Проявление в неорганической химии
Определение «водородная связь» появилось в 1920 году. Его применили учёные Латимер и Родебуш для объяснения сущности аномалий, наблюдавшихся при кипении воды, предельных одноатомных спиртов и жидкого фтороводорода. При сопоставлении точек кипения в ряду водородсодержащих родственных соединений Н2O (вода), Н2S (сероводород), Н2Se (селеноводород) и Н2Te (теллуроводород) обнаружилось, что первый участник этого списка (H2O) переходит из жидкости в пар гораздо раньше, чем можно было бы ожидать, следуя закономерности, которой подчиняются остальные члены. Истинное значение точки кипения воды оказалось на 200° C выше ожидаемого.
Это справедливо и для другого ряда — NH3 (аммиак), PH3 (фосфин), H3As (арсин), Н3Sb (стибин), где фактическая (-33 °C) температура кипения аммиака на 80 градусов превышает ожидаемую. Если считать, что молекулы в жидкости удерживаются исключительно Ван-дер-Ваальсовыми силами, разрушающимися при переходе в газообразную фазу, то эти скачки не должны наблюдаться, а объяснить их невозможно.
Неожиданные повышения температур кипения привели к выводам о присутствии дополнительно связывающих молекулы сил, изменяющих физические свойства. Водородной связи принадлежит роль в создании аномальных температур кипения спиртов, если их сравнивать с аналогами без гидроксильных групп (-ОН). В перечне заслуг H-связей не только изменение точек кипения веществ, но и упрочнение их кристаллических решёток, вызывающее повышение температур плавления, поверхностного натяжения и вязкости.
Например, борная кислота с формулой H3BO3 имеет слоистую триклинную кристаллическую решётку, где каждая из молекул посредством H-связей крепится к трём другим. В результате образуются плоские слои, которые за счёт межмолекулярных связей создают кристаллическую структуру — «паркет» из шестиугольников.
При помощи инфракрасной спектроскопии сегодня можно достоверно выявить любой тип межмолекулярного взаимодействия: группы с Н-связями заметно отличаются по спектральным характеристикам от остальных случаев. Исследования структуры вещества помогают измерить дистанцию между водородом и атомом-акцептором, сравнить её с суммой радиусов и, если первое значение не превышает второе, доказать существование явления.
Понятие водных кластеров
Земля — чемпион по содержанию воды среди других планет Солнечной системы. Моря и океаны, реки и озёра, средние глубины которых достигают 6 тыс. метров, занимают 70% земной поверхности, а в областях полюсов сосредоточились огромные запасы влаги в виде снегов и льдов.
Трудно переоценить влияние воды на возникновение и существование жизни на нашей планете. Это связано с особенностями, нехарактерными для соединений, считающихся её близкими аналогами. Только вода находится в жидком и твёрдом состоянии при условиях, в которых водородные соединения серы или селена с большей атомной массой становятся газообразными.
Присутствие H-связей в молекулах воды обуславливает образование водных кластеров или комплексов, а димеры воды служат их простейшими примерами. Энергия их водородных связей ненамного больше энергии броуновского движения при нормальных условиях, но сильно отличается от мощности ковалентных связей в гидроксильных группах, а они в 200 раз превышают тепловые показатели. Вода из простой жидкости превращается в сложную, «связанную» сетью H-связей, хотя они относительно слабы и неустойчивы, самопроизвольно возникают и исчезают при температурных изменениях.
Кристаллическая структура льда имеет объёмную сетку из этих связей, и молекулы H2O расположены так, чтобы атомы водорода одних молекул оказывались направленными к атомам кислорода соседей. В ледяном кристалле между молекулами обязательно присутствуют пустоты, их объёмы немного превышают размеры отдельных молекул воды. Именно благодаря таким «карманам» плотность льда меньше, чем у его жидкой фазы, а гигантские айсберги остаются дрейфовать на поверхности, в то время как замерзание большинства других веществ существенно увеличивает их плотность.
Водородные связи сообщают воде уникальную характеристику, обеспечивающую существование разнообразных форм жизни в областях, где окружающие температуры опускаются ниже нуля. Если на минуту представить, что лёд начнёт тонуть в воде, то моря зимой рано или поздно промёрзнут до самого дна, и рыбы будут обречены на вымирание. Люди могли бы растапливать лёд для получения живительной влаги, но это потребует больших энергозатрат.
Ещё одно проявление H-связей — голубая окраска чистой воды в её толще. Колебание одной молекулы воды вызывает движение соседних частиц, соединенных с ней водородными связями. Красные лучи из состава солнечного спектра будут расходоваться на поддержание этих колебаний, поскольку больше всего соответствуют им энергетически. Происходит фильтрация красных лучей — их энергия поглощается и рассеивается в виде тепла колеблющимися молекулами.
Начинает проступать голубой участок спектра, уравновешивающий отсутствие красного. Вода самостоятельно окрасится в волшебный небесный цвет. Для этого необходимо, чтобы солнечные лучи прошли через двухметровую толщу чистой воды и потеряли достаточное количество красного спектра.
Значение для органических соединений
Многие органические вещества не могут растворяться в воде. Но если это происходит, то процесс не обходится без активного участия H-связей. Кислород и азот, главные доноры протонов, часто играют роли акцепторов. Органические соединения, содержащие O и N, легко растворяются в воде: здесь кислород и азот выступают в качестве атомов-акцепторов, а атомом-донором является кислород из молекул воды. Возникающие H-связи перемещают органическое вещество в раствор, «растаскивая» его на молекулы.
Просматривается эмпирическая закономерность: органическое соединение будет легко растворяться в воде, если в составе его молекул на каждый атом кислорода приходится не более 3 атомов углерода. Например, бензол C6H6 в воде растворяется плохо, но замена одной группы (-СН) на (-N) даёт пиридин С5Н5N, смешивающийся с водой в любых пропорциях.
Для неводных растворов, в которых растворителями служат органические вещества, тоже характерны H-связи. В них водород частично положительно поляризован, а поблизости обнаруживается молекула с сильным акцептором — чаще всего это бывает кислород. Жирные кислоты приобретают полезную способность растворяться в хлороформе HCCl3, а растворённый в ацетоне ацетилен получил важное техническое применение. Горючий газ C2H2 под давлением чувствителен к сотрясениям и взрывоопасен, но его растворение в ацетоне C3H6O позволяет безопасно хранить и транспортировать любые объёмы.
Трудно переоценить роль H-связей в прочных полимерных и биополимерных структурах. Целлюлоза (клетчатка древесины) в строении молекулы располагает гидроксильные группы по бокам полимерной структуры, в которой чередуются циклические фрагменты. Невысокая энергия единичной Н-связи, умноженная на количество по всей длине молекулярной цепи, вызывает в итоге мощное притяжение. Из-за этого целлюлозу можно растворить только в высокополярных растворителях — дигидроксотетрааммиакате меди, известном как реактив Швейцера.
Карбонильные (=C=O) и аминогруппы (-NH2) в расположенных рядом полимерных цепочках капрона и нейлона тоже образуют связи этого типа и увеличивают механическую прочность веществ, поскольку в полиамидных структурах создаются кристаллические фрагменты. Аналогично ведут себя полиуретаны и белки: витки белковых спиралей закрепляются всё теми же H-связями, возникающими при взаимодействии функциональных групп.
Полимерная макромолекула ДНК — хранилище запасов информации о живом организме, зашифрованной в чередующихся фрагментарных циклах. Их карбонильные и аминогруппы имеют четыре типа азотистых оснований (аденин A, гуанин G, тимин T, цитозин C) и располагаются в форме боковых ответвлений по длине молекулы. От порядка их чередования зависят индивидуальные особенности всего живого на планете. Взаимодействия пар в составе аминогруппы и атома азота дают начало множеству Н-связей, которые удерживают 2 молекулы ДНК в виде классической двойной спирали.
ЧИТАТЬ КНИГУ ОНЛАЙН: Шпаргалка по неорганической химии
НАСТРОЙКИ.
СОДЕРЖАНИЕ.
СОДЕРЖАНИЕ
Ольга Владимировна Макарова
Шпаргалка по неорганической химии
1. Материя и ее движение
Материя – это объективная реальность, обладающая свойством движения. Все существующее есть различные виды движущейся материи. Материя существует независимо от сознания человека. Материя существует либо в виде вещества, либо в виде поля.
Движение материи – постоянное ее взаимодействие, а также изменения состояния объектов, вызванные этими взаимодействиями. Формы движения материи различны. Пример формы движения материи: нагревание и охлаждение тел, излучение света, электрический ток, химические и физические превращения, жизненные процессы. Классификация форм движения материи:
Неживую природу характеризует взаимосвязь физической и химической форм движения, живую – биологическая, а общество – социальная форма движения. Одни формы движения материи способны переходить в другие. Например: механическое движение переходит в тепловое, тепловое – в химическое, химическое – в электрическое. Возможен и обратный переход. Взаимопереход форм движения материи подтверждает единство и связь всех ее форм. В этом явлении отражен основной закон природы – закон вечности материи и ее движения:
1) ни один вид материи и ни одна форма движения не могут быть получены из ничего и превращены в ничто;
2) материя и ее движение неуничтожимы и несотворимы – вечно изменяясь, они вечно существуют.
Материя не может существовать вне движения, она всегда находится в состоянии движения, изменения и развития. При уничтожении движения объект прекращает свое существование, переходит в другие объекты, которым характерно движение покоя – состояния движений, обеспечивающих стабильность предмета, сохраняя его качества. Покой относителен, а движение абсолютно – это неотъемлемое свойство материи. Структурные уровни материи:
Развитие материи – переход одного качества в другое, направленное формирование новых типов организации, рождающихся из предшествующих им типов. Две разновидности процессов развития:
1) процессы качественных превращений, в рамках соответствия вида материи, определенного уровня ее организации;
2) процессы перехода от одного уровня к другому.
Свойства и движение материи – предмет изучения естествознания. Оно изучает взаимные превращения, модификации и развитие конкретных видов материи, выявляет закономерности этих явлений и связь между ними. Изучение свойств и закономерностей материи позволяет управлять природными явлениями в нужном направлении и руководить ими в полном объеме.
2 Вещества и их изменение. Предмет неорганической химии
Вещества – виды материи, дискретные частицы которых имеют конечную массу покоя (сера, кислород, известь и т. д.). Из веществ состоят физические тела.
Каждое вещество имеет определенные физические свойства: агрегатное состояние (жидкое, твердое, газообразное), температуру плавления, кипения, замерзания, плотность, растворимость. Агрегатное состояние может переходить из одного в другое. Величины, количественно отражающие свойства веществ называются физическими константами. Различают чистые вещества (сера, железо, дистиллированная вода) и смеси (природная вода, содержащая соли, сплавы). Смеси называют по веществу, преобладающему в их составе. В природе абсолютно чистых веществ не встречается. Если количество примесей ничтожно мало, то вещество считается условно чистым. Чистое вещество однородно, смеси бывают однородные и неоднородные. Однородные смеси – смесь двух или нескольких веществ, которые не обнаруживаются при помощи аппаратуры (смеси газов, многие жидкости, например, кровь, сплавы).
Различают простые и сложные вещества. Вещества, состоящие из атомов одного вида, называются простыми (S – сера, C – графит, O2 – кислород, H2 – водород, все металлы). Вещества, состоящие из атомов разного вида, называются сложными (Н2О – вода, СО2 – углекислый газ, Н2SO4 – серная кислота).
Вещества подвержены различным изменениям. Явления, сопровождающиеся коренными изменениями вещества, при которых из одних веществ образуются другие, называются химическими (Fе (железо) + S (сера) = FеS (сульфид железа)), что является предметом изучения неорганической химии. Предметом неорганической химии является изучение химических элементов и образуемых ими простых и сложных веществ (кроме соединений углерода, составляющих предмет органической химии), превращений веществ, сопровождающихся изменениями его состава, свойств и (или) строения. Неорганические вещества, или минеральные – вещества, встречающиеся в неживой природе (песок, сера, минералы, графит).
Неорганическая химия связана с другими разделами химии – аналитической, коллоидной, кристаллохимией, физической, термодинамикой, электрохимией, радиохимией, химической физикой ; на стыке неорганической и органической химии лежит химия металло-органических соединений и элементооргани-ческих соединений. Неорганическая химия соприкасается с геолого-минералогическими науками : геохимией и минералогией, а также с техническими науками – химической технологией (ее неорганической частью), металлургией и агрохимией.
3. Закон сохранения массы. Основное содержание атомно- молекулярного учения
Атомно-молекулярное учение разработал М.В. Ломоносов в 1741 г. Основные положения закона:
1) все вещества состоят из «корпускул» (молекул);
2) молекулы состоят из «элементов» (атомов);
3) частицы – молекулы и атомы – находятся в непрерывном движении. Тепловое состояние тел есть результат движения их частиц;
4) молекулы простых веществ состоят из одинаковых атомов, а молекулы сложных веществ – из различных атомов. Атомно-молекулярное учение окончательно утвердилось в 1860 г.
То есть из двух молекул бромида калия и одной молекулы хлора (т. е. в общем из трех молекул) образовалось 2 молекулы хлорида калия и одна молекула брома (т. е. образовалось три молекулы), 3 = 3. Из одной молекулы водорода и одной молекулы хлора – 2 молекулы хлороводорода. А масса веществ до и после реакции не претерпевает изменений, т. к. атомы имеют постоянную массу. Масса веществ, вступивших в химическую реакцию, равна массе веществ, образующихся в результате реакции. В 1789 г. независимо от Ломоносова этот же закон изложил французский ученый и химик Лавуазье. Он также экспериментальным путем получил неопровержимое доказательство закона, проведя опыты с многими реакциями. Закон сохранения массы веществ Ломоносов связывал с сохранением энергии. Он рассматривал эти законы с точки зрения всеобщего закона природы. Закон сохранения массы веществ и закон сохранения энергии – единые законы природы – законы вечной материи и ее движения. Взаимосвязь массы и энергии выражается уравнением