Мраморная кожа что это
Что такое мраморная болезнь и причины мраморности кожи у детей
Мраморная кожа у младенца редкое явление. Но каждым родителям, которым довелось столкнуться со зрелищем, когда у их чада кожные покровы покрыты красно-фиолетовой сеточкой, пришлось пережить немало тревог, прежде чем они выяснили причину такой аномалии. Излишне паниковать при обнаружении мраморности кожи у грудничка не стоит, но и источник такой реакции эпидермиса все же выяснить нужно. Виновником мраморности кожных покровов может быть как физиологические, так и патологические процессы кровеносной системы ребенка. И если о физиологических причинах возникновения мраморности кожи у новорожденных волноваться не стоит, то патологическое состояние понадобится лечить. Исследуем, что представляет собой мраморная болезнь, ее симптомы, причины и лечение.
Чем отличается мраморная болезнь и мраморность эпидермиса у младенцев
Мраморное заболевание опорно-двигательного характера обусловлено генетической аномалией, которая выражается в избыточном формировании костной ткани.
Мраморность кожи грудных детей ― это уже совсем другая патология и связана она с разбалансировкой сосудистой системы. Причины мраморности кожи у ребенка могут быть физиологическими либо патологическими. От этого зависит, нужно ли лечить малыша от сосудистой патологии или мраморная кожа у грудничка является временным явлением.
Физиологические причины мраморной кожи у детей
Иногда, ввиду особенности физиологии, конкретный ребенок имеет сосудистую систему, которая располагается близко к поверхности кожных покровов. Помимо этого, мраморная кожа у ребенка может быть следствием несовершенной терморегуляции. Поэтому когда изменяется температура окружающей среды в особенности в сторону похолодания, у младенца может наблюдаться мраморность кожных покровов. Особенно выражено просматривается рисунок в периферической зоне кровообращения, то есть на ногах и руках малыша.
В числе вероятных причин возникновения мраморности кожи у младенца педиатры также отмечают переедание. Если новорожденный ест грудного молока или детской смеси больше, чем требует его возраст, тогда объем крови умножается. Недостаточно окрепшей капиллярной системе не хватает тонуса, чтобы справиться с большим объемом кровотока, а кожа у новорожденного очень тонкая.
Все эти факторы приводят к тому, что капиллярная сетка становится видимой.
Дети, предрасположенные к проявлениям мраморности на коже:
Еще одной причиной мраморности кожи у ребенка является наследственность. Если один из родителей или тем более оба имеют вегетососудистые нарушения, то ребенку с большой степенью вероятности может передаться по наследству это патологическое состояние. Вегетососудистая дистония ― это не заболевание, а скорее синдром. ВСД может сопровождать человека всю жизнь, выражаясь в нервно-гуморальном расстройстве сердечно-сосудистой системы.
Особенного лечения вегетососудистая дистония не требует, понадобится приучить ребенка с самого раннего возраста к здоровому образу жизни и питания. Помогут правильный распорядок дня, закаливание и спортивные мероприятия. Мраморность кожных покровов у крохи первых месяцев жизни должна самостоятельно исчезнуть по достижению им полугодовалого возраста. Если мраморный сосудистый рисунок не проходит, то это является красноречивым признаком наличия сердечной или сосудистой патологии. Но лучше, конечно, не дожидаться шести месяцев, чтобы проверить пройдет мраморная кожа или нет, а заранее удостовериться у врача в причинах подобной сосудистой реакции организма.
Патологические причины мраморности кожи у ребенка
Физиологическую мраморность кожных покровов младенца лечить не требуется. Если в помещении прохладно, то достаточно растереть кожу малютки либо потеплее его одеть, чтобы тон кожного покрова восстановился. В случае, когда причиной появления сосудистого рисунка на теле крохи, стал перекорм, нужно просто уменьшить порции еды или увеличить промежутки между кормлением и все пройдет. Но когда вне зависимости от вышеперечисленных мероприятий симптомы мраморной кожи у новорожденного не исчезают, то стоит повнимательней изучить свое чадо на предмет обнаружения у него признаков сердечно-сосудистой патологии.
Тревожные симптомы патологической мраморности кожных покровов ребенка:
Эти симптомы могут указывать на следующие патологии:
В ситуации, когда мраморность кожных покровов у новорожденного связана с патологиями, понадобится определить конкретный источник проблемы. Лечащим врачом должно быть назначено полное обследование грудничка.
А по результатам тщательного исследования организма младенца, обязательно назначение индивидуальной терапии.
Чаще всего причиной множества патологий является кислородная недостаточность во внутриутробном развитии или асфиксия, возникающая при сложных и затяжных родах. Даже непродолжительная гипоксия во время беременности или нехватка кислорода при длительной родовой деятельности, способны привести к непредсказуемым неврологическим расстройствам у ребенка, в том числе и к сосудистым нарушениям в виде мраморной кожи.
Если причина мраморности кожных покровов в физиологии младенца, то задачей родителей является позаботиться о полноценном формировании сосудистого тонуса у своего ребенка. Это предназначение легко осуществимо, благодаря регулярному проведению массажных манипуляций, частым и продолжительным прогулкам на свежем воздухе, умеренным закаливаниям, плаванию и прочим полезным мероприятиям. Важно помнить, что крепкий иммунитет и здоровые привычки, заложенные с детства, вознаградят усилия родителей в течение всей полноценной жизни их чада.
Мраморная болезнь: симптомы, лечение
Мраморная болезнь – патология, противоположная остеопорозу. Характеризуется излишней плотностью кости и склерозным поражением костного мозга. Достаточно редко встречается, но так как малоизученна – тяжело поддается лечению. Опасна патологическими перелома
ДОСТУПНЫЕ ЦЕНЫ НА КУРС ЛЕЧЕНИЯ
Мягко, приятно, нас не боятся дети
ДОСТУПНЫЕ ЦЕНЫ НА КУРС ЛЕЧЕНИЯ
Мягко, приятно, нас не боятся дети
Мраморной болезнью (остеопетрозом или врожденным семейным остеосклерозом) называют редкое наследственное заболевание, которое проявляется излишним уплотнением костных тканей скелета, недостаточным кровообразованием в костном мозгу и патологическими переломами. Эта болезнь противоположна остеопорозу.
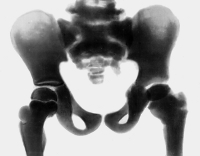
Для остеосклероза характерно утолщение костных трабекул и компактного вещества, в результате чего на рентгеновских снимках кость выглядит менее прозрачной, а губчатое вещество имеет узкопетлистую структуру.
Впервые заболевание было исследовано и описано в 1904 году. Распространенность патологии в Европе, как и во всем мире, не более 1 случая на 100-200 тыс. человек. Однако у чувашей, татар и марийцев вероятность рождения ребенка с остеопетрозом в несколько раз выше.
Этиология
Нормальный рост и развитие костей происходит при участии остеобластов (клеток, отвечающих за формирование костных тканей) и остеокластов (клеток, которые разрушают костные ткани). До конца механизм развития патологии медиками еще не изучен. Известно, что число остеокластов у пациентов с мраморной болезнью может быть уменьшено, увеличено или находиться в норме, но их функциональность в любом случае нарушена.
Нарушение костной резорбции происходит из-за дефицита фермента карбоангидразы, который вызывает дефекты протоновой помпы остеокластов. Таким образом, продолжающееся костеобразование на фоне замедленного или нарушенного разрушения кости приводит к чрезмерному уплотнению костных тканей.
До сих пор известны только генетические причины развития патологии. Причем родители могут быть носителями мутантного гена без проявления симптомов мраморной болезни, а дети наследуют дефект по аутосомно-рецессивному признаку.
В некоторых случаях может встречаться физиологический остеосклероз. Он характерен для подросткового возраста или периодов интенсивного роста организма, когда отмечаются некоторые изменения в составе костных тканей в области ростковых зон. Через некоторое время баланс остеокластов и остеобластов восстанавливается, а подобное состояние не имеет ничего общего с патологическим остеопетрозом.
Симптомы
Несмотря на повышенную плотность костных тканей, у пациентов все равно наблюдается излишняя хрупкость костей и склонность к патологическим переломам. Чаще всего это повреждения бедренных костей. Сращивание происходит практически своевременно, но в некоторых случаях может наблюдаться замедление консолидации из-за склероза костномозгового канала и неучастия в процессе остеогенеза костного эндоста.
Другие симптомы мраморной болезни:
Кроме того, избыточное разрастание костных тканей может стать причиной компрессии нервных корешков или спинного мозга, стеноза спинномозгового канала, и, следовательно, парезов или параличей конечностей или слепоты.
Диагностика и лечение
Первоначальная диагностика мраморной болезни проводится по рентгенографическим снимкам, на которых видно непрозрачные участки с небольшими склеротическими вкраплениями. Далее выявляется наличие патологии у ближайших родственников. Общий и биохимический анализ крови укажет на анемию и содержание в ней ионов кальция и фосфора.
КТ или МРТ исследование поможет установить локализацию патологических процессов и степень поражения костей. Дифференциальное диагностирование позволит размежевать мраморную болезнь и заболевания, сопровождающиеся остеопетрозом: рахит, лимфогранулематоз, болезнь Педжета, опухоли различной этиологии или метастазы и пр.
Консервативные методы лечения мраморной болезни предусматривают прием кортикостероидов, гамма-интерферона, эритропоэтинома. В раннем детском возрасте при развитии осложнений возможна терапия витамином D. Рекомендуется постоянное наблюдение у ортопеда, своевременное выявление и лечение осложнений (анемии, деформации позвоночника и осанки, пр.). При сильном поражении остеокластов проводиться трансплантация костного мозга.
В профилактических целях желательно полноценное качественное питание, физиотерапевтические процедуры, ЛФК, для укрепления мышц и нервной системы, закаливание, плавание. Не повредят организму ежегодные курсы массажа, мануальной терапии, санаторно-курортного лечения.
Для детей, страдающих мраморной болезнью, очень важно обеспечить комфортное существование: ортопедическую корпусную и мягкую мебель, специализированную ванну с низкими бортиками, регулируемое автомобильное кресло или инвалидную коляску и пр.
Мраморная болезнь – это редкое наследственное заболевание, при котором наблюдается уплотнение костей скелета и закрытие костномозговых каналов плотной костной тканью. Обычно впервые проявляется в детском возрасте. Сопровождается утомляемостью при ходьбе и болями в конечностях. Возможны патологические переломы. Из-за закрытия костномозговых каналов развивается анемия, сочетающаяся с увеличением печени и селезенки. Могут наблюдаться деформации скелета, задержка прорезывания зубов, нарушения зрения из-за сдавления зрительного нерва. Диагноз устанавливается на основании объективных данных, результатов рентгенографии и других исследований. Лечение симптоматическое, в большинстве случаев консервативное.
МКБ-10
Общие сведения
Мраморная болезнь (болезнь Албертса-Шенберга, остеопетроз, гиперостотическая дисплазия, врожденный остеосклероз, врожденный семейный диффузный остеосклероз) – редкое наследственное заболевание, сопровождающееся уплотнением костей скелета и уменьшением костномозгового пространства. Заболевание впервые описано в 1904 году немецким врачом Альбертс-Шенбергом. В среднем выявляется у 1 ребенка на 200-300 тыс. новорожденных, однако в некоторых этногенетических группах количество больных может увеличиваться. Так, в Чувашии симптомы болезни обнаруживаются у 1 ребенка из 3,5 тыс., в Мари-Эл – у 1 ребенка из 14 тыс. Такая высокая частота заболеваемости обусловлена особенностями этногенеза коренных жителей этих республик. Лечение мраморной болезни осуществляют травматологи-ортопеды.
Причины
Мраморная болезнь передается по аутосомно-рецессивному типу. Причиной изменения структуры костей являются глубокие нарушения фосфорно-кальциевого обмена и дисбаланс между разрушением старой костной ткани и образованием новой. В результате корковый слой кости утолщается, костномозговое пространство сужается вплоть до полного исчезновения. Развивается прогрессирующий остеосклероз, кости становятся очень плотными и, одновременно, хрупкими. Из-за закрытия костномозговых каналов возникает гипопластическая анемия, сопровождающаяся компенсаторным увеличением лимфатических узлов, печени и селезенки.
Патанатомия
При патологоанатомическом исследовании кости больного мраморной болезнью тяжелые, плохо распиливаются, но легко раскалываются. На распиле обнаруживается поверхность с гладкой структурой, по виду напоминающая отшлифованный мрамор. Остеосклеротические изменения развиваются преимущественно за счет эндоста. При этом могут наблюдаться разрастания периоста, из-за которых на поверхности костей образуются участки не плотного, как в норме, а губчатого костного вещества. Костномозговые каналы трубчатых костей сужены или полностью замещены плотной костной тканью. Патологические процессы сильнее выражены в зонах роста. Особенно яркие изменения выявляются в верхней трети большеберцовой и плечевой костей, а также в нижней трети бедренной и лучевой костей – эти отделы «вздуваются» и приобретают колбовидную форму.
Губчатая ткань плоских костей (позвонков, ключиц, черепа) замещается плотным костным веществом. Из-за разрастания костной ткани череп может увеличиваться и деформироваться. Сужение отверстий для выхода черепно-мозговых нервов становится причиной прогрессирующего ухудшения зрения и нарастающей тугоухости. Из-за неравномерной перестройки кортикального слоя и образования шероховатостей на внутренней поверхности черепа могут возникать эпидуральные, реже – субдуральные кровоизлияния.
При проведении гистологического исследования выявляется увеличение массы и нарушение архитектоники костного вещества. Костные клетки беспорядочно нагромождены и образуют характерные округлые слоистые структуры, неравномерно располагающиеся в областях энхондрального роста. Из-за накопления таких структур архитектоника кости нарушается, кость пациента с мраморной болезнью становится менее прочной, неспособной переносить обычные нагрузки.
Симптомы мраморной болезни
Заболевание может выявляться у женщин и мужчин любого возраста – от младенческого до старческого. Однако чаще симптомы мраморной болезни появляются в детском возрасте. В ряде случаев процесс протекает бессимптомно, и уплотнение костей становится случайной находкой при проведении рентгенологического исследования по поводу другого заболевания или травмы.
Выраженность клинической симптоматики при мраморной болезни, как правило, зависит от времени появления первых признаков. Раннее начало влечет за собой более грубые изменения со стороны различных органов и систем. При развитии мраморной болезни в первые годы жизни у детей выявляется гидроцефалия, возникающая вследствие уплотнения и разрастания костей основания черепа. Пациенты отстают в росте, поздно начинают ходить, часто страдают от нарушений слуха и зрения. Характерно также позднее прорезывание зубов и повышенная склонность к развитию кариеса.
При более позднем развитии мраморной болезни причиной обращения к специалистам в сфере травматологии и ортопедии становится утомляемость при ходьбе и боли в конечностях. Иногда мраморная болезнь диагностируется после патологического перелома. Чаще страдают бедренные кости, переломы обычно поперечные, возникают при незначительном травматическом воздействии, срастаются в обычные сроки (за исключением переломов шейки бедренной кости, при которых сращения не происходит). В некоторых случаях в области перелома развивается остеомиелит. При одонтогенной инфекции может возникать остеомиелит нижней челюсти. При осмотре физическое развитие пациента, как правило, в норме. В некоторых случаях выявляются деформации конечностей: варусное искривление верхних отделов бедренных костей, галифеобразная деформация голеней и т. д.
Диагностика
Для уточнения диагноза назначают рентгенологическое исследование плоских и трубчатых костей: рентгенографию черепа, рентгенографию позвоночника, рентгенографию бедер и т. д. На всех снимках выявляется резкое уплотнение костной ткани. Эпифизарные отделы трубчатых костей закруглены и утолщены, в области метафизов определяются булавовидные утолщения. Все кости непрозрачны для рентгеновского излучения, кортикальный слой и костномозговой канал не просматриваются. Иногда в метафизарных областях обнаруживаются участки поперечного просветления.
Уменьшение или закрытие костномозговых каналов становится причиной недостаточности кроветворения. У пациентов с мраморной болезнью развивается гипохромная анемия различной степени выраженности. Кожа бледная, возможны жалобы на головокружения, слабость, утомляемость. При осмотре выявляется компенсаторное увеличение лимфоузлов, гепатомегалия и спленомегалия. В крови определяется лимфоцитоз с появлением незрелых форм – нормобластов. Мутации в генетическом материале устанавливаются с помощью молекулярно-генетического тестирования.
При подозрении на нарушения деятельности различных органов пациентов с мраморной болезнью направляют на соответствующие исследования. При изменениях со стороны системы кроветворения назначают консультацию гематолога, общий анализ крови и УЗИ органов брюшной полости, при ухудшении зрения – консультацию офтальмолога, обзорную рентгенографию орбиты в двух проекциях, оптические и электрофизиологические исследования, при нарушении слуха – консультацию отоларинголога, аудиометрию и исследование слуховых вызванных потенциалов.
Лечение мраморной болезни
Патогенетической терапии не существует. Проводится симптоматическое лечение, направленное на укрепление нервной и костно-мышечной системы. Пациентам рекомендуют употреблять в пищу продукты, богатые витаминами (натуральные соки, творог, свежие фрукты и овощи), выдают направления на массаж, ЛФК и санаторно-курортное лечение. При анемии назначают препараты железа, проводят поддерживающую витаминную терапию, в тяжелых случаях производят переливания эритроцитарной массы.
При патологических переломах осуществляют стандартные лечебные мероприятия: репозицию, наложение гипса или скелетного вытяжения и т. д. При переломах шейки бедра выполняют эндопротезирование тазобедренного сустава. При выраженной деформации костей голеней производят корригирующую остеотомию. Лечение остеомиелита проводят по стандартной схеме, включающей в себя антибиотикотерапию, иммобилизацию, дезинтоксикационные мероприятия, стимуляцию иммунитета, вскрытие и дренирование гнойников.
Прогноз и профилактика
При своевременном предупреждении и адекватном лечении осложнений прогноз при мраморной болезни обычно благоприятный за исключением злокачественных форм с ранним началом и поражением миелогенной ткани. Летальный исход наступает в результате нарастающей анемии или септикопиемии при остеомиелите, возникшем вследствие патологического перелома или одонтогенной инфекции. Профилактика не разработана.
Синдром Рейно
Синдром Рейно (СР) — это эпизодическое нарушение периферической циркуляции вследствие локальной артериальной вазоконстрикции (спазм) дигитальных артерий и кожных сосудов в ответ на воздействие холода или эмоциональный стресс. Клинически синдром проявляет
Синдром Рейно (СР) — это эпизодическое нарушение периферической циркуляции вследствие локальной артериальной вазоконстрикции (спазм) дигитальных артерий и кожных сосудов в ответ на воздействие холода или эмоциональный стресс. Клинически синдром проявляется резко очерченными изменениями цвета кожи пальцев кистей. В основе повышенного спазма сосудов лежит дефект центральных и локальных механизмов регуляции вазомоторных реакций.
Распространенность СР в общей популяции составляет 3–5% и различается между отдельными климатическими зонами [1]. Заболевание начинается преимущественно в подростковом или молодом возрасте и у женщин встречается чаще, чем у мужчин. Наблюдается тенденция к семейной агрегации заболевания.
Выделяют первичный и вторичный СР. Первичный, или идиопатический, СР характеризуется спазмом пальцевых артерий и терморегуляторных сосудов кожи при воздействии холода, без каких-либо признаков поражения сосудов. При вторичном СР наблюдается сочетание синдрома Рейно с симптомами других заболеваний.
Наиболее часто при СР поражаются кисти рук. Основным клиническим признаком СР является последовательная смена окраски кожи пальцев кистей на холоде. В начале приступа вазоспазма обычно появляется бледная окраска кожи, после чего в течение нескольких минут кожа приобретает синевато-фиолетовый оттенок. Вазоспазм обычно длится 15–20 мин и завершается быстрым восстановлением кровотока, о чем свидетельствует интенсивно розовая окраска кожи (реактивная гиперемия).
У некоторых больных приступы вазоспазма сопровождаются ощущением замерзания кистей, онемением и покалыванием в пальцах, которые проходят после восстановления кровотока. В фазе реактивной гиперемии больные могут чувствовать боль в пальцах кистей.
На ранних этапах заболевания изменения цвета кожи могут наблюдаться на дистальной фаланге одного или нескольких пальцев кистей. В дальнейшем область поражения охватывает все пальцы кистей и, возможно, стоп, при этом большие пальцы обычно остаются интактными. Вазоспазму могут подвергаться также сосуды кожи лица и других участков. В этих случаях можно наблюдать характерные изменения окраски кончика носа, губ и ушных раковин, а также кожи над коленными суставами. У отдельных больных в процесс вовлекаются и сосуды языка, что проявляется дизартрией во время приступа вазоспазма. При эпизодах вазоспазма может появляться мраморный рисунок на верхних и нижних конечностях — симптом, называемый сетчатым ливедо (livedo reticularis). Частота и продолжительность эпизодов вазоспазма могут варьировать как у различных больных, так и у одних и тех же пациентов в разное время года (зимой более интенсивные, чем летом).
Трехфазная перемена окраски кожи (побеление–посинение–покраснение) выявляется не во всех случаях; у части больных наблюдается двухфазное или однофазное изменение цвета. В зависимости от количества фаз изменения цвета кожи, выделяют достоверный и вероятный СР.
Более чем у 80% больных выявляется первичный СР. Для верификации первичного СР применяются диагностические критерии, предложенные E. V. Allen и G. E. Brown в 1932 г. и модифицированные в последние годы. Эти критерии, разработанные с учетом клинических и некоторых лабораторных показателей, а также результатов капилляроскопии ногтевого ложа, включают [2]:
Средний возраст развития СР составляет 14 лет; только у 27% больных болезнь дебютирует в возрасте старше 40 лет [3]. При первичном СР симптомы болезни обычно умеренно выражены, и только у 12% больных наблюдаются интенсивные эпизоды вазоспазма [4]. Приблизительно у 1/4 больных СР выявляется среди родственников первой линии [5].
Вместе с тем при большом числе состояний и заболеваний, ассоциирующихся с СР, он считается вторичным (таблица).
Наиболее часто вторичный СР ассоциируется с системной склеродермией, системной красной волчанкой, другими заболеваниями соединительной ткани, гематологическими нарушениями и приемом некоторых лекарств. При длительном наблюдении за больными, которым был поставлен предварительный диагноз первичного СР, удалось выявить, что у 13% из них на определенном этапе болезни развиваются признаки системного заболевания соединительной ткани (наиболее часто — системной склеродермии) [6].
Несмотря на идентичность клинических проявлений первичного и вторичного СР, при этих двух состояниях имеются некоторые различия в отдельных признаках. На вероятность вторичного характера СР указывают следующие признаки:
Вторичный СР развивается обычно в возрасте старше 30 лет, отличается более выраженными и болезненными эпизодами вазоспазма, структурными изменениями капилляров [7]. АНФ имеет относительно низкую прогностическую ценность для заболеваний соединительной ткани (30%), тогда как выявление специфических аутоантител значительно повышает вероятность вторичного характера СР [6, 8, 9]. Приблизительно у 15–20% больных СР, у которых выявляются специфические аутоантитела и/или капилляроскопические изменения, но отсутствуют симптомы заболеваний соединительной ткани, в дальнейшем (обычно в течение двух лет) развивается то или иное заболевание соединительной ткани [10, 11].
У всех больных со впервые выявленным СР необходимо проводить специальные исследования с целью дифференциальной диагностики первичного и вторичного характера патологии.
В первую очередь следует уточнить:
Необходимо учитывать, что клинические признаки ассоциированного с СР заболевания могут развиться по истечении нескольких месяцев или лет после начала СР. Наиболее объективным и специфичным инструментальным методом дифференциальной диагностики первичного и ассоциированного с системными заболеваниями соединительной ткани (прежде всего с системной склеродермией) СР является капилляроскопия ногтевого ложа. В норме капилляроскопическая картина представляет собой правильный ряд равномерно распределенных по краю ногтевого ложа и одинакового размера капилляров. При системной склеродермии, с которой наиболее часто ассоциируется СР, изменения количества капилляров (редукция) и их размеров (дилатация) появляются на ранних стадиях и часто предшествуют развитию клинических признаков заболевания.
Дифференциальная диагностика СР
Повышенная чувствительность к холоду характерна для популяции в целом. Холодная кожа или неочерченная крапчатость кожи пальцев, кистей и конечностей считаются нормальным ответом на воздействие холода. У больных СР, помимо повышенной чувствительности, под влиянием холода эпизодически наблюдаются побледнение и цианоз дистальных отделов пальцев. СР следует отличать от акроцианоза — состояния, характеризующегося продолжительным цианозом кистей или стоп, который усиливается под влиянием холода.
Повышенную чувствительность к холоду могут вызвать карпальный туннельный синдром и другие невропатии. При дифференциальной диагностике следует учитывать такие состояния, как криопротеинемии, диспротеинемии, контакт с поливинилхлоридом, наличие опухоли или гипотиреоза. Если признаки заболевания проявляются асимметрично, необходимо провести исследования для выявления окклюзивных заболеваний крупных сосудов. Атеросклероз не сопровождается типичными симметричными признаками СР, но в ряде случаев проявляется перемежающейся хромотой при нагрузках, асимметричным поражением конечности, изолированной или персистирующей дигитальной ишемией. Васкулиты, эмболии или другие окклюзивные поражения сосудов могут приводить к критической ишемии, но не к развитию типичного СР. Имеются доказательства того, что СР может служить клиническим проявлением генерализованных вазоспастических заболеваний, таких как стенокардия Принцметал и мигрень [12].
Сетчатое ливедо наблюдается также при васкулитах, антифосфолипидном синдроме и окклюзивных заболеваниях периферических сосудов, при которых, в отличие от СР, этот признак имеет устойчивый характер.
На замерзание конечностей, их онемение и покалывание довольно часто жалуются больные с заболеваниями периферических сосудов, сопровождающимися снижением кровотока и ишемией. При СР, в отличие от заболеваний периферических сосудов, указанные симптомы наблюдаются только во время вазоспазма и полностью проходят после восстановления исходного кровотока.
Лечение СР
Общие рекомендации для больных первичным и вторичным СР:
Соблюдения указанных рекомендаций часто бывает достаточно для лечения больных первичным СР.
Дигитальные артерии и терморегуляторные сосуды кожи находятся преимущественно под симпатическим адренергическим контролем. Эмоциональный стресс может спровоцировать дигитальный вазоспазм, а состояние тревоги часто усиливает индуцированные холодом атаки Рейно [13]. В таких случаях бывает полезным назначение седативных средств. Важно избегать применения препаратов, которые могут вызвать вазоконстрикцию (симпатомиметики, клонидин, эрготамин, агонисты серотониновых рецепторов и др.). Курение может редуцировать пальцевой кровоток, вследствие чего больным СР следует отказаться от этой привычки.
Медикаментозное лечение СР
В случаях частых и продолжительных эпизодов вазоспазма при первичном СР и у больных вторичным СР необходимо назначение лекарственной терапии. Для лечения СР применяют препараты с вазодилатирующим действием или средства, влияющие на реологические свойства крови.
Блокаторы кальциевых каналов
Блокаторы кальциевых каналов обладают наибольшим вазодилатационным потенциалом. Препаратами выбора являются дигидропиридиновые производные — нифедипин, амлодипин, исрадипин и фелодипин. Обладающий кратковременным действием нифедипин в разовой дозе 10–20 мг при 3-кратном ежедневном приеме значительно уменьшает частоту и выраженность, а в некоторых случаях и продолжительность эпизодов вазоспазма [15]. Однократный прием 5–20 мг нифедипина достаточно эффективно предупреждает индуцированный холодом вазоспазм при приеме за 15–20 мин до воздействия холода. При назначении нифедипина наблюдается достоверное повышение кожного и мышечного кровотока [16]. Приблизительно у 1/3 больных на фоне приема нифедипина развиваются побочные эффекты, среди них наиболее часто встречаются артериальная гипотония, головная боль, гиперемия, тахикардия, отеки голеней. Уменьшение побочных эффектов возможно при назначении ретардных форм нифедипина в суточной дозе 20–40 мг [17]. У больных первичным СР, по сравнению со вторичным, терапевтический эффект препарата обычно проявляется в большей степени. При длительном приеме нифедипина в больших дозах возможны парестезии, боли в мышцах, а также развитие толерантности и уменьшение лечебного действия препарата.
Наряду с нифедипином, в лечении СР с успехом применяются и другие производные дигидропиридина — амлодипин, исрадипин и фелодипин, которые относятся к длительно действующим препаратам [18]. Амлодипин назначается один раз в день в дозе 5 мг, при недостаточном эффекте суточная доза может быть повышена до 10 мг. Наиболее распространенным побочным эффектом амлодипина является отек лодыжек. Исрадипин назначается в дозе 2,5 мг 2 раза в день. Побочные эффекты в виде головных болей и гиперемии обычно носят умеренно выраженный характер. Фелодипин применяют в дозе 10 мг 1 раз в сут, преимущественно в виде лекарственных форм, обеспечивающих постепенное высвобождение лекарственного вещества. Блокаторы кальциевых каналов подавляют активацию тромбоцитов, что также оказывает благоприятное действие при СР [19].
При наличии противопоказаний или непереносимости блокаторов кальциевых каналов для лечения СР применяются вазодилататоры других лекарственных групп.
Назначение симпатолитических препаратов обосновано тем, что адренергическая стимуляция играет важную роль в вазоконстрикции. Празозин достоверно уменьшает выраженность и частоту вазоспазма у больных с первичным СР [20].
Простагландины оказывают комплексное физиологическое воздействие, в частности речь идет о вазодилатации, антиоксидантном действии, подавлении агрегации тромбоцитов и др.
Алпростадил (вазапростан) при ежедневных в/в инфузиях 20–40 мкг препарата в 200 мл изотонического раствора NaCl в течение 15–20 дней достоверно уменьшает как частоту, так и интенсивность вазоспазма у больных с первичным и вторичным СР [21].
Илопрост уменьшает число атак в неделю и интенсивность вазоспазма у больных первичным и вторичным (ассоциированным с системной склеродермией) СР в среднем на 39 и 35% соответственно [22].
Пентоксифиллин обладает антиагрегационным и слабым вазодилатационным действием. Назначается в комбинации с другими сосудорасширяющими препаратами на длительное время.
В лечении СР применяется ряд вазодилататоров (нитроглицерин трансдермальный, гидралазин, папаверин, миноксидил), которые могут быть эффективными у отдельных больных. Однако частое развитие побочных эффектов (системная гипотензия, головная боль) ограничивает применение этих препаратов. Результаты исследований эффективности ингибиторов ангиотензинпревращающего фермента у больных СР весьма противоречивы, в настоящее время препараты этой группы не нашли широкого применения в клинической практике.
Ксантинола никотинат назначается в таблетках по 150 мг 3 раза в день. Длительность приема, с учетом переносимости и противопоказаний к его назначению (как и других препаратов никотиновой кислоты), устанавливается индивидуально и определяется эффективностью и переносимостью средства.
Лекарственная терапия СР имеет некоторые ограничения, включая недостаточный ответ, развитие толерантности при длительном применении, развитие ряда побочных эффектов, многие из которых становятся причиной отмены того или иного препарата. При неэффективности консервативной терапии с целью уменьшения проявлений СР возможно хирургическое лечение — локальная дигитальная симпатэктомия. Однако продолжительность и ожидаемая выраженность лечебного эффекта симпатэктомии до сих пор не уточнены, в связи с чем их трудно прогнозировать. Предполагаемая эффективность симпатэктомии может быть оценена в дооперационный период с помощью фармакологической симпатэктомии.
В большинстве случаев СР представляет собой заболевание, характеризующееся благоприятным прогнозом и стабильным течением. В дебюте заболевания, особенно при наличии факторов риска вторичного характера СР, все больные СР подлежат диспансеризации и врачебному осмотру один раз в год. Пациенты должны быть предупреждены о необходимости дополнительного визита к врачу при появлении новых симптомов, указывающих на возможное развитие заболеваний, с которыми наиболее часто ассоциируется СР, прежде всего системных заболеваний соединительной ткани.
По вопросам литературы обращайтесь в редакцию.
Р. Т. Алекперов, доктор медицинских наук
Институт ревматологии РАМН, Москва