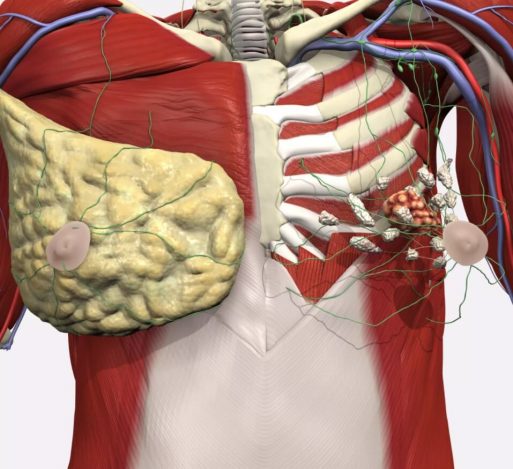
Мультифокальный рост опухоли молочной железы что это
Мультифокальный рост опухоли молочной железы что это
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздравсоцразвития России
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздрава России
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздрава России
Московский научно-исследовательский онкологический институт им. П.А. Герцена; Кафедра онкологии и радиотерапии ФПП ОВ Первого Московского государственного медицинского университета им. И.М. Сеченова
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздрава России
Современные подходы к лечению больных с карциномой in situ молочной железы
Журнал: Онкология. Журнал им. П.А. Герцена. 2013;2(4): 30-33
Пак Д. Д., Усов Ф. Н., Фетисова Е. Ю., Волченко А. А., Ефанов В. В. Современные подходы к лечению больных с карциномой in situ молочной железы. Онкология. Журнал им. П.А. Герцена. 2013;2(4):30-33.
Pak D D, Usov F N, Fetisova E Iu, Volchenko A A, Efanov V V. Current treatment options for breast carcinoma in situ. P.A. Herzen Journal of Oncology. 2013;2(4):30-33.
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздравсоцразвития России
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздравсоцразвития России
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздрава России
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздрава России
Московский научно-исследовательский онкологический институт им. П.А. Герцена; Кафедра онкологии и радиотерапии ФПП ОВ Первого Московского государственного медицинского университета им. И.М. Сеченова
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздрава России
По оценкам экспертов ВОЗ, в мире ежегодно выявляется от 800 000 до 1 млн новых случаев рака молочной железы (РМЖ). В структуре заболеваемости злокачественными новообразованиями (ЗНО) женского населения России РМЖ в 2010 г. занимал 1-е место (20,5%), как и в структуре смертности от РМЖ (1-е место — 17,2%). При этом число впервые выявленных случаев ЗНО молочной железы увеличилось с 49 548 случаев в 2005 г. до 57 241 в 2010 г. [1].
Благодаря развитию диагностических методов и внедрению скрининговых программ частота выявления карциномы in situ (CIS) молочной железы в некоторых странах составляет 15—25% от всех случаев впервые выявленного РМЖ [2, 3].
Согласно международной классификации по системе TNM, CIS относится к стадии 0, а первичная опухоль кодируется как Тis.
По данным исследований, CIS может достигать 5—10 см, а иногда и более без признаков инвазии [4].
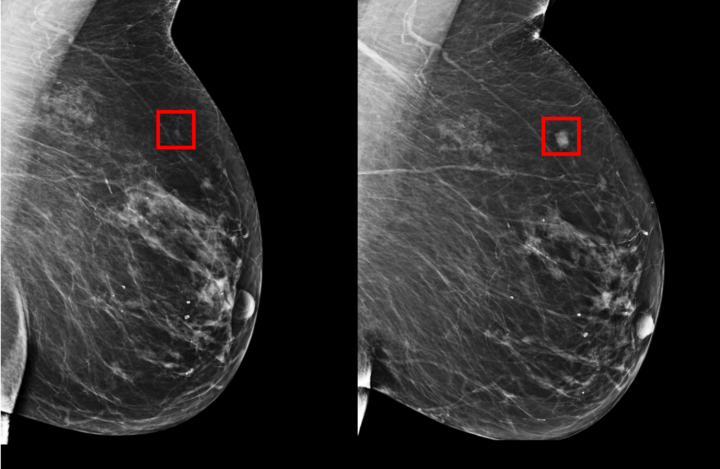
Для диагностики CIS молочной железы применяются маммография, ультразвуковое исследование (УЗИ). Магнитно-резонансную томографию (МРТ) следует применять для диагностики в сочетании с другими методами [5], особенно при планировании органосохраняющего лечения. При маммографическом исследовании протоковая CIS (DCIS) в 72% случаев проявляется только очагами микрокальцификации, чаще сгруппированными (реже рассеянные), в 12% случаев микрокальцификация сочетается с очагом уплотнения и в 6% DCIS протекает рентгенологически бессимптомно. Микрокальцификация при дольковой CIS (LCIS) наблюдается намного реже и в 60% случаев кальцификации подвергается не сама опухоль, а окружающие ткани, иногда на большом протяжении [4].
В план обследования больных с узловой патологией молочных желез обязательно должна входить пункционная биопсия. При подозрении на CIS необходимо проводить трепанобиопсию, позволяющую получить столбик ткани, достаточный как для гистологического, так и для иммуногистохимического исследования. В настоящее время наиболее информативный материал можно получить путем вакуумной биопсии аппаратом Маммотом. Этот метод позволяет при однократном введении инструмента в зону очага (узловое образование, скопление микрокальцинатов) многократно получать биопсийный материал.
После биопсии обязательно выполняют маркировку зоны, где находились непальпируемые образования и микрокальцинаты, титановой клипсой, что облегчат работу хирурга в случае последующего оперативного вмешательства. При невозможности проведения толстоигольного или вакуумного забора тканей выполняют ножевую биопсию со срочным гистологическим исследованием.
К сожалению, во многих регионах Российской Федерации практически остается нерешенной проблема диагностики непальпируемых форм РМЖ, в том числе и CIS. У большинства больных неинвазивные формы РМЖ являются случайной находкой, поэтому очень важно правильно выбрать стратегию при подозрении на клинически скрыто протекающую карциному. При этом необходим четкий алгоритм диагностических мероприятий для выявления потенциально излечимых форм РМЖ. На основании полученных нами данных разработан алгоритм обследования больных (см. рисунок). 
Диагноз DCIS требует немедленного лечения, так как выживаемость при DCIS может составлять до 100% [2, 6], а при отсутствии лечения частота развития инвазивного заболевания достигает 30% [2].
Наиболее эффективным методом лечения CIS остается хирургическое вмешательство. При этом объем оперативного вмешательства различен. В последние десятилетия подходы к хирургическому этапу лечения изменились в сторону уменьшения объема удаляемых тканей без нарушения радикализма. Все чаще при данном заболевании применяется органосохраняющее лечение, чему в немалой степени способствует использование адъювантной лучевой терапии (ЛТ) [7], снижающей риск локорегионарных рецидивов на 50% [8, 9]. Органосохраняющее лечение в сочетании с адъювантной ЛТ дает результаты, эквивалентные мастэктомии, в то время как отказ от адъювантной ЛТ значительно повышает риск местного рецидива [10, 11].
Однако, по данным некоторых исследований, можно отказаться от проведения адъювантной ЛТ при органосохраняющем лечении у пациентов с DCIS при отсутствии комедонекроза в опухоли (или его наличии и размере менее 1,5 см при условии широкого иссечения), размере очага менее 2 см в диаметре и расстоянии от края опухоли более 2 см [12]. Для проверки этих данных нужны рандомизированные исследования.
Проведены многочисленные исследования, направленные на выявление достоверных факторов возможного рецидива после первичного лечения DCIS По данным мировой литературы (мультивариантный анализ), молодой возраст (менее 40 лет), размер DCIS более 1,5 см и отказ от адъювантной ЛТ — факторы плохого прогноза в отношении развития локорегионарных рецидивов [7, 13]. При этом молодой возраст и положительный край резекции рассматриваются как важные факторы риска для развития местного рецидива даже при органосохраняющем лечении в сочетании с ЛТ [9]. Микропапиллярный гистологический тип опухоли, наличие комедонекроза и мультифокального и мультицентрического роста являются факторами неблагоприятного прогноза для развития ипсилатерального рецидива и, в ряде случаев, развития рака в контралатеральной молочной железе [13—15]. При этом выделение комедокарциномы в отдельный гистологический тип является неверным, в настоящее время рассматривается наличие или отсутствие комедонекроза в опухоли [16]. Такие факторы, как гиперэкспрессия HER2/neu и высокая пролиферативная активность опухоли (Ki-67+) DCIS, также ассоциируются с более высоким риском развития рецидива при органосохраняющем лечении DCIS [11]. Ожирение может быть связано с неблагоприятными биологическими особенностями и худшим прогнозом при инвазивном РМЖ. По данным исследований, для пациенток с DCIS такой связи не прослежено, ИМТ более 30 никак не влияет на прогноз [17].
В качестве оценки лучшего подхода к комплексному лечению при DCIS университетом Южной Калифорнии в 1996 г. был разработан и введен в практику прогностический индекс Van Nuys (VNPI) [18]. В 2003 г. он был дополнен [19] (табл. 1).
При расчете риска возможного рецидива учитываются следующие признаки: размер опухоли, ширина краев резекции, степень гистологической злокачественности, возраст. По данным исследований M.J. Silverstein и соавт. [18, 19], у пациенток при индексе 4—6 баллов лечение можно ограничивать только удалением опухоли. При индексе 7—9 баллов органосохраняющее лечение должно быть дополнено адъювантной ЛТ или рекомендуется повторная операция в случае отступа от края опухоли менее 10 мм. При индексе 10—12 баллов отмечен чрезвычайно высокий риск рецидива при органосохраняющем лечении даже в сочетании с ЛТ. В этом случае должна быть выполнена мастэктомия, по возможности с реконструкцией [19]. По результатам последних исследований, у больных с DCIS после мастэктомии при индексе 4—9 баллов рецидивов не отмечалось в течение 12 лет, в то время как при 10—12 баллах за то же время рецидивы были отмечены в 9,6% случаев. В группе риска по развитию локального рецидива находятся пациентки молодого возраста, мультифокальный и мультицентрический рост опухоли [13].
В настоящее время не выявлены четкие показания к биопсии сторожевого лимфатического узла у пациенток с DCIS в связи с крайне редким поражением регионарных лимфатических узлов при данном заболевании. Некоторые исследования показывают, что биопсия сторожевого лимфатического узла представляется целесообразной при опухолях более 2,5 см с гиперэкспрессией HER2/neu (как часть первичной хирургической процедуры) [20].
У больных с DCIS следует применять системную терапию. В настоящее время известно, что применение тамоксифена для ЭР + DCIS снижает риск рецидива [10]. Пациентки с ЭР + DCIS должны получать тамоксифен в адъювантном режиме [21].
При выявлении LCIS рекомендуется наблюдение в течение всей жизни либо хирургическое лечение. Наиболее приемлемым объемом оперативного вмешательства является тотальная мастэктомия с последующей реконструкцией молочной железы [4].
Материал и методы
В отделении общей онкологии МНИОИ им. П.А. Герцена в 1994—2011 гг. проведено лечение 108 больным с CIS молочной железы. Средний возраст больных составил 48,3 года. Частота выявления CIS составила 1,5%.
Чаще неинвазивный рак поражал левую молочную железу — в 55,6% случаев, правую — в 44,4% наблюдений. На этапе обследования диагноз CIS установлен только в 1,9% случаев по результатам гистологического исследования материала, полученного при вакуумной биопсии аппаратом Маммотом.
Результаты
При морфологическом исследовании у 93 (86,1%) больных выявлен протоковый рак, у 8 (7,4%) — дольковый и у 7 (6,5%) — сочетание протокового и долькового рака. Монофокальный рост опухоли выявлен у 58 (54%) больных, мультифокальный — у 35 (31,7%), мультицентрический — у 15 (14,3%). При протоковом раке чаще встречался монофокальный и мультифокальный рост опухоли, а при дольковом — мультицентрический. Метастазы в подмышечных лимфатических узлах обнаружены у 4,6% больных. Местный рецидив выявлен в 4 (3,7%) случаях. Пятилетняя выживаемость в первой группе составила 100%, безрецидивная выживаемость — 96,3%. Данные об объеме хирургических вмешательств представлены в табл. 2.
Заключение
Прогнозируя результаты органосохраняющего лечения при CIS следует помнить, что характерной особенностью протоковой формы заболевания является мультифокальное распространение опухолевого роста, т.е. в пределах одного сегмента поражается 1—2 протока. При дольковой CIS чаще встречаются множественные зачатки опухоли в разных отделах молочной железы (нередко в противоположной молочной железе). Органосохраняющие операции в объеме субтотальной резекции или подкожной мастэктомии с одномоментной реконструкцией являются адекватными для хирургического лечения больных с неинвазивными формами РМЖ, а также важными этапами социальной и психологической реабилитации женщин.
В данном случае полное или почти полное удаление тканей молочной железы является очень важным этапом органосохраняющего комбинированного лечения больных РМЖ.
Рак молочной железы — всё, что вы хотели узнать
По данным Всемирной организации здравоохранения рак молочной железы является наиболее распространённым видом рака: в 2020 г. было зарегистрировано свыше 2,2 миллиона случаев этого заболевания.
В то же время рак молочной железы является и главной причиной смерти женщин от онкологических заболеваний. Встаёт закономерный вопрос: почему, если выявленный на ранний стадии рак может быть излечим?
Основная проблема в том, что болезнь на столь ранней стадии или не имеет или имеет мало клинических проявлений, часто у женщины на приёме у врача жалоб нет.
С целью выявления бессимптомных ранних форм рака и предраковых заболеваний были созданы программы скрининга. Скрининг – это в данном случае комплексное врачебное обследование здоровых женщин с определённым временным интервалом.
В странах с развитыми программами скрининга (раннего выявления заболевания у бессимптомных женщин) рака груди и стандартизированными подходами к лечению и ведению данных пациентов по данным ВОЗ удалось добиться 40% (!) снижения смертности с 80-х гг, т.е. смертность снизилась почти в 2 раза.
На пути к визиту к врачу часто встаёт незнание, страх диагноза и результатов и процесса последующего лечения, многие вспоминают результаты лечения родственниц в 80-90-е гг. например, перенёсших мастэктомию по Холстеду (когда полностью удаляются молочная железа, сосково-ареолярный комплекс, большая и малая грудные мышцы, а также клетчатка подмышечной, подлопаточной и подключичной зон вместе со всеми лимфоузлами. Эта операция считалась прорывом в лечении рака груди. В дальнейшем она уступила место более прогрессивным методам хирургического вмешательства, не предполагающим столь обширного иссечения тканей.
При своевременном выявлении предраковых заболеваний груди, можно избежать или предупредить развитие рака.
Обнаруженное же на более поздней стадии онкологическое заболевание груди требует в 2,5 раза чаще проведения химиотерапии и в 3,5 раза чаще женщинам приходится удалять всю грудь (матэтомия).
Спасение и высокое качество жизни пациентки с раком груди в данном случае комплексная работа самой пациентки (редко пациента, т.к. болезнь может развиваться и у мужчин) и команды врачей.
В центрах сети «РЭМСИ Диагностика Рус» есть необходимые методы диагностики для выявления заболеваний груди (УЗИ, Маммография, МРТ с в\в контрастным усилением). Записаться на обследование и узнать больше информации можно по телефону.
В случае семейной предрасположенности к раку груди, при подтверждении носительства BRCA1/BRCA2 онкогенов или в случае радиационного воздействия на грудь, возрастом начала ежегодного обследования следует считать 30 лет, целесообразно добавить к УЗИ МРТ маммографию с в\в контрастированием в протокол обследования. Необходимо знать, что у молодых женщин (возрастная группа до 40 лет) молочная железа имеет довольно плотное строение, на фоне которого затруднительно выявить тканевые образования по данным маммографии (это типы строения C(3) или D(4) в зависимости от классификаций, которыми пользуется врач), в этом случае можно использовать комбинацию УЗИ + МРТ с в/в контрастным усилением или УЗИ + маммография (поиск микрокальцинатов) +МРТ с в/в контрастным усилением.
Маммография, усиленная опцией томосинтеза поможет избежать как пропуск мелкого образования, так и предупредит гипердиагностику.
МРТ исследование БЕЗ контрастирования для выявления злокачественной опухоли малоинформативно.
Когда рекомендуется дополнить к «золотой» стандарту (УЗИ + маммографии) методом МРТ с в/в контрастированием?
В России проведение скрининговых обследований молочных желёз осуществляется в рамках приказа М3 РФ от 13.03.2019 № 124н «Об утверждении порядка проведений профилактического медицинского осмотра и диспансеризации определённых групп взрослого населения» у женщин в возрасте 40-75 лет включительно — подробнее Вы можете уточнить у вашего участкового врача.
Возможно для знания о том как правильно относится к заболеваниям молочной железы Вам будет удобнее воспользоваться схемой маршрутизации пациентов приведённой проф. Рожковой Н.И.:
1. Самообследование молочных желёз (ежемесячно)
2. Клиническое обследование у врача-специалиста (осмотр и пальпация) –не реже 1 раза в 2 года
3. Для женщин в возрастной группе от 19 до 39 лет:
Анкетирование на предмет выявления повышенных факторов риска развития рака груди:
4. Если по результатам вышеописанного обследования у женщин выявлены изменения в молочных железах или среди всех женщин возрастной группы от 39 до 75 лет:
4.1. Если по результатам вышеописанного обследования женщина попала в категорию «Здоровая» — Маммография не реже один раз в 2 года (УЗИ) (даже при отсутствии жалоб)
4.2. Если по результатам вышеописанного обследования женщина попала в категорию «Мастопатия» — консервативное лечение у маммолога
4.3. Если по результатам вышеописанного обследования женщина попала в категорию «узловые образования» — дальнейшее обследование в территориальном онкологическом диспансере у онкомаммолога с применением инвазивных технологий (с биопсией). При раке-иммуногистохимия, специализированное лечении, мониторинг.
Подробнее о методиках, показаниях, подготовке к исследованиям, времени процедуры
Все методы диагностически ценны, отражают разные аспекты изменений, дополняют друг друга и позволяют создать целостнее представление о болезни.
Маммография
Маммография наиболее широко распространённый метод лучевой диагностики заболеваний молочной железы. Во время этой процедуры специальный прибор — маммограф — получает изображения вашей молочной железы под разными углами. Минимально необходимым является выполнение минимум 2 снимков для каждой молочной железы (в прямой и косой медиолатеральной (в переводе на обычный язык боковой под углом) проекциях).
Исследование проводят на 5-9 день менструального цикла (считать надо с первого дня последней менструации), в менопаузу в любой день.
Во время проведения маммографии грудь уплощается и сдавливается между двумя прозрачными пластинами в течение нескольких секунд, пока лаборант получает картинку, в наших центрах. Лаборант выполняет несколько снимков под разными углами. Не беспокойтесь, если он сделает дополнительные снимки, в некоторых ситуациях это необходимо для уточняющей диагностики.
Обратите внимание, что следует сообщить лаборанту о наличии родинок, шрамов, или врождённого втяжения соска груди и попросить зафиксировать этот факт в сопровождающей медицинской документации или внести эти данные в анамнестическую анкету, которая выдаётся перед исследованием.
В день проведения маммограммы нельзя использовать дезодорант или минеральную косметику/мази/кремы для груди, потому что порошок, присутствующий в их составе, создаёт на изображении груди дополнительные тени, похожие на признаки рака — микрокальцинаты. Если вы уже использовали дезодорант, следует салфеткой тщательно его убрать в пределах не затронутых им тканей, эту манипуляцию можно провести в дамской комнате или в процедурной перед исследованием.
Если вы делали маммографию раньше в другом мед учреждении, стоит взять с собой снимки/снимки на цифровых носителях и копии прошлых протоколов или попросить переслать их по почте в медицинский центр. Сравнение новых и старых изображений помогают точнее выявить минимальные изменения в Вашей груди, оценить возрастные особенности и эффект от лечения.
Продолжительность процедуры в среднем составляет: 15 мин
Томосинтез молочных желёз
Метод трёхмерно визуализации и рентгенологического послойного изучения структуры, по данным исследований на 25% повышает возможности дифференциальной диагностики ряда заболеваний на самых ранних стадиях развития.
Методика проведения аналогична маммографии.
Показания:
Продолжительность процедуры в среднем составляет: 15 мин.
В МЦ РЭМСИ на пл. Конституции — томосинтез включён в каждое маммографическое исследование
УЗИ молочных желёз
Продолжительность процедуры в среднем составляет: 15 мин.
Показания:
МРТ — маммография с контрастным усилением
Обратите внимание к процедуре есть противопоказания к которым относится наличие электронных имплантируемых устройств и нефиксированных ферромагнитных металлических объектов в организме или отягощённый аллергоанамнез (подробнее с противопоказаниями можно ознакомиться по ссылке).
Исследование проводят на 5-9 день менструального цикла (считать надо с первого дня последней менструации), в менопаузу в любой день.
Зубные импланты и маточные спирали к противопоказаниям не относятся- с ними МРТ молочных желёз проходить можно.
МРТ исследование БЕЗ контрастирования для выявления злокачественной опухоли малоинформативно.
Показания:
Продолжительность процедуры в среднем составляет: 50 мин.
Результаты диагностики
По итогам обследования в наших центрах диагностические находки в молочных железах относятся к определённой категории согласно международным стандартам Breast Imaging Reporting And Data System (BI-RADS):
Категория – 2 — доброкачественные изменения – подразумевающие плановое обследование у врача 1 раз в 1 или 2 года
Категория – 3 – возможно, доброкачественные изменения, требуют врачебного контроля через короткий промежуток времени – 1.5 или 3 или 6 месяцев на усмотрение лечащего врача
Категория – 6 — морфологически верифицированные случаи рака молочной железы-лечение у онкомаммолога
При разных методах исследования используются свои шкалы и оценки по данным УЗИ, МРТ, Маммографии могут не совпадать. Для суммарной оценки используется максимальное значение BI-RADS категории, выявленное любым методом, для каждой молочной железы.
Если на ранних стадиях рак молочной железы практически не имеет симптомов. Как же его можно выявить?
Попробуем разобраться с наиболее частыми вопросами:
Что может сделать/определить пациентка/пациент самостоятельно?
На что стоит обратить свое внимание?
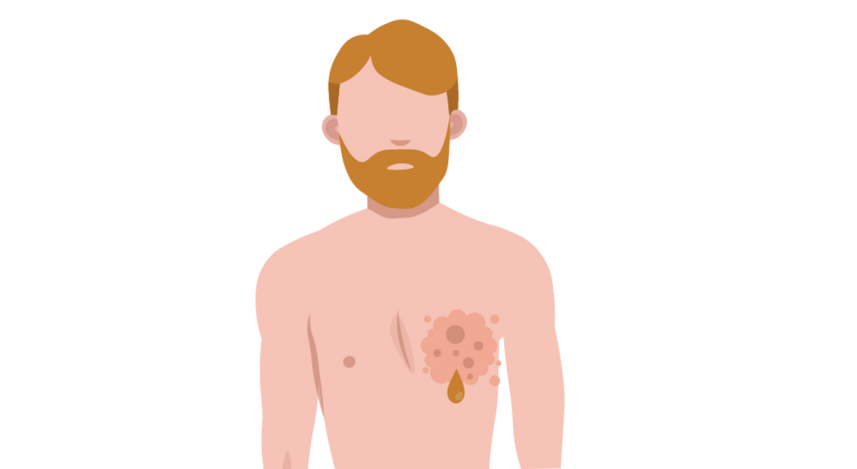
В шутливой форме основные симптомы заболевания груди изображены на популярной картинке ниже:
Здесь важна регулярность самоосмотра или самообследования молочных желёз.
Каждая женщина или мужчина из группы высокого риска (об этих группах речь несколько ниже) должна выполнять ежемесячное самообследование молочной железы. Для женщин с сохранённой менструацией следует проводить его на 7-10день менструального цикла (подсчёт с первого дня менструации), для женщин в менопаузе и постменопаузе достаточно выделить любое число месяца.
Проводить самообследование необходимо в комфортных для себя условиях и в спокойном состоянии.
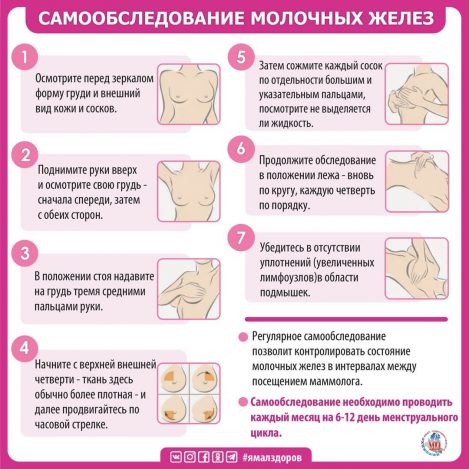
Вначале следует осмотреть внутреннюю поверхность бюстгальтера или белья на предмет выделений. Затем посмотреться в зеркало и оценить форму, цвет и симметричность груди, оценить не отмечается ли фиксация или смещение одной из молочных желёз в сторону, сжать соски и проверить наличие выделений из них.
Далее, это удобнее делать в душе, можно приступать к методике самообследования «самоощупывания» груди.
Обратите внимание, что обследование левой молочной железы проводится правой рукой, а правой – левой рукой. Ощупывание следует проводить подушечками 2,3 или 2-4 пальцев, а не их кончиками, круговыми проникающими движениями. Большой палец при этом не участвует.
Здесь есть несколько подходов, можно выбрать тот, что нравится именно Вам.
В любом случае руку на стороне той груди, которую будете ощупывать, следует положить за голову.
Далее можно разделить железу на 4 квадрата по линиям проходящим через сосок : на верхние/нижние/наружные/внутренние и последовательно ощупывать одинаковые квадраты разных желёз по очереди, сравнивая их структуру с противоположной стороной или же можно двигаться по спирали по направлению к соску. Важно ощупать пространство под соском, т.к. это зона у женщин чувствительна, часто этот шаг пропускается, им не стоит пренебрегать. Не забудьте ощупать подмышку на предмет уплотнений.
Часто выявленные изменения имеют доброкачественное происхождение, их своевременное выявление позволяет предотвратить развитие рака груди.
Однако если вас стойко что-то встревожило следует немедленно обратиться к врачу маммологу или гинекологу, сообщить о своих тревогах.
Оцените наличие/отсутствие факторов повышенного риска развития рака молочной железы
К наиболее значимым факторам повышенного риска развития рака груди относят:
При наличии каких-либо из этих факторов риска следует обратиться к врачу который поможет более точно определить вероятностные группы риска(низкий/умеренный/высокий) и разработать/ обсудить дальнейшую стратегию наблюдения за состоянием Вашей груди, также рекомендуется посетить школу репродуктивного здоровья для большей информированности.
К какому врачу обращаться?
При первичном обращении или при мастопатиях можно выбрать: предпочтительнее маммолога или же гинеколога.
При диагнозе узлового образования в груди или после лечения рака молочной железы для мониторинга рецидива — к онкомаммологу.
Врач – маммолог более профессионально сможет оценить состояние вашей груди, оценить наличие или отсутствие повышенных факторов риска развития рака груди, обсудить возраст начала профилактического обследования (в некоторых случаях существуют определённые предпочтения), при необходимости дать направление на генетическое тестирование.
Изменение режима питания, коррекция веса
Научные изыскания подтвердили, что в обычных фруктах и овощах содержаться вещества, способные снизить образования в женском организме потенциального опасного метаболита С-16.
Рационально выстроенный пищевой рацион способен снизить риск возникновения или рецидива опухолевого процесса.
Подробнее выбрать индивидуальную программу можно с врачом –диетологом/нутрициологом.
Строго следить за весом, стараясь поддерживать его на оптимальном соответствующем вашему росту, телосложению и возрасту уровне.
Истощение также вредно Вашему организму!
Общие рекомендации:
Носите удобное белье, которое не травмирует\деформирует грудь, следите за весом, занимайтесь физической активностью, высыпайтесь, больше радуйтесь, помните гормоны удовольствия опосредованно укрепляют противоопухолевую защиту организма.
При наличии высоких факторов повышенного риска развития рака груди, информируйте о них гинеколога, в случае обсуждения возможностей гормональной контрацепции-это может повлиять на выбор препарата.
Какова вероятность того, что у мужчины разовьётся рак молочной железы?
По оценкам исследователей, рак молочной железы у мужчин составляет примерно 1 процент всех диагнозов РМЖ в год на планете.
Большинство мужчин вообще не знают, что такое возможно, легкомысленно считая проблемы с молочной железой уделом женщин. Мужчины часто не обращают внимание на уплотнение в груди, нагрубание молочных желёз (гинекомастию) и приходят на запущенных стадиях патологического процесса. Основные проявления заболевания схожи с таковыми у женщин.
Как и женщины, мужчины могут быть предрасположены к этому заболеванию генетически, если у них есть наследственная мутация гена BRCA1 или BRCA2 от одного из родителей, к факторам риска относят приём гормональных препаратов, возрастное снижение тестостерона в крови.
Злоупотребление алкоголем, резкое уменьшение физических нагрузок у спортсменов и увеличение стрессовых ситуаций, различные эндокринопатии: синдром Клайнфельтера, синдром Рейфенштейна, гипотиреоз, тестикулярная феминизация, опухоли надпочечников, гипофиза, яичек.
При выявлении факторов риска или появлении симптомов болезни следует обратиться к врачу маммологу, выполнить УЗИ, МРТ с в\в контрастированием данной области.