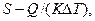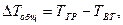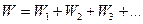На чем основан способ выпаривания
С пособы разделения смесей (и гетерогенных, и гомогенных) основаны на том факте, что вещества, входящие в состав смеси, сохраняют свои индивидуальные свойства. Гетерогенные смеси могут различаться по составу и фазовому состоянию, например: газ+жидкость; твердое вещество+жидкость; две несмешивающиеся жидкости и др. Основные способы разделения смесей представлены на схеме ниже. Рассмотрим каждый способ отдельно.
Разделение гетерогенных смесей
ФИЛЬТРОВАНИЕ
метод основанный на различной растворимости веществ и разных размерах частиц компонентов смеси. Фильтрование позволяет отделить твердое вещество от жидкости или газа.
Размер пор в фильтровальной бумаге таков, что позволяет молекулам воды и молекулам растворенного вещества беспрепятственно просачиваться. Частицы размером больше 0,01мм задерживаются на фильтре и не проходят сквозь него, таким образом формируется слой осадка.
Запомни! С помощью фильтрования нельзя разделить истинные растворы веществ, то есть растворы, в которых растворение произошло на уровне молекул или ионов.
Кроме фильтровальной бумаги в химических лабораториях используют специальные фильтры с
разным размером пор.
Фильтрование газовых смесей принципиально не отличается от фильтрования жидкостей. Разница заключается только в том, что при фильтровании газов от твердых взвешенных частиц (ТВЧ) используются фильтры специальных конструкций (бумажный, угольный) и насосы для принудительного прокачивания газовой смеси через фильтр, например фильтрация воздуха в салоне автомобиля или вытяжка над плитой.
Фильтрованием можно разделить:
ОТСТАИВАНИЕ
Данным методом можно разделять и несмешивающиеся жидкости. Для этого используют делительную воронку.
Отстаиванием можно разделить смеси:
МАГНИТНАЯ СЕПАРАЦИЯ
Метод основан на разных магнитных свойствах твердых компонентов смеси. Данный метод используют при наличии в смеси веществ-ферромагнетиков, то есть веществ, обладающих магнитными свойствами, например железа.
Все вещества, по отношению к магнитному полю, условно можно разделить на три большие группы:
Магнитной сепарацией можно разделить:
Разделение гомогенных смесей
Для разделения жидких гомогенных смесей (истинных растворов) используют следующие методы:
ВЫПАРИВАНИЕ. КРИСТАЛЛИЗАЦИЯ.
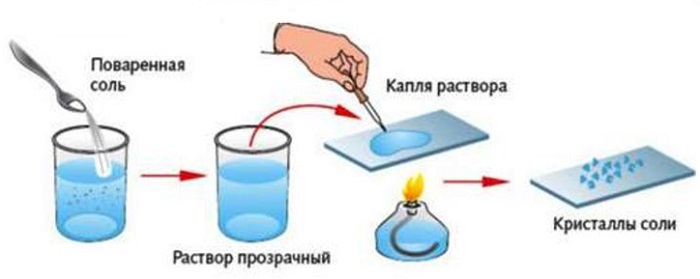
Метод основан на различных температурах кипения растворителя и растворенного вещества. Используется для выделения растворимых твердых веществ из растворов. Выпаривание обычно проводят следующим образом: раствор наливают в фарфоровую чашку и нагревают ее, постоянно перемешивая раствор. Вода постепенно испаряется и на дне чашки остается твердое вещество.
При этом испаренное вещество (воду или растворитель) можно собрать методом конденсирования на более холодной поверхности. Например, если поместить холодное предметное стекло над выпаривательной чашкой, то на его поверхности образуются капли воды. На этом же принципе основан метод дистилляции.
ДИСТИЛЛЯЦИЯ. ПЕРЕГОНКА.
В природе вода в чистом виде (без солей) не встречается. Океаническая, морская, речная, колодезная и родниковая вода – это разновидности растворов солей в воде. Однако часто людям необходима чистая вода, не содержащая солей (используется в двигателях автомобилей; в химическом производстве для получения различных растворов и веществ; при изготовлении фотографий). Такую воду называют дистиллированной, именно ее применяют в лаборатории для проведения химических опытов.
Перегонкой можно разделить:
ХРОМАТОГРАФИЯ
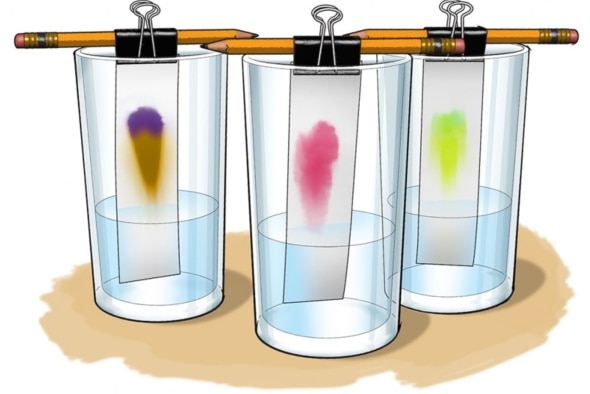
Можно самостоятельно получить хроматограмму и увидеть сущность метода на практике. Нужно смешать несколько чернил и каплю полученной смеси нанести на фильтровальную бумагу. Затем точно в середину цветного пятнышка начнем по каплям приливать чистую воду. Каждую каплю нужно вносить только после того, как впитается предыдущая. Вода играет роль элюэнта, переносящего исследуемое вещество по сорбенту — пористой бумаге. Вещества, входящие в состав смеси, задерживаются бумагой по-разному: одни хорошо удерживаются ею, а другие впитываются медленнее и продолжают некоторое время растекаться вместе с водой. Вскоре по листу бумаги начнет расползаться настоящая красочная хроматограмма: пятно одного цвета в центре, окруженное разноцветными концентрическими кольцами.
Особенно большое распространение получила тонкослойная хроматография, в органическом анализе. Достоинства тонкослойной хроматографии в том, что можно использовать простейший и очень чувствительный метод детектирования – визуальный контроль. Проявлять невидимые глазу пятна можно различными реактивами, а также используя ультрафиолетовый свет или авторадиографию.
В анализе органических и неорганических веществ применяют хроматографию на бумаге. Разработаны многочисленные методы разделения сложных смесей ионов, например смесей редкоземельных элементов, продуктов деления урана, элементов группы платины
СПОСОБЫ РАЗДЕЛЕНИЯ СМЕСЕЙ, ИСПОЛЬЗУЕМЫЕ В ПРОМЫШЛЕННОСТИ.
Способы разделения смесей, используемые в промышленности немногим отличаются от лабораторных способов, описанных выше.
Для разделения нефти чаще всего используют ректификацию (перегонку). Более подробно этот процесс описан в теме «Переработка нефти».
Самыми распространенными методами очистки и разделения веществ в промышленности являются отстаивание, фильтрация, сорбция и экстракция. Методы фильтрации и отстаивания проводятся аналогично лабораторным метода, с той разницей, что используются отстойники и фильтры больших объемов. Чаще всего, эти методы используются для очистки сточных вод. Поэтому рассмотрим подробнее методы экстракции и сорбции.
Термин «экстракция» приложим к различным фазовым равновесиям (жидкость – жидкость, газ – жидкость, жидкость – твердое тело и т.д.), но чаще его применяют к системам жидкость – жидкость, поэтому чаще всего можно встретить такое определение:
Одним из несмешивающихся растворителей обычно является вода, вторым – органический растворитель, однако это не обязательно. Экстракционный метод отличается универсальностью, он пригоден для выделения почти всех элементов в различных концентрациях. Экстракция позволяет разделять сложные многокомпонентные смеси зачастую эффективнее и быстрее, чем другие методы. Выполнение экстракционного отделения или разделения не требует сложного и дорогостоящего оборудования. Процесс может быть автоматизирован, при необходимости им можно управлять на расстоянии.
Чаще всего в промышленности методы абсорбции используют для очистки газовоздушных выбросов от частиц пыли или дыма, а также токсичных газообразных веществ. В случае поглощения газообразных веществ, между сорбентом и растворенным веществом может протекать химическая реакция. Например, при поглощении газообразного аммиака NH3 раствором азотной кислоты HNO3 образуется нитрат аммония NH4NO3 (аммиачная селитра), который можно использовать в качестве высокоэффективного азотного удобрения.
Процесс, при котором происходит абсорбция растворенного вещества за счет протекания химической реакции называется хемосорбцией.
Адсорбцию также используют для очистки воды от химических растворимых примесей. Например, фильтры для питьевой воды работают на принципе адсорбции слоем активированного угля с ионами серебра. Помимо поглощения всем объемом жидкого сорбента (абсорбции), и поверхностным слоем сорбента (адсорбции), выделяют также сорбцию твердого тела или расплава (окклюзию). При сорбции паров твердыми веществами часто происходит капиллярная конденсация.
Многие вещества на нашей планете не встречаются в чистом виде, потому ученые придумали множество методов разделения смесей. Некоторые смеси состоят из видимых невооруженному глазу частей. Но есть вещества, однородность которых сохраняется только до наступления особого состояния.
К примеру, из чего состоит гранит, видно всем, а вот структура молока становится явной только при его скисании. Ниже мы рассмотрим, как можно разделить смешанные вещества, и для чего применяется каждый из методов.
Способы разделения однородных смесей
Для выделения из готового состава растворенных компонентов принято использовать химические процессы. Разберем основные химические способы.
Выпаривание
В основу выпаривания заложены физические свойства компонентов смеси, а именно способность кипеть при разных температурах.
В ходе такого процесса состав можно разделить на жидкие и растворимые вещества. Например, вода и соль, или вода и сахар.
Выпариванием пользуются при необходимости выделения из имеющейся смеси только твердого ингредиента.
С температурами кипения отдельных веществ можно предварительно ознакомиться в справочниках по химии или физике. Данные представлены в наглядных таблицах.
Кристаллизация
Кристаллизацией называют процесс формирования кристаллов из стекол, газов, расплавов и растворов. Такую же формулировку применяют при образовании кристаллов с полученной структурой из кристаллов другого структурного класса, так называемые полиморфные превращения, либо при смене состояния вещества из жидкого на твердое кристаллическое.
Методом кристаллизации пользуются для выделения больших образований твердого вещества. Жидкость испаряется частично.
Раствор нагревают до определенной температуры и оставляют открытым на долгий период времени. При медленном испарении жидкости растворенное вещество выпадает в осадок в виде кристаллов. Таким методом в промышленных масштабах добывают соль из природной соленой воды.
Дистилляция (перегонка)
Метод перегонки основан на испарении летучих жидкостей, которые в дальнейшем превращаются в конденсат.
При нагревании раствора летучий компонент превращается в пар и оседает на стенках сосудов в виде капель конденсата.
Дистилляцию применяют в процессе опреснения морской воды, что очень актуально для стран с острой нехваткой питьевой воды.
Дистилляция – это основной метод переработки нефти, которая, по сути, является многокомпонентной смесью. В результате перегонки получают различные виды топлива.
Хроматография
Хроматография основана на способности поверхности определенных веществ с разной интенсивностью поглощать разделяемые компоненты.
Процесс можно рассмотреть на простом практическом примере – разделении красителей фильтровальной бумагой. При погружении конца полоски бумаги в раствор, растворители будут подниматься на разную высоту и с различной скоростью.
В промышленных масштабах фильтровальную бумагу заменяют углем, мелом, известняком и прочими веществами. Для разделения многокомпонентных растворов используют хроматографы. Они не только разделяют смеси, но и устанавливают их состав.
Методы разделения неоднородных составов
Для разделения нерастворимой группы смесей применяют несколько иные методики. Их задача заключается в отделении твердых нерастворимых частиц от жидкостей или твердых частиц другого вида.
Отстаивание
Это наиболее простой метод, который отличается тем, что в процессе отстаивания частицы, имеющие больший вес, чем вода, опускаются на дно сосуда.
Более легкие частицы наоборот всплывают на поверхность, где их потом и собирают.
Чем меньшего размера твердые компоненты, тем дольше длится отстаивание. Поэтому для ускорения очищения жидкости могут применять различные абсорбенты, адсорбенты и прочие химические катализаторы.
Фильтрование
Фильтрование часто используется совместно с отстаиванием. Для его осуществления понадобятся всевозможные фильтры.
Наиболее результативными являются вакуумные, дисковые и ленточные. Они задерживают твердые частицы и пропускают жидкость в емкость. Чем больше размер фильтра, тем быстрее будет происходить фильтрация.
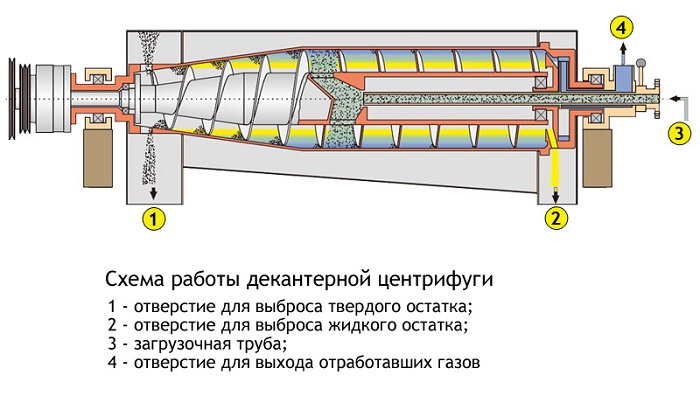
Центрифугирование
Работа высокоскоростных центрифуг заключается в разделении особо устойчивых эмульсий.
При помощи центробежной силы компоненты смеси, имеющие индивидуальную густоту, разделяются через воронки в разные емкости. В этом и состоит суть центрифугирования.
Для газовых взвесей лучше использовать скоростные циклоны. Они собирают твердые частицы на электродах или стенках устройства.
Другие методы разделения
Отделить нужный компонент из имеющейся смеси можно и другими способами.
Приведем несколько примеров:
Сушка – тепловое удаление жидкости из смесей. После сушки остается только твердый состав. Часто применяется на производстве непосредственно перед упаковкой продукции.
Электрофорез – сложное явление, заключающееся в электрокинетическом перемещении дисперсных частиц в жидком или газообразном веществе под воздействием электрического поля. Электрофорез применяется для разделения и изучения состава смеси в молекулярной биологии, химии и биохимии.
Методов разделения смесей намного больше, нежели описано в этой статье. Существуют очень сложные способы, которые предназначены для выделения из состава веществ со схожими свойствами или имеющихся в критически малых количествах в гетерогенных и гомогенных смесях.
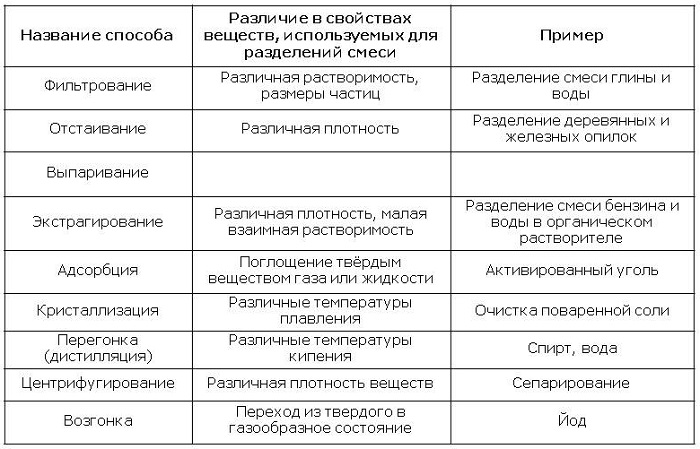
Способы разделения смесей
Для получения чистых веществ используют различные способы разделения смесей.
| Способы разделения смесей | |
|---|---|
| неоднородных (гетерогенных) | однородных (гомогенных) |
| — Отстаивание — Фильтрование — Действие магнитом — Центрифугирование | — Выпаривание. Кристаллизация. — Дистилляция (перегонка) |
Процессы разделения смесей основаны на различных физических свойствах компонентов, образующих смесь.
Отстаивание
Отстаивание — это разделение неоднородной жидкой смеси на компоненты, путём её расслоения с течением времени под действием силы тяжести.
Отстаиванием можно разделить смесь нерастворимых в воде веществ, имеющих разную плотность.
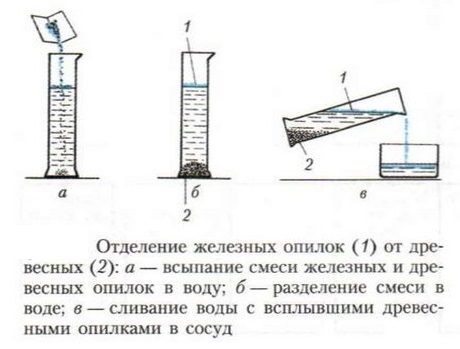
Пример. Смесь из железных и древесных опилок можно разделить, если высыпать её в сосуд с водой (1), взболтать и дать отстояться. Железные опилки опустятся на дно сосуда, а древесные будут плавать на поверхности воды (2), и их вместе с водой можно будет слить в другой сосуд (3):
На этом же принципе основано разделение смесей малорастворимых друг в друге жидкостей.
Пример. Смеси бензина с водой, нефти с водой, растительного масла с водой быстро расслаиваются, поэтому их можно разделить с помощью делительной воронки:
Отстаиванием также можно разделить вещества, которые осаждаются в воде с различной скоростью.
Пример. Смесь из глины и песка можно разделить, если высыпать её в сосуд с водой (1), взболтать и дать отстояться. Песок оседает на дно значительно быстрее глины (2):
Этот способ используется для отделения песка от глины в керамическом производстве (производство глиняной посуды, красных кирпичей и др.).
Центрифугирование
Центрифугирование — это разделение неоднородных жидких смесей путём вращения.
Пример. Если компоненты неоднородной жидкой смеси очень малы, такие смеси разделяют центрифугированием. Такие смеси помещают в пробирки и вращают с большой скоростью в специальных аппаратах — центрифугах.
Перед центрифугированием частицы смеси распределены по объёму пробирки равномерно. После центрифугирования более лёгкие частицы всплывают наверх, а тяжёлые оседают на дно пробирки.
С помощью центрифугирования, к примеру, отделяют сливки от молока.
Фильтрование
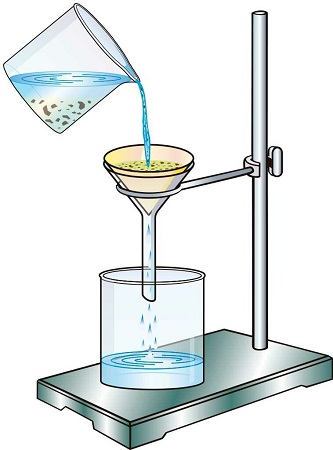
Фильтрование — это разделение жидкой неоднородной смеси на компоненты, путём пропускания смеси через пористую поверхность. В роли пористой поверхности может выступать бумажная воронка, марля, сложенная в несколько слоёв, или любой другой пористый материал, способный задержать один или несколько компонентов смеси.
Фильтрованием можно разделить неоднородную смесь, состоящую из растворимых и нерастворимых в воде веществ.
Пример. Чтобы разделить смесь, состоящую из поваренной соли и песка, её можно высыпать в сосуд с водой, взболтать и затем эту смесь пропустить через фильтровальную бумагу. Песок остаётся на фильтровальной бумаге, а прозрачный раствор поваренной соли проходит через фильтр:
При необходимости, растворённую поваренную соль из воды можно выделить выпариванием.
Действие магнитом
С помощью магнита из неоднородной смеси выделяют вещества, способные к намагничиванию.
Пример. C помощью магнита можно разделить смесь, состоящую из порошков железа и серы:
Выпаривание. Кристаллизация
Выпаривание — это способ разделения жидких смесей путём испарения одного из компонентов. Скорость испарения можно регулировать с помощью температуры, давления и площади поверхности испарения.
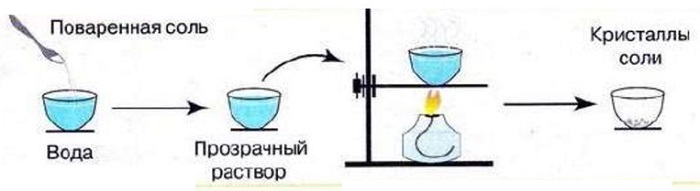
Пример. Чтобы растворённую в воде поваренную соль выделить из раствора, последний выпаривают:
Вода испаряется, а в фарфоровой чашке остаётся поваренная соль. Иногда применяют упаривание, т. е. частичное испарение воды. В результате образуется более концентрированный раствор, при охлаждении которого растворённое вещество выделяется в виде кристаллов. Этот процесс получил название кристаллизации.
Дистилляция (перегонка)
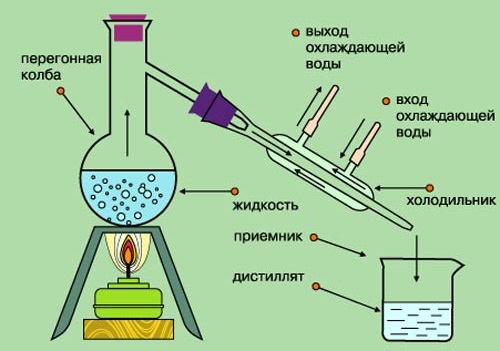
Дистилляция (перегонка) — это способ разделения жидких однородных смесей путём испарения жидкости с последующим охлаждением и конденсацией её паров. Данный способ основан на различии в температурах кипения компонентов смеси.
Пример. При нагревании жидкой однородной смеси сначала закипает вещество с наиболее низкой температурой кипения. Образующиеся пары конденсируются при охлаждении в другом сосуде. Когда этого вещества уже не останется в смеси, температура начнёт повышаться, и со временем закипает другой жидкий компонент:
Таким способом получают, к примеру, дистиллированную воду.
Основные понятия. Способы выпаривания



Выпаривание — это процесс концентрирования растворов твердых нелетучих веществ путем удаления жидкого растворителя в виде паров. Сущность выпаривания заключается в переводе растворителя в парообразное состояние и отводе полученного пара от оставшегося сконцентрированного раствора. Выпаривание обычно проводят при кипении, т.е. в условиях, когда давление пара над раствором равно давлению в рабочем объеме аппарата. Различают следующие основные способы выпаривания:
• простое (однокорпусное), проводимое в непрерывном или периодическом режиме;
• многократное (многокорпусное), осуществляемое только в непрерывном режиме;
• с применением теплового насоса.
Все перечисленные способы выпаривания в зависимости от параметров греющего пара и свойств выпариваемых растворов реализуют как под давлением, так и в вакууме.
Простое выпаривание. Этот процесс осуществляют на установках небольшой производительности. Его проведение в периодическом режиме возможно с одновременной или порционной загрузкой исходного раствора.
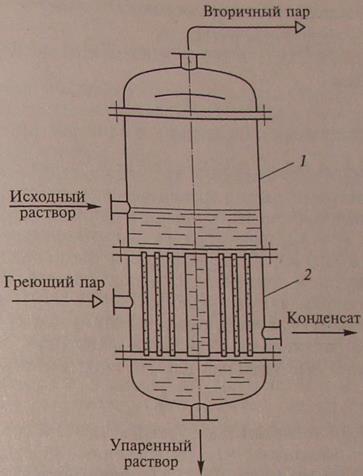
Схема однокорпусной выпарной установки непрерывного действия представлена на рис. 15.1. Аппарат состоит из сепаратора 1 и теплообменника 2. Греющий пар поступает в межтрубное пространство. Исходный раствор, подаваемый в аппарат, воспринимает теп-
Рис. 15.1. Схема однокорпусной выпарной установки непрерывного действия:
1 — сепаратор; 2 — теплообменник
лоту греющего пара, и растворитель испаряется. Образовавшийся вторичный пар и инертные газы освобождаются от брызг жидкости в сепараторе и отводятся через верхнюю часть аппарата. Упаренный раствор отбирается из штуцера, расположенного в нижней части аппарата.
Материальный баланс простого выпаривания может быть выражен двумя способами:
1)общий материальный баланс выпарного аппарата — с помощью уравнения
где GH, GK — массовый расход соответственно исходного и упаренного растворов, кг/с; W — массовый расход вторичного пара или выпариваемой воды, кг/с;
2)материальный баланс по сухому веществу, находящемуся в растворе, — с помощью уравнения
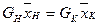
где 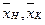
в исходном и упаренном растворах.
Из уравнений (15.1) и (15.2) найдем массовый расход выпариваемой воды:
( 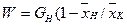
Уравнение теплового баланса имеет вид
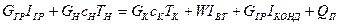
где 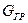
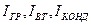
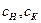
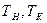
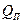
Под энтальпией (теплосодержанием) понимают сумму внутренней энергии и потенциальной энергии давления.
С учетом того, что удельная теплота конденсации пара
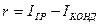
уравнение (15.3) позволяет определить массовый расход греющего пара. Расчет показывает, что для удаления 1 кг влаги из раствора может потребоваться 1,1. 1,2 кг греющего пара.
Площадь поверхности нагрева выпарного аппарата согласно основному уравнению теплопередачи (12.4) записывается в виде
где применительно к процессу выпаривания 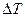
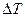
Общей разностью температур в выпарных установках называют разность температур греющего пара 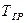
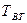
Полезная разность температур меньше общей на величину температурных потерь 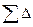
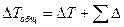
Различают три вида депрессий: температурную (физико-химическую), гидростатическую и гидравлическую.
Так как давление пара растворителя над раствором всегда ниже, чем над чистым растворителем, температура кипения раствора выше температуры кипения чистого растворителя при том же давлении. Например, в условиях, когда давление равно атмо-
сферному, вода кипит при температуре 100 °С, а 30%-ный раствор NaOH — при 117°С. Такая разность температур кипения раствора и чистого растворителя называется температурной депрессией 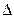
Значение температурной депрессии, зависящее от свойств растворенного вещества и растворителя, повышается с увеличением концентрации раствора и давления. Определить значение 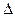
Большинство опытных данных относится к температурной депрессии 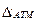
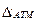
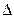
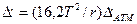
где Т — абсолютная температура кипения, К; r — удельная теплота испарения, Дж/кг, воды при данном давлении.
Повышение температуры кипения раствора обусловлено также гидростатической и гидравлической депрессиями.
Гидростатическая депрессия 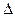
Гидравлическая депрессия 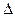
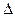
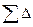
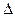
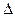
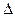
Проведение выпаривания в вакууме в большинстве случаев играет положительную роль: снижается температура кипения раствора, а это позволяет применять для нагревания выпарного аппарата пар низкого давления, который относится к тепловым отходам, образующимся при осуществлении других процессов.
Многократное выпаривание.Сущность этого способа выпаривания состоит в том, что его проводят в нескольких последовательно соединенных аппаратах, давление в которых поддерживают на таком уровне, чтобы вторичный пар предыдущего аппарата мог быть использован как греющий пар в последующем аппарате. Очевидно, что многократное выпаривание позволяет сократить расход теплоты на проведение процесса приблизительно пропорционально числу последовательно соединенных аппаратов (числу корпусов). Установки для многократного выпаривания всегда имеют несколько корпусов и поэтому называются многокорпусными.
Многокорпусные выпарные установки могут быть прямоточными, противоточными и комбинированными.
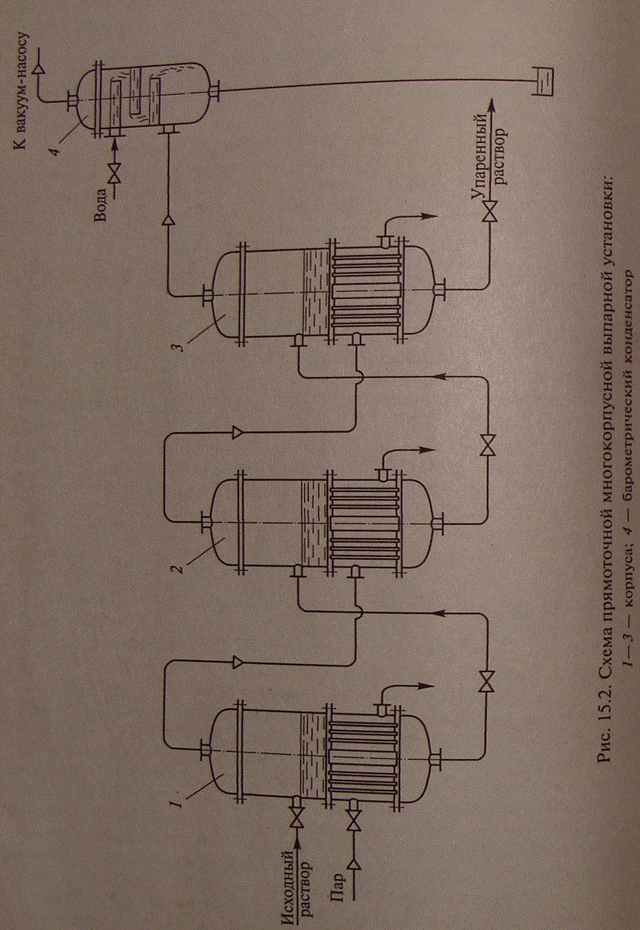
Схема прямоточной многокорпусной выпарной установки приведена на рис. 15.2. Исходный раствор подают в корпус 1, далее поступает в корпуса 2 и 3, а затем удаляется из корпуса 3 в виде готового продукта. Давление в установке уменьшается в направлении от корпуса 1 к корпусу 3, что обеспечивает перемещение раствора самотеком под действием перепада давлений.
Греющий пар перемещается в том же направлении, что и раствор: свежий пар вводится в корпус 1, а образовавшийся в этой корпусе вторичный пар направляется в качестве греющего пара в корпус 2. Образовавшийся в корпусе 2 вторичный пар применяется для обогрева корпуса 3, а вторичный пар из корпуса 3 поступает для конденсации в барометрический конденсатор 4.
Очевидным достоинством прямоточной схемы выпаривания является возможность перемещения раствора из корпуса в корпус без помощи насосов. К недостаткам этой схемы относится резкое снижение коэффициента теплопередачи от корпуса к корпусу.
Схема противоточной многокорпусной выпарной установки представлена на рис. 15.3. Свежий греющий пар поступает в корпус 1, а вторичный пар уже в качестве греющего пара перемещается от корпуса 1 к корпусу 3. Выпариваемый раствор вводится вкорпус 3, перемещается в установке в направлении от корпуса 3 к корпусу 1 и отбирается из корпуса 1. Поскольку давление в каждом последующем корпусе меньше, чем в предыдущем, для перемещения раствора используются насосы 5— 7.
Преимуществом противоточной схемы выпаривания перед прямоточной является потребность в меньшей поверхности теплообмена, а недостатком — необходимость применения насосов для перекачивания растворов.
Общий массовый расход воды, выпариваемой в многокорпусной установке,
Очевидно, что увеличение числа корпусов ограничено вследствие уменьшения полезной разности температур, значения которых при этом возрастают. Оптимальное число корпусов установок многократного выпаривания, при определении которого принимаются во внимание и экономические соображения, составляет 3—4.