На что расщепляется крахмал
На что расщепляется крахмал
а) Углеводные продукты в пище. В пищевом рационе человека встречаются только три основных источника углеводов:
(1) сахароза, которая является дисахаридом и широко известна как тростниковый сахар;
(2) лактоза, являющаяся дисахаридом молока;
(3) крахмал — полисахарид, представленный практически во всей растительной пище, в особенности в картофеле и различных видах зерновых.
Другими углеводами, усваиваемыми в небольшом количестве, являются амилоза, гликоген, алкоголь, молочная кислота, пиро-виноградная кислота, пектины, декстрины и в наименьшем количестве — производные углеводов в мясе.
Пища также содержит большое количество целлюлозы, которая является углеводом. Однако в пищеварительном тракте человека не существует фермента, способного расщепить целлюлозу, поэтому целлюлоза не рассматривается как пищевой продукт, пригодный для человека.
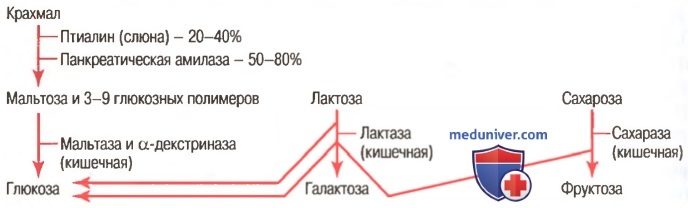
б) Переваривание углеводов в ротовой полости и желудке. Когда пища пережевывается, она смешивается со слюной, которая содержит пищеварительный фермент птиалин (α-амилазу), секретирующийся в основном околоушными железами. Этот фермент гидролизует крахмал на дисахарид мальтозу и другие небольшие глюкозные полимеры, содержащие от 3 до 9 молекул глюкозы, как показано на рисунке ниже.
Однако в ротовой полости пища находится короткое время, и, вероятно, до акта глотания гидролизуется не более 5% крахмала.
Тем не менее, переваривание крахмала иногда продолжается в теле и дне желудка еще в течение 1 ч до тех пор, пока пища не начнет перемешиваться с желудочным секретом. Затем активность амилазы слюны блокируется соляной кислотой желудочного секрета, т.к. амилаза как фермент в принципе не активна при снижении рН среды ниже 4,0. Несмотря на это, в среднем до 30-40% крахмала гидролизуется в мальтозу прежде, чем пища и сопутствующая ей слюна полностью перемешаются с желудочными секретами.
в) Переваривание углеводов в тонком кишечнике. Переваривание панкреатической амилазой. Секрет поджелудочной железы, как и слюна, содержит большое количество амилазы, т.е. он почти полностью схож в своих функциях с α-амилазой слюны, но в несколько раз эффективнее. Таким образом, не более чем через 15-30 мин после того, как химус из желудка попадет в двенадцатиперстную кишку и смешается с соком поджелудочной железы, фактически все углеводы оказываются переваренными.
В результате прежде чем углеводы выйдут за пределы двенадцатиперстной кишки или верхнего отдела тощей кишки, они почти полностью превращаются в мальтозу и/или в другие очень небольшие полимеры глюкозы.
г) Гидролиз дисахаридов и небольших полимеров глюкозы в моносахариды ферментами кишечного эпителия. Энтероциты, выстилающие ворсинки тонкого кишечника, содержат четыре фермента (лактазу, сахаразу, мальтазу и α-декстриназу), способных расщеплять дисахариды лактозу, сахарозу и мальтозу, а также другие небольшие глюкозные полимеры на их конечные моносахариды. Эти ферменты локализованы в микроворсинках щеточной каемки, покрывающей энтероциты, поэтому дисахариды перевариваются сразу, как только соприкасаются с этими энтероцитами.
Лактоза расщепляется на молекулу галактозы и молекулу глюкозы. Сахароза расщепляется на молекулу фруктозы и молекулу глюкозы. Мальтоза и другие небольшие глюкозные полимеры расщепляются на многочисленные молекулы глюкозы. Таким образом, конечными продуктами переваривания углеводов являются моносахариды. Все они растворяются в воде и мгновенно всасываются в портальный кровоток.
В обычной пище, в которой из всех углеводов больше всего крахмала, более 80% конечного продукта переваривания углеводов составляет глюкоза, а галактоза и фруктоза — редко более 10%.
Основные стадии переваривания углеводов обобщены на рисунке выше.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Процесс осахаривания крахмала
Осахаривание крахмала во время затирания — это расщепление его на простыесоставляющие (сахара) под действием ферментов солода, воды и тепла. Какпроисходит этот процесс и какие есть альтернативные методы осахариваниякрахмала — в этой статье.
Процесс осахаривания крахмала
Крахмал — это сложный сахар, полисахарид. Он состоит из полимераамилозы и полисахарида амилопектина, которые и образуют крахмальныегранулы в зерне. Задача затирания и осахаривания крахмала — растворить иразрушить сложные и нерастворимые в воде молекулы крахмала до сбраживаемогодисахарида мальтозы или до простых сбраживаемых моносахаридов глюкозы. Послеосахаривания проба на йод должна быть отрицательной.
Процесс осахаривания крахмала в зернах пшеницыпроращиванием выполняют, чтобы сэкономить время и деньги и получить вкусный зерновойсамогон. Белый (пророщенный и сушеный) или зеленый (живой, не сушеный) солодиспользуют, как источник амилолитических ферментов. А ферменты появляютсякак раз при проращивании зерна и потреблении ростком части крахмала. Какработают эти ферменты?
Сначала происходит клейстеризация при 60 о С для ячменя. Дробленое зерно отдает водекрахмал, затор густеет.
Затем начинается разжижение и осахаривание. В игру вступаютамилолитические, появившиеся в результате проращивания ферменты для осахаривания крахмала.
Бета-амилаза действует при 60-65 о С. Эта крупная молекула способна»отрезать» от концов цепочки сахаров мальтозу, «разбивая» ее на глюкозу имальтотриозу. Разрывать цепочки, снижая вязкость, она не может. При 70 о С бета-амилазадеактивируется.
Зато фермент альфа-амилаза при 72-75 о С начинает разрывать длинные цепочкиполисахаридов амилозы и амилопектина, из которых и состоит крахмал.
При этом амилопектин разрушается до составляющих его мальтозы и изомальтозы,амилоза — до мальтозы.
Надо отметить, что в присутствии альфа-амилазы усиливается действиебета-амилазы, поскольку свободных концов цепочек сахара становится больше.
В результате работы амилолитических ферментов крахмальный растворстановится менее вязким.
Здесь действуют следующие закономерности:
Чем дольше длительностьзатирания и каждая из пауз, тем концентрированнее сусло, но тем болеезамедляется осахаривание.
Чем длиннее мальтознаяпауза при 62-63 о С, тем выше:
Жидкие заторы лучшевымывают крахмал, но в густых ферменты дольше деактивируются, работают исоздают больше сбраживаемых сахаров. Чем выше концентрация углеводов в заторе,тем меньше воздействует температура на активность амилазы.
Какой продукт получают осахариванием крахмала?
Продукт получаемый осахариванием крахмала — это сахара, глюкоза и мальтоза. Экстрактводорастворимой мальтозы и глюкозы, белков, минеральных веществ, которые смогутиспользовать для роста дрожжи. Или, попросту, — это «съедобное» сусло,питательная среда.
Под действием чего крахмал расщепляется доглюкозы?
Крахмал расщепляется под действием тепла, воды,амилолитических ферментов.
Как выполнить осахаривание крахмала лимоннойкислотой?
Собственно, это процесс гидролиза (разложения) при участии воды и сильнойразбавленной кислоты.
Лимонная кислота применяется, в основном, при осахаривании готовымикомплексными ферментами амилосубтилином и глюкаваморином. Добавляется дляподкисления, активизации работы ферментов и дезинфекции сусла в такомколичестве, чтобы довести pH до 5,5.
Процесс осахаривания серной кислотой состоит из следующих этапов:
Как выполнить осахаривание крахмала солодом?
Подробный ответ на вопрос «как осахаривать зеленым солодом» или «как осахаривать белым солодом» вы можете найти в разделе «Рецепты самогона».
Кстати, перегонять крахмальную брагу лучше всего на аппарате с отбором по пару, термометром, баком из нержавеющей стали.
Параграф 30. Переваривание углеводов
Автор текста – Анисимова Елена Сергеевна.
Авторские права защищены. Продавать текст нельзя.
Курсив не зубрить.
Замечания можно присылать по почте: exam_bch@mail.ru
https://vk.com/bch_5
ПАРАГРАФ № 30. См. также п. 28, 29, 31, 8.
«Функции углеводов.
Углеводы в питании.
Переваривание углеводов.
Унификация моносахаридов.»
Нужно знать формулы глюкозы, фруктозы, галактозы, сахарозы, лактозы, мальтозы, ДОАФ, ГА и их фосфатов (1- и т.д.).
30. 1. ФУНКЦИИ. См. п. 32, 38 и 39.
1. ЭНЕРГЕТИЧЕСКАЯ функция – ГЛЮКОЗА необходима для выработки АТФ в эритроцитах и головном мозге, поэтому ее концентрация в крови должна поддерживаться на уровне не менее 3 ммоль/л, а снижение концентрации глюкозы приводит к слабости, затуманенности сознания, создает риск обморока и смерти. Глюкоза поступает в кровь из печени, в которую поступает при переваривании углеводов пищи, образуется при распаде гликогена или при синтезе из аминокислот (см. ГНГ).
2. ПЕНТОЗЫ (рибоза и дезоксирибоза) входят в состав РНК и ДНК. Образуются пентозы из глюкозы в пентозофосфатном пути. п.35 и 72.
3. Разные моносахариды входят в состав олигосахаридов и полисахаридов. Олигосахариды соединены с липидами, образуя гликолипиды, или с белками, образуя гликопротеины; гликопротеины и гликопротеины входят в состав мембран, углеводный компонент находится на внешней поверхности мембраны, участвует в узнавании (то есть выполняет РЕЦЕПТОРНУЮ ФУНКЦИЮ). Гликопротеины есть в крови. Полисахариды входят в состав соединительной ткани (хрящей и т.д.), выполняя опорно-защитную функцию. Мономеры олиго- и полисахаридов образуются из глюкозы.
4. Из глюкозы образуются метаболиты ЦТК, из которых синтезируются заменимые аминокислоты для белков и липиды (жирные кислоты, холестерин, кетоновые тела).
30. 2. Углеводы в питании:
потребность, оценка значения крахмала, сахарозы, пищевых волокон. См. 28.
В мёде и фруктах содержатся моносахариды ГЛЮКОЗА И ФРУКТОЗА, которые могут сразу всасываться.
В обычных сладостях содержится САХАРОЗА – дисахарид, состоящий из остатков глюкозы и фруктозы, соединенных 1,2-гликозидной связью, которая расщепляется в тонком кишечнике ферментом сахаразой, что приводит к образованию моносахаридов глюкозы и фруктозы.
В молоке (но не в кисло-молочных продуктах) содержится «молочный сахар» – дисахарид ЛАКТОЗА, состоящий из остатков галактозы и глюкозы, соединенных ;-1,4-гликозидной связью, расщепляемой ферментом лактаза, что приводит к образованию моносахаридов галактоза и глюкозы. Лактоза является единственным углеводом в питании грудных детей.
Моносахариды и дисахариды имеют сладкий вкус и относятся к «простым» углеводам. Из-за их быстрого переваривания их употребление приводит к быстрому повышению концентрации глюкозы в крови, поэтому они быстро нормализуют самочувствие, если оно нарушено низкой концентрацией глюкозы в крови, но поэтому же нежелательно употреблять простые углеводы в больших количествах (это привело бы к резкому повышению концентрации глюкозы в крови, способствовало бы превращению глюкозы в жир). Рекомендуют употреблять не более 30г простых углеводов в сутки, распределяя это количество на несколько приемов.
КРАХМАЛ – основной углевод картофеля, злаков и изделий из них (каш, макарон, хлеба, булочек, тортов и т.д.). В сутки рекомендуют употреблять 300г крахмала (конечно, не в чистом виде, а в составе названных продуктов). Крахмал переваривается медленнее, чем простые (сладкие) углеводы, поэтому употребление продуктов с крахмалом приводит к более медленному и плавному повышению концентрации глюкозы в крови.
Значение ПИЩЕВЫХ ВОЛОКОН. (Клетчатки).
Это нерасщепляемые ферментами человека полисахариды клеточных стенок растений и грибов (отсюда второе название волокон – клетчатка). Примеры волокон – целлюлоза, пектин. Пищевые источники клетчатки – оболочки злаков (отруби), мюсли, хлеб из муки грубого помола, каши, морская капуста, овощи, фрукты и ягоды, соки с мякотью и т.д. Поскольку пищевые волокна не расщепляются, то они не являются источниками калорий, но наличие клетчатки в пище необходимо для профилактики ряда заболеваний – атеросклероза и ИБС, ожирения, геморроя, дисбактериоза – см. таблицу.
(Таблица свойства клетчатки)
30.3. Переваривание и всасывание углеводов. Дисахаридозы.
30. 3. 1. Всасывание.
Всасываться могут моносахариды. Дисахариды и полисахариды должны сначала расщепиться до моносахаридов.
Моносахариды (глюкоза и фруктоза мёда и фруктов) всасываются в тонком кишечнике в ЭНТЕРОЦИТЫ, транспортируясь через мембраны энтероцитов внутрь с помощью белков-ТРАНСПОРТЕРОВ.
При патологии кишечника (энтериты и т.д. – см. СНПВ в п.62) всасывание моносахаридов замедляется (снижение всасывания называется мальабсорбцией), что ведет
1 – к снижению поступления моносахаридов в организм (что снижает гликемию) и
2 – к поступлению моносахаридов в толстый кишечник, в котором моносахариды подвергаются действию микрофлоры, что приводит
1 – к размножению патогенных микроорганизмов (дисбактериозу),
2 – к диарее (моносахариды превращаются микрофлорой в осмотически активные вещества, то есть в вещества, вызывающие приток воды в полость кишечника).
Сначала концентрация глюкозы в полости кишечника больше, чем в энтероцитах, а затем – меньше, поэтому транспорт глюкозы в энтероциты (всасывание) происходит сначала по градиенту концентраций глюкозы, а затем – ПРОТИВ ГРАДИЕНТА.
Для транспорта против градиента нужна энергия;
источником энергии для транспорта глюкозы против ее градиента является транспорт ионов натрия по градиенту ионов натрия тоже внутрь энтероцитов – п.25.
Транспорт глюкозы и ионов натрия осуществляется одним и тем же белком-транспортером. Способ всасывания глюкозы тем же белком, что и натрий и в том же направлении называется СИМПОРТОМ глюкозы и натрия.
Форма энергии, которая используется при транспорте глюкозы в энтероциты против градиента, называется электро-химическим потенциалом ионов натрия. Источником ионов натрия в полости кишечника является поваренная соль пищи и транспорт ионов натрия натрий-калиевой АТФ-азой (поэтому всасывание глюкозы, переваривание углеводов требует затрат энергии и поэтому неподсоленную пищу трудно есть).
Из энтероцитов глюкоза поступает в КРОВЕНОСНЫЕ капилляры, с током крови поступает в ПЕЧЕНЬ. Если при этом гликемия низкая, то глюкоза поступает в кровь, что приводит к нормализации и повышению гликемии. Если гликемия нормальная, то поступившая из кишечника глюкоза используется для синтеза гликогена (около 150г в печени). Если гликогена в печени достаточно, то глюкоза превращается в жир (поэтому лишние углеводы пищи способствуют ожирению). Также глюкозы используется печенью для синтеза пентоз, глюкуроната и гликопротеинов.
30. 3. 2. РАСЩЕПЛЕНИЕ ДИСАХАРИДОВ
лактозы, сахарозы и мальтозы до моносахаридов осуществляется в тонком кишечнике путем гидролиза ферментами лактАЗОЙ, сахаразой и мальтазой, которые называются дисахаридазами, находятся на поверхности энтероцитов (пристеночное пищеварение) и вырабатываются энтероцитами.
Поэтому патология тонкого кишечника может быть причиной дефицита дисахаридаз (пример вторичной энзимопатии) – см. дисахаридозы.
ЛАКТАЗА расщепляет (путем гидролиза) ;-1,4-гликозидную связь лактозы между остатками галактозы и глюкозы, образуя галактозу и глюкозу.
САХАРАЗА расщепляет 1,2-гликозидную связь сахарозы между остатками глюкозы и фруктозы, образуя глюкозу и фруктозу.
МАЛЬТАЗА расщепляет ;-1,4-гликозидную связь мальтозы между двумя остатками глюкоз, образуя 2 молекулы глюкозы.
Если активность дисахаридаз снижается, это ведет к замедлению расщепления дисахаридов в тонком кишечнике, поступлению части дисахаридов в толстый кишечник, возникновению диареи и дисбактериоза.
Причиной снижения активности дисахаридаз могут быть патология тонкого кишечника (пример вторичной энзимопатии)
и мутации генов, кодирующих дисахаридазы (примеры первичных энзимопатий).
Низкая активность дисахаридаз проявляется в виде диареи при поступлении в организм их субстратов. –
Низкая активность лактазы проявляется после первого же кормления новорожденного молоком; нужно исключить из питания молоко и продукты, приготовленные с использованием цельного молока; при этом кисло-молочные продукты можно употреблять (в них нет лактозы).
Низкая активность сахаразы проявляется после поступления в организм сладкой пищи или напитков. Нужно исключить из питания сахар и продукты, содержащие сахарозу (варенье, печение, конфеты и т.д.)
Низкая активность мальтазы проявляется при поступлении в организм продуктов, содержащих крахмал (крахмал является основным источником мальтозы после своего расщепления).
Нарушения обмена дисахаридов называются ДИСАХАРИДОЗАМИ.
Галактоза и фруктоза в печени превращаются в глюкозу – см. унификацию моносахаридов.
30. 3. 3. РАСЩЕПЛЕНИЕ КРАХМАЛА.
Крахмал – это полимер, состоящий из остатков глюкозы, связанных ;-1,4-гликозидными связями в длинных линейных участках (по тысяче остатков).
;-1,4-гликозидные связи крахмала расщепляются ферментом ;-амилаза, которые расщепляет связь между вторым и третьим концевыми остатками глюкозы, отщепляя молекулы мальтозы (но не глюкозы).
Амилаза.
Фермент ;-амилаза есть и работает в ротовой полости и в 12-перстной кишке (ДПК). В ротовую полость амилаза поступает в составе слюны из слюнных желез, а в ДПК – в составе панкреатического сока из поджелудочной железы (ПЖЖ).
При повреждении слюнных желез (например, при паротите) или при повреждении ПЖЖ (например, при панкреатите) амилаза поступает из поврежденных клеток в кровь, поэтому повышенная активность амилазы в крови – признак паротита или панкреатита;
но при паротите повышена активность только амилазы только в крови,
а при панкреатите в крови повышена активность ещё и липазы, а активность амилазы повышена еще и в моче (диастаза).
(Эти ведения используются пори постановке диагноза).
Расщепление крахмала начинается в ротовой полости под действием амилазы слюны, но так как люди обычно почти сразу глотают непрожёванную пищу, то продолжается расщепление крахмала во рту недолго.
В желудке расщепление крахмала почти прекращается, так как при рН желудка (около 2) амилаза не работает (разве что внутри непрожёванного пищевого комка, пока туда не попадет кислота)
В ДПК расщепление крахмала продолжается под действием панкреатической амилазы и заканчивается образованием мальтозы из крахмала. О расщеплении мальтозы до глюкозы см. выше.
;-амилаза означает, что амилаза расщепляет ;-гликозидные связи. ;-гликозидные связи целлюлозы не расщепляются ферментами человека, а если бы расщеплялись бы, то бумага, целлюлоза, трава были бы такой же пищей, как и хлеб. Целлюлоза расщепляется ферментами микроорганизмов, в том числе живущими в рубце коров (отдел желудка).
30. 4. УНИФИКАЦИЯ МОНОСАХАРИДОВ.
Это превращение галактозы и фруктозы в глюкозу.
Происходит в ПЕЧЕНИ. Галактоза и фруктоза поступают в печень с током крови из кишечника, в котором галактоза образуется при расщеплении лактозы, а фруктоза – при расщеплении сахарозы (или поступает в чистом виде при употреблении фруктов и мёда).
30. 4. 1. Унификация фруктозы.
1-я реакция в унификации фруктозы
– присоединение фосфата (фосфорилирование) по 1-му положению, в результате чего фруктоза превращается во фруктозо-1-фосфат. Источником фосфата является (как обычно) АТФ, превращающийся в АДФ. Фермент реакции называется фруктокиназой (как и все ферменты, катализирующие перенос фосфата от АТФ). Реакцию считают реакцией активации фруктозы.
2-я реакция
– расщепление фруктозы на две «половинки», две триозы – диокси/ацетонфосфат и глицериновый альдегид.
Фермент называется альдолазой фруктозо-1-фосфата (похожий фермент работает в гликолизе п.32).
3-я реакция
– фосфорилирование глицеринового альдегида, в результате которой образуется фосфоглицериновый альдегид. Фермент реакции называется киназой глицеринового альдегида, а источником фосфата является АТФ (как и в первой реакции).
Остальные реакции, как в глюконеогенезе – 4) ФГА и ДОАФ вступают в реакцию, превращаясь во фруктозо-1,6-бисфосфат, 5) от Ф-1,6-бисФ отщепляется фосфат, образуя Ф-6-Ф, 6) Ф-6-Ф изомеризуется в Г-6-Ф, 7) от Г-6-Ф отщепляется фосфат, образуя глюкозу.
30. 4. 2. Унификация галактозы.
Первая реакция такая же, как в унификации фруктозы – галактоза + АТФ = галакто-1-фосфат + АДФ. Фермент – галактокиназа.
2-я реакция – галактозо-1-фосфат превращается в УДФ-галактозу, вступая в реакцию с УТФ или УДФ-глюкозой.
3-я реакция – УТФ-галактоза превращается в УДФ-глюкозу под действием фермента эпимераза (эпимеризация – это превращение вещества в его эпимер, разновидность изомеризации).
4-я реакция – УДФ-глюкоза используется для синтеза гликогена – см. № 31.
30. 5. ЭНЗИМОПАТИИ в унификации. (Учить только педиатрам.)
Энзимопатии (п.8) – это патологии, обусловленные сниженной или повышенной активностью ферментов. Частный случай протеинопатий.
Если причиной неправильной активности фермента является мутация кодирующего его гена, то энзимопатия называется первичной, а если другой причиной, то – вторичной. Другими причинами могут быть патология органа, вырабатывающего фермент, или дефицит витамина или минерала, который нужен для работы фермента (в этом случае активность фермента снижена).
Неправильная активность ферментов потому приводит к патологии, что возникают избыточные или недостаточные количества субстратов и продуктов ферментов.
30. 5. 1. ПОСЛЕДСТВИЯ нарушения унификации моносахаридов.
Если снижена активность ФРУКТОКИНАЗЫ, то катализируемая ею реакция идет медленно, фруктоза накапливается и выводится в почками с мочой, приводя к фруктозурии (присутствию фруктозы в моче).
Это не опасно, только лишает лишает организм возможности получить калории (АТФ) за счет фруктозы.
Низкая активность фруктозо-1-фосфот\АЛЬДОЛАЗЫ приводит к тому, что фрактозо-1-фосфат не превращается в ГА и ДОАФ и накапливается, что ведет к повреждению печени и почек.
Поэтому в этой ситуации для предотвращения повреждения печени и почек желательно отказаться от поступления в организм фруктозы – от мёда, фруктов и сахарозы.
Если снижена активность ГАЛАКТОКИНАЗЫ, то галактоза накапливается и повреждает ХРУСТАЛИК, приводя к развитию КАТАРАКТЫ и слепоте. Спасти зрение можно, не употребляя молоко.
Если снижена активность фермента превращающего галакто-1-фосфата в УДФ-галактозу, то накапливаются и галактоза, и УДФ-галактоза, что ведет к повреждению хрусталика, головного мозга и печени.
Избежать этих последствий можно, исключив из пищи источник галактозы, то есть молоко, а также продукты на молоке (каши, печенье и т.д.). Это та ситуация, когда молоко матери вредно для ребенка (наряду с дефицитом лактАзы и фенилкетонурией).
30. 5. 2. ПРИЧИНЫ нарушений унификации.
Причиной низкой активности ферментов унификации могут быть мутации генов, кодирующих ферменты унификации (см. первичные энзимопатии) и патология печени (вторичные энзимопатии).
Спасти от последствий нарушения унификации можно неупотреблением молока и фруктозы, сахара.
На что расщепляется крахмал
Все биологические процессы, происходящие в окружающем мире, по своей сути являются химическими реакциями. Первую химическую реакцию человек осуществил, когда разжег костер – это реакция горения. Первое антибактериальное применение продуктов брожения и величайшее открытие в области медицины совершил Нострадамус. Большинство из нас знает его как предсказателя, но его основная заслуга состоит в том, что он нашел способ борьбы с чумой с помощью уксусной кислоты. История свидетельствует, чума лишила Нострадамуса и первой семьи, и друзей. С тех пор он искал средство борьбы от страшной болезни. Найдя чудо-лекарство, исследователь переезжал из города в город, где появлялась чума, спасая множество жизней [1].
Первым биохимиком была клетка, которая научилась энергетическому обмену: научилась поглощать свет и выделять энергию, необходимую для жизнеобеспечения. Таким образом, первый биохимик – это и есть сама жизнь. Все процессы, которые протекают в клетках живого организма, – это биохимические реакции.
Название «углеводы» появилось из-за того, что многие представители данного класса имеют общую формулу: Сn(Н2О)m, где n и m >= 4. Известно множество углеводов, не соответствующих этой формуле, но несмотря на это термин «углеводы» употребляется и по сей день. Другое общепринятое название этого класса соединений – сахара.
Все углеводы можно разделить на четыре больших класса.
Моносахариды – это гетерофункциональные соединения, содержащие оксогруппу и несколько гидроксильных групп. Они не могут быть гидролизованы до более простых форм углеводов и являются структурной единицей любых углеводов, например, глюкоза, фруктоза, рибулоза, рамноза. Содержатся в различных продуктах: фрукты, мёд, некоторые виды вина, шоколад.
Олигосахариды – это соединения, построенные из нескольких остатков моносахаридов, связанных между собой гликозидной связью. Они делятся по числу моносахаридов в молекуле на дисахариды, трисахариды и т.д. К биологически активным производным олигосахаридов относятся некоторые антибиотики, сердечные гликозиды.
Дисахариды – это углеводы, которые при гидролизе дают две одинаковые или различные молекулы моносахарида и связаны между собой гликозидной связью, например, лактоза, сахароза, мальтоза. При гидролизе из дисахаридов образуется глюкоза.
Полисахариды – имеют общий принцип строения с олигосахаридами, за исключением моносахаридных остатков – полисахариды могут содержать их сотни и даже тысячи. Примеры: крахмал, гликоген, хитин, целлюлоза [2].
Для лучшего понимания реакций расщепления углеводов в организме, рассмотрим более подробно глюкозу, участвующую в этих процессах.
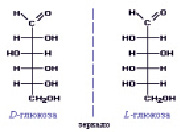
Глюкоза является одним из самых распространенных углеводов в природе, моносахарид, или гексоза С6Н12О6. Второе её название – виноградный сахар. Это растворимое в воде вещество белого цвета, сладкое на вкус. В молекуле глюкозы имеется четыре неравноценных асимметрических атома углерода (рис. 1):
Рис. 1. Строение молекулы глюкозы
Для такого соединения возможно 24 = 16 стереоизомеров, которые образуют 8 пар зеркальных оптических антиподов. Каждое из восьми соединений представляет собой диастереомер (диа – двойной) с присущими только ему физическими свойствами (растворимость, температура плавления и т.д.).
Глюкоза содержится в растительных и живых организмах. Велико ее содержание в виноградном соке, в меде, фруктах и ягодах, в семенах, листьях крапивы. Глюкоза повышает работоспособность мозга, благотворно влияет на нервную систему человека. Именно поэтому в стрессовых ситуациях люди иногда хотят чего-нибудь сладкого. Помимо этого, глюкоза применяется в медицине для приготовления лечебных препаратов, консервирования крови, внутривенного вливания и т.д. Она широко применяется в кондитерском производстве, производстве зеркал и игрушек (серебрение). Ее используют при окраске тканей и кож.
Биохимические реакции расщепления углеводов в организме человека
Для поддержания жизнедеятельности организма используется энергия, скрытая в химических связях продуктов питания. Во многих продуктах питания содержится значительное количество углеводов в виде полисахаридов (сахар, крахмал, клетчатка) и моноз (глюкоза, фруктоза, лактоза и др.). К примеру, в картофеле содержание крахмала составляет до 16 %, в рисе – 78 %, а в белом хлебе – 51 %.
Уже во рту человека начинается процесс расщепления углеводов. Происходит гидролиз крахмала под действием биологического катализатора – фермента амилазы, который содержится в пище. Под действием амилазы молекула крахмала расщепляется на довольно короткие цепочки, которые состоят из глюкозных звеньев. После этого углеводы попадают в желудок. Далее под действием желудочного сока заканчивается кислотный гидролиз крахмала. Крахмал распадается до отдельных глюкозных звеньев. Глюкоза попадает в кишечник и через стенки кишок поступает в кровь, разносящую её по всему человеческому организму.
Содержание глюкозы в крови поддерживается на постоянном уровне при помощи гормона инсулина, который выделяется поджелудочной железой. Инсулин полимеризует избыточную глюкозу в животный крахмал – гликоген, который откладывается в печени. Часть гликогена в печени может гидролизоваться в глюкозу, далее поступающую обратно в кровь. Это происходит при понижении содержания глюкозы в крови. Если поджелудочная железа не может вырабатывать инсулин, содержание глюкозы в крови повышается, что приводит к диабету. Именно поэтому людям, болеющим сахарным диабетом, необходимо регулярно вводить в кровь инсулин.
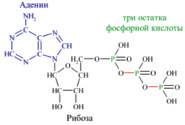
Молекула глюкозы, попадая в клетку организма, окисляется, «сгорает» с образованием воды и диоксида углерода. При этом выделяется энергия, необходимая организму для движения, согревания, осуществления различных физических нагрузок и т.д. Но биологическое окисление глюкозы похоже на обычное горение лишь по своим конечным результатам. Биологическое окисление – процесс медленный, многоступенчатый. Только малая часть высвобождаемой при окислении энергии превращается на каждой стадии данного процесса в тепло. Значительная доля энергии, заключенной в химических связях глюкозы, расходуется на образование других веществ, из которых важнейшее в биоэнергетике – аденозинтрифосфорная кислота C10H16N5O13P3 (АТФ). Это соединение состоит из трех частей – гетероцикла аденина, рибозы (сахара) и трех остатков фосфорной кислоты, образующей с рибозой сложный эфир (рис.2).
Рис. 2. Структура аденозинтрифосфорной кислоты
АТФ в клетках – универсальная энергетическая валюта. Множество ферментов умеют вести химические реакции, осуществляющиеся с затратой энергии, за счет гидролитического отщепления одного или двух остатков фосфорной кислоты от молекулы АТФ (этот процесс сопровождается выделением энергии), или наоборот, умеют использовать энергию, которая высвобождается в реакциях с выделением энергии для того, чтобы АТФ образовалась. Расщепляя АТФ, клетка использует высвобождаемую энергию на биосинтез различных соединений, а окисляя углеводы – синтезирует АТФ.
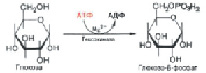
Первая стадия «сгорания» глюкозы в клетке – взаимодействие глюкозы с АТФ (рис. 3). При этом АТФ переходит в АДФ (аденозиндифосфат C10H15N5O10P2), а глюкоза – в 6-фосфат. Этот процесс фосфорилирования происходит под действием фермента гексокиназы за счет перенос остатка фосфорной кислоты (H3PO4) от фосфорилирующего агента – донора к субстрату:
Рис. 3. Взаимодействие глюкозы с АТФ
Следующий этап окисления – «рокировка» глюкозофосфата во фруктозофосфат, который происходит под действием фермента изомеразы (рис.4). Рокировка типа глюкоза–фруктоза делает доступным для фосфорилирования еще один гидроксил сахара (т.к. взаимодействовать с АТФ могут только краевые гидроксилы):
Рис. 4. Взаимодействие глюкозо-6-фосфата и фермента изомеразы
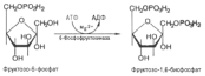
После второго фосфорилирования уже под действием другого фермента – фосфорфруктокиназы – получается в итоге фруктозо-1,6-дифосфат (C6H14O12P2 ) (рис.5):
Рис. 5. Взаимодействие фруктозо-6-фосфата и 6-фосфоруктокиназы
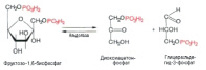
Фруктозо-1,6-дифосфат распадается на две части. Получается дигидроксиацетонфосфат ( C3H7O6P ) и глицеральдегид-3-фосфат ( C3H7O6P) (рис. 6).
Рис. 6. Распад Фруктозо-1,6-дифосфата
Клетке нужен только второй продукт, и она с помощью фермента изомеразы превращает первый фосфат во второй (чтобы не было отходов производства) (рис. 7).
Рис. 7. Превращение диоксиацетон-фосфата в глицеральдегид-3-фосфат
На данной стадии в реакцию вступают два соединения: глутатион – соединение, несущее меркаптогруппу SН и никотинамидаденинуклеотид (НАД). НАД легко присоединяет водород: НАД-Н2.
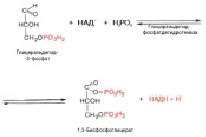
Далее развивается процесс, мало изученный в деталях, но описать его можно пока следующим образом. Под действием НАД и его восстановленной формы, фермента дегидрогеназы и фосфорной кислоты, глицеральдегид-3-фосфат превращается в смешанный ангидрид 3-фосфоглицериновой и фосфорной кислот (рис. 8).
Рис. 8. Превращение глицеральдегид-3-фосфата в смешанный ангидрид 3-фосфоглицериновой и фосфорной кислот
Всё это время энергия только поглощалась, так как АТФ переходил в АДФ. Теперь в реакции будет вступать АДФ, а в продуктах появится АТФ, и энергия будет выделяться. Так, под действием АДФ и фермента фосфоглицераткиназы образуется 3-фосфоглицериновая кислота (рис. 9).
Рис. 9. Образование 3-фосфоглицерата
В ней фермент фосфоглицеромутаза вызывает «рокировку» фосфатной группы в положение 2 (рис. 10).
Рис. 10. Превращение 3-фосфоглицерата в 2-фосфоглицерат
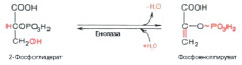
На полученный продукт воздействует фермент енолаза и АДФ – получается пировиноградная кислота (рис. 11, 12).
Рис. 11. Дегидратация 2-фосфоглицерата
Рис. 12. Перенос фосфорильной группы с фосфоенолпирувата на АДФ. Образование пирувата
Процесс превращения глюкозы в пировиноградную кислоту в клетке называется гликолизом [3]. В результате гликолиза клетка получает из одной молекулы глюкозы восемь молекул АТФ и две молекулы пировиноградной кислоты. Превращение глюкозы в пировиноградную кислоту является первой стадией, общей для нескольких процессов. То же самое происходит под действием дрожжей на раствор сахара. Но реакция не закачивается получением пировиноградной кислоты. От этой кислоты отщепляется (под действием фермента декарбоксилазы) молекула диоксида углерода и образуется уксусный альдегид, который, в свою очередь, атакуется ферментом дегидрогеназой и НАД-Н2. В результате при отсутствии кислорода получается этиловый спирт.
На самом деле уравнение этого сложного процесса выглядит довольно просто:
С6Н12О6 à 2С2Н5ОН + 2СО2
Это и есть процесс брожения. В мышцах НАД-Н2 восстанавливает пировиноградную кислоту в молочную. Это происходит при большой нагрузке, когда кровь не успевает подводить кислород в нужном количестве. Поэтому у спортсменов, пробежавших дистанцию, резко увеличивается в крови количество молочной кислоты [4].
Ферменты – это биологические катализаторы, имеющие белковую природу, помогающие ускорить химические реакции как в живых организмах, так и вне их. Ферменты обладают высокой каталитической активностью. К примеру, чтобы расщепить молекулу полиуглевода (крахмал, целлюлозу) или какой – либо белок на составные части, их нужно несколько часов кипятить с крепкими растворами щелочей либо кислот. А ферменты пищеварительных соков (пепсин, протеаза, амилаза) способны гидролизовать эти вещества буквально за несколько секунд при температуре 37 °С. Помимо этого, ферменты обладают избирательностью своего действия в отношении структуры субстрата, условий проведения реакции и её типа (фермент превращает только данный тип субстратов в определенных реакциях и условиях). Ферменты катализируют огромное количество реакций, протекающих в живой клетке при размножении, дыхании, обмене веществ и т.д. [5].
В современном понимании биохимическое расщепление углеводов – это метаболический процесс, при котором регенерируется АТФ, а продукты расщепления органического субстрата могут служить одновременно и донорами, и акцепторами водорода. Огромную роль в биохимических процессах играют микроорганизмы, ферменты и катализаторы. Считается, что анаэробный гликолиз (расщепление углеводов) был первым источником энергии для общих предков всех живых организмов до того, как концентрация кислорода в атмосфере стала достаточно высокой, и поэтому эта форма генерации энергии в клетках – более древняя. За очень редкими исключениями она существует и у всех ныне живущих клеток.
В настоящее время ученые считают, что все реакции биохимического расщепления углеводов на начальной стадии имеют общую схему вплоть до образования пировиноградной кислоты. Затем, в зависимости от условий и качества ферментов, из пировиноградной кислоты образуются конечные продукты реакции: спирты, кислоты (уксусная, лимонная, молочная, яблочная, масляная и т.д.), альдегиды, углекислый газ, водород, вода и пр.
Изучение биохимических реакций расщепления углеводов в организме человека и анализ использованных источников позволили сделать следующие выводы:
1. В общем виде схему механизма расщепления углеводов можно представить следующим образом: сложный углевод (дисахарид, полисахарид) à глюкоза à эфиры фосфорных кислот à глицериновый альдегид à глицериновая кислота à пировиноградная кислота à далее возможны любые упомянутые выше направления.
2. Биохимические реакции углеводов лежат в основе жизнедеятельности клеток живых организмов, в том числе и человека.
3. Биохимические процессы расщепления углеводов, которые изображаются простыми, на первый взгляд, уравнениями начальных и конечных продуктов, на самом деле представляют собой сложные и многоступенчатые процессы.
4. Для осуществления биохимических процессов необходимы ферменты и катализаторы, которые ускоряют реакции расщепления углеводов в тысячи раз.
Изучая сложнейшие процессы, происходящие в живой клетке, ученые задумываются: а нельзя ли, научившись у природы, провести в колбах и ретортах искусственные химические процессы, копирующие биохимические реакции? Начатые по инициативе академика Н.Н. Семенова, такие исследования в области «химической бионики» успешно ведутся в России и во всем мире [6].