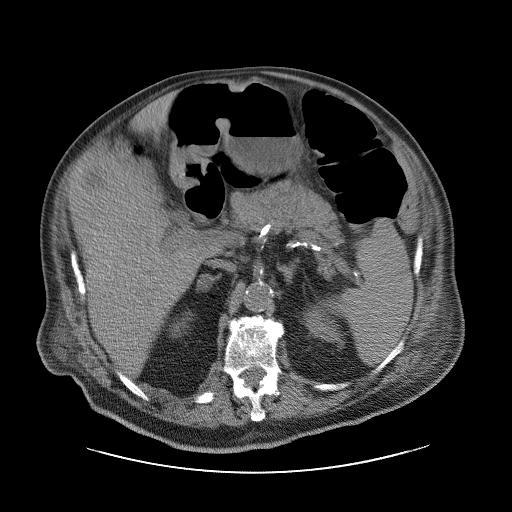
Нативная плотность что это
аденома надпочечника
Конрастируют, когда имеются сомнения в доброкачественности. В вашем случае контрастирование не нужно.
Это очень приятная новость)))
Но я успокоюсь, когда пойму почему сомнений нет)))
хотябы в двух словах, умоляю)
Это очень приятная новость)))
Но я успокоюсь, когда пойму почему сомнений нет)))
хотябы в двух словах, умоляю)

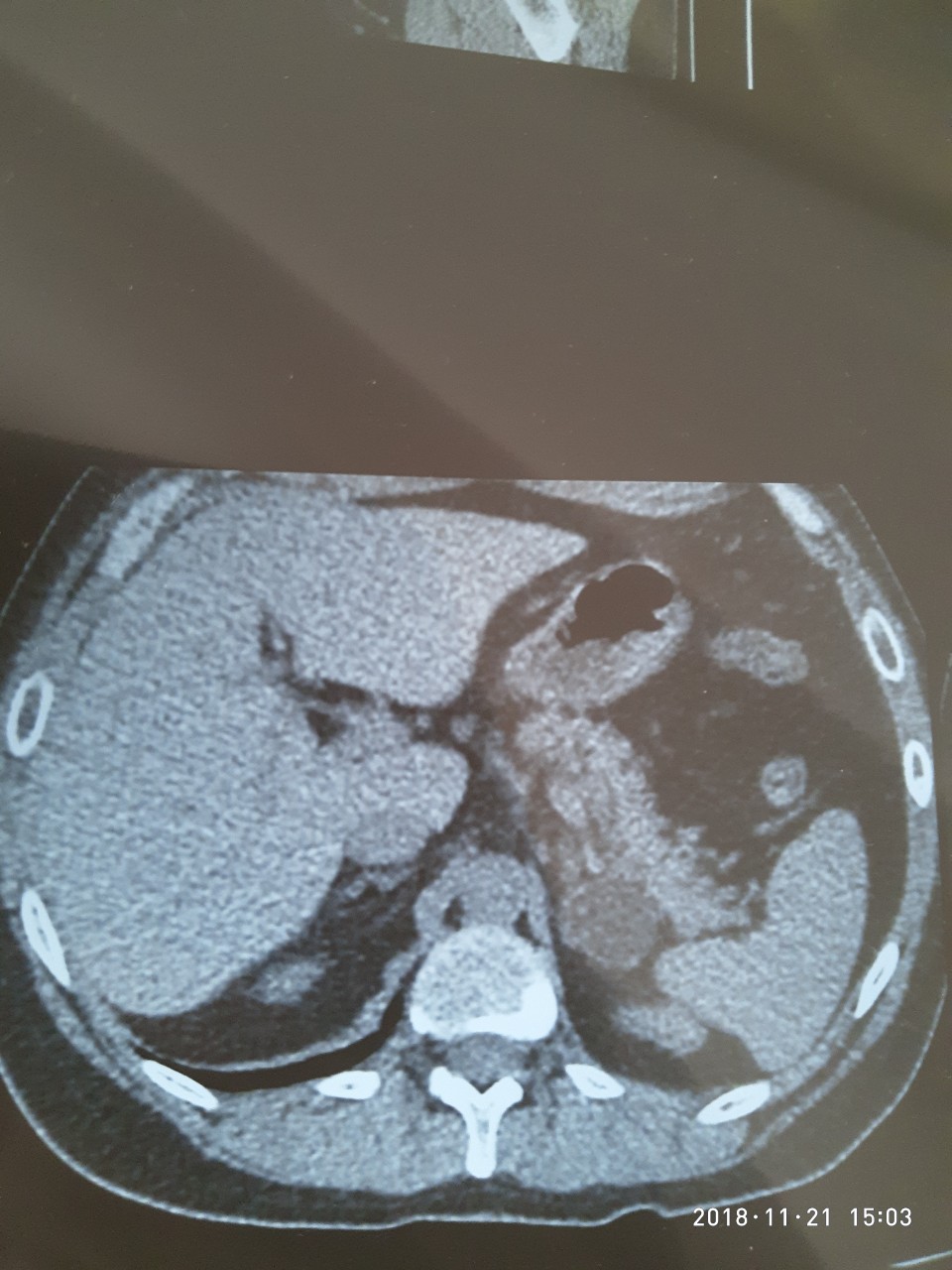





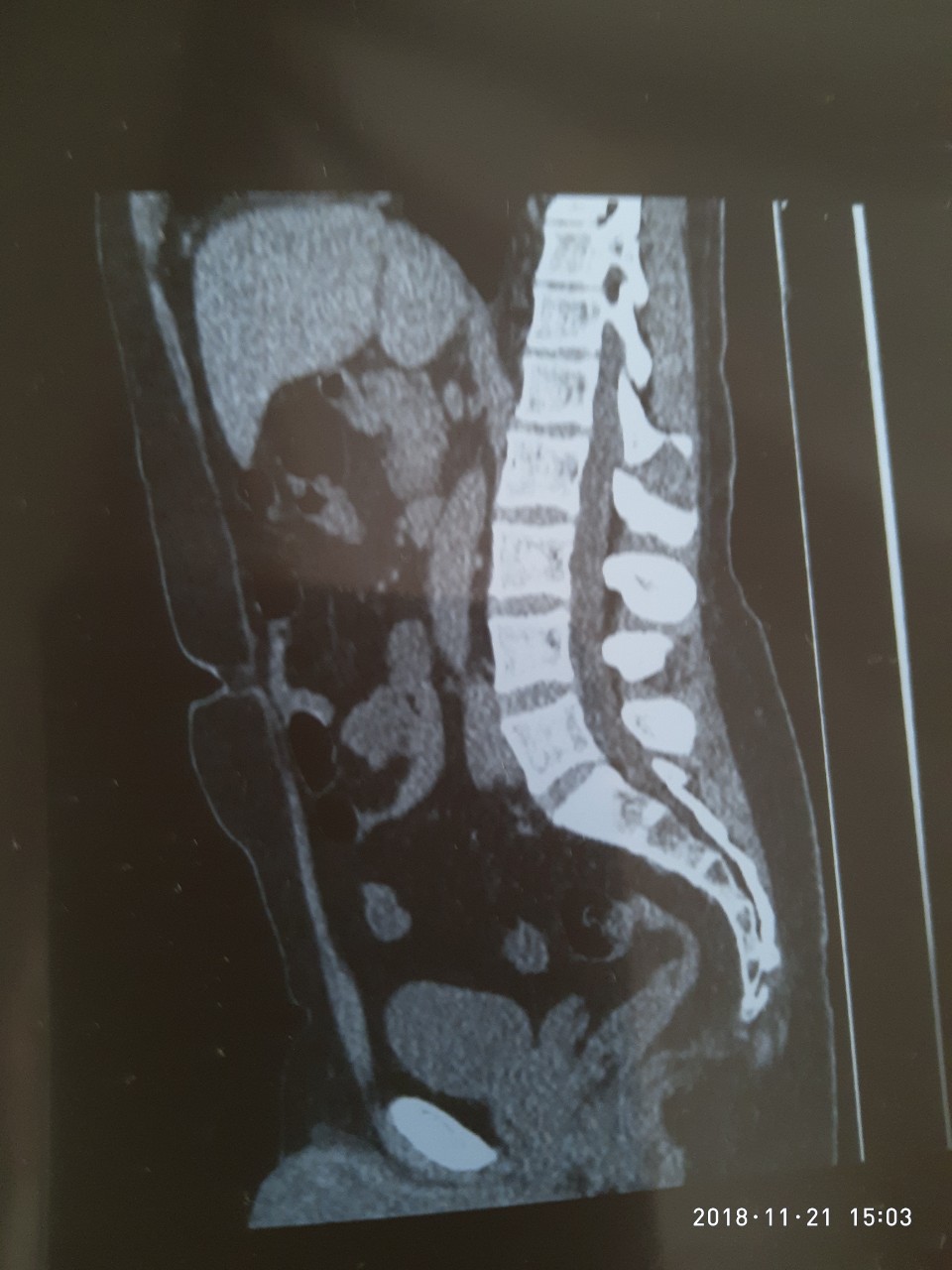
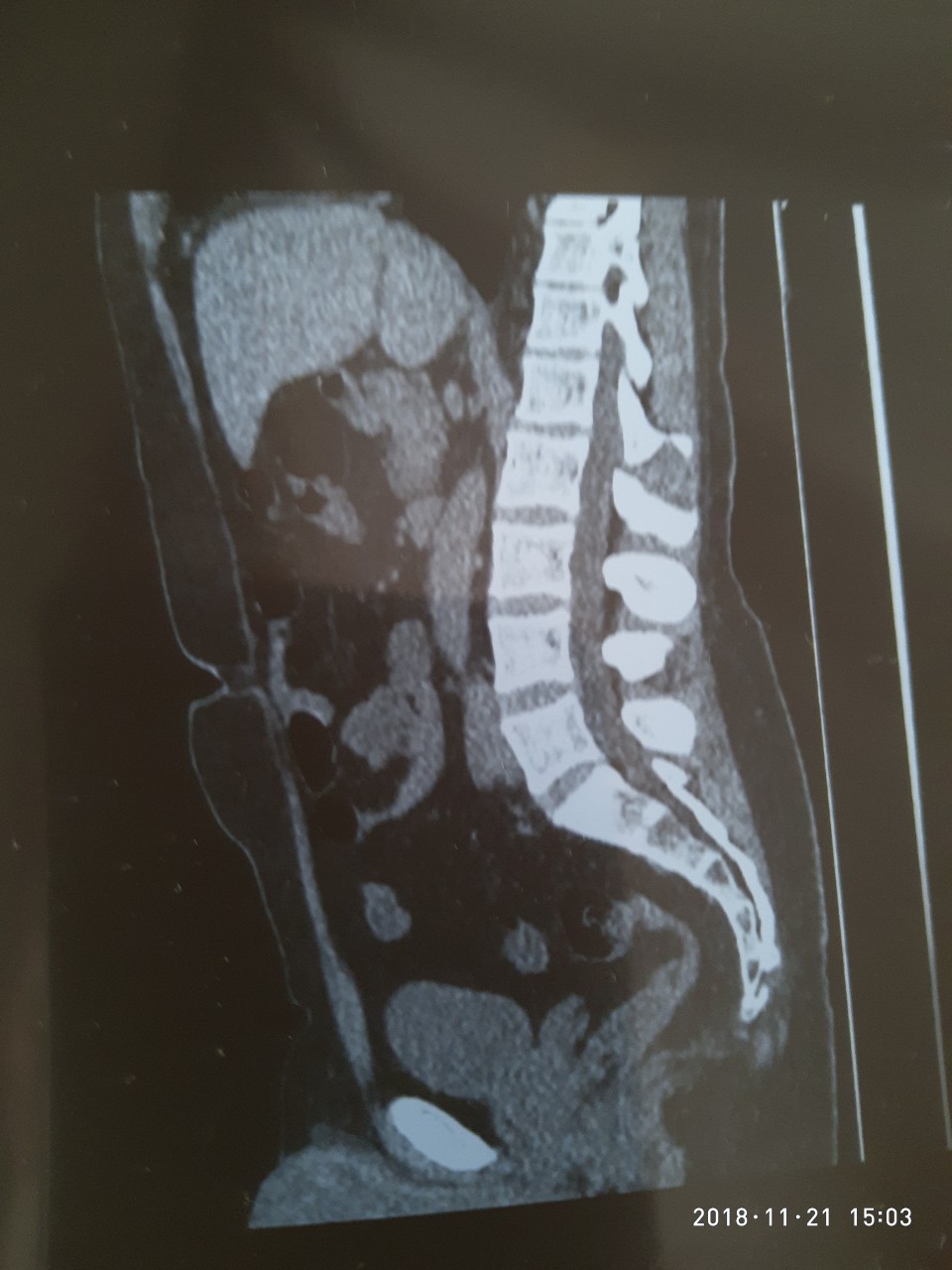
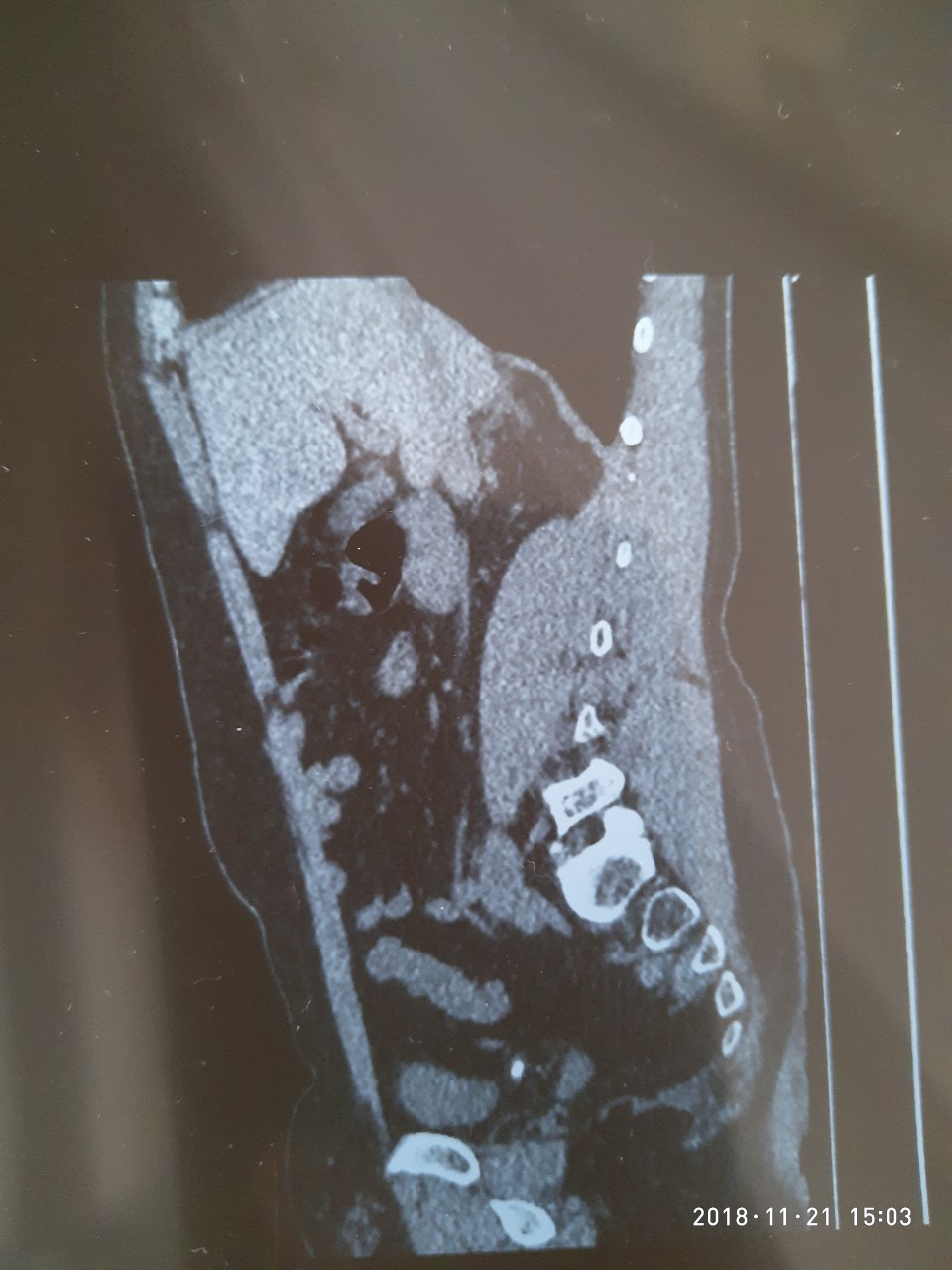

Это очень приятная новость)))
Но я успокоюсь, когда пойму почему сомнений нет)))
хотябы в двух словах, умоляю)
Есть плёнка отфотканная, правда качество может не ахти)
Повторюсь, контрастирование здесь не показано.
Повторюсь, контрастирование здесь не показано.
Спасибо Вам большое. Успокоился))) Спасибо за то, что не игнорируете такие идиотские заморочки как моя) Это очень профессионально. Удачи Вам) и успеха!
Нативная плотность что это
Эндокринологический научный центр, Москва
ФГУ Эндокринологический научный центр, Москва
ФГУ Эндокринологический научный центр, Москва
ФГУ Эндокринологический научный центр Минздравсоцразвития РФ
ФГУ Эндокринологический научный центр Минздравсоцразвития РФ
Эндокринологический научный центр, Москва
ФГУ Эндокринологический научный центр Минздравсоцразвития РФ
Городская клиническая больница №68, Москва
ФГУ Эндокринологический научный центр Минздравсоцразвития Российской Федерации
Городская клиническая больница №52, Москва
ГБОУ ВПО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России, Москва, Россия
Дифференциальная диагностика инциденталом надпочечников
Журнал: Проблемы эндокринологии. 2011;57(6): 3-8
Бельцевич Д. Г., Солдатова Т. В., Кузнецов Н. С., Ремизов О. В., Воронцов А. В., Рогаль Е. Ю., Ванушко В. Э., Кулезнева Ю. В., Кац Л. Е., Лысенко М. А., Мельниченко Г. А. Дифференциальная диагностика инциденталом надпочечников. Проблемы эндокринологии. 2011;57(6):3-8.
Bel’tsevich D G, Soldatova T V, Kuznetsov N S, Remizov O V, Vorontsov A V, Rogal’ E Iu, Vanushko V É, Kulezneva Iu V, Kats L E, Lysenko M A, Melnichenko G A. Differential diagnostics of adrenal incidentalomas. Problemy Endokrinologii. 2011;57(6):3-8.
Эндокринологический научный центр, Москва
Эндокринологический научный центр, Москва
ФГУ Эндокринологический научный центр, Москва
ФГУ Эндокринологический научный центр, Москва
ФГУ Эндокринологический научный центр Минздравсоцразвития РФ
ФГУ Эндокринологический научный центр Минздравсоцразвития РФ
Эндокринологический научный центр, Москва
ФГУ Эндокринологический научный центр Минздравсоцразвития РФ
Городская клиническая больница №68, Москва
ФГУ Эндокринологический научный центр Минздравсоцразвития Российской Федерации
Городская клиническая больница №52, Москва
ГБОУ ВПО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России, Москва, Россия
Собирательный термин «инциденталома» надпочечника включает разнообразную по морфологии группу опухолей более 1 см в диаметре, случайно выявленных при радиологическом обследовании. Выявленное образование может оказаться как гормонально неактивным, так и активно производящим различные гормоны, может исходить из различных зон надпочечника или иметь неспецифичную органную принадлежность, может быть как злокачественным, так и доброкачественным. По данным сводной аутопсийной статистики [1, 6], распространенность случайно выявленных опухолей надпочечника колеблется от 1 до 32%, составляя в среднем 6%. По данным КТ, «случайные» образования надпочечника выявляются приблизительно у 4% обследованных пациентов [2]. В возрасте до 30 лет инциденталома встречается приблизительно у 0,2% обследованных, но в группе пациентов старше 70 лет ее частота возрастает до 7%.
Актуальны два основных вопроса: 1) доказательный диагноз в отношении гормональной активности опухоли и 2) определение злокачественного потенциала опухоли. В отношении первичной гормональной диагностики опухолей надпочечников клинические рекомендации имеют достаточную доказательную базу [3—5]. При оценке же злокачественного потенциала опухоли основным критерием показаний к операции является размер новообразования. Данные о семиотике лучевых методов исследования достаточно обширны, однако их интерпретация в отношении возможной злокачественности опухоли надпочечника крайне противоречива. Основное внимание при диагностике адренокортикального рака (АКР) сконцентрировано на количественных показателях трехфазного КТ, однако агрессивность (1 раз в 6 мес) динамического КТ-наблюдения ставит вопрос об индуцированных онкологических заболеваниях [3]. Тотальная пункционная биопсия опухолей надпочечников не продемонстрировала улучшения дифференциальной диагностики инциденталом. Напротив, она привела к росту осложнений, а также ложноположительным и ложноотрицательным заключениям.
Чувствительность современных радиологических методов в отношении выявления опухолей надпочечников близка к абсолютной. Однако отсутствие специфичных критериев злокачественности привело к тому, что основным фактором в решении вопроса о необходимости операции у больных с отсутствием гормональной активности является размер опухоли.
Мы сформулировали следующие вопросы:
1. Какова специфичность описательных характеристик КТ, МРТ, УЗИ в дифференциальной диагностике АКР и аденом надпочечника?
2. Каково диагностическое значение (cut-off) нативной КТ-плотности, меньше которого практически отсутствует вероятность АКР?
3. Какие дополнительные преимущества имеет трехфазное КТ перед однофазным?
4. Какова вероятность феохромоцитомы при инциденталоме с низкой нативной КТ-плотностью?
5. Каковы показания к пункции опухоли надпочечника?
6. Является ли безопасным динамическое наблюдение больных с гормонально неактивными опухолями с низкой нативной КТ-плотностью?
Материал и методы
Для ретроспективного анализа корреляции между морфологическим вариантом опухоли и дооперационными радиологическими данными использовались истории болезни 177 больных, оперированных в ЭНЦ с 2006 по 2010 г. Мужчины составили 32,2% (n=57), женщины — 67,8% (n=120).
У всех больных определяли:
— утренние уровни кортизола в плазме на фоне подавляющего теста с 1 мг дексаметазона (автоматизированная система Vitros);
— содержание метанефрина, норметанефрина в суточной моче методом иммуноферментного анализа с помощью коммерческих наборов фирмы IBL (Германия);
— уровень альдостерона, активность ренина плазмы («Immunotech», РИА), соотношение альдостерон/активность ренина плазмы. Данные показатели определяли только при наличии у пациента артериальной гипертонии (АГ).
Морфологические варианты удаленных опухолей представлены в табл. 1. 
Статистический анализ был выполнен с помощью программы Statistica, StatSoft, США, версия 6.0. Количественные признаки, имеющие приближенно нормальное распределение, описывались в виде M±SD. Количественные признаки, не имеющие приближенно нормального распределения, а также количественные признаки малых выборок независимо от вида распределения описывались медианой и интерквантильным размахом Me(X¼;X¾). За критический уровень значимости принималось значение p=0,05.
Результаты
Оценка чувствительности и специфичности УЗИ, КТ, МРТ, пункционной биопсии в дифференциальном диагнозе опухолей надпочечников
При выполнении УЗИ, КТ, МРТ выявлялись все опухоли надпочечников (в том числе двусторонние) независимо от размера. Таким образом, чувствительность всех методов лучевой диагностики в отношении выявления опухолей надпочечников достигает 100%. Мы не установили каких-либо различий между ультразвуковыми критериями АКР, феохромоцитом и аденом надпочечников больших размеров. Все указанные опухоли имели гипоэхогенную структуру. Среди феохромоцитом отмечались полициклические опухоли, имеющие вследствие этого бугристый контур; в то же время среди 12 больных с АКР в 6 наблюдениях контуры опухоли были четкими, структура однородная. Специфичность УЗИ при АКР — 50%; при миелолипомах и кистах надпочечников — 100%.
При МРТ у феохромоцитомы и АКР была отмечена наиболее высокая интенсивность сигнала (по сравнению с паренхимой печени) на Т2-взвешенных изображениях. Однако у 7 из 24 больных с аденомами надпочечников при изменениях печени (жировой гепатоз, гепатит) был также отмечен гиперинтенсивный Т2-сигнал. Основным недостатком МРТ (без применения chemical shift imagine) является невозможность количественной оценки плотностных характеристик. При МРТ лишь в 1 наблюдении из 6 было высказано предположение о кистозной природе образования, в 5 наблюдениях поставлен диагноз опухоли солидного строения. При миелолипоме (n=6), по данным МРТ, всем пациентам был поставлен неспецифический диагноз (опухоль надпочечника).
Таким образом, УЗИ и рутинная МРТ надпочечников эффективны при выявлении опухоли и целесообразны для динамического контроля за размерами опухоли. Дифференциальный диагноз АКР и аденом надпочечников больших размеров на основании УЗИ и МРТ нецелесообразен. УЗИ высокоспецифично при дифференциальном диагнозе опухолей надпочечника с кистами и миелолипомами.
При оценке данных КТ описательные характеристики опухоли, как и при УЗИ и МРТ, не являются определяющими в дифференциальном диагнозе инциденталом. Тем не менее четко прослеживается возможность разделения опухолей по признаку нативной плотности. Отмечается высокая нативная плотность у АКР (37,4±5,8 ед. Н), феохромоцитомы (31,4±3,7 ед. Н), ганглионейромы (36,6±5 ед. Н) и метастазов (43,6±9 ед. Н). С другой стороны, отмечается низкая плотность у аденом надпочечника (0,4±10,7 ед. Н) независимо от отсутствия или наличия гормональной активности, миелолипом (–48±27,7 ед. Н) и кист (6±8,2 ед. Н). Различия между указанными группами высокой и низкой нативной КТ-плотности статистически значимы (р 
В дифференциальном диагнозе между гормонально-неактивными аденомами и АКР показатели высокой нативной КТ-плотности продемонстрировали абсолютную чувствительность (ни один АКР не был пропущен); специфичность составила 95% (3 из 59 больных с аденомами 4, 5 и 6 см в диаметре продемонстрировали нативную КТ-плотность более 25 ед. Н и были прооперированы).
В табл. 3 указаны параметры, демонстрирующие, что при АКР, метастазах и феохромоцитоме в сравнении с аденомами и миелолипомами отмечается большее амплитудное повышение плотности при контрастировании и задержка контраста в отсроченную фазу. Однако именно у 3 из 59 больных с аденомами, у которых была отмечена относительно высокая нативная КТ-плотность, наблюдалось амплитудное повышение контрастной плотности и замедленное вымывание контраста. Таким образом, роль трехфазного КТ в нашем исследовании сомнительна; применение метода не дало никаких преимуществ по сравнению с определением нативной плотности при дифференциальной диагностике аденомы от АКР. В тех наблюдениях, где отмечена низкая нативная плотность, применение контрастирования не привело к дополнительной настороженности в отношении АКР, однако в нескольких наблюдениях дало возможность поставить диагноз кисты (из-за отсутствия колебаний КТ-плотности на разных фазах). Тем не менее 4-кратное увеличение лучевой нагрузки для постановки диагноза кисты нецелесообразно при возможности патогномоничного диагноза кисты с помощью УЗИ.
Ранее для оценки злокачественного потенциала опухоли наиболее часто использовался такой критерий, как размер опухоли. Считается, что показанием к адреналэктомии является размер опухоли 4—5 см; при размере более 6 см риск АКР возрастает до 25%. В табл. 4 
Таким образом, использование в качестве критерия лишь размер опухоли более 4 см в оценке вероятного АКР привело к необоснованным оперативным вмешательствам у 1 /3 пациентов с аденомами. Диагностический комплекс «размер опухоли и нативная КТ-плотность» повышает специфичность дифференциального диагноза аденомы и АКР.
На основании плотностных КТ-характеристик дифференциальный диагноз между АКР и феохромоцитомой невозможен. Однако при достижении феохромоцитомой размеров более 3 см во всех наблюдениях уровень метилированных производных катехоламинов был достоверно повышен. Таким образом, рассматривая диагностический комплекс «нативная КТ-плотности + фракционированные метанефрины», нужно констатировать его абсолютную чувствительность в отношении феохромоцитомы (ни одна феохромоцитома не была пропущена). Cпецифичность составила 94% за счет 3 больных с ганглионейромами, которые имели высокую нативную КТ-плотность и значительно повышенный уровень норметанефрина.
При феохромоцитоме суточная экскреция фракционированных метанефринов (метанефрина и норметанефрина) была значительно повышена, что свидетельствовало об опухолевой секреции катехоламинов. Медиана уровня фракционированных метанефринов при различных вариантах опухолей надпочечников представлена в табл. 5.
Чувствительность метода определения фракционированных метанефринов (метилированных производных катехоламинов — МПК) в отношении феохромоцитомы составила 100%, специфичность — 86,8%. Повышение уровня норметанефрина отмечено у 12 из 114 пациентов с опухолями надпочечников нехромаффинного генеза (у 1 больной с АКР, у 2 с миелолипомами, у 9 с аденомами коры надпочечника). Средний уровень норметанефрина в этих наблюдениях составил 512±132 мкг/сут (норма до 430 мкг/сут), что значительно отличалось от таковой у пациентов с феохромоцитомой. У 3 пациентов с ганглионейромами надпочечника отмечено повышение уровня норметанефрина до значительных цифр (1871±129 нмоль/сут). У этих больных опухоли 4, 8 и 12 см в диаметре имели высокую нативную КТ-плотность, что не противоречило диагнозу феохромоцитомы.
У 56 пациентов с аденомами и низкой нативной плотностью по КТ независимо от наличия или отсутствия АГ диагноз феохромоцитомы не подтвердился. В то же время у 49 пациентов с феохромоцитомой нативная КТ-плотность тканевого компонента опухоли была не менее 25 ед. Н. Из этого следует, что при опухолях надпочечника солидного строения с низкой нативной КТ-плотностью вероятность феохромоцитомы крайне мала, и поэтому определение метилированных производных катехоламинов нецелесообразно. Для повышения специфичности метода определения фракционированных метанефринов при опухолях надпочечников используют пробу с клонидином, сцинтиграфию с МИБГ, исследование хромогранина А. По результатам нашей работы можно сделать вывод, что при низкой нативной КТ-плотности опухоли надпочечника солидного строения повышение уровня фракционированных метанефринов можно считать ложноположительным результатом. Таким образом, показатель нативной КТ-плотности необходимо учитывать при трактовке результатов уровня фракционированных метанефринов.
Предоперационная биопсия. Пункция опухоли надпочечников была произведена у 22 больных. Во всех случаях АКР, в которых проводилась пункция, размер опухоли был более 10 см. Только у 2 больных на фоне некротического детрита выявлены клетки злокачественной опухоли, у 2 — подозрение на феохромобластому, у 1 двукратно получен неинформативный материал. Таким образом, правильный диагноз АКР при предоперационном цитологическом исследовании установлен в 2 из 5 наблюдений (чувствительность 40%); ни в одном случае это исследование не повлияло на лечебную тактику.
У 8 пациентов с феохромоцитомой пунктированные опухоли имели размер от 6 до 12 см. В 5 из 8 наблюдений уровень фракционированных метанефринов был значительно выше референсных значений, не вызывая сомнений в диагнозе феохромоцитомы, у 3 на момент пункции определение метанефринов не проводили. Результаты цитологического исследования у больных с феохромоцитомой были следующими: в 2 наблюдениях — АКР, в 3 — опухоль хромаффинной ткани, в 3 — результат исследования неинформативен. У 1 больной в результате пункции развился пневмоторакс, у 1 (при отсутствии предоперационной подготовки) интраоперационно развилась «неуправляемая гемодинамика». Таким образом, правильный диагноз феохромоцитомы при предоперационном цитологическом исследовании установлен в 3 из 8 наблюдений (чувствительность 37,5%).
У 9 больных пункционная биопсия проводилась в связи с наличием в анамнезе рака вненадпочечниковой локализации. У 6 пациентов из 9 выявлены метастазы в надпочечники (у 3 — рак почки, у 2 — рак предстательной железы, у 1 — рак желудка). В 3 наблюдениях пункции были неинформативными; у 1 больной гистологически подтверждена светлоклеточная аденома надпочечников; у 2 больных на основании длительного наблюдения и низкой нативной КТ-плотности не было достаточных оснований подозревать метастазы рака иной локализации. Пункционная биопсия позволила у всех больных выявить метастазы опухолей иной локализации в надпочечник. Чувствительность пункционной биопсии при подозрении на метастазы составила 100%.
Таким образом, метод пункционной биопсии опухолей надпочечников имеет высокую чувствительность при дифференциальной диагностике метастатического поражения надпочечников. В остальных случаях (когда нет анамнестических данных о раке иного органа) чувствительность и специфичность метода неудовлетворительны, результаты цитологического исследования не влияют на лечебную тактику.
Результаты динамического наблюдения гормонально-неактивных опухолей с низким злокачественным потенциалом
Проанализированы данные 136 пациентов, которые были направлены на консультацию в ЭНЦ по поводу инциденталомы в 2009—2010 гг. В данной подгруппе было 25% мужчин (n=19) и 75% женщин (n=57). Средний возраст составил 59±17 лет. В результате проведенного гормонального и дополнительного топического обследования у 60 (44,1%) пациентов установлены показания к операции, исходя из доказанной гормональной активности или высокого злокачественного потенциала опухоли. Среди оперированных больных 26 (43,3%) мужчин и 34 (56,3%) женщины.
У 76 (55,9%) из 136 больных показаний к операции не установлено. При стандартном обследовании доказаны отсутствие гормональной активности и низкий злокачественный потенциал опухоли (на основании нативной КТ-плотности менее 20 ед. Н. или жидкостной структуры опухоли по данным УЗИ). Возраст больных колебался от 21 года до 83 лет (в среднем 59±17 лет).
Срок наблюдения за больными колебался от 8 до 120 мес (медиана срока наблюдения 24,9±19 лет). В течение последних 2 лет больным проводилось УЗИ или КТ для контроля за размером образования. Периодичность обследования составляла 6—12 мес. Ежегодно проводилось повторное гормональное исследование в указанном объеме. За время наблюдения ни у одного пациента не выявлено «быстрого» (более 0,5 см за 6 мес) роста опухоли, которое могло свидетельствовать о злокачественном характере образования. Ни у одного больного не выявлено феохромоцитомы и гиперальдостеронизма. У 1 пациентки выявлен субклинический гиперкортицизм. Таким образом, в выделенной по указанным критериям группе больных за время динамического наблюдения диагностических ошибок отмечено не было.
Выводы
1. Дифференциальный диагноз АКР и аденом надпочечников на основании УЗИ и рутинного МРТ нецелесообразен. УЗИ и МРТ показаны для динамического контроля размеров опухоли. УЗИ имеет высокую специфичность в диагностике кист и миелолипом.
2. При высокой нативной КТ-плотности опухоли надпочечника более 20 ед. H — динамическое наблюдение нецелесообразно.
3. Динамическое наблюдение при опухолях надпочечников показано при отсутствии гормональной активности (по результатам стандартизированного гормонального обследования) и при нативной КТ-плотности менее 20 ед. H, а также при кистозной структуре опухоли по данным УЗИ.
4. При низкой КТ-плотности опухоли надпочечника солидного строения вероятность феохромоцитомы крайне мала. Показатель нативной КТ-плотности необходимо учитывать при трактовке результатов уровня фракционированных метанефринов. При опухолях надпочечников солидного строения с низкой КТ-плотностью диагностический поиск феохромоцитомы нецелесообразен.
5. Метод пункционной биопсии опухолей надпочечников имеет высокую чувствительность при дифференциальном диагнозе метастатического поражения надпочечников. В остальных случаях цитологическое исследование не показано.
6. Определение уровня фракционированных метанефринов обладает высокой чувствительностью и специфичностью в дифференциальном диагнозе АКР и феохромоцитомы при опухолях с высокой нативной плотностью (>20 ед. H).
7. Предложен алгоритм диагностики инциденталом надпочечника (см. рисунок). 
Работа выполнена в рамках проекта «Оптимизация методов диагностики и лечения нейроэндокринных опухолей» Федеральной целевой программы «Научные и научно-педагогические кадры инновационной России» на 2009—2013 гг.
Аденома надпочечника: диагностика, симптомы, лечение
ЧТО ТАКОЕ АДЕНОМА НАДПОЧЕЧНИКА
Аденома коры надпочечника является распространенной доброкачественной опухолью, возникающей из коры надпочечников — маленьких парных органов внутренней секреции, расположенных вблизи верхнего края почек. Чаще она встречается у взрослых, но может обнаруживаться у лиц любого возраста. Эти образования могут быть как гормонально активными и выделять повышенные количества гормонов, так и клинически «немыми». Аденомы не считаются потенциально опасными в отношении озлокачествления.
Аденому коры надпочечников можно диагностировать с высокой степенью точности: специфичность анализа результатов методов визуализации, таких как КТ и МРТ, варьирует в пределах от 95 до 99%, а чувствительность превышает 90%. Эти впечатляющие цифры являются результатом относительно высокой распространенности надпочечниковых аденом в общей популяции и обширных рентгенологических исследований при помощи методов визуализации, в первую очередь КТ и МРТ.
Сделать КТ надпочечников в Санкт-Петербурге
ПРИЧИНЫ И СИМПТОМЫ
Точная причина, которая приводит к адреноме надпочечников, неизвестна. Однако некоторые ученые и исследователи считают, что это состояние может быть вызвано мутацией в определенных генах. Во-вторых, в большинстве случаев установлено, что адренома надпочечников присутствует у людей, страдающих наследственными генетическими нарушениями. Адреномы надпочечников могут быть двух типов: функциональных и нефункциональных. Некоторые аденомы выделяют гормоны, и, следовательно, они известны как функциональные аденомы. Другие аденомы не выделяют гормоны и, следовательно, они нефункциональны. Функциональные аденомы более опасны, так как гормоны, продуцируемые этими аденомами, могут вызывать серьезные расстройства, такие как синдром Кушинга (из-за гормонального кортизола), синдром Конна (из-за гормона альдостерона), гиперандрогенизм (из-за гормональных андрогенов). Специфических симптомов, связанных с адреномой надпочечником, нет, однако можно наблюдать симптомы, связанные с любым из вышеупомянутых состояний.
АДЕНОМА ИЛИ МЕТАСТАЗ РАКА?
Среди всех органов надпочечник находится на четвертом месте по частоте метастазирования злокачественных опухолей. Наиболее часто метастазируют в надпочечники опухоли легкого, молочной железы, рака толстой кишки и рака поджелудочной железы. Метастазы надпочечников встречаются у 25% пациентов с выявленными первичными опухолевыми очагами. Поэтому радиологи часто сталкиваются с задачей определить, является ли образование доброкачественным или злокачественным. Решение это вопроса является крайне важным и может непосредственно повлиять на тактику лечения пациента. Например, дополнительное обследование пациента по поводу операбельного рака легкого поможет выявить наличие надпочечникового образования и предположить возможность метастатического поражения. В случае неоднозначных результатов исследования для снижения риска врачебных ошибок прибегают ко второму мнению. Повторная оценка результатов КТ или МРТ осуществляется специалистом высокой квалификации из профильного медицинского центра.
Дифференциальная диагностика опухолей надпочечников включает множество первичных, метастатических, доброкачественных и злокачественных новообразований, большинство из которых здесь подробно не обсуждаются. Вместо этого статья содержит практическую информацию, которая относится к надпочечниковым аденомам.
ЛУЧЕВАЯ ДИАГНОСТИКА АДЕНОМ НАДПОЧЕЧНИКОВ
Методами выбора при оценке образования надпочечников являются компьютерная томография (КТ), магнитно-резонансная томография (МРТ) и позитронно-эмиссионная томография (ПЭТ). Ультразвуковое исследование играет определенную роль в оценке возможного наличия опухолей надпочечников у младенцев, но не существует специфических УЗИ-признаков для определения доброкачественной аденомы надпочечников. При анализе снимков врачам нужно обращать внимание, что на КТ- и МРТ-сканах внешний вид внутрицитоплазматических липидов отличается от макроскопического жира, как в случае миелолипомы.
РАСШИФРОВКА КТ И МРТ НАДПОЧЕЧНИКОВ
Как следует рентгенологу приступать к оценке случайно выявленного небольшого образования надпочечника? Необходимо ответить на два важных вопроса.
Во-первых, есть ли у пациента гормональные или биохимические нарушения, которые могут быть вызваны увеличенной надпочечниковой железой? Если это так, то очаговое образование должно быть удалено хирургическим путем, независимо от особенностей изображения.
Во-вторых, есть ли у пациента выявленное злокачественное заболевание? При отсутствии установленного рака вероятность того, что небольшое, хорошо ограниченное надпочечниковое образование является злокачественным, почти равна нулю. Описание характера образования имеет решающее значение для пациентов с установленным злокачественным заболеванием, для которых диагноз метастазов в надпочечники исключает хирургическое вмешательство.
Исследователи полагают, что КТ без внутривенного контрастного усиления должно быть стартовым исследованием. Если плотность объемного образования меньше 10 единиц Хаунсфилда (HU), то можно поставить диагноз аденомы надпочечников. Если надпочечниковое образование составляет по плотности более 10 HU, должно последовать КТ с внутривенным введением контрастного вещества и расчет его вымывания; доброкачественные образования обычно демонстрируют более 50% вымывания. В случаях, когда результаты КТ сомнительные, следует провести МРТ с выполнением программ, чувствительных к феномену химического сдвига. Если результаты обоих методов неубедительны, можно воспользоваться вторым мнением. Биопсия надпочечника рекомендована только в случае наличия злокачественной опухоли другого органа.
ОГРАНИЧЕНИЯ МЕТОДОВ
По очевидным соображениям следует принять во внимание доступность и стоимость КТ и МРТ. Промедление с выполнением КТ-визуализации из-за очереди на томограф потенциально снижает эффективность самой процедуры, так как может привести к многочисленным предварительным обследованиям, а также подвергнуть пациента дополнительному воздействию ионизирующего излучения. МРТ-исследование позволяет проводить диагностику, не подвергая пациента воздействию радиации; однако МРТ не может быть настолько доступной, как КТ, и может оказаться дороже.
РЕНТГЕНОГРАФИЯ ПРИ АДЕНОМЕ НАДПОЧЕЧНИКА
Несмотря на то, что простые рентгенограммы могут быть полезны для описания старого кровоизлияния в надпочечник или, главным образом, кальцинированных надпочечниковых новообразований, они не играют существенной роли в диагностике аденомы коры надпочечников и в настоящее время выполняться не должны.
КОМПЬЮТЕРНАЯ ТОМОГРАФИЯ ПРИ АДЕНОМЕ НАДПОЧЕЧНИКА
КТ, наряду с МРТ, является одним из методов выбора при диагностике опухоли надпочечниковой железы. При КТ-сканировании аденомы коры надпочечников являются хорошо контурированными объемными образованиями, гомогенными по своим характеристикам плотности. Оценка должна выполняться с использованием толщины среза в 5 мм или еще меньше для гарантии того, что на измерения плотности не повлияет объемное усреднение.
Как выглядит аденома надпочечника? В правом надпочечнике видно однородное, четко ограниченное образование овоидной формы с рентгеновской плотностью 7-HU; его обнаружение является характерным для доброкачественной аденомы.
КТ БЕЗ КОНТРАСТНОГО УСИЛЕНИЯ
Результаты нескольких исследований подтверждают, что плотность в 10 HU или менее является диагностическим признаком аденомы коры надпочечников с 79% чувствительностью и 96% специфичностью. При пороге в 0 HU диагноз может быть поставлен с 47% чувствительностью и 100% специфичностью. Решение о том, как измерять плотность, должно приниматься тщательно. Выбранная зона интереса должна быть как можно больше, но не включать смежные ткани, особенно окружающую железу жировую ткань.
КТ С КОНТРАСТНЫМ УСИЛЕНИЕМ
Начальные паттерны контрастирования аденомы коры надпочечников и метастазов во многом совпадают; поэтому простые измерения плотности не имеют значения для их дифференциальной диагностики. Отсроченное измерение плотности (спустя 10 минут после инъекции) в 30 HU или менее является диагностическим критерием доброкачественной аденомы, но это обнаруживается только в небольшом проценте случаев надпочечниковых аденом.
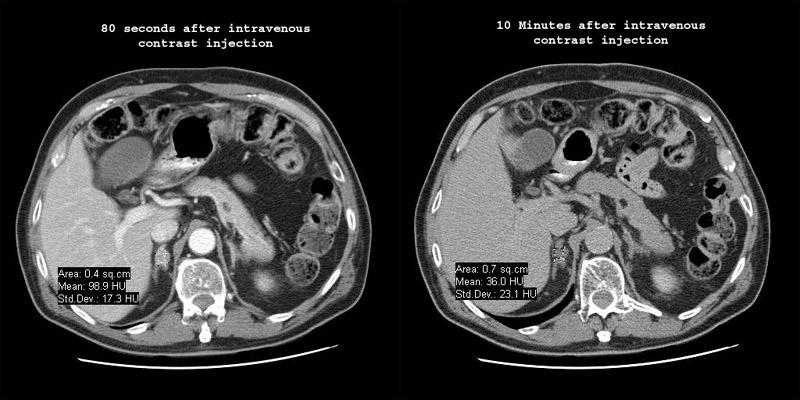
Расчет, называемый вымыванием контрастного вещества, может использоваться для надежного определения, доброкачественным или злокачественным является образование надпочечника. Вымывание рассчитывается следующим образом:
В группе из 101 опухоли надпочечников вымывание более 50% было специфичным в случаях доброкачественной аденомы надпочечников, а вымывание менее 50% было характерным для метастазов. Интересно, что эти показатели не коррелируют с долей внутрицитоплазматического жира, а физиологический механизм, приводящий к данному различию, не совсем понятен. При пороге в 50% использование значения вымывания дает 98% чувствительность и 100% специфичность.
В данной группе 2 пропущенных новообразования оказались доброкачественными аденомами, которые имели вымывания 0% и 40%. Оба образования имели значения плотности менее 30 HU на отсроченных изображениях и были правильно диагностированы как доброкачественные аденомы коры надпочечников без использования критериев вымывания. Если из группы исключить 2 новообразования, то точность этого метода составит 100%.
Для подтверждения этих удивительных результатов дополнительно необходимы более многочисленные группы. Важно помнить, что доброкачественные объемные образования, такие как гематомы надпочечников или псевдокисты, не увеличивают плотность при внутривенном введении контрастного вещества; поэтому они не подходят для оценки вымывания вообще.
Исследования, сравнивающие анализ КТ-гистограммы и анализ средней КТ-плотности для оценки очагов в надпочечниках, показали, что анализ гистограммы имеет большую чувствительность в диагностике аденомы. При изучении бедной липидами аденомы на КТ без усиления Хо и соавт. обнаружили, что хотя оба метода имеют 100% специфичность, использование порога более 10% отрицательных пикселей дало чувствительность 84%, по сравнению с 68 % для порога средней плотности менее 10 HU.
При неоднозначных результатах КТ или сомнениях в диагнозе можно отправить исследование на пересмотр в специализированный центр с целью получения Второго мнения.
Объемное образование правого надпочечника. Динамическое и отсроченное КТ с контрастным усилением демонстрирует гомогенно усиливающееся образование в правом надпочечнике. Степень уменьшения контраста со временем называется вымыванием, которое может быть рассчитано с использованием следующей формулы: [1 — (плотность через 10 минут / плотность через 80 секунд)] х 100, где плотности выражаются в единицах Хаунсфилда. В этом случае вымывание равно [1 — (36/99)] х 100 или 64%. Выводы из недавней публикации в крупном журнале показывают, что любое вымывание, превышающее 50%, является диагностическим критерием доброкачественного новообразования.
МРТ НАДПОЧЕЧНИКОВ ПРИ АДЕНОМЕ
На МРТ аденомы коры надпочечников представляют собой хорошо ограниченные объемные образования, для которых характерны однородная интенсивность и усиление сигнала. Для небольших новообразований ( В ряде источников вы можете столкнуться с описанием различных травяных и других «естественных» средств для лечения аденомы надпочечников. Следует отметить, что это состояние нельзя лечить «естественными» методами. Хирургическое удаление опухоли или аденомы является единственным методом лечения этого состояния. На сегодняшний день о сновным видом операции, проводящимся для удаления доброкачественной опухоли надпочечников, является лапароскопическая адреналэктомия. В случае лапароскопической адреналэктомии для выполнения этой процедуры проводятся несколько крошечных разрезов, в то время как в случае лапаротомии производится крупный разрез брюшной стенки. Для восстановления после брюшной лапаротомии пациенту требуется больше времени. Возраст при операции опухолей надпочечников не имеет значения, если нет сопутствующих тяжелых заболеваний.
В большинстве случаев лечение аденомы надпочечников является успешным. Тем не менее, важно, чтобы человек в свое время проконсультировался с врачом. Также для эффективного лечения болезни важно контролировать гормональный фон.
Разработанной профилактики заболевания на сегодняшний момент не существует.
Следует помнить, что аденома надпочечников — серьезное нарушение здоровья, которое может привести к осложнениям. Поэтому разумно немедленно диагностировать и лечить состояние. В любом случае, помните, что для правильно выбранного лечения прежде всего необходим точный диагноз.
При составлении статьи использованы материалы: