Назофарингеальная карцинома что это такое и сколько проживет человек
Назофарингеальная карцинома что это такое и сколько проживет человек
Назофарингеальная карцинома в детском возрасте: клинические случаи
Описание клинических случаев
Клинический пример № 1
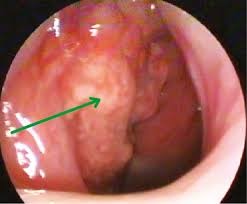
Мальчик Т., 11 лет, переведен в отделение онкологии детской краевой больницы из ЛОР-отделения той же больницы в связи с обнаружением образования в носоглотке. При поступлении предъявлял жалобы на утомляемость, заложенность носа, головную боль в течение последних 3 мес, боль в шее при повороте головы, отмечена бледность кожных покровов.
При поступлении в отделение онкологии неврологический статус без особенностей. Кожные покровы бледные, чистые. Слизистые оболочки полости рта яркие, чистые. Имеется нависание мягкого неба. Отечность тканей. Подкожная жировая клетчатка соответствует возрасту, нормального питания. Лимфатические узлы не увеличены, при пальпации не определяются. Дыхание через нос затруднено. Выделения из носа скудные, слизистые. В легких дыхание везикулярное, выслушивается с обеих сторон, хрипов нет. Живот мягкий, при пальпации безболезненный. Печень не определяется. Селезенка не увеличена. Стул оформленный, 1 раз/сут. Половые органы развиты по мужскому типу, соответствуют возрасту. Мочеиспускание достаточное, регулярное. Вес — 34,7 кг, рост — 145 см.
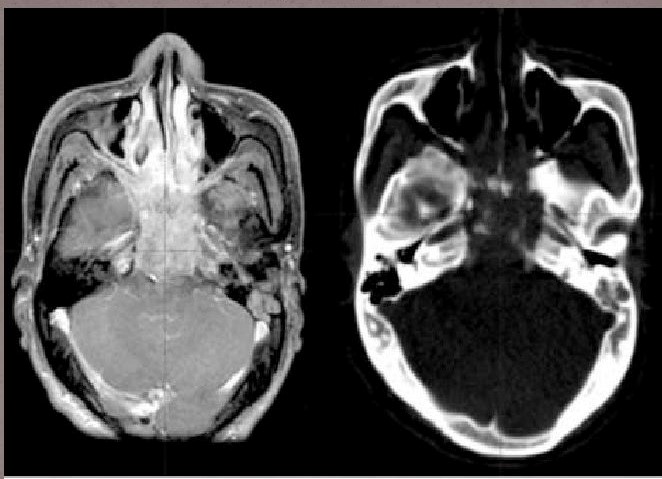
Окончательный диагноз: Назофарингеальная карцинома носоглотки, носовых ходов, основной пазухи с контактной деструкцией крыловидного отростка клиновидной кости слева и тела клиновидной кости. T3N1M0. Состояние после интенсивной химиотерапии. Состояние после лучевой терапии СОД = 59,5 Гр. Состояние после интерферонтерапии.
Клинический пример № 2
О пациенте Мальчик А., 14 лет, самостоятельно обратился в онкологическое отделение краевой детской клинической больницы в конце марта 2018 г. Предъявлял жалобы на гнусавость голоса в течение месяца и увеличение лимфатических узлов шеи с двух сторон. За 3 мес., со слов матери, мальчик похудел на 2 кг.
Первые признаки заболевания появились в начале января 2018 г. на фоне полного здоровья. Заболевание началось остро, с увеличения одного шейного лимфатического узла на шее (со слов матери) — лечились самостоятельно компрессами с диметилсульфоксидом на область шеи. В конце января зафиксирован подъем температуры тела до 37,6 °С. Осмотрен педиатром (повторно) и инфекционистом.
При осмотре в онкологическом отделении Краевой детской клинической больницы определяются конгломераты лимфоузлов шеи с двух сторон, больше с левой стороны, безболезненные, плотные. Кожные покровы бледные, чистые. Слизистая оболочка полости рта яркая, чистая. Отмечается нависание мягкого неба. Подкожная жировая клетчатка соответствует возрасту, нормального питания, без признаков гнойного воспаления. Подмышечные лимфатические узлы не пальпируются, единичные паховые — до 2–3-й степени, безболезненные, без признаков гнойного воспаления. Дыхание через нос затруднено. Выделения из носа скудные, слизистые. В легких дыхание везикулярное, выслушивается с обеих сторон, хрипов нет. Живот мягкий, безболезненный при пальпации. Печень не определяется. Селезенка не увеличена. Стул оформлен, 1 раз/сут. Половые органы сформированы по мужскому типу, соответствуют возрасту. Мочеиспускание достаточное, регулярное. Вес — 47 кг, рост — 174 см.
Окончательный клинический диагноз: Назофарингеальная карцинома, поражение носоглотки. Состояние после биопсии пораженного шейного лимфатического узла слева. Метастатическое поражение лимфатических узлов шейной группы с обеих сторон. T2bN2Mx. Состояние после 3 курсов химиотерапии по протоколу NPC-GPOH-2003. Положительная динамика. Лучевая терапия на область пораженных лимфатических узлов и область инициального распространения опухоли носоглотки РОД 1,8, СОД 59,4 Гр. Осложнения: постлучевой стоматит, катаральный синдром.
Прогноз по болезни неблагоприятный, поскольку полной регрессии первичного образования достичь не удалось. Социальная адаптация — ребенок способен к дальнейшему обучению и социализации. По нашему мнению, требуется тщательный диспансерный надзор с целью предупреждения поздних осложнений противоопухолевой терапии, а также развития вторичных онкологических заболеваний в старшем возрасте.
Заключение
Таким образом, авторами показано, что наличие головной боли, нарушения носового дыхания, потери массы тела, лихорадки в сочетании с увеличенными лимфатическими узлами шеи требует настороженности в отношении рака носоглотки при исключении другой инфекционной и воспалительной природы заболевания.
Рак носоглотки долгое время может оставаться незамеченным, имитируя такие заболевания, характерные для детского возраста, как отит, гипертрофия миндалин, воспаление респираторного тракта. Первичным симптомом злокачественного новообразования может стать метастатическое поражение лимфатических узлов шеи. Стертая картина заболевания, разнообразие клинических симптомов приводят к длительной диагностике и служат причиной позднего обнаружения рака носоглотки. Представленные нами случаи иллюстрируют запоздалую диагностику злокачественного новообразования с возможным регрессом первичной опухоли.
Источник:
Назофарингеальная карцинома в детском возрасте: клинические случаи.
Вопросы современной педиатрии. 2021; 20 (2):155-165.
Рак носоглотки
Злокачественная опухоль представляет собой разрастание эпителиальных клеток неороговевающего слоя органа.
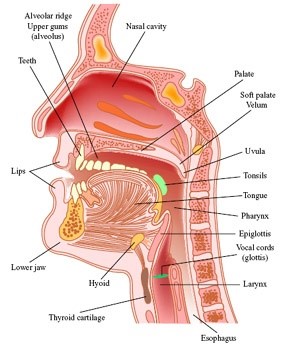
Строение полости
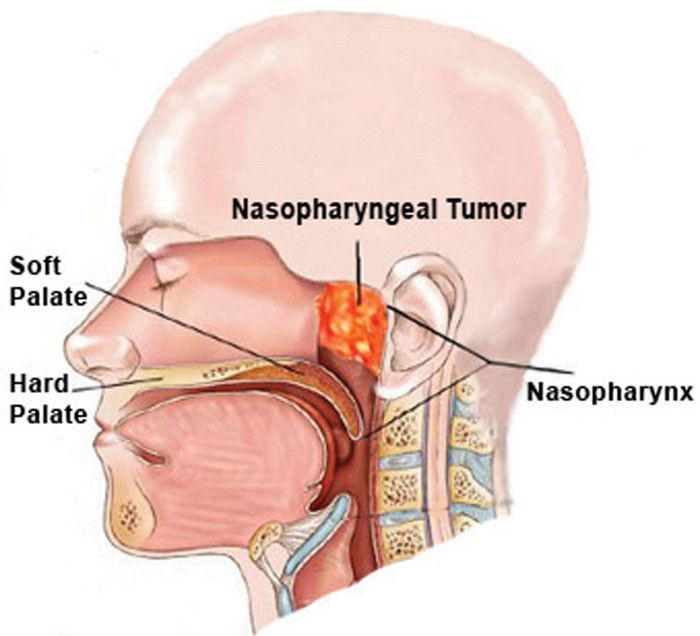
Носоглотка – это полость, соединяющая верхнюю часть гортани с носовыми проходами. Она начинается от задней поверхности твердого неба. Ее анатомическое строение следующее:
Злокачественная опухоль носоглотки прорастает в нескольких направлениях:
Классификация
В зависимости от морфологии и локализации патологии онкологические процессы делятся на несколько групп:
Юношеская ангиофиброма диагностируется наиболее часто среди доброкачественных опухолей носоглотки. В половине случаев опухоль начинается на верхней стенке органа в глоточно-основной фасции свода. Реже патология зарождается в клиновидной кости или надкостнице шейных позвонков. Доброкачественное новообразование бывает сфеноэтмоидальным, базальным и крыловерхнечелюстным. Оно состоит из сплетения кровеносных сосудов с плотными участками соединительной ткани, участков гиалиноза, некротических фокусов, миксоидного отека и кровоизлияний. В основном патология развивается у мальчиков-подростков. В момент полового созревания опухоль или затухает, или стремительно развивается. В последнем случае эпителиальные клетки быстро прорастают в основание черепа, глазницу, пазухи носа и саму полость носа.
В числе наиболее выявляемых злокачественных опухолей носоглотки стоит отметить поражения эпителиального слоя – недифференцированный рак, плоскоклеточный ороговевающий рак, плоскоклеточный неороговевающий рак. Эти виды опухолей диагностируются в 70% случаев. Строение злокачественных опухолей идентичное с раком слизистых на других участках тела. Микроскопия недифференцированного рака отличается преобладанием в составе новообразования округлых клеток, мелких тяжей, пучков, солидных структур. В основном недифференцированный тип выявляется у больных вирусом Эпштейна-Барр.
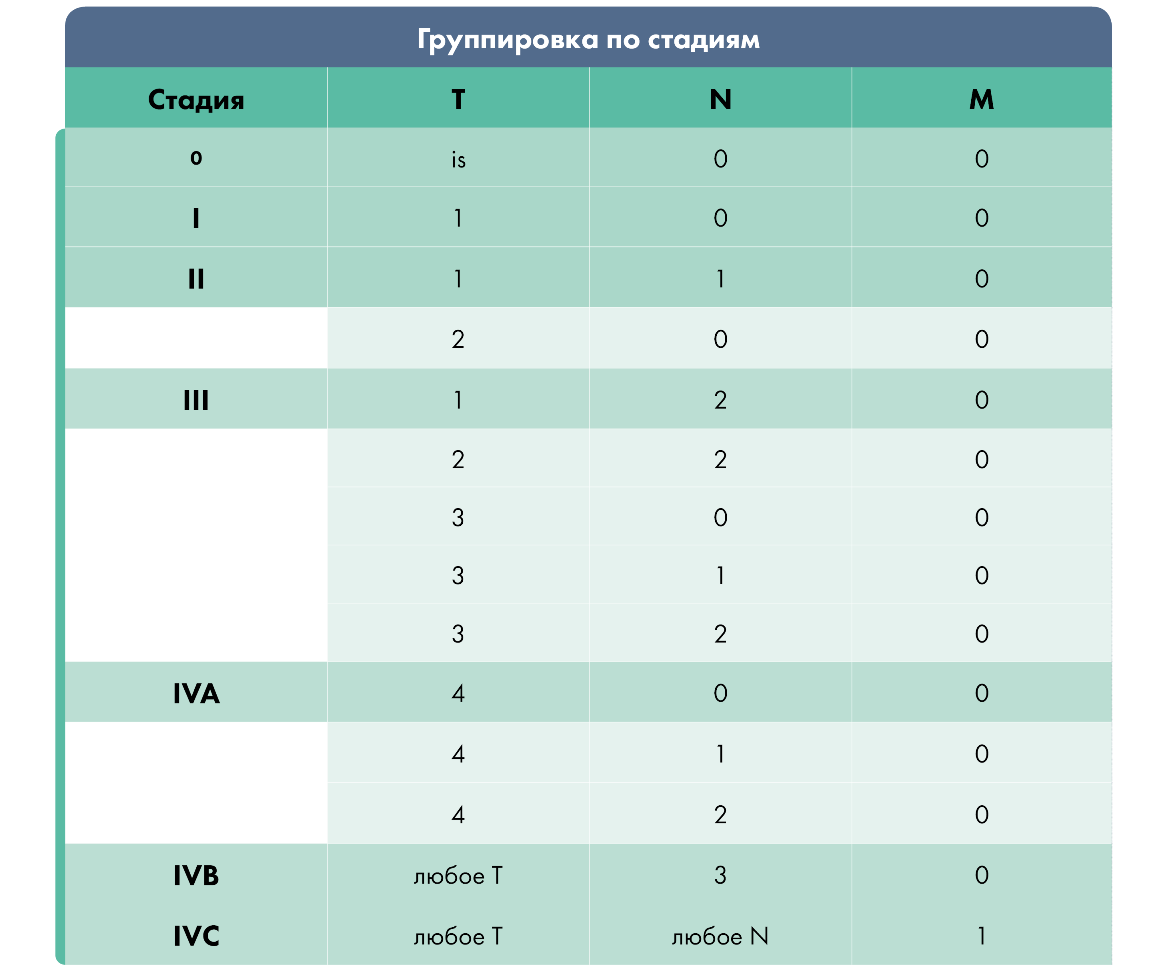
Классификация TNM
В медицинской практике распространение эпителиальных злокачественных клеток подразделяется на следующие группы:

Причины возникновения
Из числа всех онкологических заболеваний рак носоглотки встречается у 0,1-3% больных. Исходя из практики, больше всего болезни подвержены мужчины-азиаты в возрасте до 25 лет и после 40-летнего рубежа. В России заболеваемость составляет 0,1-0,2%, при этом у мужчин рак диагностируется чаще, чем у женщин.
Отличительная черта рака носоглотки – отсутствие влияния вредных привычек на рост злокачественных клеток. Заболевание не связано с курением или употреблением алкоголя.
В группу риска попадают больные, у которых выявлены хронические метаплазийные или гиперлазийные воспалительные процессы слизистой носоглотки. Также на формирование патологической среды влияет инфицирование вирусом Эпштейна-Барр.
Симптомы
Клинические особенности доброкачественной опухоли носоглотки завуалированы. Поначалу сложно определить заболевание, ведь симптомы схожи с обычными проявлениями ЛОР-болезни:
Опухоль быстро увеличивается в размере. На снимках она показывается в виде ярко-красного полипа, который по мере роста округляется и синеет. Через время изменяется форма мягкого неба, а форма верхней челюсти изменяется. У больного становятся выпученными глаза, кровотечения из носа усиливаются, а дыхание носом невозможно.
Признаки злокачественной опухоли носоглотки зависят от направления роста и точного расположения патологического узла. В зависимости от направления роста рак бывает экзофитным, дольчатым, эндофитно-язвенным. В первом случае очаг патологии в своде носоглотки, который быстро разрастается в орбиту и носовую полость. Врач видит четкие границы опухоли, а слизистая оболочка не изменяется. Больной жалуется на кровотечение из носа и сложное дыхание. Эндофитно-язвенная опухоль образуется на задней стенке носоглотки. Она медленно развивается, поэтому носовые выделения слабые. Пациент жалуется на головную боль и снижение остроты слуха с одной стороны. Врач при осмотре выявляет бугорок без четких границ с красной каймой слизистой оболочки. Дольчатая опухоль подразумевает поражение устья слуховой трубы, поэтому снижается слух, а из носа выделяется обильно слизь и кровь. По мере роста новообразования сжимаются черепно-мозговые нервы, в результате чего присоединяется неврологическая симптоматика.
Клиническая картина злокачественного рака носоглотки:
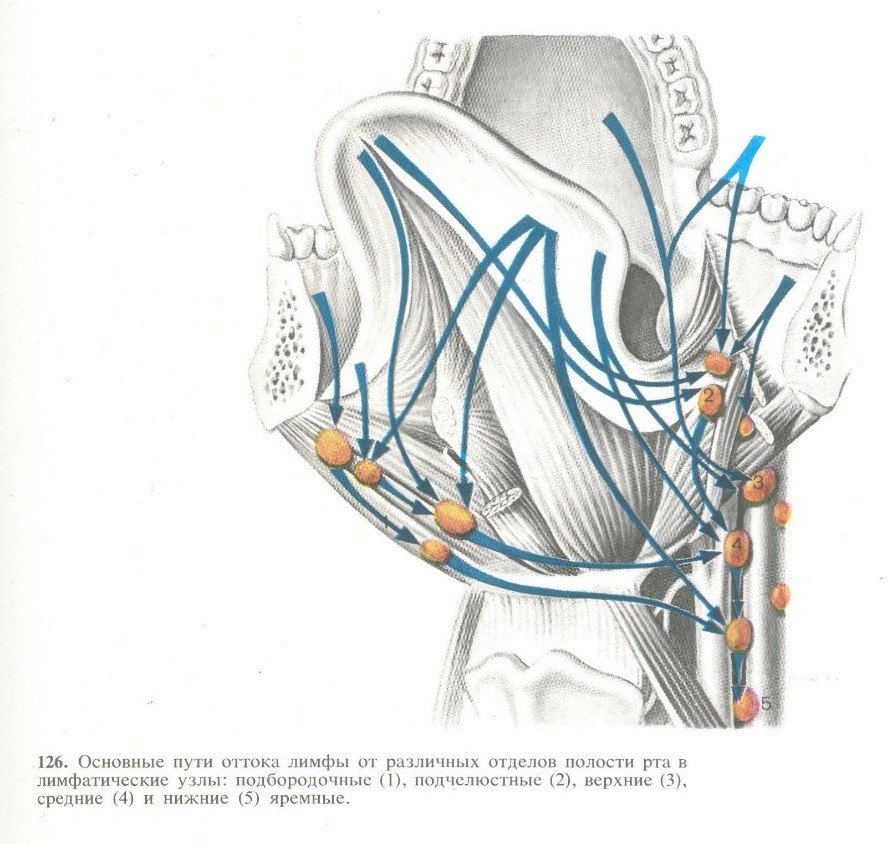
Отличительная черта злокачественной опухоли носоглотки – раннее метастазирование. Очаги появляются в лимфатических узлах вдоль спинномозгового корешка добавочного нерва, глубоких яремных лимфатических узлах, заглоточных лимфатических узлах на шее. У каждого больного количество и расположение метастазов различно. Зачастую они сливаются воедино, вызывая сильнейшую боль и нарушенную иннервацию глаза. Отдаленные метастазы развиваются при разрастании регионарных более чем на 6 см. Очаги прорастают в костях скелета, в почки, печень и легкие.
Диагностика
Дифференциальная особенность доброкачественной опухоли заключается в рассмотрении красного новообразования с гладкими стенками посредствам риноскопии. Если опухоль выпирает в ротоглотку, при прикосновении к ней металлическим инструментом она кровоточит. Рентгенография подтверждает разрушение клиновидной кости.
В отличие от юношеской ангеофибромы, злокачественные новообразования проще диагностируются, но из-за позднего обращения к врачу сложно определить точную локализацию опухоли. Аппаратное и инструментальное обследование сводится к следующему:
Лечение
Юношеская ангиофиброма сложно поддается лечению. Так, лучевая терапия не оказывает должного результата, поэтому операция обязательна. Хирургическое вмешательство проводится эндоназально при условии отсутствия метастазов в пазухах носа и орбите. Если опухоль проросла в скулы, орбиту, нос или его пазухи, ее удаляют через глотку и рот, используя верхнечелюстной доступ.
Лечение злокачественной опухоли носоглотки делится на несколько этапов.
Лучевая терапия
Метод подходит для лечения онкологии первой стадии. Врач подбирает высокую дозу облучения для устранения первичной опухоли и ее метастазов в лимфатических узлах. Злокачественные клетки в носоглотке чувствительны к облучению, поэтому эффективность лечения высока. Дополнительно курс лучевой терапии шейных лимфатических узлов проводится отдельными полями с профилактической целью после пройденного курса терапии.
Радиолог назначает два курса облучения с перерывом в 14 дней. Суммарная очаговая доза за все сеансы не превышает 70 гр. После достижения зоны 40-50 гр объем облучения уменьшается, пока не достигнет суммарной дозы. Наибольшая эффективность лечения достигается при увеличении суммарной очаговой дозы до 60-69 гр.
После терапии опухолевые клетки остаются у 40% больных. Вероятность рецидивов снижается практически до 6%, если источник радиоактивного облучения вводится в носоглотку автоматически или вручную. Этот способ помогает повысить очаговую дозу до 90-120 гр. Внутриполостное облучение, очаговая доза которого 6-7 гр за сеанс с перерывов в одну неделю на протяжении 21 дня, не вызывает осложнений в позднем периоде. Подобный способ помогает достичь пятилетней ремиссии.
В сферу облучения входит не только первичная опухоль, но и шейно-надключичные, заглоточные лимфатические узлы с двух сторон, парафарингеальное пространство, основание черепа. Поскольку рядом с этими участками находятся жизненно-важные органы, на которые нежелательно направлять облучающие лучи, радиолог тщательно подбирает программу облучения. Обычно лучевое воздействие начинается с участков регионарного лимфооттока и щечно-височных фигурных полей. Если злокачественные клетки обнаружили в полости носа и его пазухах, то доза облучения распределяется с помощью фигурных полей с зоны скул и заушных лимфатических узлов.
На сегодняшний день используются не только стандартные программы облучения. Трехплоскостное планирование обучения оптимально распределяет дозу между самой опухолью и окружающими тканями, поэтому нагрузка на ткани вокруг снижается.
Если после курса лучевой терапии остались метастазы на шее, то осуществляется операция. Если рак носоглотки диагностирован уже на второй стадии, проводится химиолучевая терапия. В целом облучение помогает достичь ремиссии практически 90% больным. Продолжительность жизни на 5 лет повышается на 53%, на 10 лет повышается на 45%, на 20 лет – на 39%. Однако стоит отметить, что у каждого третьего больного возникают отдаленные метастазы после пройденного курса лечения.
Химиотерапия перед операцией
Неоадъювантная химиотерапия вкупе с лучевой терапией назначается при высокой склонности к метастазированию, диагностировании недифференцированного рака.
Назначается 2-3 курса. Больному вводятся препараты цетуксимаба, блеомицина, доксорубицина, винбластина, платинов, винкристина, метотрексата, циклофосфомида, а через 14 день после начала приема приступают к облучению.
Основные схемы лечения таковы:
В настоящий момент эти схемы лечения подтвердили свою эффективность, но специалисты продолжают изучать новые схемы применения таксанов. Локализованный рак носоглотки может быть вылечен посредством лучевой терапии, при этом эффективнее метод внутриполостного облучения. Если диагностировано местное распространение злокачественных клеток, а также метастазы на шее, то проводится химиолучевая терапия. При полном разрушении раковых клеток проводится адъювантная химиотерапия для предотвращения образования метастазов в легких, печени и почках. Если первичная опухоль распалась, а остались остаточные метастазы, то проводится операция Крайля через месяц-полтора после прохождения химиотерапии.
Прогноз
В целом лечение доброкачественной опухоли носоглотки благоприятное, если операция проведена на начальной стадии развития заболевания, однако стоит отметить склонность к рецидиву.
Прогноз лечения недифференцированного рака неуточненный. Как правило, новообразование метастазирует и в возрасте 40 лет диагностируется рецидив. Исходя из практики, на выживаемость влияет морфология опухоли, наличие метастазов, распространение раковых клеток. Выживаемость на протяжении пяти лет подтверждается у больных недифференцированным раком носоглотки в 52%, а у больных плоскоклеточным раком носоглотки в 18%.
Список литературы по теме:
Недифференцированный рак носоглотки
Общая информация
Краткое описание
Для практической работы наибольшее признание в онкологических учреждениях получила Международная гистологическая классификация опухолей носоглотки.
Название: Недифференцированный рак носоглотки
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Диагностика
Всем больным необходимо проведение тщательного инструментального отоларингологического осмотра, пальцевое обследование рото- и носоглотки.
1. Рентгенологические методы диагностики: стандартные рентгенологические укладки (боковой снимок носоглотки, прямой снимок придаточных пазух носа), а также обзорная краниография в аксиальной и полуаксиальной проекциях, позволяют в большинстве случаев получить достаточный объем информации.
2. В более сложных случаях необходимо применение рентгеновской томографии и компьютерной томографии, которая имеет большее диагностическое значение. По показаниям – КТ или МРТ головного мозга с контрастированием.
Лабораторная диагностика
Лечение
Профилактические мероприятия: профилактика цитотоксических, постлучевых осложнении, симптомов ВЧД – сопроводительная терапия (антибактериальная, антиэметогенная, колоностимулирующая, дезинтоксикационная, дегидратационная, гармонотерапия, и т.д.).
Дальнейшее ведение: после окончания лечения необходимо регулярное обследование с целью выявления рецидивов или прогрессирования заболевания – КТ или МРТ с контрастированием.
Назофарингеальная карцинома что это такое и сколько проживет человек
НФК — назофарингеальная карцинома;
КТ — компьютерная томография;
ПЭТ — позитронно-эмиссионная томография;
ve — верификация (визуализация).
Назофарингеальная карцинома (НФК, рак носоглотки) является одной из самых сложных опухолей с точки зрения правильной постановки диагноза на начальном этапе из-за отсутствия специфических назальных симптомов. Кроме того, НФК является сравнительно редкой опухолью. Так, в России удельный вес рака носоглотки составляет около 0,1—0,2% в структуре онкологической заболеваемости. У мужчин заболеваемость НФК достигает 0,55 случая на 100 000 населения (в европейских странах — 0,9), у женщин — 0,29 (в европейских странах — 0,26) [1]. В Японии регистрируется 0,29 случая на 100 000 человек в год [2]. Существуют определенные регионы (Россия, Китай, страны Юго-Восточной Азии, Северной Африки, коренные народы Арктического региона), в которых НФК выявляется намного чаще, чем у жителей других стран [2]. Классификация Всемирной организации здравоохранения (2005) выделяет следующие гистологические типы НФК: ороговевающий плоскоклеточный рак (SCC); неороговевающий рак (NCC) с дифференцированным НФК (CNK) и недифференцированным (UCNK) подтипами.
НФК развивается из эпителия верхней части носоглотки и значительно отличается от других типов опухолей головы и шеи по своему генезу, причинам, клиническому течению и лечебной тактике.
Недифференцированный неороговевающий тип НФК является наиболее распространенным и прочно ассоциируется с вирусом Эпштейна—Барр практически в 100% случаев [3]. Наиболее частой локализацией НФК является боковая стенка носоглотки, особенно розенмюллерова ямка, и верхнезадняя стенка в области глоточной миндалины. Более половины пациентов предъявляют жалобы на назальные симптомы (затруднение носового дыхания, слизисто-геморрагическое, гнойное отделяемое с примесью крови), симптомы, связанные с обструкцией слуховой трубы (серозный отит), которые возникают из-за особенностей локализации опухоли. Так, при локализации опухоли на боковой стенке впереди устья слуховой трубы развивается симптомокомплекс Троттера: понижение слуха на стороне поражения, невралгия и анестезия веточек третьей ветви тройничного нерва, а также одностороннее ограничение подвижности мягкого неба. При локализации опухоли вблизи устья слуховой трубы на первый план выступают явления снижения слуха, ощущение шума, чувство заложенности носа [4]. Головная боль и вовлечение черепных нервов являются признаками более поздних стадий развития опухоли. Боковое распространение НФК может вовлекать в процесс третью ветвь тройничного нерва. Подобное, периневральное распространение НФК является одним из наиболее частых и важных направлений в отношении дальнейшей заинтересованности кавернозного синуса [5]. В область орбиты НФК распространяется крайне редко, однако в этом случае нарушения зрительного анализатора могут быть первым и единственным симптомом карциномы [6—8].
Дифференциальная диагностика и верификация НФК основываются на данных эндоскопического, рентгенологического (в том числе магнитно-резонансное, КТ и ПЭТ-КТ, сцинтиграфия костей) и морфологического исследований, включая тонкоигольную аспирационную биопсию метастатических узлов шеи [4].
Патоморфологическая характеристика рака носоглотки важна для определения прогноза и тактики ведения заболевания. Гистологические виды НФК по ядерной градации: G0 — оценка затруднена, G1 — высокодифференцированная карцинома, G2 — умеренно дифференцированная, G3 — низкодифференцированная, G4 — недифференцированная [9]. Одним из ключевых методов морфологической оценки НФК и ее типов является иммуногистохимический. Однако усовершенствование выбора панели антител иммунофенотипирования является приоритетным с учетом того, что отечественных исследований в этом направлении практически не проводится, а данных зарубежных исследований явно недостаточно.
Цель исследования — оценка иммуногистохимических особенностей назофарингеальной карциномы.
Материал и методы
Ретроспективное исследование операционного материала проводили в патологоанатомических отделениях Медицинского радиологического научного центра им. А.Ф. Цыба (Обнинск) и Научном клиническом центре ОАО «РЖД» в период с октября 2014 г. по декабрь 2016 г.
Объект ретроспективного исследования — опухоли носоглотки, полученные в ходе операций у пациентов (n=119), находившихся на стационарном лечении в отделении лучевого и хирургического лечения заболеваний верхних дыхательных путей, были изучены с помощью методов световой микроскопии и иммуногистохимии.
Фрагменты опухолей носоглотки фиксировали в забуференном формалине, дегидратировали в батарее спиртов восходящей концентрации и заливали в парафин. Срезы тканей толщиной ≈5 мкм помещали на обычные, а для иммуногистохимического исследования (ИГХ) — на специальные адгезивные предметные стекла, депарафинировали согласно принятой стандартной методике. Впоследствии срезы окрашивали гематоксилином и эозином для гистологического исследования.
Иммуногистохимический метод (ИГХ). После депарафинизации и регидратации парафиновых срезов проводили ИГХ-исследование по стандартному протоколу в автоматическом режиме в иммуногистостейнере Bond-Max («Leica», Германия) на выявление диагностических маркеров в тканях опухолей.
В качестве первичных антител использовали моноклональные мышиные антитела (Novocastra, Великобритания, в готовом к использованию разведении) к Pan-cytokeratin, EBV, СК5/6, CK7, CK19, S-100, Vimentin, Desmin, р16. Вторичные антитела — универсальные (HiDefDetection HRP Polymersystem, «CellMarque», США). Для данных маркеров выполняли контрольные реакции для исключения псевдопозитивных и псевдонегативных результатов. Ядра докрашивали гематоксилином Mayer; стекла промывали под проточной водой; дегидратировали; срезы заключали в гель Aquatex (aqueousmountingagent, «AndwinScience», Франция) под покровные стекла.
Интенсивность окрашивания срезов оценивали с учетом количества иммунопозитивных клеток (на 100), при подсчете в трех случайно выбранных полях зрения светового микроскопа при увеличении 40 (D. Dabbs, 2014): – — отсутствие экспрессии, + — слабая экспрессия (1—10% клеток), ++ — умеренная экспрессия (11—50% клеток), +++ — выраженная экспрессия (высокоинтенсивная иммунопероксидазная реакция, ≥51% клеток). Визуализацию биопсийного материала выполняли на светооптическом микроскопе CarlZeiss Lab. A1 («CarlZeiss», Германия), совмещенном с видеокамерой AxioCam ERc5s («CarlZeiss Microscopy GmbH», Германия) и программным обеспечением ZEN Lite.
Статистический анализ. Полученные в результате подсчета данные обрабатывали с использованием компьютерной программы SPSS 7.5 for Windows («IBM Analytics», США). Рассчитывали среднюю арифметическую величину с ее предельными отклонениями и среднеквадратичную ошибку. Соответствие данных нормальному распределению подтвердили с применением критерия Колмогорова — Смирнова. При статистической обработке для оценки достоверности различий средних значений между группами использовались следующие непараметрические критерии: U-критерий Манна—Уитни, Н-критерий Краскела—Уоллиса. При отсутствии нормального распределения данных использовали непараметрический критерий F. Wilcoxon (Statistical methods for research workers) с уровнем значимости p 
Размер опухолей носоглотки варьировал от 1,0 см (n=18; 15%) и 2,0 см (n=87; 73,1%) до 3,0 см (n=14; 11,7%) в диаметре. Опухоли светло-желтого цвета, с участками кровоизлияний (рис. 1). 
Микроскопическое описание опухолей. Образцы с недифференцированной НФК (n=97). В препаратах: фрагменты злокачественного новообразования с массивными полями некроза и кровоизлияния. На всем протяжении опухолевого ареала определяются два вида клеточных популяций. Одни клетки — синцитиальные (по типу Regaud), другие — эпителиоидные, с четкими краями (по типу Schminke), с 2—3 хорошо выраженными ядрышками; фигур митоза ≥50/10 в полях зрения (рис. 2). 

Диффузная крупноклеточная В-лимфома (n=18). Опухолевый инфильтрат представлен крупными неопластическими лимфоидными клетками, множеством малых лимфоцитов и единичными гистиоцитами. При ИГХ-исследовании в опухолевых клетках обнаружено положительное окрашивание цитолеммы с антителами к CD20 (ve+/3), что может свидетельствовать о В-клеточной дифференцировке (рис. 3, б). Отрицательные реакции на CD3 (ve–) исключают Т-клеточную лимфому, а на СК 5/6 (ve) — плоскоклеточную природу опухоли. Кроме того, лимфоидные клетки были иммунонегативными на EBV (ve–).
Неороговевающая плоскоклеточная НФК (n=1) представляла собой опухолевый узел с тенденцией к гнездообразованию с хорошо очерченными границами и зонами комедонекрозов, без десмопластической реакции стромальных структур. Раковые клетки почти веретеновидной формы с гиперхромными ядрами и едва заметными ядрышками демонстрируют положительные ядерные и цитоплазматические ИГХ-реакции с антителами к СК 5/6 (ve+/3) и p16 (ve+/2) (рис. 3, в) и отрицательную на EBV (ve–). Выявленные реакции имеют важное значение при обнаружении метастазов изучаемого рака в лимфатических узлах ротоглотки.
Меланома носоглотки (n=2) характеризуется узловой пролиферацией меланинсодержащих (пигментных) атипичных клеток в собственной пластинке с фокальным поражением эпителиально-субэпителиального сочленения. Ядра этих клеток — плеоморфные, гиперхромные, с хорошо различимыми ядрышками. Также были обнаружены гигантские опухолевые клетки с фигурами патологических митозов. Многослойный плоский неороговевающий эпителий с гиперпластическими изменениями и изъязвлениями. Иммуногистохимическое исследование подтвердило меланоцитарное происхождение пролиферирующих опухолевых клеток. Таким образом, один из основных маркеров клеток-меланоцитов — HMB-45 — показал диффузное положительное цитоплазматическое иммуномечение в опухолевых клетках. Интенсивность иммуноокрашивания отличалась в разных частях опухоли, подчеркивая области умеренной интенсивности HMB45 (ve+/2), чередуя их с зонами выраженного маркирования HMB45 (ve+/3). Мезенхимальный маркер Vimentin и нейральный S-100 также показали диффузную позитивную цитоплазматическую ИГХ-реакцию в клетках опухоли (ve+/3). В отличие от перечисленных маркеров цитоплазматическое иммуноокрашивание на меланин было фокально положительным — Melan A (ve+/2). На антитела к СК 5/6 (ve–) и EBV (ve–) маркирование было иммунонегативным.
Рабдомиосаркома носоглотки (n=1). Опухолевые клетки — крупные, почти овальной или веретеновидной формы с сильно эозинофильной цитоплазмой, обладающие выраженной пролиферативной активностью и местами образующие альвеолярные структуры Часть клеток — многоядерные, богатые гликогеном (PAS-положительные). В клетках опухоли визуализируется положительное цитоплазматическое ИГХ-окрашивание на белок промежуточных филаментов саркомеров — Desmin (ve+/3) и отрицательное — на СК 5/6 (ve–) и EBV (ve–).
НФК образована клетками эпителиальной выстилки носоглотки. Кроме эпителиальных клеток, недифференцированные НФК содержат много клеток лимфо- и иммунопоэза, особенно лимфоцитов. В связи с этим целесообразно использовать термин «лимфоэпителиома» носоглотки. Однако наличие лимфоцитов в опухолевом узле, как правило, не влияет на выбор тактики лечения [12—14]. Наличие лимфоцитарной инфильтрации, возможно, послужит началом разработки новых методов лечения НФК, так как лимоциты могут пытаться «отторгнуть» злокачественное образование, особенно у детей [15, 16].
Нами была проведена дифференциальная диагностика НФК с другими злокачественными новообразованиями носоглотки, которая отражена в таблице иммунофенотипирования (табл. 2). 
Проведенное ретроспективное исследование показало, что среди опухолей носоглотки часто встречаются недифференцированная назофарингеальная карцинома (81%) и диффузная крупноклеточная В-лимфома (15%). Недифференцированная назофарингеальная карцинома при иммуногистохимическом исследовании демонстрирует коэкспрессию маркеров на вирус Эпштейна—Барр, Pan-cytokeratin и СК 5/6.
Авторы заявляют об отсутствии конфликта интересов.