Медицинский термин рфп что это такое
Медицинский термин рфп что это такое
Современное радиоизотопное исследование основано на участии радионуклидов в физиологических процессах организма и отличается большой степенью информативности. Методы функциональной визуализации радиоизотопной диагностики называют сцинтиграфическими. Такое название они получили, благодаря термину «сцинтилляция», который обозначает кратковременную вспышку под воздействием ионизирующего излучения.
По сути, один РФП – это одно направление диагностики или лечения. Современная общемировая радиофармацевтическая индустрия насчитывает десятки препаратов, применяющихся в различных сферах медицины, прежде всего в онкологии, кардиологии и эндокринологии.
В лаборатории радиоизотопной диагностики «НМИЦ онкологии им. Н.Н. Блохина» в повседневной практике детям выполняют следующие сцинтиграфические исследования:
Сцинтиграфия костей с 99m-фосфанатами (или остеосцинтиграфия)
Сцинтиграфия с 123I-MIBG
Подготовка к MIBG-сканированию очень индивидуальна, её предусмотрит лечащий врач. Перед сканированием ребёнок должен принять йод в виде раствора Люголя, чтобы снизить лучевую нагрузку на щитовидную железу, которая более восприимчива к радиоактивности, чем другие органы.
Что происходит во время самого сканирования?
Сканирование с MIBG выполняется в течение 2-х дней. В первый день ребёнку сделают инъекцию радиофармацевтического препарата. Во второй день проходит сканирование на гамма-камере. Время сканирования очень просто рассчитать, поскольку оно связано с ростом пациента и составляет 5 сантиметров в минуту. Вторым этапом может быть выполнено томографическое исследование, которое занимает около 30 минут на одну зону интереса.
Существуют ли какие-нибудь риски?
В редких случаях встречается индивидуальная непереносимость препарата – покраснение кожи или повышение артериального давления, но эти симптомы проходят самостоятельно и не требуют лечения. Ребёнок получает небольшую дозу ионизирующего излучения, это абсолютно безопасно и не вызывает каких-либо непосредственных или отсроченных эффектов.
Сцинтиграфия мягких тканей с 99mTc-технетрилом
Метод основан на избирательном повышенном накоплении 99mТс-Технетрила в опухолевой ткани по сравнению с окружающими её здоровыми тканями. Опухолевые клетки по сравнению с нормальными клетками обладают более высоким трансмембранным потенциалом, так что РФП здесь выступает надежным агентом для визуализации опухолевых очагов.
При помощи сцинтиграфии через 20 минут после внутривенного введения злокачественные опухоли визуализируются. Результаты многих исследований показывают, что концентрация РФП одинакова как в первичных опухолях, так и в очагах метастастазирования различных опухолей.
Злокачественные опухоли мягких тканей головы и шеи, грудной клетки, верхних и нижних конечностей.
Сцинтиграфия щитовидной железы с 99mTc-пертехнетатом
Комплексная реносцинтиграфия
Реносцинтиграфия у детей с онкологическими заболеваниями как правило, проводится после курсов химиотерапии для оценки функционального состояния почек, т.к. в зависимости от особенностей схемы назначенного лечения почки могут подвергнуться токсическому воздействию химиопрепаратов.
О радионуклидной ВИЗУАЛИЗАЦИИ (сцинтиграфии) для врача общей практики
Первое применение радиоактивных индикаторов относят к 1911 году и связывают с именем Дьердя де Хевеши. Молодой ученый, живший в дешевом пансионе, начал подозревать, что остатки пищи, которые он не доел, подавали ему вновь на следующий день.
Первое применение радиоактивных индикаторов относят к 1911 году и связывают с именем Дьердя де Хевеши. Молодой ученый, живший в дешевом пансионе, начал подозревать, что остатки пищи, которые он не доел, подавали ему вновь на следующий день. Он добавил радиоизотопный индикатор к несъеденной порции и с помощью детектора излучения доказал своей хозяйке, что дело обстояло именно так. Хозяйка выгнала молодого ученого из пансиона. Он же продолжал начатую работу, результатом которой стала Нобелевская премия за использование радионуклидов в качестве индикаторов в биологии Радионуклидная (радиоизотопная) диагностика охватывает все виды применения открытых радиоактивных веществ в диагностических и лечебных целях.
Клиническое применение радиоиндикаторов вошло в практику в 50-х годах. Развиваются методы, позволяющие детектировать наличие (радиометрия), кинетику (радиография) и распределение (сканирование) радиоиндикатора в исследуемом органе. Принципиально новый этап радиоизотопной визуализации связан с разработкой устройств широкого поля зрения (сцинтилляционные гамма-камеры) и метода визуализации — сцинтиграфии. Нередко термином «сцинтиграфия» обозначают исследования, проведенные с использованием как линейного сканера, так и сцинтиляционной гамма-камеры. С этим терминологическим стереотипом связано формирование неверных представлений о диагностических возможностях методов.
Сканирование и сцинтиграфия — это различные методы радиоизотопной визуализации. Сцинтиграфия существенно превосходит сканирование по объему и точности диагностической информации. Современные сцинтилляционные камеры представляют собой компьютеро-сцинтиграфические комплексы, позволяющие получать, хранить и обрабатывать изображения отдельного органа и всего тела в широком диапазоне сцинтиграфических режимов: статическом и динамическом, планарном и томографическом. Независимо от типа получаемого изображения оно всегда отражает специфическую функцию исследуемого органа. По сути, это картирование функционирующей ткани. Именно в функциональном аспекте заключается принципиальная отличительная особенность сцинтиграфии от других методов визуализации. Попытка взглянуть на результаты сцинтиграфии с анатомических или морфологических позиций — еще один ложный стереотип, влияющий на предполагаемую результативность метода.
Диагностическая направленность радиоизотопного исследования определяется используемым радиофармацевтическим препаратом (РФП). Что же такое РФП? Радиофармацевтический препарат — это химическое соединение с известными фармакологическими и фармакокинетическими характеристиками. От обычных фармацевтических средств он отличается не только радиоактивностью, но и еще одной важной особенностью — количество основного вещества настолько мало, что при введении в организм не вызывает побочных фармакологических эффектов (например, аллергических). Специфичность РФП по отношению к определенным морфофункциональным структурам определяет его органотропность. Понимание механизмов локализации РФП служит основой для адекватной интерпретации радионуклидных исследований. Введение РФП связано с небольшой дозой облучения, неспособной вызвать какие-либо неблагоприятные специфические эффекты. В этом случае принято говорить об опасности переоблучения, однако при этом не учитываются темпы развития современной радиофармацевтики.
Лучевая нагрузка определяется физическими характеристиками радиоиндикатора (период полураспада) и количеством введенного РФП. Сегодняшний день радионуклидной диагностики — использование короткоживущих радионуклидов. Наиболее популярным из них является технеций-99m (период полураспада — 6 часов). Этот искусственный радионуклид получают непосредственно перед исследованием из специальных устройств (генераторов) в форме пертехнетата и используют для приготовления различных РФП. Величины радиоактивности, вводимые для проведения одного сцинтиграфического исследования, создают уровни лучевой нагрузки в пределах 0,5-5% допустимой дозы. Важно подчеркнуть — длительность сцинтиграфического исследования, количество получаемых изображений или томографических срезов уже не влияют на «заданную» дозу облучения.
l Клиническое применение
Коротко остановимся на реальных диагностических возможностях наиболее распространенных («рутинных») сцинтиграфических исследований.
Визуализация костной системы (остеосцинтиграфия) — наиболее точный метод выявления участков нарушенного костного метаболизма. Остеотропные РФП (Тс-фосфонаты) обладают высоким сродством к кристаллам фосфата кальция, поэтому они связываются преимущественно с минеральным компонентом костной ткани. Уровень накопления РФП в различных типах костей и участках скелета обусловлен степенью остеобластической и метаболической активности, величиной кровотока, что необходимо учитывать при дифференциации нормального и патологического накопления РФП. В частности, повышенное накопление РФП наблюдается в метаэпифизарных отделах трубчатых костей, в областях с постоянной физической нагрузкой.
Заболевания костей сопровождаются патологической перестройкой костной ткани, реактивным или опухолевым костеобразованием — основными механизмами, обусловливающими изменение костного метаболизма и накопление остеотропных РФП в пораженных отделах. В зависимости от сочетания указанных процессов возрастает уровень накопления остеотропных РФП при опухолевых, воспалительных, дегенеративных, травматических заболеваниях.
Основная и наиболее ответственная задача остеосцинтиграфии — поиск метастатических и оценка распространенности опухолевых поражений скелета. Сцинтиграфическая манифестация патологии может проявиться на 3-12 месяцев раньше, чем появятся рентгенологические признаки. Связано это с тем, что локальное изменение обмена остеотропных РФП возникает на ранних фазах развития патологии, еще до появления не только рентгенологической, но и клинической симптоматики. По этой причине радионуклидное исследование обладает наибольшей эффективностью в до- и послеоперационном обследовании больных опухолями с высокой частотой метастазирования в кости (молочная железа, легкие, предстательная железа, почки).
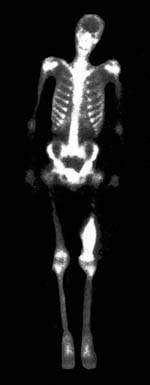 |
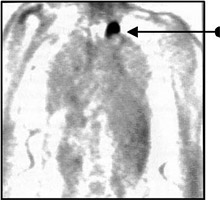
| Рисунок 1. Остеогенная саркома бедра. Обширная область высокого накопления РФП в дистальном отделе левого бедра |
Сцинтиграфическая манифестация метастатических поражений — множественные и реже одиночные локальные зоны высокого накопления РФП («горячие» очаги). Наиболее высокие концентрации РФП отмечаются в остеобластических и смешанных метастазах, низкие — в остеолитических. Ложноположительные ошибки чаще всего связаны с выраженными остеодистрофическими изменениями, а также с травматическими повреждениями ребер и позвоночника. Опухоли костей остеогенного происхождения отличаются наиболее высокой кумуляцией РФП. Например, остеогенная саркома отличается выраженной гиперфиксацией РФП не только в элементах самой опухоли, но и в окружающих мягких тканях за счет реактивной гиперемии (рис. 1). В опухолях неостеогенного происхождения накопление РФП более низкое. Однако практически не представляется возможным дифференцировать отдельные виды опухолей по степени накопления в них РФП. Некоторые опухоли, так же как и их метастазы, могут быть накоплением РФП. К таким опухолям относится, в частности, ретикулосаркома и множественная миелома. Визуализация почек (динамическая реносцинтиграфия) — простой и точный метод одновременной оценки функционального и анатомотопографического состояния мочевыводящей системы. В основу положена регистрация транспорта нефротропного РФП и последующий расчет параметров, объективизирующих два последовательных этапа.
Анализ сосудистой фазы (ангиофазы) направлен на оценку симметричности прохождения «болюса» по почечным артериям и относительных объемов крови, поступающих к каждой почке в единицу времени. Анализ паренхиматозной фазы предусматривает характеристику относительной функции почек (вклад в суммарную очистительную способность) и времени прохождения РФП через каждую почку или ее отделы. Клиническая интерпретация в значительной степени определяется механизмом элиминации РФП. В методах динамической визуализации могут быть использованы два вида РФП:
l гломерулотропные (производные ДТПА), практически полностью фильтруются клубочками и отражают состояние и скорость клубочковой фильтрации;
l тубулотропные (аналоги гиппурана) секретируются эпителием проксимальных канальцев и отражают состояние канальцевой секреции, а также эффективного почечного кровотока. Показания к исследованию включают урологическую и нефрологическую патологию, а также заболевания, где почки являются органами-мишенями.
При различных клинических ситуациях может меняться как форма кривых, так и их количественные характеристики. Следует, однако, подчеркнуть, что характер и величины изменений малоспецифичны для конкретной патологии и прежде всего отражают тяжесть патологического процесса. Наибольшая информативность реносцинтиграфии проявляется при дифференциации одно- или двустороннего поражения почек.
Ведущий признак, определяющий сторону поражения, — асимметрия амплитудно-временных характеристик ангионефросцинтиграмм. Асимметрия сосудистых параметров, и прежде всего выраженная разница времени поступления РФП в почечные артерии, — один из критериев стеноза почечной артерии. Симметричность изменений паренхиматозной функции более характерна, в частности, для гломерулонефрита; асимметрия — довольно постоянный признак пиелонефрита не только при одно-, но и при двустороннем процессе. Аналогичные изменения могут сопровождать различные варианты аномалий почек и верхних мочевых путей (нефроптоз, удвоение собирательной системы, гидронефроз).
В основе метода визуализации печени (гепатосцинтиграфии) лежит использование меченых коллоидов, которые после внутривенного введения фагоцитируются и распределяются в морфофункциональных структурах, содержащих клетки РЭС в соответствии с локальными значениями органного кровотока. В норме в печени локализуется более 90%, в селезенке — около 5%, а в костном мозге — менее 1% введенного радиоколлоида. В зависимости от характера и тяжести патологии эти соотношения меняются. Наиболее общим показанием к гепатосцинтиграфии является гепато- и/или спленомегалия неясного генеза. Основная задача исследования — дифференциация характера и уточнение тяжести поражения печени.
Диффузные заболевания печени манифестируются изменением размера и формы изображения, распределения радиоколлоида в печени и его внеорганного накопления, параметров фагоцитарной способности РЭС и печеночного кровотока. Следует подчеркнуть, что исследование не позволяет дифференцировать клинические или клинико-морфологические формы заболевания печени (например, хронический гепатит). Наибольшая информативность метода проявляется в возможности выявления синдрома портальной гипертензии (СПГ).
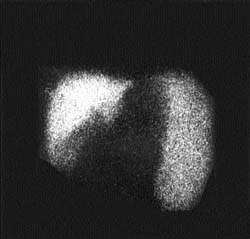 |
| Рисунок 2. Внепеченочная блокада портального кровообращения. Синдром портальной гипертензии манифестируется высоким захватом радиоколлоида увеличенной селезенкой |
Независимо от причин повышенного давления в системе воротной вены (внутри- или внепеченочные формы), сцинтиграфически СПГ манифестируется высоким захватом радиоколлоида и увеличенной селезенкой. Сочетание указанных признаков позволяет выявить СПГ с точностью до 98% (рис. 2). Очаговые поражения печени в зависимости от их распростаненности проявляются наличием одиночных или множественных дефектов накопления РФП в пределах одной или обеих долей печени (рис. 3). В практике нередко выявление участков, где отсутствует накопление РФП («холодные» очаги), прочно ассоциируют с объемными процессами, чаще всего опухолевого генеза. Это представление ложно. Достаточно широкий спектр заболеваний, связанных с вовлечением печени в патологический процесс, сцинтиграфически может манифестировать очаговыми изменениями как следствием локальных гемодинамических или функциональных нарушений (цирроз печени, амилоидоз, гистиоцитоз). Необходимо также помнить, что некоторые органные структуры (аномально расположенный желчный пузырь, молочная железа) могут «экранировать» изображение печени и формировать сцинтиграфический феномен «псевдоопухоли». Именно поэтому по характеру дефекта накопления РФП без учета клинической информации практически невозможно дифференцировать специфику очагового поражения.
A. | B.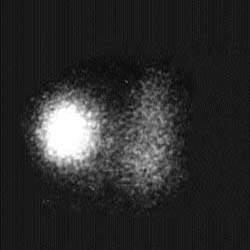 |
| Рисунок 3. Сцинтиграфические варианты узловых поражений щитовидной железы. «Холодный» узел нижнего отдела левой доли — коллоидная киста (А), «горячий» узел правой доли — тиреотоксическая аденома (Б) | |
Возможность выявления очаговой патологии зависит и от разрешающей способности гамма-камеры. Очаги менее 1 см, как правило, сцинтиграфически не манифестируются.
Визуализация желчевыделительной системы (гепатохолесцинтиграфия) основана на использовании серии гепатотропных РФП, аналогичных по своей фармакокинетике красителям (бромсульфалеин, вофавердин). После внутривенного введения они связываются с белками крови, поглощаются полигональными клетками печени и выводятся в составе желчи. Основным преимуществом гепатохолесцинтиграфии является непрерывность визуальной и количественной регистрации процесса кинетики РФП.
Визуальный анализ серии изображений позволяет выявить некоторые органические изменения желчных протоков (расширение), желчного пузыря (деформации), а также функциональные изменения двенадцатиперстной кишки.
Анализ кривых позволяет получить количественные критерии, характеризующие поглотительно-выделительную функцию печени, наполнение желчного пузыря, длительность латентного периода после желчегонного завтрака, скорость опорожнения желчного пузыря. Дискинезии желчного пузыря дифференцируются на основе изменения скорости его опорожнения (гипо- или гипермоторная дискинезия). Следует подчеркнуть, что точность радиологической оценки двигательной функции желчного пузыря превышает рентгенологическую или эхографическую. Это связано с тем, что при сравнении площадей изображения органа до и через фиксированное время после желчегонного завтрака практически невозможно учесть длительность латентного периода желчеотделения и выделить собственно фазу опорожнения желчного пузыря.
Гепатохолесцинтиграфия имеет ограниченное значение в диагностике воспалительной патологии и камней желчного пузыря. Первоочередная задача заключается в оценке тяжести нарушения проходимости шеечно-протоковой зоны и наполнения желчного пузыря. При полной обтурации пузырного протока возникает сцинтиграфический феномен «отключенного желчного пузыря».
Визуализация щитовидной железы (тиреосцинтиграфия) проводится с использованием Тс-пертехнетата и основывается на сходстве в поведении ионов йода и пертехнетата. Однако это сходство прослеживается только на начальной неорганической фазе внутритиреоидного транспорта. Пертехнетат, в отличие от йода, не переходит в органическую фазу, то есть не включается в состав тиреоидных гормонов. Эта особенность исключает возможность его использования при послеоперационном поиске метастазов рака щитовидной железы (последнее проводится только с радиоактивным йодом).
Узловые поражения щитовидной железы и дифференциальная диагностика выявленных клинически или эхографически узловых образований шеи — наиболее частое показание к тиреосцинтиграфии. Основная задача исследования — оценить степень функционирования узлов, идентифицировать солитарные или множественные образования, установить связь узлов с тиреоидной тканью. В зависимости от функциональной активности и степени накопления радиопертехнетата узлы традиционно разделяют на «горячие», «теплые» и «холодные». Однако такое деление относится только к их сцинтиграфической оценке.
Под термином «горячий» узел подразумевают ситуацию, когда РФП накапливается почти исключительно в области узла и не накапливается в других отделах органа. Подобные находки характерны для автономной тиреоидной ткани, токсической аденомы, аутоиммунного тиреоидита, врожденной аплазии доли. Отсутствие накопления РФП в окружающий узел ткани объясняется продукцией автономным узлом тиреоидных гормонов, уменьшающих выделение ТТГ и обусловливающих подавление функции нормальной ткани.
Функционально неактивные («холодные») узлы характеризуются отсутствием или резким снижением накопления радиопертехнетата. Эта менее специфическая находка сопровождает широкий спектр патологии: узловой зоб, коллоидные кисты, аденому, неспецифический струмит, в 15-25% случаев — рак щитовидной железы (рис. 3).
Наибольшие затруднения представляет идентификация «теплых» узлов. Эти узлы рассматривают как разновидность «горячих», но в отличие от последних в них отсутствует или слабо выражено функциональное подавление нормальной тиреоидной ткани. В силу этого накопление РФП в узлах может не отличаться от окружающей паренхимы и приводить к ложноотрицательным трактовкам данных сцинтиграфии.
Радионуклидная диагностика в онкологии
ГУ – Медицинский радиологический научный центр РАМН,
Обнинск, ул. Королева 4, 249036 г., Калужская область, Российская Федерация
Адрес для переписки: Герман Анатольевич Давыдов; e-mail:
Ключевые слова: онкология, диагностика, радионуклиды.
Ранняя диагностика злокачественных новообразований остается одной из наиболее актуальных задач современной медицины. Возможности методов ядерной медицины в онкологии основаны в первую очередь на выявлении метаболических нарушений в опухолях и окружающих тканях. Принцип функциональной визуализации опухолей отличает методы ядерной медицины от анатомо-топографических методов лучевой диагностики (ультразвуковой томографии, рентгеновской компьютерной томографии и магнитно-резонансной томографии), которые оценивают динамику новообразований по изменению их размеров и структуры. Особенности радионуклидных методов позволяют использовать их для выявления опухолевых поражений в ситуациях, когда структурные изменения не определяются или неспецифичны, а также для оценки раннего ответа опухоли на специфическую терапию, в целях прогнозирования результатов лечения.
Наряду с однофотонной эмиссионной компьютерной томографией (ОФЭКТ), основанной на использовании гамма-излучающих радионуклидов, все большую диагностическую роль в онкологии играет позитронная эмиссионная томография (ПЭТ). Использование в качестве метки биологически важных ультракороткоживущих позитрон-излучающих радионуклидов ( 11 C, 13 N, 15 O, 18 F), позволило создать радиофармпрепараты, обладающие уникальными свойствами (РФП). ПЭТ обеспечивает лучшие возможности для дифференциальной диагностики злокачественных и доброкачественных новообразований, определения распространенности опухолевого процесса, раннего выявления рецидивов и оценки эффективности проводимого лечения.
Основными задачами радионуклидной диагностики при исследовании онкологических больных являются следующие:
РФП для сцинтиграфической диагностики опухолевого процесса
Применяемые для диагностики опухолей РФП разделяют на следующие группы:
РФП, способные накапливаться в интактных тканях, окружающих опухоль
РФП этой группы отличаются тропностью к той или иной ткани организма, что позволяет выявить наличие опухоли как область пониженного накопления индикатора – «дефект накопления». К ним относятся: 99m Тс-коллоид, который аккумулируется в купферовских клетках печени. 99m Тс-пертехнетат и изотопы йода ( 123 I или 131 I), использующиеся для диагностики опухолей щитовидной железы. Недостатком методик с использованием этих препаратов является невысокая специфичность, так как любое объемное поражение (например, киста) визуализируется аналогичным образом.
РФП, способные накапливаться в тканях, подверженных неспецифическим изменениям со стороны опухоли
Использование РФП данной группы основано на свойстве их повышенного включения в участки ткани, окружающие новообразование. Так, окружающие костную опухоль ткани реагируют на ее рост повышенной остеобластической активностью. Фосфатные комплексы 99m Тс, накапливаясь в остеобластах этих участков, позволяют визуализировать костные метастазы и первичные опухоли костей на самой ранней стадии их развития как очаги гиперфиксации РФП. Метод остеосцинтиграфии обладает высокой чувствительностью, однако специфичность его невысока. Высокое накопление указанных РФП в костной ткани может наблюдаться также при травмах, воспалительных и дистрофических заболеваниях.
С целью паллиативной терапии метастазов в кости применяются меченный самарием-153 этилендиаминтетраэтиленфосфонат и меченный рением-186 этидронат, накапливающиеся в участках с повышенной остеобластической активностью.
РФП, тропные к мембранам опухолевых
клеток по реакции «антиген-антитело»
В основе диагностического применения РФП данной группы в онкологии лежит реакция связывания меченых моноклональных антител с антигенами мембран раковых клеток. В радионуклидной диагностике нашли применение как целые антитела типа IgG, так и их фрагменты (Fab-fragments of antibody). Для диагностики колоректального рака применяется препарат на основе целых антител – 111 In-Онкосцинт, а также фрагментов антител – 99m Tc-КЭА-Скан. Преимуществом фрагментов меченых антител является более высокая онкоспецифичность. Однако ускоренный клиренс фрагментов антител из крови за счет более быстрого, по сравнению с большими молекулами иммуноглобулинов, выведения почками может снижать соотношение «опухоль/фон» в злокачественных новообразованиях с обедненным кровотоком. Кроме того, технология получения Fab является достаточно трудоемкой и дорогостоящей.
РФП, тропные к мембранам опухолевых
клеток по механизму клеточной рецепции
Применение таких РФП для сцинтиграфической диагностики основано на их тропности к некоторым рецепторам мембран опухолевых клеток.
Из индикаторов такого типа наиболее часто используются аналоги соматостатина – окреотид, меченный 111 In, и 99m Тс-депреотид (NeoSpect). Соматостатин представляет собой тетрадекапептид, секретируемый гипоталамусом, который подавляет выделение нейроэндокринных гормонов (гормон роста, глюкагон, инсулин и гастрин). Во многих злокачественных опухолях и при некоторых воспалительных заболеваниях плотность рецепторов соматостатина значительно повышается. Гиперэкспрессия рецепторов соматостатина наблюдается в большинстве нейроэндокринных опухолей, включая мелкоклеточный рак легкого, а также в перитуморальных венах некоторых опухолей человека.
Меченые аналоги соматостатина нашли применение для диагностики ряда нейроэндокринных опухолей (карциноид, феохромацитома, параганглиома, меланома), мелкоклеточного рака легких, новообразований центральной нервной системы и лимфом. Чувствительность и специфичность сцинтиграфического выявления таких злокачественных новообразований с применением 111 In-окреотида превышает 80%. Вместе с тем, диагностика онкологических поражений печени и селезенки с этим РФП существенно затруднена по причине высокого уровня неспецифической аккумуляции данного индикатора в указанных органах. Депреотид, меченный 99m Тс, используется преимущественно для выявления рака легкого. При этом чувствительность диагностики злокачественных солитарных легочных новообразований в комбинации сцинтиграфии с КТ или рентгенографией грудной клетки достигает 97% при специфичности 73% [1].
В последние годы в онкологической практике нашли применение меченные 123 I пептиды, которые также способны связываться с мембранами опухолевых клеток. Среди них следует отметить 123 I-вазоактивные кишечные пептиды для визуализации злокачественных новообразований желудочно-кишечного тракта и поджелудочной железы; 123 I-ά-меланоцитостимулирующий гормон для диагностики меланом; 123 I-инсулин, накапливающийся в гепатомах, и 123 I-нейропептиды для выявления мелкоклеточного рака легкого.
Специфические РФП, проникающие в опухолевые клетки
Радиофармпрепараты указанной группы включаются в специфический метаболизм опухолей. К ним относятся изотопы йода 123 I и 131 I, 123 I-метайод-бензил-гуанидин ( 123 I-МИБГ) и пятивалентный 99m Тс (V)-ДМСА.
Йод-131 уже более 50 лет успешно используется для диагностики метастазов фолликулярного и папиллярного рака щитовидной железы, поскольку дифференцированные опухоли щитовидной железы сохраняют способность захватывать йод и включать его в синтез тиреоидных гормонов. Метастазы раковой опухоли обнаруживаются в виде участков экстратиреоидного эктопического накопления.
В последние годы для выполнения радиодиагностических процедур все чаще вместо 131 I используют 123 I, который имеет ряд преимуществ: оптимальный для регистрации спектр энергетического излучения (159 кэВ) и короткий период полураспада (13,2 часа), способствующий уменьшению лучевой нагрузки на пациента.
К специфическим опухолетропным препаратам относится также 123 I-МИБГ, который через норэпинефриновый механизм поглощения превращается в катехоламины адренергических нервных окончаний и клеток мозгового слоя надпочечников, позволяя тем самым визуализировать надпочечники. Наряду с этим была показана высокая эффективность использования указанного РФП для диагностики и терапии нейроэндокринных опухолей, особенно феохромоцитом, нейробластом, карциноида, медуллярного рака щитовидной железы и параганглиом. Для радиотерапевтических целей используется МИБГ, меченный 131 I.
К РФП этой группы также относят пятивалентный 99m Тс(V)-ДМСА, специфично накапливающимся в клетках медуллярного рака щитовидной железы. Однако механизм аккумуляции 99m Тс(V)-ДМСА в опухоли остается неизученным [1, 7].
Неспецифические РФП, проникающие в опухолевые клетки
Цитрат галлия-67 ( 67 Ga-цитрат) уже много лет успешно используется как туморотропный радиофармпрепарат. 67 Ga после внутривенного введения образует комплекс с трансферрином крови, который связывается с рецепторами некоторых опухолевых клеток. Посредством инвагинации целлюлярной мембраны 67 Gа-трансферрин попадает внутрь клетки и, образовав комплекс с лактоферрином, остается в ней [1, 7].
67 Ga-цитрат хорошо зарекомендовал себя в качестве РФП для радионуклидной диагностики лимфом и мелкоклеточного рака легких. В литературе описаны случаи применения этого РФП и для выявления других злокачественных образований. В то же время, неспецифическая аккумуляция 67 Ga-цитрата в печени и экскреция в желудочно-кишечный тракт ограничивают его использование для диагностики опухолей брюшной полости. Специфичность метода снижает также аккумуляция 67 Ga-цитрат в зонах инфекции и воспаления. Сцинтиграфия с этим РФП особенно эффективна для динамического наблюдения за больными с верифицированными злокачественными новообразованиями в динамике химио- или лучевой терапии.
Изотопы таллия ( 201 Тl и 199 Тl), являясь биологическим аналогом калия, поступают внутрь клетки с помощью натрий-калиевого АТФ-зависимого насоса и локализуются в митохондриях. Эти РФП аккумулируются преимущественно в тканях с интенсивным энергетическим обменом (к числу которых относятся атипичные клетки) и широко используются для диагностики самых разнообразных опухолей, включая новообразования бронхов, лимфомы, рак щитовидной железы, костей и головного мозга. Как и цитрат 67 Ga, изотопы таллия успешно применяют для динамической оценки противоопухолевой терапии.
В последнее время в ядерной онкологии стали активно использоваться комплексы технеция-99m с метокси-изобутил-изонитрилом ( 99m Тс-МИБИ) и тетрофосмином (миовью), благодаря способности этих РФП к усиленной аккумуляции в митохондриях злокачественных клеток. Наиболее активно эти индикаторы используют для выявления рака молочной железы, опухолей легких, лимфом и миеломной болезни [1, 7].
РФП для позитронно-эмиссионной томографии
Позитронно-излучающий РФП 18 F-фтордезоксиглюкоза ( 18 F-ФДГ) позволяет с высокой чувствительностью выявлять самые разнообразные злокачественные новообразования.
Аккумуляция этого индикатора в клетке прямо пропорциональна эффективности функционирования белкового переносчика глюкозы и коррелирует с активностью гексокиназы II – фермента, реализующего обмен гидроксильной группы глюкозы на фосфатный комплекс АТФ. Фосфорилированный метаболит 18 F-фтордезоксиглюкозы теряет способность к транспорту через мембрану клетки и остается интрацеллюлярно. Таким образом, ФДГ в отличие от обычной глюкозы, попадая внутрь клетки, участвует только в начальных этапах гликолиза, поэтому не распадается, за счет чего и происходит ее прогрессивное накопление в клетке (феномен «метаболической ловушки»). Высокое соотношение концентрации РФП «опухоль/фон» достигается, таким образом, за счет заметно более высокой активности гексокиназы II в малигнизированных клетках. Визуализация опухолей осуществляется за счет повышенной гликолитической активности клеток опухолевой ткани и повышенной активности глюкозных транспортеров на мембранах опухолевых клеток, осуществляющих захват глюкозы внутрь клетки. При этом биологическая активность опухоли прямо пропорциональна степени метаболического захвата глюкозы 3.
Применение другого неспецифического позитронно-излучающего РФП 11 С-метионина для диагностики опухолей базируется на высоком уровне аминокислотного обмена в активно пролиферирующих клетках злокачественных опухолей. Этот индикатор используется при выявлении лимфом, злокачественных новообразований шеи и головы.
Для диагностики новообразований методом ПЭТ применяется ряд туморотропных РФП, визуализирующих злокачественные опухоли как очаги нарушения метаболизма. Для изучения нарушений углеводного обмена (клеточная энергетика) применяется 18F-фтордеоксиглюкоза (18F-ФДГ); клеточного транспорта аминокислот – 11С-метионин; процессов клеточного синтеза белков – 11С-тирозин, 11С-лейцин; скорости клеточной пролиферации – 11С-тимидин (как маркер синтеза ДНК) и 11С-холин (участвующий в биосинтезе клеточной мембраны); синтеза липидов – (11С-ацетат); степени гипоксии опухолевой ткани – 18F-фтормизонидазол [4].
Индикаторы гипоксии являются перспективными РФП для сцинтиграфической диагностики злокачественных новообразований. Визуализация малигнизированных тканей в этом случае становится возможной потому, что в центральных областях опухоли имеют место обеднение кровотока и сопутствующая гипоксия. Нитроимидазол путем диффузии проникает внутрь клетки за счет липофильности своей молекулы, образуя в условиях гипоксии ряд недоокисленных продуктов своего превращения. Эти метаболиты связываются с компонентами клетки и, в отличие от нормы, фиксируются интрацеллюлярно [2, 8].
КЛИНИЧЕСКОЕ ПРИМЕНЕНИЕ ПЭТ В ОНКОЛОГИИ
ПЭТ в настоящее время нашла широкое применение во многих областях медицины. Первый опыт использования этого метода был посвящен функциональным исследованиям головного мозга. В дальнейшем ПЭТ стала успешно использоваться для диагностики различных форм деменции, очаговых форм эпилепсии.
В кардиологии ПЭТ-исследования сердца дают уникальную информацию о жизнеспособности миокарда, таким образом определяя целесообразность кардиохирургических вмешательств. Однако самым востребованным метод ПЭТ оказался в онкологии. Этому способствовало появление и начало серийного изготовления установок для ПЭТ «всего тела», а также разработка большого ассортимента позитронно-излучающих туморотропных РФП. Ценнейшая информация, получаемая при исследованиях больных злокачественными новообразованиями, сделала ПЭТ одним из ведущих диагностических методов. Это обстоятельство привело к резкому возрастанию относительной доли онкологических ПЭТ-исследований, которая в настоящее время составляет около 90%.
Самой распространенной и наиболее освоенной методикой является ПЭТ с 18F-фтордеоксиглюкозой (18F-ФДГ). Количество этих исследований приобрело такой размах, что, по мнению ведущих специалистов ядерной медицины, 18F-ФДГ завоевала в 1990-х гг. номинацию «молекулы века» [4, 6].
Применение ПЭТ в диагностике рака легких
ПЭТ c ФДГ высоко эффективна в дифференциальной диагностике первичных опухолей у больных с солитарными легочными узлами: прогностическая ценность положительного результата – 90%, отрицательного результата – до 100%.
Ложноотрицательный результат может наблюдаться при поражениях менее 1 см, опухолях с низкой метаболической активностью (например, карциноидных), бронхоальвеолярном раке. Повышенное включение ФДГ возможно при различных воспалительных заболеваниях. В сомнительных случаях поражения с повышенным захватом ФДГ должны считаться злокачественными, пока не будет доказано обратное.
Оценка региональных лимфоузлов средостения у потенциально операбельных больных немелкоклеточным раком легкого превышает результаты КТ и составляет: чувствительность 89%, специфичность 92% и точность 90%. Лучшие результаты ПЭТ объясняются тем, что размеры лимфоузлов являются относительным критерием метастатического поражения. Лимфоузлы могут быть увеличены вследствие воспаления или инфекции, а мелкие узлы могут содержать метастазы.
При выявлении внутригрудных метастазов ПЭТ несколько точнее КТ. По сравнению со стандартной остеосцинтиграфией с 99m Tc-метилендифосфонатом, ПЭТ имеет большую специфичность (98% против 61%) при аналогичной чувствительности (до 90%) при визуализации метастазов в кости. Интерпретация сцинтиграфии костей с МДФ затруднена из-за ложноположительных результатов при воспалительных и дистрофических изменениях костей и суставов.
Отмечается высокая эффективность ФДГ-ПЭТ в выявлении рецидивов немелкоклеточного рака легкого. При подозрении КТ на рецидив ПЭТ способна дифференцировать посттерапевтические рубцы и опухоли с чувствительностью 97-100%, специфичностью 62-100% и точностью 78-98% (Рис.1). Чтобы избежать ложноположительных результатов ПЭТ вследствие лучевого пневмонита или гликолиза макрофагов внутри опухолевого некроза, исследование рекомендуется проводить через 4-6 месяцев по окончании лечения.
Показаниями к проведению ПЭТ с ФДГ у больных немелкоклеточным раком легкого являются: дифференциальная диагностика первичной опухоли, определение распространенности опухолевого процесса, выявление рецидивов.
Рис. 1. Результат ПЭТ-исследования. Выявление рецидивной опухоли верхушки левого легкого.
Применение ПЭТ в диагностике рака толстой кишки
Основными задачами ПЭТ с ФДГ при исследовании больных раком толстой кишки являются:
Метод ПЭТ недостаточно эффективен при диагностике регионарных лимфоузлов. Причина низкой чувствительности объясняется расположением большинства лимфоузлов вблизи первичной опухоли или наличием в них микрометастазов. Однако отсутствие вовлечения лимфоузлов не вызывает изменения в лечении, поскольку удаление брыжейки без первичного поражения является частью лечебной процедуры. ПЭТ является наиболее чувствительным (90-95%) методом выявления метастазов в печень колоректального рака, в чем превосходит КТ, при специфичности 88-100%. Исключение отдаленных метастазов до операции и повторных резекциях является важным показанием ФДГ-ПЭТ у больных колоректальным раком.
Показаниями к ПЭТ у больных с выявленным или подозреваемым рецидивом являются: увеличение опухолевых маркеров, аномальное поражение при стандартной визуализации (КТ и МРТ), дифференциальная диагностика местных рецидивов и посттерапевтических (хирургических, лучевых и химиотерапевтических) изменений. ПЭТ позволяет дифференцировать рецидив опухоли от захвата ФДГ вследствие лучевой терапии (спустя 6 месяцев после лечения). По данным ПЭТ выявляется больше поражений, чем при КТ, что приводит к серьезным изменениям в лечении у 48% больных.
Примером успешной дифференциальной диагностики между рецидивом опухоли и послеоперационной рубцовой тканью является выявление, по данным ПЭТ, рецидива рака прямой кишки после брюшно-промежностной экстирпации прямой кишки, когда эндоскопия оказалась невозможной, а УЗИ и КТ не позволяли дифференцировать рецидив и послеоперационные рубцовые изменения (Рис.2).
Рис. 2. ПЭТ с 18F-ФДГ. Визуализация рецидива рака прямой кишки (а) на фоне физиологического накопления
радиофармпрепарата в головном мозге и почках.
Применение ПЭТ в диагностике гемобластозов
При исследовании больных злокачественными лимфомами перед ФДГ-ПЭТ ставятся задачи по определению стадии опухолевого процесса, оценке эффективности лечения, выявлению рецидивов заболевания. Диагностическое обследование больных злокачественными лимфомами является одним из наиболее значимых показаний для проведения ПЭТ с ФДГ.
При стадировании злокачественной лимфомы ФДГ-ПЭТ имеет одинаковую специфичность с РКТ (90%), однако превосходит ее в чувствительности (92% и 65% соответственно). Точность оценки состояния селезенки при первичном стадировании злокачественной лимфомы для ФДГ-ПЭТ составляет около 100% (для КТ –57%), а точность диагностики поражения костного мозга посредством ФДГ-ПЭТ сопоставима с таковой при биопсии костного мозга.
ПЭТ с ФДГ успешно применяется для оценки эффективности проводимого лечения. Контроль ответа на химиотерапию обычно проводится через 3-4 цикла лечения. По данным некоторых исследователей, прогностическая информация может быть получена уже после первого цикла химиотерапии (Рис.3).
Рис. 3. ПЭТ-исследование при злокачественной лимфоме:
а) до лечения (поражение правых шейно-надключичных и медиастинальных лимфоузлов);
б) после эффективного лечения (отсутствие активных очагов специфической ткани).
Применение ПЭТ в диагностике метастазов меланомы
Меланома относится к опухолям с наиболее выраженным гликолизом, высоким захватом ФДГ и соотношением «опухоль-кровь». Основными задачами ПЭТ с ФДГ при обследовании больных меланомой являются: диагностика местной и региональной распространенности опухолевого процесса у больных меланомой высокого риска (толщина первичной опухоли больше 4,0 мм с прорастанием в подкожные ткани), выявление отдаленных метастазов и рецидивов опухоли.
В диагностике первичной опухоли и пораженных регионарных лимфоузлов в стадиях 1-2 метод ПЭТ с ФДГ обладает низкой чувствительностью, большая по величине опухоль выявляется отчетливо. В стадии 3 визуализируются практически все метастазы в регионарные лимфоузлы размерами более 10 мм, 83% метастазов размерами 6-10 мм и 13% метастазов меньших размеров.
В диагностике метастазов во внутренние органы общая чувствительность ПЭТ с ФДГ составляет 80-100%. Наиболее полезна ПЭТ у больных с наличием метастазов в брюшной полости (чувствительность – до 100%). По сравнению со стандартной КТ, ПЭТ более чувствительна и специфична в визуализации метастазов в кости, тонкую кишку и лимфоузлы, в то время как метастазы в легкие выявляются хуже. В диагностике метастазов в печень ПЭТ более чувствительна, чем УЗИ, КТ и МРТ.
Применение ПЭТ в диагностике
распространенности рака пищевода и желудка
Основными задачами исследования ПЭТ с ФДГ у больных раком пищевода и желудка являются: стадирование лимфоузлов и выявление отдаленных метастазов у больных с резектабельной опухолью.
Первичные опухоли пищевода и желудка, ограниченные слизистой оболочкой, с помощью ФДГ-ПЭТ визуализируются плохо. Их выявление становится возможным только при инвазии опухоли в подслизистый слой. Специфичность ПЭТ в стадировании лимфоузлов выше, чем у других методов лучевой диагностики (КТ, эндоскопической сонографии). В оценке отдаленных метастазов (в лимфоузлах, печени, плевре, грудной клетке и костях) ПЭТ с ФДГ имеет большую точность по сравнению со стандартным использованием СКТ и УЗИ. ПЭТ обладает высокой диагностической эффективностью в выявлении рецидивов рака пищевода, однако в диагностике перианастомотических рецидивов часто дает ложноположительные результаты из-за накопления ФДГ в участках воспаления. Отмечается высокая эффективность ПЭТ с ФДГ в оценке ответа на лучевую и химиотерапию опухолей пищевода и желудка.
Применение ПЭТ в диагностике
распространенности опухолей головы и шеи
Эффективность лечения больных раком органов головы и шеи в существенной мере зависит от точности оценки местной и регионарной распространенности опухолевого процесса.
Первичные опухоли, региональные и отдаленные метастазы характеризуются интенсивным захватом ФДГ. Метастазы в лимфоузлы характеризуются высоким захватом ФДГ и хорошо контрастируются. Установлено, что в выявлении метастатического поражения шейных лимфатических узлов у больных раком органов головы и шеи чувствительность и специфичность ПЭТ с ФДГ составили 90 и 94%, в то время как аналогичные показатели для КТ были 82 и 85%, МРТ – 80 и 79%.
ПЭТ с ФДГ также является эффективным и объективным инструментом оценки эффективности химиотерапии и лучевого лечения злокачественных опухолей головы и шеи. Метод позволяет дифференцировать жизнеспособную опухолевую ткань от фиброзно-склеротического процесса после лучевой терапии (Рис.4).
Рис. 4. ФДГ-ПЭТ и МРТ при плоскоклеточном раке слизистой левой щеки: А, B – до лечения; С, Д – после химиорадиотерапии.
При ФДГ-ПЭТ констатирован полный эффект в виде исчезновения гиперметаболического очага (истинно отрицательный результат), хотя на МРТ визуализируется остаточный субстрат (ложноположительный результат).
ФДГ позволяет эффективно выявить пораженные ЛУ средостения, а также отдаленные метастазы в легкие, печень, кости. Отсутствие захвата ФДГ обычно исключает остаточную или рецидивную опухоль.
При обследовании больных дифференцированным раком щитовидной железы наиболее важной задачей ФДГ-ПЭТ является выявление рецидивов у больных с повышенным уровнем опухолевого маркера (тиреоглобулина) на фоне отрицательного скана «всего тела» с 131 I. По мнению большинства исследователей, ФДГ-ПЭТ является эффективным методом выявления йод-негативного метастатического поражения шейно-надключичных, медиастинальных лимфоузлов и легких.
Применение ПЭТ в диагностике
распространенности рака молочной железы
Основной задачей ФДГ-ПЭТ при исследовании больных раком молочной железы является прогностическая оценка биологической активности первичной опухоли, диагностика регионарных и отдаленных метастазов, оценка эффективности проводимого противоопухолевого лечения и выявление местных рецидивов заболевания. Некоторые исследователи при наблюдении за группой больных местно-распространенным раком молочной железы отметили, что при высокой метаболической активности первичной опухоли, определяемой ФДГ-ПЭТ, можно прогнозировать низкую эффективность неоадъювантной химиотерапии. Что касается предоперационного стадирования рака молочной железы, то, по данным ряда зарубежных авторов, чувствительность ФДГ-ПЭТ при диагностике мультифокального поражения оказалась вдвое выше, чем при комбинированном применении маммографии и ультразвукового метода (63 и 32% соответственно). Чувствительность и специфичность ФДГ-ПЭТ при диагностике метастатического поражения аксиллярных лимфатических узлов составили 79 и 92% соответственно.
Влияние результатов ФДГ-ПЭТ на установление стадии заболевания и выбор тактики лечения рака молочной железы проанализировано в ряде зарубежных работ. Авторы указывают, что с учетом находок ФДГ-ПЭТ клиническая стадия была изменена в 36% наблюдений (28% – в сторону увеличения, 8% – в сторону уменьшения), вид лечения был скорректирован у 28%, а объем лечения – у 30% больных. Диагностическая чувствительность и специфичность ФДГ-ПЭТ при обследовании пациентов с подозрением на рецидив рака молочной железы, имеющих асимптоматическое повышение уровня опухолевых маркеров, составляют 96 и 90% соответственно [2, 4, 5].
Позитронные томографы обладают сравнительно невысоким пространственным разрешением, что затрудняет визуальный анализ ПЭТ-изображений. В связи с этим ПЭТ-сканеры производятся в конфигурации со сканерами рентгеновской компьютерной томографии (КТ), совмещенными в одной установке. Совмещение метаболических (ПЭТ) и анатомо-топографических (КТ) данных позволяет повысить точность локализации опухоли и определения распространенности заболевания. Совмещенная ПЭТ/КТ-технология позволяет получать более информативные изображения по сравнению с изображениями, получаемыми КТ- и ПЭТ-методами (Рис.5).
Рис. 5. КТ-изображение (А) и ПЭТ-изображение (В) плоскоклеточного рака левого легкого с метастазами в лимфоузлы средостения. Совмещенное КТ-ПЭТ-изображение (С) позволяет констатировать в рентгенологически выявленном очаге в легком наличие активной опухолевой ткани по периферии образования и очаг некроза в центре опухоли (помечено стрелкой).
Проблемы применения ПЭТ c ФДГ в онкологии
Клиническое применение ПЭТ с ФДГ выявило ряд ограничений, обусловленных, в частности, неспособностью эффективно выявлять опухоли малых размеров (до 10 мм), визуализировать некоторые опухоли мозга и опухоли мочеполовой системы, а также неспособностью дифференцировать злокачественные заболевания от воспалительных изменений. Поэтому задача разработки новых альтернативных ФДГ радиофармпрепаратов с более высокой туморотропностью и специфичностью является актуальной.
Согласен Данный веб-сайт содержит информацию для специалистов в области медицины. В соответствии с действующим законодательством доступ к такой информации может быть предоставлен только медицинским и фармацевтическим работникам. Нажимая «Согласен», вы подтверждаете, что являетесь медицинским или фармацевтическим работником и берете на себя ответственность за последствия, вызванные возможным нарушением указанного ограничения. Информация на данном сайте не должна использоваться пациентами для самостоятельной диагностики и лечения и не может быть заменой очной консультации врача.
Сайт использует файлы cookies для более комфортной работы пользователя. Продолжая просмотр страниц сайта, вы соглашаетесь с использованием файлов cookies, а также с обработкой ваших персональных данных в соответствии с Политикой конфиденциальности.