Миртазапин или триттико что лучше
ЛЕКАРСТВА ОТ ДЕПРЕССИИ
Депрессия — одно из самых распространенных заболеваний. По распространенности уступает лишь сердечно-сосудистым заболеваниям. И из всех страдающих депрессией за квалифицированной помощью обращаются не более 20%.
В этой статье мы расскажем Вам о всех препаратах, применяемых для лечения депрессии.
Все лекарства с антидепрессивным действием можно разделить на несколько групп:
Антидепрессанты
Изначально препараты этой группы разрабатывались для лечения депрессии. В настоящее время показания к приему антидепрессантов расширились. Их применяют и при других расстройствах психики: неврозы, расстройства личности, агрессивность, психозы, шизофрения. А так же при многих заболеваниях: хронические боли, синдром раздраженного кишечника, энурез, бессонница. Применяются на практике с 1957 года. Основа действия антидепрессантов — восстановление нарушенного обмена серотонина. Измененный обмен нейромедиаторов — один из основных механизмов развития депрессии, поэтому его нормализация обеспечивает антидепрессивный эффект. Антидепрессанты убирают симптомы депрессии, на человека с нормальным настроением они никакого действия не окажут.
Список наиболее распространенных и эффективных антидепрессантов
Трициклические антидепрессанты.
Амитриптилин — один из самых сильных и эффективных антидепрессантов. При тяжелых депрессиях является препаратом первого выбора. При внутривенном и внутримышечном введении действует быстро, поэтому применяется в скорой психиатрической помощи. Из недостатков — побочные эффекты: сонливость, сухость во рту, нечеткость зрения, легкие координационные нарушения.
Кломипрамин (анафранил) — также обладает сильным антидепрессивным эффектом и часто встречающимися побочными эффектами. Помимо антидепрессивного эффекта уменьшает навязчивости и тревогу.
Имипрамин (мелипрамин) — отличается выраженным стимулирующим эффектом. Эффективен при депрессиях, протекающих с апатией и заторможенностью. Как и все трициклические антидепрессанты отличается большим количеством побочных эффектов (сухость во рту, склонность к запорам и др.)
Азафен. Из всех трициклических антидепрессантов отличается хорошей переносимостью, поэтому часто рекомендуется пожилым и лицам с сопутствующими болезнями внутренних органов.
Ингибиторы монооаминооксидазы (МАО)
Ниаламид. Препарат первого поколения этой группы, ушел из практики много лет назад.
Пиразидол. Высокоэффективный антидепрессант широкого спектра действия с минимальными побочными эффектами. Применяется и в наше время.
Моклобемид (аурорикс). Отличается противотревожным действием, это делает его эффективным при депрессиях, сопровождающихся социофобией и тревогой.
Избирательные ингибиторы обратного захвата норадреналина
Мапротилин (людиомил). Хорошо проявил себя при депрессии с утомляемостью, утратой чувств, заторможенностью. Большой плюс этого препарата — наличие форм в виде ампул, позволяющих вводить его внутривенно, что дает возможность быстрого наступления лечебного эффекта.
Доксепин (синекван). Редко используемый препарат.
Избирательные (селективные) ингибиторы обратного захвата серотонина СИОЗС
Эти антидепрессанты в настоящее время— самые часто назначаемые. Такой «популярности» они достигли благодаря ряду преимуществ: эффективны, просты в подборе доз, хорошо переносятся, широко рекламируются фарм.компаниями. Их всего семь, по своей эффективности они примерно одинаковые:
Избирательные ингибиторы обратного захвата норадреналина и серотонина
Эта группа эффективна при резистентных (не поддающихся традиционному лечению) депрессиях.
Антидепрессанты блокаторы рецепторов
Лекарства этой группы отличаются наличием успокоительного эффекта и восстанавливающим сон действием.
Новый класс антидепрессантов
Характерно несильное антидепрессивное действие, но отличная переносимость: побочные эффекты встречаются крайне редко. Применяются при нетяжелых депрессиях.
Агомелатин (вальдоксан). Нормализует сон.
Вортиоксетин (бринтелликс). Улучшает когнитивные функции.
Нормотимические препараты
Лекарства этой группы оказывают антидепрессивное действие только в случаях, когда депрессивное состояние вызвано хроническими аффективными болезнями, такими как биполярное аффективное расстройство (БАР, маниакально-депрессивный психоз), циклотимия, дистимия, шизоаффективное расстройство. Наиболее часто используемые лекарства:
Нейролептики
Несмотря на то, что большинство нейролептических средств угнетают нервную систему, среди них есть препараты с антидепрессивным действием:
Флупентиксол (флюанксол). Антидепрессивный эффект дает лишь при назначении в малых дозах (менее 2 мг в сутки).
Арипипразол. Эффективен при депрессии в рамках биполярного аффективного расстройства и шизитипических расстройствах.
Левомепромазин (тизерцин). Назначают при эндогенных депрессиях, сопровождающихся бессонницей.
Транквилизаторы
Бромдигидрохлорфенилбензодиазепин (феназепам). Препарат выбора при невротических состояниях с депрессией, при постстрессовых состояниях. То есть в тех случаях, когда требуется кратковременное лечение.
Клоназепам. Сильное противотревожное и успокоительное действие. При длительном приеме вызывает зависимость.
Альпразолам. Назначают при тревожно-депрессивных состояниях. Рекомендован короткими курсами (не более 10 дней) из-за риска развития привыкания и зависимости.
Ноотропы и метаболические средства
Средства этой группы помогают выйти из депрессивного состояния, которое развилось на фоне стресса, переутомления, энцефалопатии, последствий травм и отравлений. Улучшая кровоснабжение нейронов и энергетический обмен внутри клеток они способствуют активации когнитивных функций и памяти. Наиболее действенные препараты этой группы:
Как использовать миртазапин в клинической практике?
М. Ю. Дробижев, С. В. Кикта
ГОУ ВПО ММА им. И.М.Сеченова, ГМУ УД президента РФ.
С появлением значительного числа новых антидепрессантов (тимоаналептиков), открываются возможности для индивидуального подбора препарата наиболее адекватного психопатологическим особенностям курируемого состояния. Реализация такой возможности сопряжена с точной оценкой спектра психотропной активности препарата, включая симптомы (синдромы мишени) и их соответствие механизмам действия препарата. Вместе с тем эта имеющаяся в открытой печати информация порой разноречива.
Возьмем, к примеру, миртазапин, доступный в настоящее время в нашей стране как в виде брендового препарата (Ремерон), так его дженериков, включая Миртазонал (произведенный фирмой Актавис). Характеристики спектра психотропной активности этого антидепрессанта можно встретить в различных источниках. Так, в распространенном и доступном для практикующих психитаров справочнике Vidal сообщается, что Миртазонал ослабляет выраженность таких симптомов депрессии как ангедония, психомоторная заторможенность, нарушения сна, снижение массы тела, суицидальные мысли, колебания настроения, потеря интереса к жизни (6). При этом указывается, что этих эффектов препарат достигает за счет блокады центральных пресинаптических α2-рецепторов, которые повышают норадренергическую нейротрансмиссию, а также усиления нейротрансмиссии в серотонинергических синапсах только через серотониновые 5-HT1-рецепторы, т.к. другие серотониновые 5-HT2- и 5-HT3-рецепторы блокируются.
Что же касается того, как Миртазонал (равно как и другие антидепрессанты) достигает указанных эффектов, то сообщается следующее. Депрессии с проявлениями позитивной аффективности поддаются лечению этим препаратом (наряду с иными антидепресантами) вне зависимости от его фармакологических свойств (воздействие на серотонинергические, норадернергические структуры мозга и т.д.). При депрессивных состояниях с негативной аффективностью Миртазонал (равно как и другие современные антидепрессанты, обладающие высокой, по сравнению с ТЦА, нейрохимической селективностью) легче переносятся, не сопряжен с поведенческой токсической, и гипотетически более эффективен.
В пределах терапевтической схемы, которая развивается другой известной школой отечественной психофармакологии, возглавляемой профессором С.Н. Мосоловым, место Миртазонала представляется следующим образом. В первом издании справочного руководства по психотропным и противоэпилептическим препаратам, разрешенным к применению в России (7) сообщается, что препарат может назначаться как при депрессиях с тревогой и ажитацией, так и заторможенностью, апатией, поскольку относится к сбалансированным антидепрессантам с преобладанием анксиолитического и мягкого седативного действия. Иная версия показаний излагается в следующем издании справочного руководства (3). В качестве показаний для Миртазонала фигурирует лишь депрессии с тревогой и ажитацией. В то же время сам препарат рассматривается уже в качестве седативного антидепрессанта. Важно, также, что в обоих случаях не уточняется, как представленный спектр психотропной активности соотносится с механизмом действия этого медикаментозного средства: селективное воздействие на определенный подтип постсинаптических серотониновых рецепторов.
Наконец, приведем данные фундаментального обзора, посвященного рассматриваемому препарату, напечатанному в одном из наиболее солидных отечественных изданий, посвященных психиатрии и психофармакологии (2). Автор этой публикации П.В. Морозов, обобщая накопленный опыт работы с антидепрессантом, сообщает о высокой эффективность препарата при лечении депрессий с тревогой и бессонницей и быстроте начала действия. Однако и из этого обзора остается неясно, как психотропная активность антидепрессанта связана с его довольно сложным механизмом действия. Так, указывается лишь, что препарат является специфическим антагонистом центральных α2-рецепторов и обладает незначительным действием на α1-рецепторы. Блокада пресинаптических α2-рецепторов вызывает увеличение высвобождения норадреналина. Последующая активация α1-рецепторов ведет к активизации серотониновых клеток, а непосредственная блокада ингибирования α2-гетерорецепторов, расположенных на окончаниях этих нейронов, ведет к увеличению высвобождения серотонина. Причем указанный нейротрансмиттер действует в дальнейшем только серотониновые рецепторы первого типа (5HT1-рецепторы), в то время как 5HT2-, 5HT3-рецепторы (второго и третьего типа) блокированы рассматриваемым антидепрессантом.
Таблица 1.
Показатели, характеризующие практику применения антидепрессантов, в сравнении с рекомендациями, представленными в справочнике Vidal (4, 6)
| Антидепрессант | Доля больных, принимавших препарат | суточные дозы (мг) | ||||||
| Средняя | Минимальная | Максимальная | ||||||
| абс. | % | Циркадиан ± ст. отклон. | Vidal | Циркадиан | Vidal | Циркадиан | Vidal | |
| амитриптилин | 839 | 25,7 | 87,0±54,2 | 150-200 | 10 | 25-50 | 350 | 400 |
| кломипрамин | 152 | 4,7 | 90,3±51,6 | 100-150 | 25 | 75 | 350 | 250 |
| имипрамин | 138 | 4,2 | 73,1±43,5 | 150 | 20 | 25 | 225 | 200 |
| пипофезин | 81 | 2,5 | 86,4±34,3 | 150-200 | 25 | 25-50 | 200 | 400 |
| пирлиндол | 158 | 4,8 | 124,2±74,3 | 150-300 | 25 | 50-75 | 400 | 400 |
| венлафаксин | 129 | 4,0 | 123,6±72,3 | — | 37,5 | 75 | 450 | 375 |
| дулоксетин | 50 | 1,5 | 68,0±23,4 | 60 | 30 | 30-60 | 120 | 120 |
| милнаципран | 84 | 2,6 | 86,8±45,8 | 100 | 25 | — | 300 | 250 |
| миртазапин | 39 | 1,2 | 31,2±9,4 | 30 | 15 | — | 60 | — |
| миансерин | 75 | 2,3 | 40,7±21,2 | 30-90 | 15 | 30-45 | 120 | — |
| мапротилин | 95 | 2,9 | 90,2±42,4 | 25-150 | 20 | 25 | 200 | 150 |
| сертралин | 215 | 6,6 | 79,0±42,4 | — | 20 | 50 | 200 | 200 |
| циталопрам | 44 | 1,3 | 28,6±11,6 | — | 10 | 20 | 60 | 60 |
| эсциталопрам | 128 | 3,9 | 14,92±8,1 | 10 | 5 | — | 60 | 20 |
| пароксетин | 322 | 9,9 | 27,2±12,2 | 20 | 10 | — | 80 | 50 |
| флуоксетин | 125 | 3,8 | 30,8±15,4 | — | 20 | 20 | 80 | 80 |
| флувоксамин | 178 | 5,5 | 134,0±76,7 | 100 | 25 | 50-100 | 400 | 300 |
| тианептин | 640 | 19,6 | 36,9±6,8 | 37,5 | 12,5 | — | 100 | 37,5 |
Его получали лишь 1,2% из числа обследованных больных. На практике это означает, что нередки случаи, когда практикующие психиатры имеют весьма незначительный опыт использования миртазапина.
Таблица 2.
СДМ, депрессивные синдромы и их тяжесть (1).
| Депрессивные синдромы | СДД | СДН | СДС |
| тяжелые | + | + | + |
| среднетяжелые | |||
| с заторможенностью и апатией по С.Н. Мосолову (3) | + | + | — |
| с негативной аффективностью по А.Б. Смулевичу (5) | + | + | — |
| с позитивной аффективностью по А.Б. Смулевичу (5) | — | + | + |
| тоскливые | — | + | + |
| соматизированные | — | + | + |
| деперсонализационные | + | + | — |
| тревожно-апатические | + | — | + |
| дисфорические | — | + | + |
| астено-адинамические | + | + | — |
| легкие | |||
| с тревогой и ажитацией по С.Н. Мосолову (3) | — | — | + |
| тревожные | — | — | + |
| астенические | — | + | — |
| адинамические | — | + | — |
| апатические | + | — | — |
| ангедонические | + | — | — |
Важно, что между проявлениями СДД, СДН, СДС и механизмом действия антидепрессантов устанавливаются значимые соотношения. Действительно, подавляющее большинство современных препаратов, обладающих тимоаналептическими свойствами, можно дифференцировать на группы, в соответствии с их способностью восполнять недостаток одного, двух или даже трех моноаминов, что рассматривается в качестве т.н. первичных фармакологических свойств антидепрессантов (таблица 3).
Таблица 3.
Классификация антидепрессантов: группы и механизмы действия (1).
Возвращаясь теперь к Миртазоналу, укажем, что согласно современным представлениям, этот антидепрессант относится к препаратам тройного действия, восполняющего дефицит трех моноаминов (дофамина, серотонина, норадреналина). Происходит это следующим образом (рисунок 1).
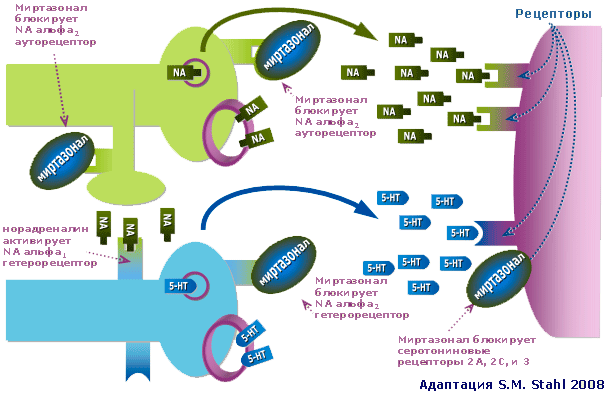
Рис 1. Норадренергический и серотонинергический нейроны при депрессии: действие Миртазонала
Миртазонал блокирует различные регуляторные α1 и α2 адренорецепторы (10). Последние (α2 адренорецепторы) необходимы, прежде всего, для самого норадреналинового нейрона, что он «понимал» достаточно ли он эффективно действует. Располагаясь на этом нейроне (за это они называются ауторецепторами) α2 адренорецепторы как бы тестируют окружающее пространство на наличие норадреналина. Если последнего много, он воздействует на α2 аутоадренорецепторы и норадреналиновый нейрон перестает выбрасывать рассматриваемый нейротрансмиттер. Блокада этих рецепторов приводит к обратному результату. Норадреналиновый нейрон продолжает «работать», выбрасывая норадреналин. В результате подвергаются редукции симптомы, связанные с СДН.
Однако регуляторные α2 адренорецепторы имеются и на серотониновом нейроне (за это они называются гетерорецепторами). Воздействуя на эти гетерорецепторы, норадреналин способен прекратить выброс серотонина. Блокада этих рецепторов, напротив, способствует выделению указанного нейротрансмиттера. В результате подвергаются редукции симптомы, связанные с СДС. Кроме того, уровень серотонина повышается и иным способом.
Наконец, назначение Миртазонала ведет к усилению нейротрансмиссии в серотонинергических синапсах через серотониновые рецепторы первого типа (5-HT1), т.к. аналогичные рецепторные структуры 2-го и 3-го типов (5-HT2 и 5-HT3) блокируются этим антидепрессантом.
Следует, однако, отметить, что роль серотониновых рецепторов 2-го типа в механизме действия Миртазонала на этом не исчерпывается. Дело в том, что блокада серотониновых рецепторов типа 2А и 2С способствует выделению в головном мозге дофамина и норадреналина. Происходит это следующим образом (рисунок 2).
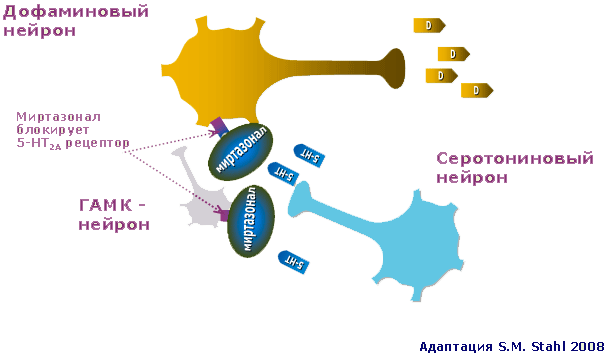
Рис. 2. Серотониновый, дофаминовый и ГАМК-нейроны при депрессии: действие Миртазонала
Регуляторные серотониновые рецепторы типа 2А (5-НТ2А) располагаются как на ГАМКергическом, так и на дофаминовом нейроне. При воздействии на них серотонина способны работа этих нейронов затрудняется. В результате редуцируется активирующее воздействие ГАМК на дофаминовый нейрон. Последний, кроме того, тормозится при непосредственном воздействии серотонина на его собственные 5-НТ2А рецепторы. Миртазонал, блокируя эти серотониновые рецепторы способствует активации дофаминовых нейронов. Это в свою очередь ведет к увеличению содержания в головном мозге дофамина. В результате подвергаются редукции симптомы, связанные с СДД.
В многом сходное действие оказывает Миртазонал на серотониновые рецепторы типа 2С (5-НТ2С) (рисунок 3).
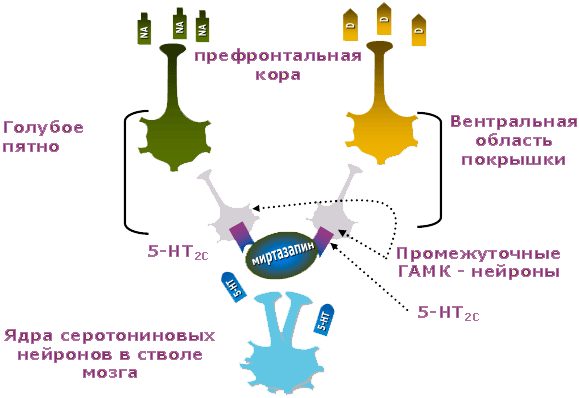
Рис. 3. Серотониновый, дофаминовый и норадреналиновый нейроны при депрессии: действие Миртазонала
Эти регуляторные рецепторы под действием серотонина способны затормозить ГАМКергические нейроны. Последние, в свою очередь, снижают активность норадреналиновых и дофаминовых нейронов. Миртазонал, блокируя серотониновые рецепторы типа 2С (5-НТ2С), напротив, растормаживает ГАМКергические нейроны. Те в свою очередь повышают активность норадреналиновых и дофаминовых нейронов. В результате в головном мозге растет уровень норадреналина и дофамина, а симптомы, свойственные СДН и СДД, редуцируются.
Кроме того, широкому использованию препарата могут препятствовать т.н. дополнительные фармакологические свойства Миртазонала. Имеется в виду способность препарата блокировать H1 гистаминовые, серотониновые рецепторы 3-го типа (5-НТ3). Это приводит к развитию седативного эффекта, улучшению сна, аппетита (блокада H1 гистаминовых рецепторов), а также выраженному противорвотному действию (блокада 5-НТ3 рецепторов) (10). Кроме того, по некоторым данным Миртазонал является частичным агонистом каппа 3 опиоидных рецепторов (9). Соответственно, предполагается, что антиноцицептивное (обезболивающее) действие препарата, весьма важное при лечении соматизированных депрессий, реализуется не только через нормализацию обмена норадреналина и серотонина, но и в результате воздействия на опиоидную систему. Казалось бы, все эти дополнительные фармакологические свойства могут быть только терапевтически желательными при лечении депрессий. Однако следует учитывать, что все указанные свойства, в отличие от первичных, развиваются достаточно быстро, уже в первые дни приема. В результате у практикующего психиатра вполне может сложиться впечатление, что Миртазонал наиболее востребован лишь при лечении тревожных и соматизированных депрессий, протекающих с нарушениями сна и аппетита. Между тем, такое использование свойств препарата будет чрезмерно узким. Соответственно, частота назначений Миртазонала может напрямую зависеть от информированности врачей относительно механизмов действия антидепрессантов.
Выбор антидепрессанта по эффективности и переносимости
Представлена классификация побочных эффектов антидепрессантов и семь категорий переносимости. С помощью этих категорий можно искать наиболее эффективный и переносимый антидепрессант и решать иные практические задачи.
Резюме
Представлена классификация побочных эффектов антидепрессантов. Побочные эффекты могут быть токсическими или нейрональными. Нейрональные побочные эффекты разделяются на «внелечебные» (стойкие или обратимые), а также «паралечебные». Определены семь категорий переносимости антидепрессантов. В самую низкую VII категорию вошли кломипрамин, имипрамин, мапротилин, агомелатин. К VI категории относится амитриптилин, к V – пипофезин, тразодон, миансерин и миртазапин, к IV – вортиоксетин, к III – венлафаксин и дулоксетин, к II – сертралин, пароксетин, циталопрам, эсциталопрам, флуоксетин, флувоксамин и милнаципран, к I – пирлиндол и моклобемид. Из числа наиболее эффективных антидепрессантов (амитриптилин, имипрамин, венлафаксин в высоких суточных дозах) лучшая категория переносимости оказалась у венлафаксина. Этот препарат является наиболее эффективным и переносимым антидепрессантом. Обсуждаются иные варианты практического использования классификаций.
Summary
A classification of the side effects of antidepressants is presented. Side effects can be toxic or neuronal. Neuronal side effects are divided into «extratherapeutic» (persistent or reversible), as well as «paratherapeutic». Seven antidepressant tolerability categories have been identified. The lowest VII category included clomipramine, imipramine, maprotiline, agomelatine. Amitriptyline belongs to the VI category, pipofezin, trazodone, mianserin and mirtazapine to the V category, vortioxetine belong to the IV category, venlafaxine and duloxetine to the III category, sertraline, paroxetine, citalopram, escitalopram, fluoxetine, fluvoxamine and milnacipran to the II category, and pirlindole and moclobemide to the I category. Among the most effective antidepressants (amitriptyline, imipramine, venlafaxine in high daily doses), venlafaxine was in the best category of tolerability. This drug is the most effective and tolerable antidepressant. Other options for the practical use of classifications are discussed.
В предыдущей статье была представлена характеристика механизма действия различных антидепрессантов (трициклических – ТцА, сертонинмодулирующих – СмА, четырехциклических – ЧцА, обратимых ингибиторов моноаминоксидазы типа «А» – ОИМАО-А, селективных ингибиторов обратного захвата серотонина – СИОЗС, селективных ингибиторов обратного захвата серотонина и норадреналина – СИОЗСН, норадреналиновых и селективных серотониновых – НаССА, мелатонинэргических – МэА, мультимодальных – МмА) (табл.1).
Таблица 1. Известные в России антидепрессанты, их влияние на нейроны и «формула» механизма действия (1-4).
*- белый цвет – препарат не влияет на нейроны, темно-серый – выраженное повышение активности, светло-серый – умеренное повышение активности, **- в высоких дозах, ИОЗ – ингибиторы обратного захвата нейромедиаторов, СВРР – средства, влияющие на регуляторные рецепторы, ОИМАО-А – обратимые ингибиторы моноаминоксидазы типа «А».
Все эти препараты в разной степени способствуют активизации серотониновых (↑С или ↑с), норадреналиновых (↑Н или ↑н), дофаминовых (↑Д или ↑д) или мелатониновых (↑М или ↑м) нейронов, «тонус» которых снижается при депрессии. Но наиболее выраженно на жизнедеятельность нейронов влияют ↑СНд-антидепрессанты: амитриптилин и имипрамин (ТцА), а также венлафаксин (СИОЗСН) в высоких суточных дозах. Не случайно многие эксперты относят к их наиболее эффективным препаратам для лечения депрессий (5).
Конечно, выбор любого антидепрессанта должен быть связан не только с его лечебными свойствами (эффективность), но и с побочными эффектами (переносимость). Подавляющее большинство авторов согласны с тем, что переносимость лучше всего у СИОЗС и хуже у ТцА (6-9), а остальные препараты располагаются между ними (1). Такая оценка переносимости антидепрессантов является правильной, но носит обобщенный характер. Для ее уточнения следует обратиться к данным о механизмах формирования побочных эффектов.
Меньшая их часть обусловлена токсическим влиянием антидепрессантов на органы и ткани пациентов. Такие «токсические» побочные эффекты очень опасны (10). Например, на фоне приема некоторых ТцА (кломипрамин, имипрамин), а также МэА (агомелаптин) наблюдаются лекарственные гепатиты, которые приводят к смерти больных (10, 11). Серьезные токсические побочные эффекты имеются и у мапротилина, который вызывает агранулоцитоз и лейкопению (12). К счастью, токсические побочные эффекты наблюдаются очень редко и могут быть своевременно выявлены по результатам анализов.
Например, когда выяснилось, что агомелатин вызывает тяжелые и лекарственные гепатиты, в его инструкцию внесли подробные указания о мерах предосторожности (11). Они включают биохимический анализ крови, который назначают всем больным (без исключения) до назначения препарата, а также на фоне его приема. Аналогичный анализ требуется и пациентам, получающим кломипрамин и имипрамин (13,14). Однако при назначении этих антидепрессантов биохимический анализ требуется только больным с уже имеющимися заболеваниями печени. Наконец, регулярные общие анализы крови, направленные на выявление агранулоцитоза и лейкопении, необходимы и при лечении мапротилином (12).
Очевидно, что потребность в проведении дополнительных анализов может существенно затруднить использование антидепрессантов. К счастью, это требуется только при использовании перечисленных препаратов. При назначении остальных антидепрессантов не нужно прибегать к дополнительным обследованиям. Однако их переносимость может ухудшаться из-за неблагоприятного влияния препаратов на нейроны. В результате формируются «нейрональные» побочные эффекты, которые, впрочем, не угрожают напрямую жизни больных и легко диагностируются по их жалобам.
Некоторые из нейрональных побочных эффектов обусловлены воздействием антидепрессанта на гистаминовые и ацетилхолиновые нейроны, которые не снижают своей активности при формировании психических расстройств, являющихся показаниями для назначения антидепрессантов (2,15). Соответственно, такие фармакологические свойства можно обозначить как «внелечебные» (лишние, не имеющие отношения к лечебному процессу) побочные эффекты. Они лишь увеличивают количество нейрональных систем, которые страдают у больного. Чаще всего «внелечебные» побочные эффекты являются стойкими. Они могут наблюдаться в течение всего курса лечения, в частности тогда, когда антидепрессант блокирует возбуждающие рецепторы на гистаминовых и ацетилхолиновых нейронах (15).
Такой механизм действия, свойственный скорее нейролептикам, нежели антидепрессантам, приводит к резкому падению активности (торможению) указанных нервных клеток (↓Г и ↓А) (1,2). Причем нормальные гистаминовые и ацетилхолиновые нейроны не могут восстановить свои функции, поскольку для этого нет эффективных компенсаторных механизмов. Соответственно, у больных появляются стойкие психические и соматические симптомы, которые серьезно затрудняют лечение (табл. 2).
Таблица 2. Основные «внелечебные» побочные эффекты антидепрессантов, связанные с блокадой возбуждающих рецепторов на гистаминовых и ацетилхолиновых нейронов (1,2)
Характерны сонливость, утомляемость, ухудшение памяти и внимания. Появляются жалобы на сухость во рту, нарушения аккомодации и мочеиспускания, запоры, боли в глазах из-за роста внутриглазного давления, нарушения ритма сердца, повышение аппетита и прибавку веса.
Существует, однако, антидепрессант, у которого «внелечебные» побочные эффекты не носят стойкого характера. Этим препаратом является вортиоксетин. Он не тормозит гистаминовые и ацетилхолиновые нейроны (за счет блокады возбуждающих рецепторов), а повышает их «тонус» за счет влияния на регуляторные рецепторы (16). С одной стороны это обеспечивает вортиоксетину уникальный характер «внелечебных» побочных эффектов. В частности, при приеме этого антидепрессанта могут наблюдаться возбуждение, гнев, «необычные» сновидения, бессонница (табл. 3).
Таблица 3. «Внелечебные» побочные эффекты вортиоксетина (16,17).
Характерны кетоацидоз, соматические жалобы на головокружение, зуд (включая генерализованный), потливость, приливы, тошноту, диарею, рвоту. С другой стороны, указанные побочные явления принципиально обратимы, поскольку у нейронов есть специальные механизмы, которые направлены на борьбу с излишней активизацией. Для этого они могут, например, снизить чувствительность своих регуляторных рецепторов (механизм, известный как саморегуляция). Поэтому «внелечебные» побочные эффекты вортиоксетина часто редуцируются самостоятельно в первые недели две недели лечения (16).
Переходя теперь к остальным антидепрессантам, укажем, что у подавляющего большинства из них вообще нет «внелечебных» побочных эффектов, которые увеличивают число пораженных нейрональных систем (2). Многие препараты не влияют на гистаминовые и ацетилхолиновые нейроны. Более того, они повышают активность лишь тех нейронов (серотониновых, норадреналиновых и дофаминовых), чей «тонус» снижается при психических расстройствах, являющихся показаниями для назначения антидепрессантов. Однако даже эта особенность не может избавить антидепрессанты от «нейрональных» побочных эффектов. Последние будут возникать из-за того, что в пределах любой пораженной системы нейронов снижается активность только части нервных клеток, а функции другой части не нарушаются. Антидепрессанты как активизируют «пораженные» нейроны и создают терапевтические эффекты, так и повышают «тонус» нормально функционирующих нервных клеток и вызывают побочные эффекты.
При этом переносимость антидепрессантов парадоксальным образом оказывается «заложником» их терапевтических свойств. Чем эффективнее препарат активизирует пораженные нейроны, тем больше он воздействует на аналогичные нервные клетки, которые все еще функционируют на должном уровне. Поэтому рассматриваемые побочные эффекты целесообразно обозначить как «паралечебные». Они проявляются беспокойством, неусидчивостью, бессонницей и тревогой (табл. 4).
Таблица 4. Основные «паралечебные» побочные эффекты антидепрессантов (15)
Представленные данные по токсическим и нейрональным побочным эффектам могут быть использованы для распределения антидепрессантов по семи категориям переносимости, где последняя, седьмая, является худшей, а первая – лучшей (табл. 5).
Таблица 5. Категории переносимости антидепрессантов с учетом токсических и нейрональных побочных эффектов.
Так, антидепрессанты из самой низкой VII категории (кломипрамин, имипрамин, мапротилин, агомелатин) обладают токсическими побочными эффектами, которые непосредственно угрожают жизни пациентов. Более того, при их назначении требуется дополнительное обследование больных. Проблемы с переносимостью остальных антидепрессантов обусловлены уже нейрональными побочными эффектами. Все они не носят фатального характера, и для их выявления обычно не требуется дополнительного обследования.
Нейрональные побочные эффекты делятся на «внелечебные» и «паралечебные». Первые, как о том уже указывалось выше, связаны с «дополнительным» нарушением функций гистаминовых и ацетилхолиновых нейронов, которые не снижают своей активности при психических расстройствах, являющихся показаниями для назначения антидепрессантов. Соответственно, «внелечебные» побочные эффекты, расширяющие круг пораженных нейрональных систем, определяют принадлежность препаратов к более низким категориям переносимости (VI, V и IV). В частности, амитриптилин способствует стойкому снижению активности гистаминовых и ацетилхолиновых нейронов и поэтому отнесен к VI категории переносимости. «Внелечебные» побочные эффекты у антидепрессантов, отнесенных к V категории, носят более ограниченный характер. Ведь пипофезин, тразодон, миансерин и миртазапин способствуют стойкому снижению активности только гистаминовых нейронов. К следующей – более высокой IV категории переносимости – отнесен вортиоксетин. Этот антидепрессант обладает способностью повышать активность гистаминовых и ацетилхолиновых нейронов. Однако связанные с этим побочные эффекты зачастую обратимы.
К наиболее высоким I – III категориям переносимости отнесены антидепрессанты, которые воздействуют только на серотониновые, норадреналиновые и дофаминовые нейроны, которые страдают при психических расстройствах, являющихся показаниями для назначения препаратов. Для этих препаратов характерны «паралечебные» побочные эффекты, которые не увеличивают число пораженных нейрональных систем (табл. 5). Они возникают вследствие активизации части серотониновых, норадреналиновых и дофаминовых нейронов, которые все еще сохраняют нормальный «тонус» (2). При этом выраженность «паралечебных» побочных эффектов зависит, в первую очередь, от способности антидепрессанта воздействовать на серотониновые и норадреналиновые нервные клетки, поскольку на дофаминовые все они действуют слабо (табл. 1).
Соответственно, к III категории переносимости отнесены антидепрессанты, которые одновременно эффективно активизируют серотониновые и норадреналиновые нейроны. Этими препаратами являются венлафаксин и дулоксетин (табл. 1 и 5). Первый их них в зависимости от дозы является ↑СН- или ↑СНд-антидепрессантом. Что же касается дулоксетина, то он обладает свойствами ↑СН-препарата. Во II категорию включены антидепрессанты, которые способствуют выраженной активизации только серотониновых или только норадреналиновых нейронов (табл. 1 и 5). К ним относятся все ↑С-антидепрессанты (сертралин, пароксетин, циталопрам, эсциталопрам, флуоксетин, флувоксамин), а также ↑сНд-антидепрессант – милнаципран. Наконец, самой высокой I категорией переносимости обладают препараты, которые не способны на сильную активизацию серотониновых, норадреналиновых нейронов (табл. 1 и 5). Это два ↑снд-антидепрессанта – пирлиндол и моклобемид.
В заключении следует указать, что представленная классификация антидепрессантов по переносимости не претендует на всеобъемлющий характер. Однако она дает ясные критерии для оценки основных побочных эффектов, которые позволяют сопоставлять различные препараты между собой. Представляется, что это особенно значимо в ситуации, когда отсутствуют какие-либо четкие рекомендации по учету побочных эффектов при назначении антидепрессантов. Например, в настоящее время в различных публикациях и инструкциях используется обобщенная формула. Антидепрессант предлагается использовать «только после тщательной оценки соотношения ожидаемой пользы к возможному риску у пациентов» (11). Но результаты такой «тщательной оценки», как правило, оказываются в пользу назначения препарата.
В частности, об агомелатине пишут, что если соблюдены все требования инструкции по назначению антидепрессанта, то риск развития лекарственного гепатита становится минимальным (19). При этом уникальный механизм действия, приписываемый агомелатину, позволяет заявить, что пользы от назначения антидепрессанта значительно больше, нежели определенных неудобств, которые связаны с его гепатотоксичностью (19). Между тем, вся уникальность механизма действия агомелатина сводится к возможности влияния на нейроны супрахиазмального ядра, нейромедиатором которых является мелатонин. А данный эффект вовсе не требуется для лечения депрессий, поскольку компенсировать дефицит мелатониновой активности может любой антидепрессант, активизирующий серотониновые и норадреналиновые нейроны (20).
Представленные рекомендации по «тщательной оценке» вовсе не являются единственным примером легковесных суждений относительно переносимости антидепрессантов. Некоторые авторы считают, что побочные эффекты слабо связаны с механизмом действия препаратов. Утверждается, что побочные эффекты носят неспецифический, вероятностный характер и потому почти непредсказуемы (18). Другие авторы хотя бы ищут причины формирования побочных эффектов для того, чтобы учесть их при назначении антидепрессантов. К сожалению, эти причины они находят не в механизмах действия препаратов, а в особенностях депрессий, общественном мнении или психологии больного.
Так, сообщается, что даже при применении любых «наиболее легко переносимых препаратов у 80% больных с легкими и умеренно выраженными депрессиями» (21), отмечаются разнородные неблагоприятные явления. Чаще всего они встречаются при дистимии, первых депрессивных состояниях, с тревогой и соматическими симптомами (21, 22), у лиц старше 45 лет, с высоким дефицитом массы тела (22), отрицательными реакции на плацебо в анамнезе (23). Сообщается, что плохая переносимость антидепрессантов связана с высокими требованиями пациентов к качеству жизни (24), их беспокойством по поводу социальной дезадаптации (25). Свой вклад в проблему вносит также изначально негативное отношение к психиатрии со стороны общественного мнения, малая информированность больного о собственной болезни и рекомендуемой врачом терапии, неудовлетворительным опытом предыдущего лечения и т.д. (22, 26).
Умозрительность таких построений очевидна. Для их опровержения достаточно сказать, что побочные эффекты лекарств, согласно определению ВОЗ, вызываются их фармакологическими свойствами (37). Трудно представить, чтобы торможение гистаминовых и ацетилхолиновых нейронов возникало из-за высоких требований пациента к качеству жизни, чрезмерная активизация серотониновых, норадреналиновых и дофаминовых нейронов из-за негативного отношения к психиатрии со стороны общественного мнения, а лекарственный гепатит из-за беспокойства по поводу социальной дезадаптации.
Таким образом, представленная классификация антидепрессантов по категориям переносимости позволяет вернуть изучение побочных эффектов в русло биологической психиатрии. К тому же, данную классификацию легко использовать в практической медицине. В частности, чем ниже категория переносимости антидепрессанта, тем больше потребность в специальном обосновании для его назначения (эффективность, положительный опыт лечения в прошлом, желание больного и т.д.). В свою очередь, появление такого развернутого обоснования в истории болезни позволит избежать многих проблем (психологических, социальных и иных), возникающих в процессе лечения между врачом его пациентом.
С помощью представленной классификации легко решить вопрос о выборе наиболее эффективного и переносимого антидепрессанта. Для этого требуется лишь сопоставить категории переносимости у наиболее эффективных препаратов: амитриптилина (ТцА), имипрамина (ТцА) и венлафаксина (СИОЗСН) (5). Первый из них (амитриптилин) относится к VI категории переносимости (табл. 5). Побочные эффекты второго антидепрессанта (имипрамин) еще серьезнее. Этот препарат относится к VII категории переносимости. Что же касается венлафаксина, то побочные эффекты у этого антидепрессанта гораздо слабее, и этот препарат относится к III категории переносимости. Таким образом, венлафаксин при его использовании в высоких дозах является самым эффективным и переносимым препаратом при лечении депрессий.
Венлафаксин хорошо известен в нашей стране под торговым наименованием Велаксин (Эгис). Этот препарат изучен в ведущих научных организациях, осуществляющих передовые исследования в области психиатрии. Среди них Федеральные государственные бюджетные учреждения «Государственный научный центр социальной и судебной психиатрии имени им В.П. Сербского» и «Московский НИИ психиатрии» Минздрава Росиии, Санкт-Петербургский научно-исследовательский институт им. В.М. Бехтерева (28,29). Хорошо известны и капсулы пролонгированного действия (Велаксин ретард) (30), при применении которых отмечается значительное снижение частоты такого побочного эффекта препарата, как тошнота (31). Кроме того, изучение Велаксина с успехом проводилось не только в психиатрии, но и неврологии (32).
Видео М.Ю Дробижева на ту же тему можно посмотреть по ссылке: https://www.youtube.com/watch?v=SwtO_bC_838&t=11s
Список литературы
М.Ю. Дробижев, доктор медицинских наук, Руководитель образовательного отдела Учебного центра Ассоциации медицинских и фармацевтических вузов России. Контактная информация – dmyu2001@mail.ru
Е.Ю. Антохин, кандидат медицинских наук, доцент, заведующий кафедрой клинической психологии и психотерапии ФГБОУ ВО «Оренбургский государственный медицинский университет» Минздрава России.
Р.И. Палаева – ассистент кафедры клинической психологии и психотерапии ФГБОУ ВО «Оренбургский государственный медицинский университет» Минздрава России.
С. В. Кикта, кандидат медицинских наук, зав. отделением ФГБУ «Поликлиника №3» Управления делами Президента РФ, Москва
1 Вероятно, существуют и побочные эффекты, обусловленные излишней активизацией мелатониновых нервных клеток. Однако они пока не описаны даже в инструкции агомелатина – мелатонинэргического препарата, который оказывает на них прямое воздействие (11).
2 Теоретически, «паралечебные» побочные эффекты могут наблюдаться даже на фоне «внелечебных». Ведь любые антидепрессанты в разной степени активизируют серотониновые, норадреналиновые или дофаминовые нейроны. Однако у препаратов доминируют «внелечебные» побочные эффекты, хотя бы потому, что чаще всего носят стойкий характер. В то же время «паралечебные» побочные эффекты всегда обратимы. К тому же далеко не все антидепрессанты, обладающие, «внелечебными» побочными эффектами способны на серьезную активизацию серотониновых, норадреналиновых и дофаминовых нейронов.

.gif)
.gif)
.gif)
.gif)
.gif)