Мышечный слой интактен что означает
Основы венозной системы нижних конечностей
Своеобразное строение венозных сосудов и состав их стенок определяет их емкостные свойства. Вены отличаются от артерий тем, что являются трубками с тонкими стенками и просветами сравнительно большого диаметра. Так же как и стенки артерий, в состав венозных стенок входят гладкомышечные элементы, эластические и коллагеновые волокна, среди которых последних гораздо больше.
В венозной стенке выделяются структуры двух категорий:
— опорные структуры, к которым относятся ретикулиновые и коллагеновые волокна;
— упруго-сократительные структуры, к которым относятся эластические волокна и гладкомышечные клетки.
Коллагеновые волокна в обычных условиях поддерживают нормальную конфигурацию сосуда, а если на сосуд оказывается какое-либо экстремальное воздействие, то эти волокна сохраняют ее. В формировании тонуса внутри сосуда коллагеновые сосуды участия не принимают, а также они не оказывают влияние на сосудодвигательные реакции, так как за их регуляцию отвечают гладкомышечные волокна.
Вены состоят из трех слоев:
— адвентиция – наружный слой;
— медиу – средний слой;
— интиму – внутренний слой.
Между этими слоями находится эластические мембраны:
— внутренняя, которая выражена в большей степени;
— наружная, которая весьма слабо различается.
Среднюю оболочку вен в основном составляют гладкомышечные клетки, которые расположены по периметру сосуда в виде спирали. Развитие мышечного слоя зависит от ширины диаметра венозного сосуда. Чем больше диаметр вены, тем мышечный слой развит больше. Число гладкомышечных элементов становится больше сверху вниз. Мышечные клетки, составляющие среднюю оболочку, находятся в сети коллагеновых волокон, которые сильно извиты и в продольном, и в поперечном направлении. Эти волокна распрямляются только тогда, когда происходит сильное растяжение венозной стенки.
Поверхностные вены, которые располагаются в подкожной клетчатке, имеют весьма развитый гладкомышечный строй. Это объясняет тот факт, что поверхностные вены в отличие от расположенных на том же уровне имеющих такой же диаметр глубоких вен, отлично противостоят и гидростатическому, и гидродинамическому давлению за счет того, что их стенки имеют эластическое сопротивление. Венозная стенка имеет толщину, которая обратно пропорциональна величине окружающего сосуд мышечного слоя.
Наружный слой вены, или адвентицию, составляет плотная сеть коллагеновых волок, которые создают своеобразный каркас, а также небольшое количество мышечных клеток, которые имеют продольное расположение. Этот мышечный слой с возрастом развивается, наиболее отчетливо его можно наблюдать в венозных сосудах нижних конечностей. Роль дополнительной опоры играют венозные стволы более или менее крупного размера, окруженные плотной фасцией.
Строение стенки вены определяется ее механическими свойствами: в радиальном направлении венозная стенка имеют высокую степень растяжимости, а в продольном направлении – малую. Степень растяжимости сосуда зависит от двух элементов венозной стенки – гладкомышечных и коллагеновых волокон. Жесткость венозных стенок во время их сильной дилатации зависит от коллагеновых волокон, которые не дают венам очень сильно растягиваться исключительно в условиях значительного повышения давления внутри сосуда. Если же изменения внутрисосудистого давления имеют физиологических характер, то за упругость венозных стенок отвечают гладкомышечные элементы.
Венозные клапаны
Венозные сосуды имеют важную особенность – в них есть клапаны, с помощью которых возможен центростремительный ток крови в одном направлении. Количество клапанов, а также их расположение служит для обеспечения кровотока к сердцу. На нижней конечности самое большее число клапанов расположено в дистальных отделах, а именно немного ниже того места, где находится устье крупного притока. В каждой из магистралей поверхностных вен клапаны расположены на расстоянии 8-10 см друг от друга. У коммуникантных вен, за исключением бесклапанных перфорантов стопы, также есть клапанный аппарат. Часто перфоранты могут впадать в глубокие вены несколькими стволами, которые по внешнему виду напоминают канделябры, что препятствует ретроградному кровотока вместе с клапанами.
Клапаны вен обычно имеют двустворчатое строение, и на то, как они распределяются в том или ином сегменте сосуда, зависит от степени функциональной нагрузки.
Каркасом для основы створок венозных клапанов, которые состоят из соединительной ткани, служит отрог внутренней эластической мембраны. У створки клапаны есть две покрытые эндотелием поверхности: одна – со стороны синуса, вторая – со стороны просвета. Гладкомышечные волокна, расположенные у основания створок, направленные вдоль оси вены, в результате изменения своего направления на поперечное создают циркулярный сфинктер, пролабирующий в синус клапана в виде своеобразного ободка крепления. Строму клапана формируют гладкомышечные волокна, которые пучками в виде веера идут на створки клапана. С помощью электронного микроскопа можно обнаружить имеющие продолговатую форму утолщения – узелки, которые расположены на свободном крае створок клапанов крупных вен. По мнению ученых, это своеобразные рецепторы, которые фиксируют тот момент, когда створки смыкаются. Створки интактного клапана имеют длину, превышающую диаметр сосуда, поэтому если они закрыты, то на них наблюдаются продольные складки. Избыточной длиной створок клапана, в частности, обусловлен физиологический пролапс.
Венозный клапан – это структура, имеющую достаточную прочность, которая может выдерживать давление до 300 мм рт. ст. Однако в синусы клапанов крупных вен через впадающие в них тонкие притоки, не имеющие клапанов, сбрасывается часть крови, из-за чего давление над створками клапана снижается. Помимо этого, ретроградная волна крови рассеивается об ободок крепления, что приводит к снижению ее кинетической энергии.
С помощью при жизни проведенной фиброфлебоскопии можно представить себе, как работает венозный клапан. После попадания ретроградной волны крови в синусы клапана, его створки приходят в движение и смыкаются. Узелки передают сигнал о том, что они соприкоснулись, мышечному сфинктеру. Сфинктер начинает расширятся до тех пор, пока не достигнет того диаметра, при котором створки клапана вновь раскроются и надежно перекроют ретроградной волны крови путь. Когда в синусе давление становится выше порогового уровня, то происходит раскрытие устья дренирующих вен, что приводит к снижению венозной гипертензии до безопасного уровня.
Анатомическое строение венозного бассейна нижних конечностей
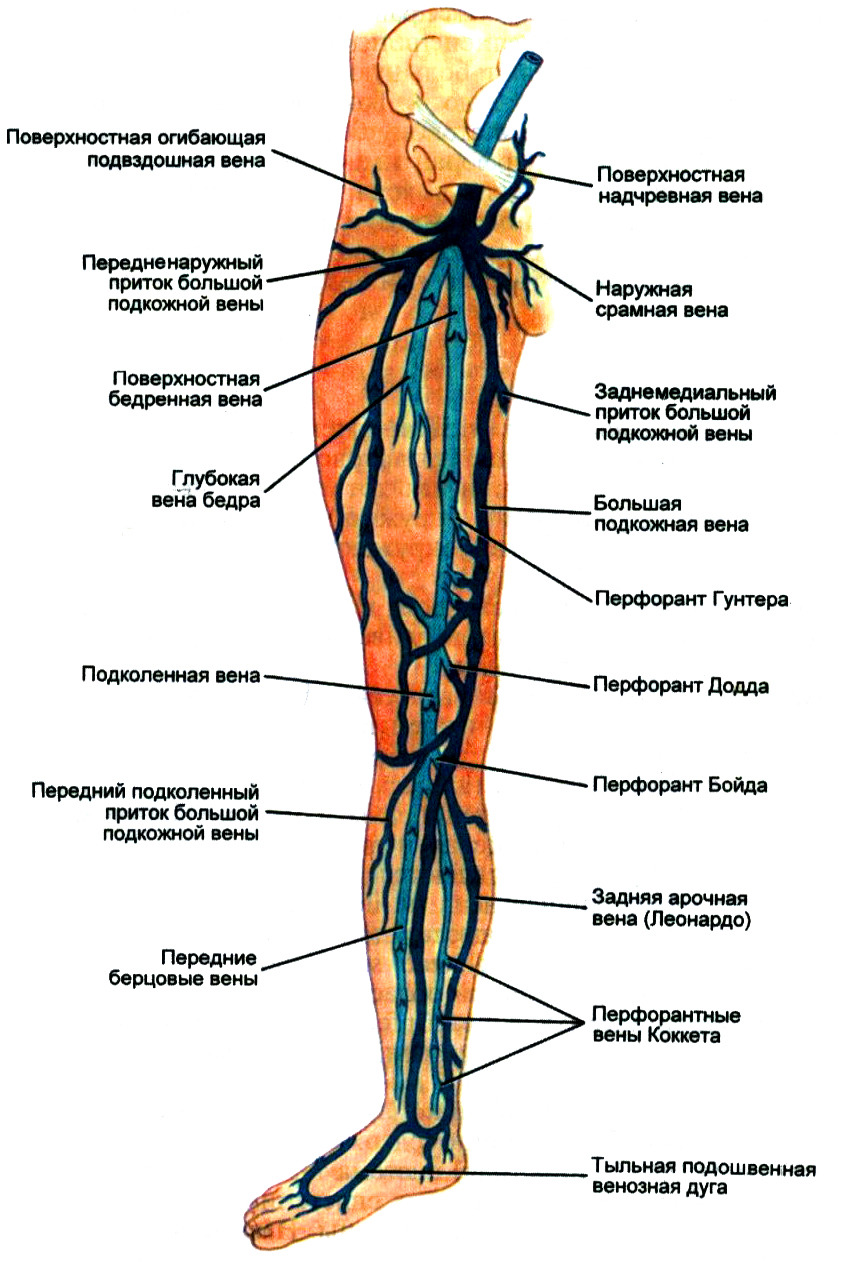
Вены нижних конечностей делятся не поверхностные и глубокие.
К поверхностным венам относятся кожные вены стопы, расположенные на подошвенной и тыльной поверхности, большие, малые подкожные вены и их многочисленные притоки.
Подкожными венами в области стопы формируются две сети: кожная венозная подошвенная сеть и кожная венозная сеть тыла стопы. Общими тыльными пальцевыми венами, которые входят в кожную венозную сеть тыла стопы, в результате того, что они анастомозируют между собой, образуется кожная тыльная дуга стопы. Концы дуги имеют продолжение в проксимальном направлении и образуют два ствола, идущих в продольном направлении – медиальную краевую вену (v. marginalis medialis) и краевую латеральную вену (v. marginalis lateralis). На голени эти вены имеют продолжение в виде большой и малой подкожной вены соотвественно. На подошвенной поверхности стопы выделяется подкожная венозная подошвенная дуга, которая широко анастомозируя с краевыми венами, отправляет межголовчатые вены в каждый из межпальцевых промежутков. Межголовчатые вены, в свою очередь, анастомозируют с теми венами, которые образуют тыльную дугу.
Продолжением медиальной краевой вены (v. marginalis medialis) является большая подкожная вена нижней конечности (v. saphena magna), которая по переднему краю внутренней стороны лодыжки переходит на голень, а затем, проходя по медиальному краю большеберцовой кости, огибает медиальный мыщелок, выходит на внутреннюю поверхность бедра с задней стороны коленного сустава. В области голени БПВ находится около подкожного нерва, с помощью которого происходит иннервация кожного покрова на стопе и голени. Эта особенность анатомического строения должна учитываться при флебэктомии, так как из-за повреждения подкожного нерва могут появиться долговременные, а иногда и пожизненные нарушения иннервации кожного покрова в области голени, а также привести к парестезиям и каузалгиям.
В области бедра большая подкожная вена может иметь от одного до трех стволов. В области имеющей овальную форму ямки (hiatus saphenus) находится устье БПВ (сафенофеморальный анастомоз). В этом месте ее терминальный отдел делает перегиб через сероповидный отросток широкой фасции бедра и, в результате прободения решётчатой пластинки (lamina cribrosa), впадает в бедренную вену. Местоположение сафенофеморального анастомоза может располагаться на 2-6 м ниже того места, где находится пупартовая связка.
К большой подкожной вене по всей ее длине присоединяется много притоков, которые несут кровь не только с области нижних конечностей, из наружных половых органов, с области передней брюшной стенки, а также с кожи и подкожной клетчатки, находящихся в ягодичной области. В нормальном состоянии большая подкожная вена имеет ширину просвета 0,3 – 0,5 см и имеет от пяти до десяти пар клапанов.
Постоянные венозные стволы, которые впадают в терминальный отдел большой подкожной вены:
Малая подкожная вена, проходя по месту соединения средней и верхней третей голени, проникает в зону глубокой фасции, располагаясь между ее листками. Доходя до подколенной ямки, МПВ проходит сквозь глубокий листок фасции и чаще всего соединяется с подколенной веной. Однако в некоторых случаях малая подкожная вена проходит над подколенной ямкой и соединяется либо с бедренной веной, либо с притоками глубокой вены бедра. В редких случаях МПВ впадает в один из притоков большой подкожной вены. В зоне верхней трети голени между малой подкожной веной и системой большой подкожной вены образуется множество анастомозов.
Самым крупным постоянным приустьевым притоком малой подкожной вены, имеющим эпифасциальное расположение, является бедренно-подколенная вена (v. Femoropoplitea), или вена Джиакомини. Эта вена связывает МПВ большой подкожной веной, расположенной на бедре. Если по вене Джиакомини из бассейна БПВ возникает рефлюкс, то из-за этого может начаться варикозное расширение малой подкожной вены. Однако может сработать и обратный механизм. Если возникает клапанная недостаточность МПВ, то варикозную трансформацию можно наблюдать на бедренно-подколенной вене. Кроме того, в данный процесс будет вовлечена и большая подкожная вена. Это нужно учитывать во время хирургического вмешательства, так как в случае сохранения бедренно-подколенная вена может быть причиной возврата варикоза у пациента.
Глубокая венозная система
К глубоким венам относятся вены, расположенные с тыльной стороны стопы и подошвы, на голени, а также в зоне колена и бедра.
На голени венозная система состоит из трех пар глубоких вен – передней и задней большеберцовой веной и малоберцовой веной. Основная нагрузка по оттоку крови с периферии возложена на задние большеберцовые вены, в которые, в свою очередь, дренируются малоберцовые вены.
Система суральных вен состоит из парных икроножных мышц (vv. Gastrocnemius), дренирующих в подколенную вену синус икроножной мышцы, и непарной камбаловидной мышцы (v. Soleus), отвечающей за дренаж в подколенную вену синуса камбаловидной мышцы.
На уровне суставной щели в подколенную вену общим устьем или раздельно, выходя из головок икроножной мышцы (m. Gastrocnemius), впадает медиальная и латеральная икроножная вена.
Рядом с камбаловидной мышцей (v. Soleus) постоянно проходит одноименная артерия, которая в свою очередь является ветвью подколенной артерией (а. poplitea). Камбаловидная вена самостоятельно впадает в подколенную вену или же проксимальнее того места, где находится устье икроножных вен, или же впадает в него.
Бедренная вена (v. femoralis) большинством специалистов подразделяется на две части: поверхностная бедренная вена (v. femoralis superfacialis) расположена дальше от места впадения глубокой вены бедра, общая бедренная вена (v. femoralis communis) расположена ближе к тому месту, где в нее впадает глубокая вена бедра. Данное подразделение важно как в анатомическом отношении, так и в функциональном.
Кроме большое подкожной вены, в общую бедренную вену также впадает медиальная латеральная вены, которые идут вокруг бедра. Медиальная вена находится проксимальнее, чем латеральная. Место ее впадения может располагаться либо на одном уровне с устьем большой подкожной вены, либо немного выше его.
Перфорантные вены

Прямые и непрямые перфорантные вены
Прямые перфорантные вены – это сосуды, с помощью которых глубокая и поверхнастная вены соединяются между собой. В качестве самого типичного примера прямой перфорантной вены можно привести сафеноподколенное соустье. Количество прямых перфорантных вен в организме человека не так много. Они являются более крупными и в большинстве случаев располагаются в дистальных областях конечностей. Например, на голени в сухожильной части расположены перфорантные вены Коккета.
Основной задачей непрямых перфорантных вен является соединение подкожной вены с мышечной, которая имеет прямое или опосредованное сообщение с глубокой веной. Количество непрямых перфорантных вен достаточно большое. Это чаще всего очень мелкие вены, которые в большей части находятся там, где расположены мышечные массивы.
Синдром Х в кардиологии («микроваскулярная стенокардия»)
Наличие типичной стенокардии при неизмененных коронарных артериях впервые описал Н. Kemp в 1973 году [1]. Этот синдром получил название «синдром Х (икс)».
Приблизительно у 10–20% больных, которым проводится диагностическая коронарография в связи с острым или хроническим кардиальным ишемическим синдромом, коронарные артерии оказываются интактными. Если даже предположить, что у части из них симптомы ишемии могут быть обусловлены другими кардиальными и некардиальными причинами, то, по крайней мере, у одного из десяти больных с наличием типичной стенокардии отсутствуют гемодинамически значимые стенозы коронарных артерий. Наличие типичной стенокардии при неизмененных коронарных артериях впервые описал Н. Kemp в 1973 году [1]. Этот синдром получил название «синдром Х (икс)».
Кардиальный синдром Х – это патологическое состояние, характеризующееся наличием признаков ишемии миокарда на фоне отсутствия атеросклероза коронарных артерий и спазма эпикардиальных венечных артерий на коронарографии (признаки ишемии миокарда: типичных приступов стенокардии и депрессии сегмента ST ≥ 1,5 мм (0,15 мВ) продолжительностью более 1 минуты, установленной при 48-часовом мониторировании ЭКГ).
Таким образом, кардиальный синдром Х диагностируется у больных:
• с типичными загрудинными болями;
• с положительными нагрузочными тестами;
• с ангиографически нормальными эпикардиальными коронарными артериями и отсутствием клинических или ангиографических доказательств наличия спазма коронарных артерий;
• с отсутствием системной артериальной гипертонии с гипертрофией левого желудочка и без нее, а также с отсутствием нарушений систолической функции левого желудочка в покое.
В редких случаях у больных с синдромом Х возникает блокада левой ножки пучка Гиса с последующим развитием дилатационной кардиомиопатии. Следует обратить внимание на то, что при отсутствии изменений в коронарных артериях при ангиографии часто имеется окклюзионная патология дистальных сосудов (микроваскулярная стенокардия).
Некоторые авторы используют термин «микроваскулярная стенокардия», подразумевая под этим наличие у больных с типичной стенокардией нормальной коронарограммы и сниженного коронарного резерва.
Синдром Х обычно относят к одной из клинических форм ИБС, поскольку понятие «ишемия миокарда»’ включает все случаи дисбаланса поступления кислорода и потребности миокарда в нем, независимо от причин, его вызывающих.
Следует отметить, что возможности метода ангиографии при оценке состояния коронарного русла, в частности, микрососудистого, ограничены. Поэтому понятие «ангиографически неизмененные коронарные артерии» весьма условно и свидетельствует только об отсутствии суживающих просвет сосудов атеросклеротических бляшек в эпикардиальных коронарных артериях. Анатомические особенности мелких коронарных артерий остаются «ангиографически невидимыми».
Причины кардиального синдрома Х:
Этиология кардиального синдрома Х остается до конца не выясненной и установлены лишь некоторые патофизиологические механизмы, приводящие к развитию типичных клинико–инструментальных проявлений заболевания:
• увеличенная симпатическая активация;
• дисфункция эндотелия;
• структурные изменения на уровне микроциркуляции;
• изменения метаболизма (гиперкалиемия, гиперинсулинемия, «окислительный стресс» и др.);
• повышенная чувствительность к внутрисердечной боли;
• хроническое воспаление;
• повышенная жесткость артерий и др.
Существует ряд гипотез, которые определяют патогенез синдрома Х. Согласно первой из них болезнь обусловлена ишемией миокарда вследствие функциональных или анатомических нарушений микроциркуляции в интрамускулярных (интрамуральных) преартериолах и артериолах, т.е. в сосудах, которые не могут быть визуализированы при коронароангиографии. Вторая гипотеза предполагает наличие метаболических нарушений, приводящих к нарушению синтеза энергетических субстратов в сердечной мышце. Третья гипотеза предполагает, что синдром Х возникает при повышении чувствительности к болевым стимулам (снижение болевого порога на уровне таламуса) от различных органов, включая сердце.
Несмотря на интенсивные исследования в последние 35 лет относительно патогенеза коронарного синдрома Х, многие важные вопросы остаются без ответа.
Среди больных с кардиальным синдромом Х преобладают лица среднего возраста, в основном женщины. Менее чем у 50% больных с кардиальным синдромом Х наблюдается типичная стенокардия напряжения, у большей части – болевой синдром в груди атипичен.Симптомы кардиального синдрома Х:
В качестве основной жалобы фигурируют эпизоды болей за грудиной стенокардитического характера, возникающих во время физической нагрузки или провоцирующихся холодом, эмоциональным напряжением; с типичной иррадиацией в ряде случаев боли более продолжительные, чем при ИБС, и не всегда купируются приемом нитроглицерина (у большинства больных препарат ухудшает состояние).
Сопутствующие кардиальному синдрому Х симптомы напоминают вегето-сосудистую дистонию. Нередко кардиальный синдром Х обнаруживают у людей мнительных, с высоким уровнем тревожности, на фоне депрессивных и фобических расстройств. Подозрение на эти состояния требует консультации у психиатра.
В качестве диагностических критериев кардиального синдрома Х выделяются:
• типичная боль в грудной клетке и значительная депрессия сегмента ST при физической нагрузке (в том числе на тредмиле и велоэргометре);
• преходящая ишемическая депрессия сегмента ST ≥ 1,5 мм (0,15 мВ) продолжительностью более 1 минуты при 48-часовом мониторировании ЭКГ;
положительная дипиридамоловая проба;
• положительная эргометриновая (эрготавиновая) проба, снижение сердечного выброса на ее фоне;
• отсутствие атеросклероза коронарных артерий при коронароангиографии;
• повышенное содержание лактата в период ишемии при анализе крови из зоны коронарного синуса;
• ишемические нарушения при нагрузочной сцинтиграфии миокарда с 201 Tl.
Синдром Х напоминает стабильную стенокардию. Однако клинические проявления у больных с синдромом Х весьма вариабельные, а помимо стенокардии напряжения могут наблюдаться и приступы стенокардии покоя.
При диагностике кардиального синдрома Х также должны быть исключены:
• пациенты со спазмом коронарных артерий (вазоспастическая стенокардия),
• пациенты, у которых объективными методами документированы внесердечные причины болей в грудной клетке, например:
— мышечно-костные причины (остеохондроз шейного отдела позвоночника и др.);
— нервно-психические причины (тревожно–депрессивный синдром и др.);
— желудочно-кишечные причины (спазм пищевода, желудочно–пищеводный рефлюкс, язва желудка или двенадцатиперстной кишки, холецистит, панкреатит и др.);
— легочные причины (пневмония, туберкулезный процесс в легких, плевральные наложения и др.);
— латентно протекающие инфекции (сифилис) и ревматологические заболевания.
Лечение кардиального синдрома Х:
Лечение группы больных с синдромом Х остается до конца не разработанным. Выбор лечения часто затруднен как для лечащих врачей, так и для самих больных. Успешность лечения обычно зависит от идентификации патологического механизма заболевания и в конечном итоге определяется участием самого пациента. Часто необходим комплексный подход к лечению больных с кардиальным синдромом Х.
Существуют различные подходы к медикаментозному лечению: антиангинальные препараты, ингибиторы АПФ, антагонисты рецепторов ангиотензина II, статины, психотропные препараты и др.
Антиангинальные препараты, такие как антагонисты кальция (нифедипин, дилтиазем, верапамил, амлодипин) и β–адренергические блокаторы (атенолол, метопролол, бисопролол, небиволол и др.) необходимы больным с документированной ишемией миокарда или с нарушенной миокардиальной перфузией. Сублингвальные нитраты эффективны у 50% больных с кардиальным синдромом Х. Имеются доказательства в отношении эффективности никорандила, обладающего брадикардическим эффектом, α1–адреноблокатора празозина, L–аргинина, ингибиторов АПФ (периндоприла и эналаприла), цитопротекторов (триметазидина).
Общие советы по изменению качества жизни и лечению факторов риска, особенно проведение агрессивной липидснижающей терапии статинами (снижение общего холестерина до 4,5 ммоль/л, холестерина ЛПНП менее 2,5 ммоль/л), должны рассматриваться в качестве жизненно необходимых компонентов при любой выбранной стратегии лечения.
Физические тренировки. При кардиальном синдроме Х снижается толерантность к физическим нагрузкам, наблюдается физическая детренированность и неспособность выполнять нагрузку из–за низкого болевого порога. Физические тренировки увеличивают болевой порог, нормализуют эндотелиальную функцию и «отодвигают» появление боли при нагрузке у этой категории больных.
Прогноз.
Прогноз больных с кардиальным синдромом «Х», как правило, благоприятный. Осложнения, характерные для больных ИБС со стенозирующим атеросклерозом коронарных артерий (в частности, инфаркт миокарда), встречаются крайне редко. Выживаемость при длительном наблюдении составляет 95–97%, однако у большей части больных повторные приступы стенокардии на протяжении многих лет отрицательно влияют на качество жизни. Если кардиальный синдром Х не связан с увеличением смертности или с увеличением риска кардиоваскулярных «событий», то он часто серьезно ухудшает качество жизни пациентов и представляет существенную нагрузку для системы здравоохранения. Необходимо подчеркнуть, что прогноз благоприятный при отсутствии эндотелиальной дисфункции. В этих случаях пациента следует информировать о доброкачественном течении заболевания. При исключении больных с блокадой левой ножки пучка Гиса и пациентов с вторичной микроваскулярной стенокардией вследствие серьезных системных заболеваний, таких как амилоидоз или миеломная болезнь, прогноз больных с кардиальным синдромом Х благоприятный как в отношении выживаемости, так и сохранения функции левого желудочка, однако у некоторых пациентов клинические проявления заболевания сохраняются достаточно долго.
Заболевания слюнных желез и их протоков причины, признаки, лечение
В обязанности стоматолога-хирурга, помимо удаления зубов, входит контроль состояния слюнных желез и удаление кистозных образований. В клинику часто обращаются пациенты с жалобами на вязкость слюны или ее отсутствие, появление в ротовой полости гноя, болезненности при жевании, ощущение инородного тела. Все это может говорить о наличии кисты в слюнной железе. Это заболевание сопровождается специфическими симптомами и требует хирургического лечения.
Причины новообразований слюнных желез
Новообразование в слюнной железе может возникнуть независимо от возраста и стати. Одинаково часто с этой проблемой сталкиваются маленькие дети и пожилые люди. Основными факторами риска выступает изменение консистенции слюны на фоне системных заболеваний организма. Также спровоцировать кистозный процесс могут неправильное питание, несоблюдение правил гигиены.
Другие частые причины образования кист:
Есть несколько видов заболеваний протоков слюнных желез.
Когда нужно обратиться к стоматологу-хирургу?
Как только начинается образование кисты, нельзя вывить определенных симптомов. Но уже тогда начинает нарушаться отток слюны. Сухость слизистой оболочки, тяжесть глотания может указывать на начало патологического процесса. Со временем киста увеличивается и уже создает значительный дискомфорт.
Как выявить кисту в слюнной железе?
После того как пациент обращается со специфическими симптомами, необходимо подтвердить диагноз для начала лечения. С этой целью проводится пальпация, осмотр стоматологом ротовой полости, лабораторное исследование ротовой жидкости и слюны из железы. Как дополнительные мероприятия используют ультразвуковую диагностику и КТ.
Как удаляются кисты протоков слюнных желез?
Некоторые специалисты до сих пор стараются победить новообразования проток слюнных желез консервативными методами. Но такой подход все чаще оказывается бесполезным и только усугубляет течение заболевания. Лучше сразу проводить хирургическое удаление с последующей восстановительной терапией.
Во время проведения операции удаляется киста и часть здоровой ткани, дабы предупредить риск развития повторного заболевания. Операция проводится под местным обезболиванием непосредственно в хирургическом кабинете стоматологической клиники. Удаление кисты оперативным методом гарантирует полное выздоровление.
Для скорейшего восстановления необходимо некоторое время после операции воздержаться от соленой, острой, кислой, твердой пищи. Во-первых, это будет очень болезненно, а во-вторых, может спровоцировать осложнение в виде воспаления с припухлостью.
Если есть подозрение на новообразование в районе челюсти, нужно немедленно обращаться в клинику. Повышен риск непроизвольного разрыва капсулы, что грозит распространением инфекции и интоксикацией организма. В лучшем случае разрыв кисты приведет к инфицированию слизистой оболочки ротовой полости. Также могут возникнуть осложнения со стороны пищеварительной системы при проглатывании инфицированной слюны. Немалый риск поражения дыхательных органов, что связано с их близким расположением.
В качестве профилактики нужно соблюдать гигиенические правила, следить за состоянием слюны, пить много жидкости и проходить регулярные консультации у стоматолога.
Если новообразование случилась у ребенка, его также нужно отвести к детскому хирургу для дальнейшего удаления. Но на самом деле развитие кисты у ребенка – это очень сложный процесс, особенные трудности возникает в момент лечения. Страх ребенка перед операцией может привести к проблемному удалению кисты. Но, если учитывать, что сегодня стоматологические клиники достаточно адаптированы для детской аудитории, лечение обещает быть быстрым и со стопроцентной гарантией.