На что расщепляется водород
Проект Заряд
Автономное энергоснабжение. Свободная и альтернативная энергия будущего. Бестопливные генераторы и «вечные двигатели» в каждый дом!
Генератор водорода путем ослабления межатомных связей высокой температурой
Предложенный способо основан на следующем:
Возможность осуществления изобретения подтверждается примерами, осуществляемыми в трех вариантах установок.
Все три варианта установок изготавливаются из одинаковых, унифицированных изделий цилиндрической формы из стальных труб.
Первый вариант
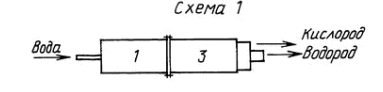
Работа и устройство установки первого варианта (схема 1)
Во всех трех вариантах работа установок начинается с приготовления перегретого пара в незамкнутом пространстве с температурой пара 550 o C. Незамкнутое пространство обеспечивает скорость по контуру разложения пара до 2 м/с.
Приготовление перегретого пара происходит в стальной трубе из жаропрочной стали /стартер/, диаметр и длина которого зависит от мощности установки. Мощность установки определяет количество разлагаемой воды, литров/с.
Один литр воды содержит 124 л водорода и 622 л кислорода, в пересчете на калории составляет 329 ккал.
Перед пуском установки стартер разогревается от 800 до 1000 o C /разогрев производится любым способом/.
Один конец стартера заглушен фланцем, через который поступает дозированная вода для разложения на рассчитанную мощность. Вода в стартере нагревается до 550 o C, свободно выходит из другого конца стартера и поступает в камеру разложения, с которой стартер соединен фланцами.
В камере разложения перегретый пар разлагается на водород и кислород электрическим полем, создаваемым положительным и отрицательным электродами, на которые подается постоянный ток с напряжением 6000 В. Положительным электродом служит сам корпус камеры /труба/, а отрицательным электродом служит труба из тонкостенной стали, смонтированная по центру корпуса, по всей поверхности которой имеются отверстия диаметром по 20 мм.
Труба — электрод представляет собой сетку, которая не должна создавать сопротивление для входа в электрод водорода. Электрод крепится к корпусу трубы на проходных изоляторах и по этому же креплению подается высокое напряжение. Конец трубы отрицательного электрода оканчивается электроизоляционной и термостойкой трубой для выхода водорода через фланец камеры. Выход кислорода из корпуса камеры разложения через стальной патрубок. Положительный электрод /корпус камеры/ должен быть заземлен и заземлен положительный полюс у источника питания постоянного тока.
Выход водорода по отношению к кислороду 1:5.
Второй вариант
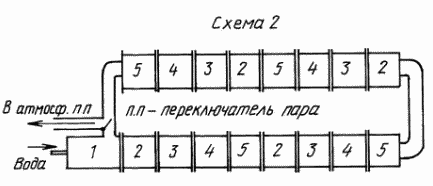
Работа и устройство установки по второму варианту (схема 2)
Установка второго варианта предназначена для получения большого количества водорода и кислорода за счет параллельного разложения большого количества воды и, окисления газов в котлах для получения рабочего пара высокого давления для электростанций, работающих на водороде /в дальнейшем ВЭС/.
Работа установки, как и в первом варианте, начинается с приготовления перегретого пара в стартере. Но этот стартер отличается от стартера в 1-м варианте. Отличие заключается в том, что на конце стартера приварен отвод, в котором смонтирован переключатель пара, имеющий два положения — «пуск» и «работа».
Полученный в стартере пар поступает в теплообменник, который предназначен для корректировки температуры восстановленной воды после окисления в котле /К1/ до 550 o C. Теплообменник /То/ — труба, как и все изделия с таким же диаметром. Между фланцами трубы вмонтированы трубки из жаропрочной стали, по которым проходит перегретый пар. Трубки обтекаются водой из замкнутой системы охлаждения.
Из теплообменника перегретый пар поступает в камеру разложения, точно такую же, как и в первом варианте установки.
Водород и кислород из камеры разложения поступают в горелку котла 1, в которой водород поджигается зажигалкой, — образуется факел. Факел, обтекая котел 1, создает в нем рабочий пар высокого давления. Хвост факела из котла 1 поступает в котел 2 и своим теплом в котле 2 подготавливает пар для котла 1. Начинается непрерывное окисление газов по всему контуру котлов по известной формуле:
В результате окисления газов восстанавливается вода и выделяется тепло. Это тепло в установке собирают котлы 1 и котлы 2, превращая это тепло в рабочий пар высокого давления. А восстановленная вода с высокой температурой поступает в следующий теплообменник, из него в следующую камеру разложения. Такая последовательность перехода воды из одного состояния в другое продолжается столько раз, сколько требуется получить от этого собранного тепла энергии в виде рабочего пара для обеспечения проектной мощности ВЭС.
После того, как первая порция перегретого пара обойдет все изделия, даст контуру расчетную энергию и выйдет из последнего в контуре котла 2, перегретый пар по трубе направляется в переключатель пара, смонтированный на стартере. Переключатель пара из положения «пуск» переводится в положение «работа», после чего он попадает в стартер. Стартер отключается /вода, разогрев/. Из стартера перегретый пар поступает в первый теплообменник, а из него в камеру разложения. Начинается новый виток перегретого пара по контуру. С этого момента контур разложения и плазмы замкнут сам на себя.
Вода установкой расходуется только на образование рабочего пара высокого давления, которая берется из обратки контура отработанного пара после турбины.
Недостаток силовых установок для ВЭС — это их громоздкость. Например, для ВЭС на 250 МВт нужно разлагать одновременно 455 л воды в одну секунду, а для этого потребуется 227 камер разложения, 227 теплообменников, 227 котлов /К1/, 227 котлов /К2/. Но такая громоздкость стократ будет оправдана уже только тем, что топливом для ВЭС будет только вода, не говоря уже о экологической чистоте ВЭС, дешевой электрической энергии и тепле.
Третий вариант
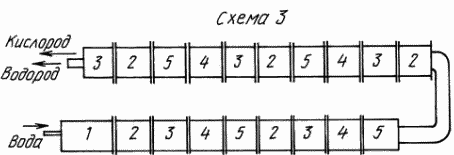
3-й вариант силовой установки (схема 3)
Это точно такая же силовая установка, как и вторая.
Разница между ними в том, что эта установка работает постоянно от стартера, контур разложения пара и сжигания водорода в кислороде не замкнут сам на себя. Конечным изделием в установке будет теплообменник с камерой разложения. Такая компоновка изделий позволит получать кроме электрической энергии и тепла, еще водород и кислород или водород и озон. Силовая установка на 250 МВт при работе от стартера будет расходовать энергию на разогрев стартера, воду 7,2 м 3 /ч и воду на образование рабочего пара 1620 м 3 /ч/вода используется из обратного контура отработанного пара/. В силовой установке для ВЭС температура воды 550 o C. Давление пара 250 ат. Расход энергии на создание электрического поля на одну камеру разложения ориентировочно составит 3600 кВт/ч.
Силовая установка на 250 МВт при размещении изделий на четырех этажах займет площадь 114 х 20 м и высоту 10 м. Не учитывая площадь под турбину, генератор и трансформатор на 250 кВА — 380 х 6000 В.
ИЗОБРЕТЕНИЕ ИМЕЕТ СЛЕДУЮЩИЕ ПРЕИМУЩЕСТВА
Изобретение может найти применение в промышленности путем замены углеводородного и ядерного топлива в силовых установках на дешевое, распространенное и экологически чистое — воду при сохранении мощности этих установок.
ФОРМУЛА ИЗОБРЕТЕНИЯ
Способ получения водорода и кислорода из пара воды, включающий пропускание этого пара через электрическое поле, отличающийся тем, что используют перегретый пар воды с температурой 500 — 550 o C, пропускаемый через электрическое поле постоянного тока высокого напряжения для диссоциации пара и разделения его на атомы водорода и кислорода.
Расщепление воды с эффективностью 100%: полдела сделано
Если найти дешёвый и простой способ электролиза/фотолиза воды, то мы получим невероятно богатый и чистый источник энергии — водородное топливо. Сгорая в кислороде, водород не образует никаких побочных выделений, кроме воды. Теоретически, электролиз — очень простой процесс: достаточно пропустить электрический ток через воду, и она разделяется на водород и кислород. Но сейчас все разработанные техпроцессы требуют такого большого количества энергии, что электролиз становится невыгодным.
Теперь учёные решили часть головоломки. Исследователи из Технион-Израильского технологического института разработали метод проведения второго из двух шагов окислительно-восстановительной реакции — восстановления — в видимом (солнечном) свете с энергетической эффективностью 100%, значительно превзойдя предыдущий рекорд 58,5%.
Осталось усовершенствовать полуреакцию окисления.
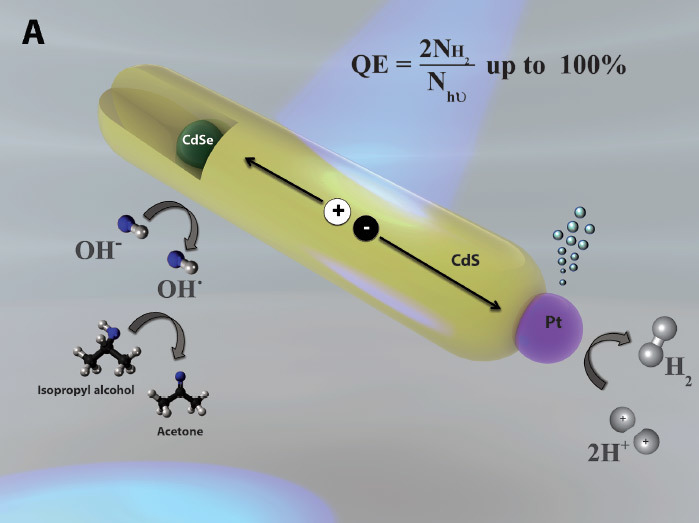
Столь высокой эффективности удалось добиться благодаря тому, что в процессе используется только энергия света. Катализаторами (фотокатализаторами) выступают наностержни длиной 50 нм. Они абсорбируют фотоны от источника освещения — и выдают электроны.
В полуреакции окисления производятся четыре отдельных атома водорода и молекула О2 (которая не нужна). В полуреакции восстановления четыре атома водорода спариваются в две молекулы H2, производя полезную форму водорода — газ H2,
Эффективность 100% означает, что все фотоны, поступившие в систему, участвуют в генерации электронов.
На такой эффективности каждый наностержень генерирует около 100 молекул H2 в секунду.
Сейчас учёные работают над оптимизацией техпроцесса, который пока что требует щелочной среды с невероятно высоким pH. Такой уровень никак не приемлем для реальных условий эксплуатации.
К тому же, наностержни подвержены коррозии, что тоже не слишком хорошо.
Тем не менее, сегодня человечество стало на шажок ближе к получению неиссякаемого источника чистой энергии в виде водородного топлива.
Научная работа опубликована в журнале Nano Letters (зеркало).
Перспективы и недостатки водородной энергетики
Для хранения и выработки энергии от водорода используются топливные элементы. Первый водородный топливный элемент был сконструирован английским ученым Уильямом Гроувом в 30-х годах 19 века. Гроув и работавший параллельно с ним Кристиан Шенбейн продемонстрировали возможность производства энергии в водородно-кислородном топливном элементе с использованием кислотного электролита.
В 1959 году Фрэнсис Т. Бэкон из Кембриджа добавил в водородный топливный элемент ионообменную мембрану для облегчения транспорта гидроксид-ионов. Изобретением Бэкона сразу заинтересовались правительство США и NASA, обновленный топливный элемент стал использоваться на космических аппаратах «Аполлон» в качестве главного источника энергии во время их полетов.
В отличие от кислорода водород практически не встречается на земле в чистом виде и поэтому извлекается из других соединений с помощью различных химических методов.
По этим способам его разделяют на цветовые градации.
Зеленый — производится из возобновляемых источников энергии методом электролиза воды. Все, что необходимо для этого: вода, электролизер и большое снабжение электроэнергией.
Голубой — производится из природного газа, а вредные отходы улавливаются для вторичного использования. Тем не менее идеально чистым этот метод не назовешь.
Розовый или красный — произведенный при помощи атомной энергии.
Серый — водород получают путем конверсии метана. При его производстве вредные отходы выбрасываются в атмосферу.
Коричневый — водород получают в результате газификации угля. Этот метод также после себя оставляет парниковые газы.
Еще существуют технологии получения биоводорода из мусора и этанола, но их доля чрезвычайно мала.
Себестоимость производства по видам водорода, доллар за килограмм
Водородная энергетика
На переработку угля приходится 18% производства водорода, 4% обеспечивается за счет зеленого водорода и 78% — переработкой природного газа и нефти. Методы производства, основанные на ископаемом топливе, приводят к образованию 830 млн тонн выбросов CO2 каждый год, что равно выбросам Великобритании и Индонезии, вместе взятым. И тем не менее водород — это более чистая альтернатива традиционному топливу.
В мире три основных источника выбросов, способствующих потеплению климата: транспорт, производство электроэнергии и промышленность. Водород может использоваться во всех трех областях. При использовании в топливных элементах водородная энергия оставляет минимальные потери, а после использования в качестве побочного продукта остается только вода, из которой снова можно добывать водород.
Перспективы отрасли
Согласно докладу МЭА, к 2050 году мировой спрос на водород должен достичь 528 млн тонн — против 87 млн в 2020, — а его доля в мировом потреблении составит 18%, из них 10% будет приходиться на зеленый водород.
В июне 2020 года Германия объявила о реализации национальной водородной стратегии с инвестициями в 7 млрд евро, чтобы стать лидером в этой области.
Япония, Франция, Южная Корея, Австралия, Нидерланды и Норвегия начали свой курс на водород раньше Германии, а Япония сделала это раньше всех — в декабре 2017 года.
В июле 2020 года Минэнерго подготовило план развития в РФ водородной энергетики на период 2020—2024 годов. Производить водород собираются «Росатом», «Газпром» и «Новатэк». В дорожной карте предусмотрены следующие меры:
В 2021 году HydrogenOne Capital — первый в мире инвестиционный фонд, ориентированный на зеленый водород, заявил о листинге на Лондонской бирже. Фонд инвестирует в проекты мощностью 20—100 МВт с возможностью их расширения до 500 МВт.
Как сделать ремонт и не сойти с ума
Преимущества водородной энергетики
Высокая применимость. Электрификация транспорта поможет снизить выбросы в атмосферу, но авиацию, морские и грузовые перевозки на дальние расстояния трудно перевести на использование электроэнергии, потому что для этих секторов требуется топливо с высокой плотностью энергии. Зеленый водород может удовлетворить эти потребности. Например, Airbus представил концепции самолетов с водородным двигателем и надеется ввести его в эксплуатацию к 2035 году.
Nikola строит полуприцепы, работающие как на аккумуляторных батареях, так и на водороде. Компания заявляет, что ее топливные элементы могут работать при более низких температурах, чем батареи. И они легче, что делает их более практичными для грузовиков и другой тяжелой техники. Nikola также утверждает, что дальность хода такого грузовика составит 900 миль на баке с водородом. Для сравнения: у Tesla Semi с батарейным питанием, который может быть запущен в производство в конце этого года или в 2022 году, заявленная дальность — 200—300 миль.
Также свои аналогичные модели транспорта представили компании Toyota, Honda и BMW.
Время заправки электромобиля на топливных элементах в среднем составляет менее четырех минут. При этом в отличие от батарей они не нуждаются в перезарядке. Поскольку они могут работать независимо от сети, то могут использоваться как запасные генераторы электричества или тепла.
Важный элемент перехода на водород — его применение в ЖКХ. Кроме пилотных проектов в Великобритании Лидс станет первым городом, энергоснабжение которого будет полностью водородным. Согласно плану, все газовые сети и транспортное оборудование переведут на него.
Запасы водорода практически безграничны. Так как он встречается почти всюду, его можно использовать там, где он производится. В отличие от батарей, которые не могут хранить большое количество электроэнергии в течение продолжительного времени, водород можно производить из избыточной возобновляемой энергии и хранить в больших количествах.
Энергоэффективность. Водород содержит почти в три раза больше энергии, чем ископаемое топливо, поэтому для выполнения какой-либо работы его требуется гораздо меньше. Например, по сравнению с электростанцией, работающей на сжигании топлива с КПД от 33 до 35%, водородные топливные элементы выполнят ту же функцию с КПД до 65%. Для примера, у солнечных элементов КПД — 20%, а у ветряных — 40%.
Весной 2020 года в городе Фукусима была запущена самая крупная в мире электростанция, работающая на водороде. Для питания электролизных установок на ней размещены солнечные батареи общей мощностью 20 МВт. Всего станция вырабатывает 1,2 тысячи кубических метров водорода в час.
В автомобилях топливные элементы используют 40—60% энергии топлива, а также обеспечивают сокращение его расхода на 50%.
Зеленый водород — отличная среда для хранения энергии. Например, у Германии существует проблема с энергосистемой. В ясные и ветреные дни солнечные экраны и ветряные турбины на севере производят больше электроэнергии, чем может потребить эта часть страны. Из-за этого Германия вынуждена продавать излишки электроэнергии соседним странам себе в убыток. Избыток электроэнергии из ВИЭ можно хранить в виде водорода, а затем сжигать для выработки электроэнергии, когда это необходимо.
Недостатки водородной энергетики
Стоимость зеленого водорода. Как уже говорилось выше, именно стоимость добычи самого чистого вида водорода ставит наиболее сильные препятствия в его развитии. По словам и прогнозам Минэнерго РФ, перспективы водородной энергетики связаны с удешевлением стоимости водорода, производимого электролизом воды. В качестве основных факторов обеспечения конкурентоспособности зеленого водорода рассматривается перспективное снижение капитальных затрат на электролизеры, а также стоимости электроэнергии из ВИЭ.
Водород – рождающий воду
Содержание
При горении водорода в кислороде образуется чистое, некоптящее и не имеющее четких границ пламя температурой до 2800°С.
Теоретически для полного сгорания 1 мг водорода требуется 0,5 мг кислорода. Практически в горелку на 1 мг водорода подается 0,25 мг кислорода.
История открытия водорода
Доподлино установить кто открыл водорода невозможно, поскольку он известен с XVI века. Алхимики заметили, что при взаимодействии железных опилок с соляной или серной кислотой выделяется «горючий воздух», или «искусственный воздух». Однако его все-таки считали воздухом, получившим почему-то способность гореть.
Но вот сторонник точных измерений Генри Кавендиш (Henry Cavendish) выделил водород из серной и соляной кислот железом, цинком, оловом. Он собирал его в газометре и узнал, что при горении «горючего воздуха» образуется чистая вода. Поэтому считается, что лавры открытия водорода принадлежат именно ему.
Интересны первые русские наименования водорода: «водотворный газ», «водотвор». Легкость водорода, пожалуй, поразила первых наблюдателей больше, чем остальные его свойства. Думали даже, что он и есть тот таинственный с «отрицательным весом» флогистон, который, проникая в тела, сообщает им способность гореть.
Избыток водяных паров, непрерывно поступающих в трубу, проходил через холодильник, а водород по трубам направлялся в аэростат и надувал его.
Когда железо израсходуется, его опять можно получить из накаленной окалины, если через трубу пропустить светильный газ. Уравнение показывает, что 3?56=168 г железа могут вытеснить 8 г водорода, или 4?22,4=89,6 л водорода.
Аэростаты, наполненные водородом, применили впервые революционные войска Франции в битве при Флёрюсе в 1794 г.
В войнах 1904-1905 и 1914-1918 гг. привязанные канатами аэростаты служили главным образом для наблюдения за прицельностью артиллерийского огня, за передвижением войск. Во время Великой Отечественной войны 1941-1945 гг. они защищали военные объекты от авиации противника. Летчики, опасаясь столкновений с аэростатом и канатами, летали на большой высоте, поэтому их бомбовые удары в значительной мере теряли прицельность.
Первый в мире полет на аэростате с научной целью совершил ученый Захаров Яков Дмитриевич в 1804 г. А в 1887 г. для наблюдения солнечного затмения и изучения воздуха поднялся в воздух Менделеев Дмитрий Иванович.
Получение водорода
В промышленности технический водород получают:
Получение водорода из кислот
Вместо цинка можно взять железо в виде стружек или алюминий. Водород получается, загрязненный побочными продуктами разложения серной кислоты, и, если это требуется, его приходится очищать.
Добыча водорода из промышленных газов
При переработке каменного угля на кокс дополнительно получается деготь и коксовый газ. В состав газа входит до 50-60% водорода (H2), 20-25% метана (СН4), окись углерода (СО), азот (N) и др.
В статье о свойствах гелия и способах его производства описан процесс получения гелия методом фракционной конденсации. Так же поступают и с коксовым газом. Но чтобы отделить водород от других составных частей, требуется очень глубокое охлаждение из-за низкой критической температуры водорода.
Производство водорода из воды
Единственным исходным сырьем для добычи водорода электролитическим методом служит вода. Чистая, дистиллированная вода обладает огромным сопротивлением и почти совершенно не проводит электрический ток. Вот почему для того чтобы сделать воду электропроводной, в ней нужно растворить какую-нибудь соль, кислоту или основание, которые дают ионы.
В результате получения 2 м 3 водорода, как побочный продукт получается 1 м 3 кислорода.
Большой расход электроэнергии является главным недостатком данного способа, поэтому применение водорода полученного при помощи электролиза целесообразно при одновременном использовании вместе с кислородом. В связи с этим в последнее время портативные водородные сварочные аппараты для газовой сварки и пайки пользуются все большей популярностью.
Применение водорода
Основными направлениями применения водорода являются:
Применение водорода в сварке
Водород использовался в качестве защитного газа еще при первых попытках защиты дугового пространства от воздуха. Однако водород может оказать в ряде случаев вредное воздействие. Это объясняется тем, что при применении водорода в металле сварных швов образуются дефекты в виде пор, а также является одним из главных факторов образования холодных трещин. С увеличением толщины свариваемых элементов пористость в металле сварных швов становится значительной. Поэтому его использование в дальнейшем было значительно ограничено. В чистом виде (и в виде водородно-азотных смесей, получаемых при диссоциации аммиака) он в настоящее время применяется при атомно-водородной сварке (хотя и сам этот способ заменен теперь другими, в частности сваркой неплавящимся электродом).
Если струю водорода пропускать через пламя вольтовой дуги, то водород диссоциирует на атомы с поглощением значительного количество тепла (103,6 ккал/моль) что приводит к значительному увеличению напряжения дуги. Она становится устойчивой только при повышении напряжения источника тока. Так, например, при режимах атомно-водородной сварки наиболее эффективной «звенящей» дугой при вольфрамовых электродах и силе тока 10-20 А напряжение дуги составляет около 100 А, напряжение холостого хода питающего источника должно быть не менее 200-220 В (обычно около 300 В). В этом случае водород является не только защитным газом, но и переносит тепловую энергию из дуги на поверхность не включенного в цепь тока изделия.
Образовавшийся атомный водород направляют на твердую свариваемую поверхность, где происходит нагревание и расплавление металла за счет поглощения тепла, которое выделяется при рекомбинации атомов до молекулярного водорода. Ассоциация атомарного водорода на холодной поверхности металла (в том числе и расплавленной, так как температура плавления большинства металлов ниже температуры возможного существования заметных количеств атомарного водорода) приводит к выделению тепла, потребленного в дуге на диссоциацию. За счет выделяющегося тепла температура свариваемой поверхности металла повышается до 3528-4028°С. Такая атомно-водородная сварка позволяет обрабатывать и сваривать самые тугоплавкие металлы, высококачественные стали, коррозионно-устойчивые материалы, цветные металлы.
Несмотря на то, что атмосфера, окружающая металл, при атомно-водородной сварке представляет собой смесь молекулярного и атомарного водорода, при отсутствии на металле значительного количества окислов швы получаются достаточно плотными и применительно к низкоуглеродистой стали не имеют большого количества диффузионно-подвижного и остаточного водорода.
При струйной защите иногда используется водяной пар. Однако в этом случае получается значительно меньшая стабильность качества сварных швов, чем при сварке с защитой дуги углекислым газом. В связи с этим такой процесс широкого распространения не получил.
При TIG сварке аустенитной нержавеющей стали с целью увеличения напряжения дуги, увеличения теплоэффективности и снижения оксидирования используют аргоно-водородные смеси газов (15% Н2). Более высокая температуру и сжатие дуги, в свою очередь увеличивает глубину проплавления металла. Однако при этом необходимо учитывать возможность вредного влияния растворяющегося в металле водорода. Более широко водород применяют в специальных областях сварки и металлургии, например в порошковой металлургии при спекании изделий из порошковых материалов.
В других случаях применение водорода и водородосодержащих газов, как защитных при дуговой сварке, нецелесообразно.
Применяют водород для составления плазмообразующих смесей при плазменной сварке и резке. Так, для защиты сварочной ванны от окисления при плазменной сварке легированной стали, меди, никеля и сплавов на его основе используют смесь аргона с 5-8% водорода.
Аргоно-водородную смесь, имеющую до 20% Н2, применяют при микроплазменной сварке. Наличие водорода в смеси обеспечивает сжатие столба плазмы, делает его более сконцентрированным. Кроме того, водород создает необходимую в ряде случаев восстановительную атмосферу.
Взрывоопасность водорода
При работе с водородом особое внимание следует обращать на герметичность аппаратуры и газовых коммуникаций, так как водород способен проникать через мельчайшие неплотности, образовывать с воздухом взрывоопасные концентрации. В смеси с кислородом (2:1) образует взрывчатую смесь, называемую гремучим газом.
Температура самовоспламенения 510°С. Водород физиологически инертен, при высоких концентрациях вызывает удушье. При высоком давлении проявляется наркотическое действие. При работе в среде водорода необходимо пользоваться изолирующим противогазом (кислородным или шланговым).
Хранение и транспортировка водорода
Водород технический поставляют по ГОСТ 3022. Хранят и транспортируют водород в стальных баллонах вместимостью 40 и 50 дм 3 по ГОСТ 949 под давлением 15 МПа. Баллон окрашивается в темно-зеленый цвет с красной надписью «ВОДОРОД».
Характеристика водорода
Характеристики H2 представлены в таблицах ниже:
Коэффициенты перевода объема и массы H2 при Т=15°С и Р=0,1 МПа
| Масса, кг | Объем | |
|---|---|---|
| Газ, м 3 | Жидкость, л | |
| 0,0841 | 1 | 1,188 |
| 0,0708 | 0,842 | 1 |
| 1 | 11,891 | 14,126 |
Коэффициенты перевода объема и массы H2 при Т=0°С и Р=0,1 МПа
| Масса, кг | Объем | |
|---|---|---|
| Газ, м 3 | Жидкость, л | |
| 0,09 | 1 | 1,258 |
| 0,0708 | 0,975 | 1 |
| 1 | 11,124 | 14,126 |
Водород в баллоне
| Наименование | Объем баллона, л | Масса газа в баллоне, кг | Объем газа (м 3 ) при Т=15°С, Р=0,1 МПа |
|---|---|---|---|
| H2 | 40 | 0,54 | 6,0 |
Благодаря этой таблице теперь можно легко дать ответы на вопросы, которые очень часто задают сварщики:
Рекомендуем к просмотру видео об открытии водорода, его характеристиках и производстве.