Наследственный ангионевротический отек что это
Наследственный ангионевротический отек
Наследственный ангионевротический отек – генетическое заболевание, при котором наблюдается дефицит ингибитора С1-компонента комплемента. Симптомами являются рецидивирующие отеки кожи, слизистых оболочек и органов брюшной полости, которые могут сопровождаться удушьем (при отеке гортани), рвотой и болями в животе (при поражении брюшной полости). Диагностика производится на основании осмотра, изучения наследственного анамнеза, определения С1-ингибитора, компонентов С4 и С2 в плазме крови, молекулярно-генетических исследований. Лечение осуществляется путем компенсирования абсолютного или функционального дефицита С1-ингибитора, применения блокаторов брадикинина и калликреина, использования свежезамороженной донорской плазмы.
Общие сведения
Наследственный ангионевротический отек (НАО) – вариант первичного иммунодефицита, обусловленный нарушением ингибирования системы комплемента, точнее, его основной фракции С1. Впервые это состояние было описано в 1888 году У. Осиером, который выявил рецидивирующие отеки у молодой женщины, а также установил, что подобное заболевание имелось как минимум у пяти поколений ее семьи. Примечательно, что собственно ангионевротический отек был открыт И. Квинке всего за 6 лет до обнаружения наследственной формы этой патологии – в 1882-м году. Наследственный ангионевротический отек имеет аутосомно-доминантный характер передачи и с одинаковой частотой поражает как мужчин, так и женщин. По некоторым данным, у женщин заболевание протекает тяжелее и возникает раньше, однако достоверных исследований по этому поводу не производилось. Встречаемость наследственного ангионевротического отека, по всей видимости, значительно варьирует у разных этнических групп, что дает весьма неоднородные цифры этого показателя – от 1:10 000 до 1:200 000.
Причины наследственного ангионевротического отека
Непосредственной причиной развития наследственного ангионевротического отека является первичный иммунодефицит, заключающийся в дефиците или функциональной неполноценности ингибитора эстеразы одного из компонентов комплемента – С1. В результате этого также нарушается ингибирование активации других компонентов этой системы – С4 и С2, что приводит к еще большему расстройству работы данного иммунного механизма. Врачам-генетикам удалось установить ген, отвечающий за 98% форм наследственного ангионевротического отека – им является C1NH, расположенный на 11-й хромосоме и кодирующий вышеуказанный ингибитор эстеразы С1. Различные мутации способны приводить к неодинаковым по своему течению формам заболевания, которые обладают достаточно сходными клиническими проявлениями, но различаются при проведении ряда диагностических тестов.
При одних типах мутации гена C1NH происходит полное прекращение синтеза белка-ингибитора С1, в результате чего он отсутствует в плазме крови, а остановка системы комплемента производится малоэффективными побочными путями. В других случаях наследственный ангионевротический отек возникает на фоне нормального содержания ингибитора в крови, при этом генетический дефект C1NH приводит к нарушению структуры активного центра данного фермента. В результате ингибитор С1 становится функционально неполноценным, что и служит причиной развития патологии. Существуют также редкие формы наследственного ангионевротического отека, при которых не наблюдается как изменений количества или активности ингибитора эстеразы С1, так и мутаций в гене C1NH – этиология и патогенез таких заболеваний на сегодняшний день неизвестны.
Остановка ингибирования активности компонентов комплемента (С1, С2, С4) приводит к запуску иммунной реакции, сходной по своему течению с аллергической, особенно крапивницей. Компоненты комплемента способны расширять кровеносные сосуды глубоких слоев дермы, повышать проницаемость их стенок, что провоцирует диффундирование компонентов плазмы крови в межклеточное пространство тканей кожи и слизистых оболочек и приводит к их отеку. Кроме того, немаловажную роль в патогенезе наследственного ангионевротического отека играют вазоактивные полипептиды – брадикинин и калликреин, которые еще больше увеличивают степень отека, а также способны вызывать спазм гладкомышечной мускулатуры органов желудочно-кишечного тракта. Эти процессы обуславливают все разнообразие симптомов наследственного ангионевротического отека: отечность кожи (в области конечностей, лица, шеи) и слизистых оболочек (ротовой полости, гортани, глотки), боли в животе и диспепсические расстройства, провоцируемые сочетанием отеков и спазмов.
Классификация наследственного ангионевротического отека
Всего на сегодняшний день выявлено три основных типа наследственного ангионевротического отека. Их различия в плане клинического течения патологии очень незначительны, для определения формы заболевания используют специальные диагностические методики. Врачу-иммунологу крайне важно выяснить тип наследственного ангионевротического отека, так как от этого во многом зависит тактика лечения данной патологии:
Симптомы наследственного ангионевротического отека
Как правило, при рождении и в детском возрасте (за исключением редких случаев) наследственный ангионевротический отек ничем себя не проявляет. Довольно часто первые признаки заболевания возникают в подростковом периоде, так как их провоцируют стрессы и гормональные перестройки, происходящие в организме в это время. Однако нередко наследственный ангионевротический отек появляется позже – в возрасте 20-30 лет или даже у пожилых лиц. Чаще всего развитию первого приступа предшествует какое-либо провоцирующее явление: мощный эмоциональный стресс, серьезное заболевание, хирургическое вмешательство, прием некоторых лекарственных средств. В дальнейшем «порог чувствительности» по отношению к провоцирующим факторам снижается, приступы возникают все чаще – наследственный ангионевротический отек приобретает рецидивирующий характер.
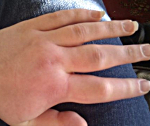
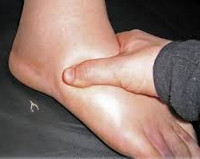
Основным проявлением заболевания у большинства больных является отек кожи и подкожной клетчатки на кистях, стопах, иногда лице и шее. В более тяжелых случаях отечные явления возникают на слизистых оболочках полости рта, гортани и глотки – при этом может развиваться удушье (асфиксия), являющееся наиболее частой причиной смерти от наследственного ангионевротического отека. В других случаях на первый план выступают симптомы со стороны желудочно-кишечного тракта: тошнота, рвота, боли и рези в животе, иногда подобная клиническая картина приобретает черты «острого живота». В отдельных случаях наследственный ангионевротический отек характеризуется сочетанием отека кожи, слизистых оболочек и поражения желудочно-кишечного тракта.
Диагностика наследственного ангионевротического отека
Для выявления наследственного ангионевротического отека используют данные физикального осмотра больного, изучения его наследственного анамнеза, определения в крови количества ингибитора С1, а также компонентов комплемента С1, С2, С4, и молекулярно-генетических исследований. Осмотр в фазу обострения заболевания выявляет отек кожи или слизистых оболочек, пациенты могут жаловаться на боли в животе, рвоту, диарею. В крови при наличии наследственного ангионевротического отека 1-го типа ингибитор эстеразы С1 полностью отсутствует, значительно снижены концентрации индикаторных компонентов комплемента. При 2-м типе заболевания в плазме крове может определяться незначительное количество ингибитора С1, в редких случаях его уровень соответствует норме, но соединение имеет пониженную функциональную активность. При всех трех вариантах наследственного ангионевротического отека уровень С1, С2 и С4 не превышает 30-40% от нормы, поэтому этот показатель является ключевым в диагностике данного состояния.
Изучение наследственного анамнеза пациента зачастую обнаруживает наличие подобного заболевания как минимум у нескольких поколений его предков и у других родственников. Однако отсутствие признаков семейного характера патологии не является однозначным критерием, позволяющим исключить наследственный ангионевротический отек – примерно у четверти больных это состояние обусловлено спонтанными мутациями и выявляется впервые в семье. Молекулярно-генетическая диагностика осуществляется путем автоматического секвенирования гена C1NH с целью выявления мутаций. Дифференциальную диагностику следует производить с ангионевротическим отеком аллергического генеза и приобретенными формами дефицита ингибитора С1.
Лечение наследственного ангионевротического отека
Терапию наследственного ангионевротического отека разделяют на два типа – лечение для купирования острого приступа заболевания и профилактический прием препаратов для предупреждения их развития. В случае острого отека Квинке, обусловленного НАО, традиционные противоанафилактические меры (адреналин, стероиды) неэффективны, необходимо использовать нативный или рекомбинантный ингибитор С1, антагонисты брадикинина и калликреина, при их отсутствии показано переливание свежезамороженной плазмы. Начинать такое лечение нужно как можно раньше, в идеале – при самых первых приступах наследственного ангионевротического отека.
Долгосрочная профилактика заболевания производится в тех случаях, когда приступы возникают слишком часто (чаще раза в месяц), если в анамнезе имелись случаи отека гортани или удушья, либо госпитализация в реанимационное отделение. Профилактика включает в себя использование андрогенов, экзогенных (рекомбинантных или нативных) форм ингибитора эстеразы С1, антифибринолитических препаратов. При доброкачественном течении наследственного ангионевротического отека – редких приступах и их относительно быстром исчезновении – такое лечение может не назначаться. Однако накануне хирургических или стоматологических вмешательств, физических и умственных нагрузок рекомендуется краткосрочно принимать вышеуказанные средства для уменьшения риска развития приступа.
Прогноз и профилактика наследственного ангионевротического отека
В большинстве случаев прогноз наследственного ангионевротического отека относительно благоприятный в плане выживаемости – при разумном лечении и профилактике приступы возникают крайне редко и не угрожают жизни больного. При этом всегда сохраняется риск отека гортани, что может привести к асфиксии и летальному исходу. Таким больным следует не только избегать значительных физических и эмоциональных нагрузок, но и желательно иметь при себе карточку или медальон с указанием диагноза. Огромное количество смертей от наследственного ангионевротического отека было обусловлено неверными действиями медиков, не знающих диагноза и поэтому использующих традиционные при аллергическом отеке Квинке препараты, которые неэффективны при НАО.
Наследственный ангионевротический отек
Общая информация
Краткое описание
Одобрен
Объединенной комиссией по качеству медицинских услуг
Министерства здравоохранения Республики Казахстан
от «18» апреля 2019 года
Протокол №62
Наследственный ангионевротический отек (НАО) – первичный иммунодефицит, развивающийся в результате генетически опосредованного количественного дефицита ингибитора С1 или снижение его активности.
Название протокола: Наследственный ангионевротический отек
Код (ы) МКБ-10:
| МКБ-10 | |
| Код | Название |
| Т78.3 | Ангионевротический отек |
| D84.1 | Дефект в системе комплемента |
Дата разработки/пересмотра протокола: 2018 год.
Сокращения, используемые в протоколе:
| АТ | – | антитела |
| АТ к С1-ингибитору | – | антитела к С1-ингибитору |
| иАПФ | – | ингибиторы ангиотензинпревращающего фермента |
| ИНГ | – | ингибитор |
| ГКС | – | глюкокортикостероиды |
| ЛС | – | лекарственные средства |
| НАО | – | наследственный ангионевротический отёк |
| НПВП | – | нестероидные противовоспалительные препараты |
| С1-ингибитор | – | ингибитор первого компонента комплемента |
| С1-INH95 Kd | – | C1-ингибитор низкомолекулярной массы с весом 95 килодальтон |
| С1q | – | фактор первого компонента комплемента |
| С4 | – | компонент комплемента |
| IgE | – | иммуноглобулин класса Е |
| IgG | – | иммуноглобулин класса G |
| IgМ | – | иммуноглобулин класса М |
| Ф XII | – | коагуляционный фактор XII |
Пользователи протокола: аллергологи-иммунологи, врачи общей практики, педиатры, терапевты, хирурги, реаниматологи.
Категория пациентов: взрослые, дети.
Шкала уровня доказательности:
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты которых могут быть распространены на соответствующую популяцию. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или Высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+). Результаты которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию. |
| D | Описание серии случаев или неконтролируемое исследование или мнение экспертов. |
| GPP | Наилучшая фармацевтическая практика. |
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
| Форма | Характеристика | |
| АО связанные с патологией системы комплемента (D 84.1) | НАО 1-го типа (85 % случаев) | Дефицит С1-ингибитора в плазме, обусловленный нефункционирующим геном. При этом уровень С1-ингибитора может варьировать от неопределяемого до менее 30% от нормального. Аутосомно-доминантный тип наследования. |
| НАО 2-го типа (15 % случаев) | Нормальной или повышенной выработкой С1-ингибитора, но снижена его функциональная активность. Аутосомно-доминантный тип наследования. | |
| НАО 3-го типа | Недавно описанное эстрогензависимое заболевание, которым преимущественно болеют женщины. Считается, что он связан с генетическим нарушением контроля ХII фактора свёртывания крови, отличительной особенностью НАО 3 типа является нормальный уровень С1-ингибитора и его функциональной активности. При эстрогензависимом НАО клинические симптомы идентичны таковым при первых двух типах наследственных комплементзависимых отеков. Его особенностью является зависимость симптомов от высокого уровня эстрогенов и, соответственно, для него характерны обострения во время беременности, при применении пероральных контрацептивов или заместительной терапии эстрогенами при лечении климактерического синдрома. | |
| Приобретенная форма ангиоотёка (ПАО) | Тип 1 | Дефицит С1-ингибитора у больных с лимфопролиферативными заболеваниями или другими злокачественными новообразованиями. |
| Тип 2 | Наличие в сыворотке пациента одномоментно как аутоантител к С1- ингибитору (часто моноклональных), так и циркулирующего низкомолекулярного белка С1- ингибитора (С1-INH95 Kd). Может встречаться у гетерогенной группы больных (заболевания соединительной ткани, онкологическая патология, заболевания печени и у лиц без признаков каких-либо заболеваний). | |
| АО, не связанные с патологией в системе комплемента (T 78.3) | АО, вызванные высвобождением вазоактивных медиаторов из тучных клеток, в 50% случаев сопровождают крапивницу; в этом случае крапивница и АО имеют общую этиологию, патогенез, лечение и прогноз. |
Диагностика
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ [1,4-9]
Диагностические критерии
Дифференциальный диагноз
Дифференциальный диагноз и обоснование дополнительных исследований
Дифференциальный диагноз АО проводится со следующими заболеваниями:
Гипотиреоз:
• Слабость, сонливость, утомляемость, непереносимость холода, уменьшение потоотделения, сухость кожи, снижение тембра голоса. Периорбитальный отек, макроглоссия, отек рук.
• Нормальные уровни С1-ингибитора, С4 и С1q компонентовᴮ.
• Повышение уровня тиреотропного гормона, снижение свободного Т4 при первичном гипотиреозе, нормальный уровень свободного Т4 при субклинической форме.
Уртикарный васкулит:
• Сохранение элементов в течение более 24 часов.
• Наличие остаточной пигментации.
• Жалобы на жжение и боль в области поражения.
• Повышение СОЭ, концентрации СРБ свидетельствуют в пользу уртикарного васкулита.
• Могут быть признаки системной патологии (артралгии, миалгии).
• Возможно сочетание с АО, особенно в случаях гипокомплементемии.
• Антинуклеарных АТ и ревматоидного фактора, как правило, не обнаруживают.
• При биопсии выявляют признаки лейкоцитокластического васкулита.
Постоянный отек кожи лица и шеи:
• Может быть связан со сдавлением верхней полой вены. Показано рентгенологическое исследование грудной клетки для выявления опухоли, расширения средостения.
Синдром Мелькерссона-Розенталя:
• Постоянный плотный отек лица, складчатый язык.
• При биопсии пораженной ткани обнаруживают гранулематозное воспаления.
Анасарка:
• Генерализованный отек может быть признаком гипопротеинемии (например, при нефротическом синдроме, болезнях печени (циррозе печени), белководефицитной энтеропатии). Отеки тканей постоянные, присутствуют другие признаки соматической патологии.
• В отличии от АО анасарка развивается относительно медленно, симметрично, не характерны поражения губ, гортани, кишечника, отсутствуют признаки анафилаксии.
При проведении дифференциальной диагностики АО с любым другим заболеванием, сопровождающимся отеком любой локализации, следует помнить о том, что симптомы при АО длятся от часов до нескольких суток, если отек сохраняется более длительное время, то диагноз АО исключается.
Лечение
Препараты (действующие вещества), применяющиеся при лечении
| Аминокапроновая кислота (Aminocaproic acid) |
| Гидрокортизон (Hydrocortisone) |
| Даназол (Danazol) |
| Дезлоратадин (Desloratadine) |
| Икатибант (Icatibant) |
| Ингибитор С1 – эстеразы человеческой |
| Клемастин (Clemastine) |
| Левоцетиризин (Levocetirizine) |
| Метилпреднизолон (Methylprednisolone) |
| Метилтестостерон (Methyltestosterone) |
| Плазма свежезамороженная |
| Преднизолон (Prednisolone) |
| Рупатадина фумарат (Rupatadine fumarat) |
| Транексамовая кислота (Tranexamic acid) |
| Фуросемид (Furosemide) |
| Хлоропирамин (Chloropyramine) |
| Цетиризин (Cetirizine) |
| Эпинефрин (Epinephrine) |
Лечение (амбулатория)
ТАКТИКА ЛЕЧЕНИЯ НА АМБУЛАТОРНОМ УРОВНЕ [1,4,6,9]
Купирование острого приступа НАО (при тяжелом и жизнеугрожающем отеке):
Неотложная терапия НАО проводится без отмены препаратов базисной терапии.
1) Подкожное введение икатибанта (УД – С): 3 мл (30мг). В большинстве случаев однократного ведения препарата достаточно для купирования симптомов НАО. В случае недостаточной эффективности или рецидива НАО, икатибант вводят повторно в дозе 30мг через 6 часов. Если после повторного введения препарата симптомы НАО сохраняются или приступ НАО рецидивирует, третья доза препарата может быть введена еще через 6 часов. Не рекомендуется превышать максимальную суточную дозу препарата – 90 мг (3 инъекции) [6,7].
2) В/в введение концентрата Ингибитора С1- эстеразы человеческой (500-1500 ЕД).
3) Свежая или свежезамороженная нативная плазма в объеме 250-300 мл.
4) Антифибринолитические препараты:
— транексамовая кислота в дозе 1г внутрь или 0,5-1г в/в медленно каждые 3-4 часа;
-ε-аминокапроновая кислота в/в капельно в дозе 5-10г, затем в дозе 5г в/в капельно каждые 4ч или 7-10 г/сут внутрь до полного купирования обострения [4].
5) При отсутствии достоверных данных о наличии АО, связанного с патологией системы комплемента, возможно введение системных ГКС. При жизнеугрожающих отеках возможно дополнительное введение фуросемида в дозе 40-80 мг в/в. Необходима госпитализация больного в ЛОР-отделение или реанимационное отделение, так как может понадобиться трахеостомия или интубация.
6) Пациенты с III типом НАО не отвечают на терапию ингибитором С1- эстеразы человеческой и антифибринолитическими препаратами. Главная цель терапии в такой ситуации состоит в поддержании проходимости дыхательных путей, объема циркулирующей крови (симптоматическая терапия) и отмене приема эстрогенов.
Перечень основных лекарственных средств
Адреномиметические средства:
| Препараты | Разовая доза | Кратность введения |
| Адреналин | ||
| Эпинефрин |
| Препараты | Разовая доза | Кратность введения |
| Преднизолон | 0,5-1 г/кг | 1-3 раза вдень |
| Метилпреднизолон | 1-3 раза вдень | |
| Гидрокортизон | 0,08–0,25 г/кг | 1-3 раза вдень |
| Препараты | Разовая доза | Кратность введения |
| Цетиризины | 10-20 мг | 1-2 раза в день |
| Левоцетиризины | 5-10 мг | 1-2 раза в день |
| Дезлоратидины | 5-10 мг | 1-2 раза в день |
| Хлоропирамин | 2-4 мл | 1-3 раза в день |
| Клемастин | 1-4 мг | 1-3 раза в день |
| Рупатадин фумарат | 10-20 мг | 1-2 раза в день |
Хирургическое вмешательство: нет
Наследственный ангионевротический отек (НАО)
Наследственный ангионевротический отек (НАО) характеризуется дефицитом ингибитора С1 — белка, который угнетает один из
белков системы комплемента — С1. Это проявляется повторяющимися приступами отека кожи и слизистых оболочек ЖКТ, верхних
дыхательных путей (ВДП) и мочеполовой системы, которые проходят самопроизвольно через 1—3 дня.
Заболевание чаще всего появляется в возрасте около 7 лет и редко продолжается даже после 60 лет.
Каковы причины НАО?
Причиной НАО является генетический дефект в образовании ингибитора С1. Ген расположен на хромосоме 11. Наследование является
аутосомно-доминантным. Приобретенная форма дефицита ингибитора С1 также встречается редко.
Это может быть связано со следующими причинами: образование аутоантител против него или чрезмерная активация С1 с повышенным
потреблением ингибитора С1, что превышает скорость его синтеза в клетках печени.
Какие изменения происходят при НАО?
Ингибитор C1 представляет собой белок плазмы, также называемый ингибитором эстеразы C1, поскольку он ингибирует эстеразу C1.
Когда ингибитор C1 является дефицитным, каскад комплемента активируется классическим способом, и образуются C3a и C5a, известные
как анафилатоксины. Они вызывают дегрануляцию тучных клеток, которые высвобождают медиаторы, что приводит к повышенной
проницаемости сосудов и отеку.
Существует три типа НАО:
тип I — имеет количественный дефицит ингибитора С1 — встречается в 85% случаев;
тип II — имеется качественный дефицит ингибитора C1 — функционально дефектный ингибитор образуется в нормальном или даже увеличенном количестве;
тип III — эстрогензависимая НАО. Уровни ингибитора С1 в норме.
Факторами, провоцирующими приступ НАО, являются:
Каковы симптомы НАО?
НАО клинически проявляется периодическим отеком кожи и слизистых оболочек. Частота судорог варьируется. Один приступ может происходить
в месяц или чаще — один раз в неделю, либо они могут быть достаточно редкими.
Отечный синдром включает в себя:
отечность кожи — она бледная, твердая, не зудит, иногда болезненна, проявляется или находится на коже лица, вокруг рта, век, языка, рук, шеи и проходит самопроизвольно через 1-2 дня;
отек слизистой оболочки ЖКТ — возникает при коликоподобных болях, тошноте, рвоте, проходит через 1-3 дня;
Диагноз НАО основан на:
НАО следует отличать от аллергического отека Квинке, на который влияют противоаллергические препараты.
Лечение НАО включает:
Криотиротомия или трахеостомия может быть выполнена в срочном порядке в случае отека гортани и риска удушья.
В межприступном периоде профилактическое лечение анаболическими стероидами может проводиться в течение 2-4 недель. Однако у них есть ряд
побочных эффектов — они приводят к усилению роста волос, изменениям либидо и нарушениям менструального цикла у женщин.
В случае предстоящих родов или удаления зубов, профилактическое лечение проводится путем переливания плазмы, введения антифибринолитиков
или профилактики анаболическими стероидами в течение 7 дней.
Ингибиторы АПФ (лекарства, используемые для лечения высокого кровяного давления) не должны использоваться у пациентов с НАО из-за риска отека.